名校
解题方法
1 . 下列反应的化学方程式正确的是
A.铁与稀硝酸反应: |
B.稀硫酸与Ag反应: |
C.浓硝酸和碳酸钙反应: |
D.稀硝酸和FeO反应: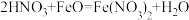 |
您最近半年使用:0次
2020-04-29更新
|
183次组卷
|
4卷引用:西藏自治区日喀则市拉孜高级中学2019-2020学年高一下学期期末考试化学试题
解题方法
2 . 亚硝酸钠广泛用于媒染剂、漂白剂等。某兴趣小组用下列装置制取较纯净的NaNO2。
甲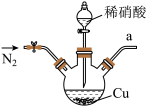 乙
乙 丙
丙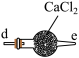 丁
丁
反应原理为:2NO+Na2O2=2NaNO2。已知:NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+。下列分析错误的是
甲
 乙
乙 丙
丙 丁
丁
反应原理为:2NO+Na2O2=2NaNO2。已知:NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+。下列分析错误的是
| A.甲中滴入稀硝酸前需通入N2 |
| B.仪器的连接顺序为a-f-g-d-e-b |
| C.丙中CaCl2用于干燥NO |
| D.乙中吸收尾气时发生的离子反应为3MnO4-+5NO+4H+=3Mn2++5NO3-+2H2O |
您最近半年使用:0次
2020-04-10更新
|
593次组卷
|
6卷引用:西藏自治区昌都市第一高级中学2020届高三下学期第二次模拟考试理综化学试题
西藏自治区昌都市第一高级中学2020届高三下学期第二次模拟考试理综化学试题四川省成都市2020届高中毕业班第二次诊断性检测理综化学试题湖南省邵阳市重点学校2020届高三综合模拟考试理综化学试题(已下线)第二单元 化学物质的变化测试题-2021年高考化学一轮复习名师精讲练(已下线)第26讲 化学实验基本操作及实验安全-2021年高考化学一轮复习名师精讲练福建省龙岩市第一中学锦山学校2021-2022学年高三上学期第三次月考化学试题
3 . 氧化亚铜(Cu2O)是一种用途广泛的光电材料,某工厂以硫化铜矿石(含CuFeS2、Cu2S等)为原料制取Cu2O的工艺流程如下:
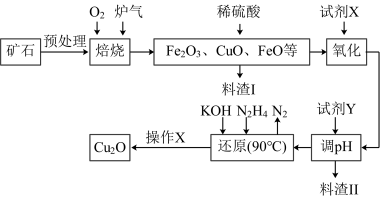
常温下几种物质开始形成沉淀与完全沉淀时的pH如下表:
(1)炉气中的有害气体成分是__________ ,Cu2S与O2反应时,氧化剂与还原剂的物质的量之比为__________ 。
(2)若试剂X是H2O2溶液,写出相应反应的离子方程式:________ 。当试剂X是______ 时,更有利于降低生产成本。
(3)加入试剂Y调pH时,pH的调控范围是___________ 。
(4)写出用N2H4制备Cu2O的化学方程式:________ ,操作X包括_________ 、洗涤、烘干,其中烘干时要隔绝空气,其目的是____________ 。
(5)以铜与石墨作电极,电解浓的强碱性溶液可制得纳米级Cu2O,写出阳极上生成Cu2O的电极反应式:__________ 。

常温下几种物质开始形成沉淀与完全沉淀时的pH如下表:
| Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀 | 7.5 | 2.7 | 4.8 |
| 完全沉淀 | 9.0 | 3.7 | 6.4 |
(1)炉气中的有害气体成分是
(2)若试剂X是H2O2溶液,写出相应反应的离子方程式:
(3)加入试剂Y调pH时,pH的调控范围是
(4)写出用N2H4制备Cu2O的化学方程式:
(5)以铜与石墨作电极,电解浓的强碱性溶液可制得纳米级Cu2O,写出阳极上生成Cu2O的电极反应式:
您最近半年使用:0次
2020-03-16更新
|
674次组卷
|
11卷引用:西藏自治区拉萨市拉萨中学2020届高三第六次月考理科化学试题
西藏自治区拉萨市拉萨中学2020届高三第六次月考理科化学试题【市级联考】河南省安阳市2019届高三下学期二模考试理科综合化学试题重庆市云阳江口中学校2020届高三上学期第二次月考理综化学试题2019年秋高三化学复习强化练习—— 离子反应方程式及离子共存2020届人教版高三化学二轮复习非选择题专攻练——工艺流程云南省楚雄州禄丰县第一中学2020届高三下学期3月线上模拟考试理综化学试题山东省2020届高三模拟考试化学(二)山西省运城市稷山县第二中学2020届高三上学期第三次月考化学试题四川省成都实验中学2021届高三上学期11月月考理综化学试题云南省大理州祥云四中2020届高三下学期3月线上模拟考试理综化学试题四川省内江市威远中学2021-2022学年高三上学期第三次月考化学试题
名校
解题方法
4 . 二氧化氯是一种黄绿色具有刺激性气味的气体,常用于自来水消毒和果蔬保鲜等方面。氯酸钠还原法是目前使用较为广泛的 制备方法,其中是用
制备方法,其中是用 与
与 在催化剂、
在催化剂、 时,发生反应得到
时,发生反应得到 ,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
已知:
① 的浓度较大时易分解,实验室用稳定剂吸收
的浓度较大时易分解,实验室用稳定剂吸收 ,生成
,生成 ,使用时加酸只释放出
,使用时加酸只释放出 一种气体
一种气体
② 与KI反应的离子方程式为:
与KI反应的离子方程式为: 。
。
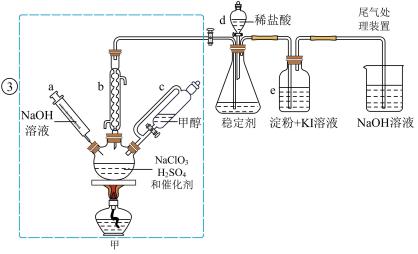
(1)仪器b在装置中的作用是______________ ;比较仪器c和d,实验中c的优点是_____________ 。
(2)制备装置甲中需改进的一项措施是________________ 。
(3)反应中甲醇被氧化为甲酸,写出制备 的化学方程式:
的化学方程式:________________ ;该制备法可选用不同的还原性物质作为还原剂,例如草酸,相比甲醇法,草酸法的优点是________________ 。
(4)下列有关说法正确的是__________ 。
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的
B.装置e主要用于检验是否有 生成
生成
C.在 释放实验中,发生的离子反应方程式是:
释放实验中,发生的离子反应方程式是: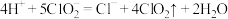
D. 和
和 都为强氧化剂,在相同条件下,等物质的量时
都为强氧化剂,在相同条件下,等物质的量时 的氧化能力是
的氧化能力是 的2.5倍
的2.5倍
(5)自来水厂用碘量法检测水中 的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用
的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用 标准溶液滴定碘单质
标准溶液滴定碘单质 ,达到滴定终点时用去15.00mL
,达到滴定终点时用去15.00mL 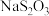 标准溶液,测得该水样中
标准溶液,测得该水样中 的含量为
的含量为__________  。
。
 制备方法,其中是用
制备方法,其中是用 与
与 在催化剂、
在催化剂、 时,发生反应得到
时,发生反应得到 ,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。已知:
①
 的浓度较大时易分解,实验室用稳定剂吸收
的浓度较大时易分解,实验室用稳定剂吸收 ,生成
,生成 ,使用时加酸只释放出
,使用时加酸只释放出 一种气体
一种气体②
 与KI反应的离子方程式为:
与KI反应的离子方程式为: 。
。| 物质 |  |  |  |
| 沸点 | 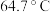 | 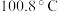 | 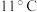 |

(1)仪器b在装置中的作用是
(2)制备装置甲中需改进的一项措施是
(3)反应中甲醇被氧化为甲酸,写出制备
 的化学方程式:
的化学方程式:(4)下列有关说法正确的是
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的

B.装置e主要用于检验是否有
 生成
生成C.在
 释放实验中,发生的离子反应方程式是:
释放实验中,发生的离子反应方程式是: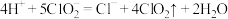
D.
 和
和 都为强氧化剂,在相同条件下,等物质的量时
都为强氧化剂,在相同条件下,等物质的量时 的氧化能力是
的氧化能力是 的2.5倍
的2.5倍(5)自来水厂用碘量法检测水中
 的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用
的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用 标准溶液滴定碘单质
标准溶液滴定碘单质 ,达到滴定终点时用去15.00mL
,达到滴定终点时用去15.00mL 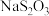 标准溶液,测得该水样中
标准溶液,测得该水样中 的含量为
的含量为 。
。
您最近半年使用:0次
2020-02-27更新
|
950次组卷
|
8卷引用:西藏拉萨中学2021届高三上学期第四次月考理综化学试题
解题方法
5 . 氨法溶浸氧化锌烟灰制取高纯锌的工艺流程如图所示。溶浸后氧化锌烟灰中锌、铜、镉、砷元素分别以 、
、 、
、 、
、 的形式存在。
的形式存在。
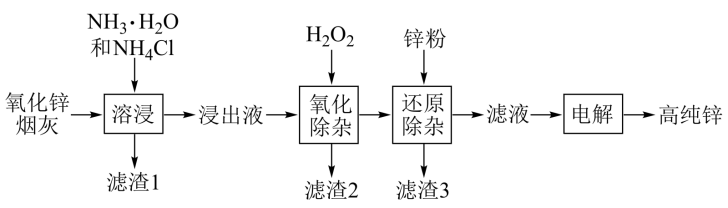
回答下列问题:
 中Zn的化合价为
中Zn的化合价为_______ ,“溶浸”中ZnO发生反应的离子方程式为_______ 。
 锌浸出率与温度的关系如图所示,分析
锌浸出率与温度的关系如图所示,分析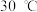 时锌浸出率最高的原因为
时锌浸出率最高的原因为_______ 。
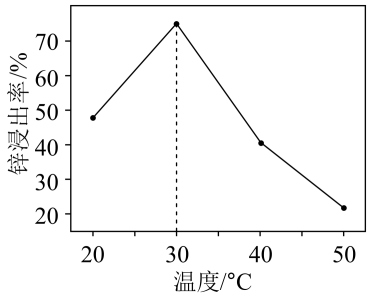
 “氧化除杂”中,
“氧化除杂”中, 转化为
转化为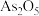 胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为
胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为_______ 。
 “滤渣3”的主要成分为
“滤渣3”的主要成分为_______ 。
 “电解”时
“电解”时 在阴极放电的电极反应式为
在阴极放电的电极反应式为______ 。阳极区放出一种无色无味的气体,将其通入滴有KSCN的 溶液中,无明显现象,该气体是
溶液中,无明显现象,该气体是_______  写化学式
写化学式 。电解后的电解液经补充
。电解后的电解液经补充_______  写一种物质的化学式
写一种物质的化学式 后可返回“溶浸”工序继续使用。
后可返回“溶浸”工序继续使用。
 、
、 、
、 、
、 的形式存在。
的形式存在。
回答下列问题:
 中Zn的化合价为
中Zn的化合价为 锌浸出率与温度的关系如图所示,分析
锌浸出率与温度的关系如图所示,分析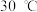 时锌浸出率最高的原因为
时锌浸出率最高的原因为
 “氧化除杂”中,
“氧化除杂”中, 转化为
转化为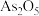 胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为
胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为 “滤渣3”的主要成分为
“滤渣3”的主要成分为 “电解”时
“电解”时 在阴极放电的电极反应式为
在阴极放电的电极反应式为 溶液中,无明显现象,该气体是
溶液中,无明显现象,该气体是 写化学式
写化学式 。电解后的电解液经补充
。电解后的电解液经补充 写一种物质的化学式
写一种物质的化学式 后可返回“溶浸”工序继续使用。
后可返回“溶浸”工序继续使用。
您最近半年使用:0次
2020-02-03更新
|
180次组卷
|
2卷引用:西藏拉萨市2020届高三第一次模拟考试理科综合化学试题
名校
6 . I.下列物质:①氢氧化钠溶液、②铝片、③液态HCl 、④葡萄糖、⑤熔融的NaCl、⑥SO2 气体、⑦碳酸氢钠、 ⑧氧化铝
(1)属于电解质的是______________________ 。(填编号)
(2)能导电的是____________________________________ 。(填编号)
(3)①和②反应的离子方程式________________________________ 。
II.实验室可通过K2Cr2O7溶液测定补铁剂中FeSO4的含量,反应如下K2Cr2O7 +□FeSO4 +□H2SO4 =□Cr2(SO4)3+□Fe2(SO4)3+□K2SO4+□H2O
(1)配平上述方程式,并在方程式上面用“双线桥”标明电子转移的方向和数目。_______________
(2)该反应的还原产物为__________ 。若反应中消耗1 mol K2Cr2O7,则转移电子数为______ 。
(1)属于电解质的是
(2)能导电的是
(3)①和②反应的离子方程式
II.实验室可通过K2Cr2O7溶液测定补铁剂中FeSO4的含量,反应如下K2Cr2O7 +□FeSO4 +□H2SO4 =□Cr2(SO4)3+□Fe2(SO4)3+□K2SO4+□H2O
(1)配平上述方程式,并在方程式上面用“双线桥”标明电子转移的方向和数目。
(2)该反应的还原产物为
您最近半年使用:0次
2019-12-29更新
|
81次组卷
|
2卷引用:西藏山南市第二高级中学2021届高三上学期第二次月考理综化学试题
7 . 下表标出的是元素周期表前四周期的部分元素。

强调:必须用相应的化学符号回答下列问题
(1)表中用字母标出的14种元素中,化学性质最不活泼的元素是____________ ,属于过渡元素的是_____________ (该空用字母表示)。
(2)G元素原子结构示意图为___________ 。K元素简单离子结构示意图为__________ 。
(3)D、G、I、L简单离子半径大小顺序是________________ 。(用离子符号表示)
(4)C、D、H的气态氢化物的稳定性大小顺序是_______________ 。(用分子式表示)
(5)表中所给元素的最高价氧化物水化物中碱性最强的是_________ 。(填化学式)
(6)E、F、G简单离子的氧化性大小顺序是________________ 。(用离子符号表示)
(7)写出元素G的氧化物与E的氢氧化物反应的离子方程式________________ 。
(8)I的某种氧化物和J单质的水溶液发生反应的方程式________________ 。

强调:必须用相应的化学符号回答下列问题
(1)表中用字母标出的14种元素中,化学性质最不活泼的元素是
(2)G元素原子结构示意图为
(3)D、G、I、L简单离子半径大小顺序是
(4)C、D、H的气态氢化物的稳定性大小顺序是
(5)表中所给元素的最高价氧化物水化物中碱性最强的是
(6)E、F、G简单离子的氧化性大小顺序是
(7)写出元素G的氧化物与E的氢氧化物反应的离子方程式
(8)I的某种氧化物和J单质的水溶液发生反应的方程式
您最近半年使用:0次
8 . 汽车尾气主要含有CO2、CO、SO2、NOx等物质,逐渐成为城市空气主要污染源。
(1)写出CO2的电子式_____________ ;CO2带来的主要环境问题是________ 。
(2)汽车尾气中的CO来自于________________ ,NO来自于_________________ 。
(3)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式___________________ 。
(4)在适宜温度下采用合适催化剂,CO和NO相互反应生成参与大气循环的无毒气体。写出反应化学方程式_______________ 。
(5)在催化剂作用下,可用氨气将NO和NO2转化为无毒气体,写出NO2和NH3反应生成无毒气体的化学方程式______________ 。
(6)当燃油中含硫量较高时,尾气中SO2在O2作用下与氨气形成(NH4)2SO4,用化学方程式表示(NH4)2SO4的形成_________________ 。
(1)写出CO2的电子式
(2)汽车尾气中的CO来自于
(3)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式
(4)在适宜温度下采用合适催化剂,CO和NO相互反应生成参与大气循环的无毒气体。写出反应化学方程式
(5)在催化剂作用下,可用氨气将NO和NO2转化为无毒气体,写出NO2和NH3反应生成无毒气体的化学方程式
(6)当燃油中含硫量较高时,尾气中SO2在O2作用下与氨气形成(NH4)2SO4,用化学方程式表示(NH4)2SO4的形成
您最近半年使用:0次
9 . NF3(三氟化氮)在常温常压下是无色、无味的气体,是微电子工业中一种优良的等离子蚀刻气体。回答下列问题:
(1)NF3的电子式为______ ,N元素的化合价为______ 。
(2)F2与NH3直接反应生成NF3的化学方程式为______ 。
(3)实验室模拟工业上利用电解熔融NH4HF2(NH4F•HF)法制取NF3,阳极为以Ni为基本材料的合金(内含其他金属,忽略镍及其他金属的反应),阴极为碳素钢,电解废液可回收再利用。
①电解时NF3在______ 极生成;阴极产生的气体是______ (填化学式)。
②电解后废液(含Ni少量Fe和Cu的单质及NH4HF2等)可经如下流程进行回收再利用:
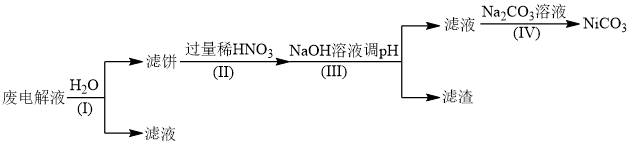
已知该实验条件下,部分金属离子开始沉淀与沉淀完全的pH如下表
步骤I的目的是______ ;步骤Ⅱ滤饼中Ni溶于硝酸的离子方程式为______ (HNO3的还原产物为NO);步骤Ⅲ调节pH时,理论上pH应控制的范围是______ 。
(1)NF3的电子式为
(2)F2与NH3直接反应生成NF3的化学方程式为
(3)实验室模拟工业上利用电解熔融NH4HF2(NH4F•HF)法制取NF3,阳极为以Ni为基本材料的合金(内含其他金属,忽略镍及其他金属的反应),阴极为碳素钢,电解废液可回收再利用。
①电解时NF3在
②电解后废液(含Ni少量Fe和Cu的单质及NH4HF2等)可经如下流程进行回收再利用:

已知该实验条件下,部分金属离子开始沉淀与沉淀完全的pH如下表
| 金属离子 | Ni2+ | Fe2+ | Cu2+ | Fe3+ |
| 开始沉淀时的pH | 7.2 | 7.0 | 4.7 | 1.9 |
| 沉淀完全时的pH | 9.2 | 9.0 | 6.7 | 3.2 |
您最近半年使用:0次
2019-10-28更新
|
220次组卷
|
3卷引用:西藏自治区拉萨中学2020届高三上学期第四次月考理综化学试题
名校
10 . 铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上综合利用铝土矿的部分工艺流程如下。

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。 该过程中涉及某氧化还原反应如下,请完成:□Fe2++□ClO-+ = □Fe(OH)3↓+□Cl-+ 。_________
(2)检验滤液B中是否还含有Fe2+的方法为:__________ 。
(3)将滤液B中的铝元素以沉淀形式析出,选用的最好试剂为______ (填代号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
(4)由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、_________ (填操作名称)、过滤、洗涤。
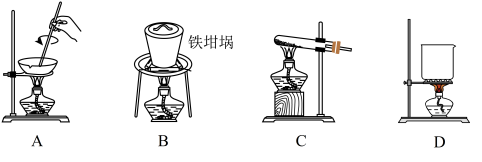
(5)滤渣的主要成分是____________ (填化学式),其与NaOH固体焙烧制备硅酸钠,可采用的装置为____ (填代号),该反应的化学方程式是 ________________________ 。

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。 该过程中涉及某氧化还原反应如下,请完成:□Fe2++□ClO-+ = □Fe(OH)3↓+□Cl-+ 。
(2)检验滤液B中是否还含有Fe2+的方法为:
(3)将滤液B中的铝元素以沉淀形式析出,选用的最好试剂为
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
(4)由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、
(5)滤渣的主要成分是

您最近半年使用:0次
2019-10-09更新
|
455次组卷
|
3卷引用:西藏日喀则市上海实验学校2020-2021学年高三上学期第二次月考理综化学试题



