2021高三·全国·专题练习
解题方法
1 . 向含4molHCl的浓盐酸中,加入足量的MnO2,加热,充分反应后,生成NA个Cl2。(_____)
您最近一年使用:0次
2 . 为制取含 浓度较高的溶液,下列图示装置和原理均正确,且能达到实验目的的是
浓度较高的溶液,下列图示装置和原理均正确,且能达到实验目的的是
 浓度较高的溶液,下列图示装置和原理均正确,且能达到实验目的的是
浓度较高的溶液,下列图示装置和原理均正确,且能达到实验目的的是 | 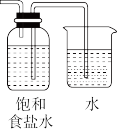 | 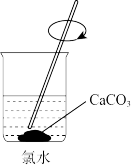 | 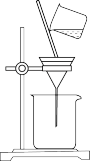 |
| A.制取氯气 | B.制取氯水 | C.提高 浓度 浓度 | D.过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-06-30更新
|
422次组卷
|
7卷引用:考点28 化学实验仪器与基本操作-备战2022年高考化学一轮复习考点帮(浙江专用)
(已下线)考点28 化学实验仪器与基本操作-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点29 化学实验基础-备战2022年高考化学一轮复习考点帮(全国通用)江苏省南通、扬州、泰州市2017届高三第三次模拟考试化学试题四川省绵阳市三台县芦溪中学2018届高三第一次诊断性考试理综化学试题江苏省南通市如东县、海安市2021-2022学年高二下学期期末考试化学试题广西北海市普通高中2022届高三第四次模拟考试化学试题江苏省常熟市2022-2023学年高二下学期期中考试化学试题
名校
3 . 用所给试剂与图示装置能够制取相应气体的是(夹持仪器略)
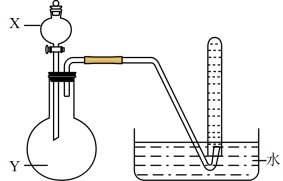

| A | B | C | D | |
| X 中试剂 | 浓盐酸 | 浓硫酸 | 双氧水 | 浓氨水 |
| Y 中试剂 | MnO2 | C2H5OH | MnO2 | NaOH |
| 气体 | Cl2 | C2H4 | O2 | NH3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-26更新
|
2065次组卷
|
10卷引用:浙江省舟山市舟山中学2021-2022学年高三上学期开学考试化学试题
浙江省舟山市舟山中学2021-2022学年高三上学期开学考试化学试题浙江省名校协作体2023-2024学年高二上学期开学适应性考试化学试题广东省惠州市2022届高三第一次模拟考试化学试题(已下线)微专题24 氯气、氨气、二氧化硫的实验室制备与应用-备战2023年高考化学一轮复习考点微专题(已下线)微专题44 以气体制备为主体的实验-备战2023年高考化学一轮复习考点微专题(已下线)【知识图鉴】单元讲练测必修第二册第五单元 03巩固练广东省阳山县南阳中学2022-2023学年高一下学期第一次月考化学试题广西防城港市实验高级中学2022-2023学年高一下学期期中考试化学试题(已下线)专题突破卷04?非金属及其化合物?-2024年高考化学一轮复习考点通关卷(新教材新高考)(已下线)专题突破卷13 化学实验基础(二)-2024年高考化学一轮复习考点通关卷(新教材新高考)
4 . 次氯酸(HClO)消毒液高效安全,适用于一般物体表面消毒、手部消毒,以及地面、空间和环境消毒。下图装置在D中制得颜色类似于氯气的Cl2O气体,E中得到次氯酸(HClO)。已知Cl2O气体45℃可分解,与水反应生成HClO。
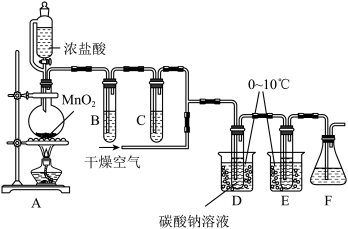
(1)装置A中使用该漏斗的目的是_______ 。
(2)装置A中发生反应的离子方程式为_______ 。
(3)C装置、F装置中分别盛装_______ 、_______ 。
(4)D中盛装碳酸钠溶液用来吸收氯气制备Cl2O。D中生成的气体中含有CO2,则生成Cl2O的化学方程式为_______ 。
(5)实验时,一直要通入干燥的空气,主要作用是_______ ,同时还可以抑制Cl2O的分解,保证实验安全。
(6)为了探究反应条件对产物的影响,另取一定量的石灰乳,缓慢、匀速地通入足量氯气,得出了ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示如图(不考虑氯气和水的反应)。已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH-
两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示如图(不考虑氯气和水的反应)。已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH- 5Cl-+ClO
5Cl-+ClO +3H2O
+3H2O
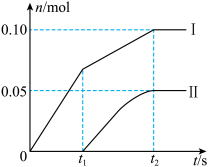
①图中曲线I表示_______ 离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为_______ mol,参加反应的氯气的体积为_______ (标况下)
③另取一份与②等物质的量的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl-的物质的量为0.37 mol,则产物中 =
=_______ 。

(1)装置A中使用该漏斗的目的是
(2)装置A中发生反应的离子方程式为
(3)C装置、F装置中分别盛装
(4)D中盛装碳酸钠溶液用来吸收氯气制备Cl2O。D中生成的气体中含有CO2,则生成Cl2O的化学方程式为
(5)实验时,一直要通入干燥的空气,主要作用是
(6)为了探究反应条件对产物的影响,另取一定量的石灰乳,缓慢、匀速地通入足量氯气,得出了ClO-、ClO
 两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示如图(不考虑氯气和水的反应)。已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH-
两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示如图(不考虑氯气和水的反应)。已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH- 5Cl-+ClO
5Cl-+ClO +3H2O
+3H2O
①图中曲线I表示
②所取石灰乳中含有Ca(OH)2的物质的量为
③另取一份与②等物质的量的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl-的物质的量为0.37 mol,则产物中
 =
=
您最近一年使用:0次
名校
解题方法
5 . 下列说法正确 的是
| A.将铂丝用硫酸洗净后,在外焰上灼烧至火焰颜色与酒精灯火焰一致,再蘸取碳酸钾灼烧,直接可观察到火焰呈紫色 |
| B.容量瓶检漏方法:往瓶内加适量水,塞好瓶塞,用手指按住瓶塞,另一手托住瓶底,将瓶倒立,观察瓶塞周围是否漏水,若不漏水,将瓶正立后把瓶塞旋转180°,再把瓶倒立过来,观察瓶塞周围否漏水,经检查不漏水的容量瓶才能使用 |
| C.用饱和NaHCO3溶液均可除去CO2和Cl2中混有的HCl杂质 |
| D.在实验室制氯气实验中,可以取烧瓶中剩余的溶液少量于试管中,先加入稀硝酸,再加入硝酸银,若出现白色沉淀,即可说明盐酸仍有剩余 |
您最近一年使用:0次
名校
6 . 实验能力和创新意识是化学学科核心素养的重要内容之一、请回答以下问题:
Ⅰ.某实验小组需要 的
的 溶液,请回答:
溶液,请回答:
(1)配制所需主要玻璃仪器除了烧杯、玻璃棒、量筒外,还需要___________ ;
(2)需要称取的 固体的质量为
固体的质量为___________ 。
Ⅱ.某兴趣小组在实验室中模拟工业上用氯气制备无水氯化铝[无水 (183℃升华)遇潮湿空气即产生大量白雾)],可用下列装置制备:
(183℃升华)遇潮湿空气即产生大量白雾)],可用下列装置制备:

(3)装置B中盛放___________ ,其作用是___________ 。F中的是___________ ,其作用是___________ 。
(4)装置A实验开始时,先检查装置的气密性,接下来的操作依次是___________ (填序号)。
①往烧瓶中加入 粉末;②加热;③往烧瓶中加入浓盐酸
粉末;②加热;③往烧瓶中加入浓盐酸
(5)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,同学们提出如下方案:让残留的液体与足量Zn反应,测量生成的 体积。装置如图所示(夹持器具略去),请回答:
体积。装置如图所示(夹持器具略去),请回答:

①使丫形管中的残余清液与锌粒反应的正确操作是将___________ 转移到___________ 中;
②平视读数前应依次进行的两步操作是___________ 。
Ⅰ.某实验小组需要
 的
的 溶液,请回答:
溶液,请回答:(1)配制所需主要玻璃仪器除了烧杯、玻璃棒、量筒外,还需要
(2)需要称取的
 固体的质量为
固体的质量为Ⅱ.某兴趣小组在实验室中模拟工业上用氯气制备无水氯化铝[无水
 (183℃升华)遇潮湿空气即产生大量白雾)],可用下列装置制备:
(183℃升华)遇潮湿空气即产生大量白雾)],可用下列装置制备:
(3)装置B中盛放
(4)装置A实验开始时,先检查装置的气密性,接下来的操作依次是
①往烧瓶中加入
 粉末;②加热;③往烧瓶中加入浓盐酸
粉末;②加热;③往烧瓶中加入浓盐酸(5)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,同学们提出如下方案:让残留的液体与足量Zn反应,测量生成的
 体积。装置如图所示(夹持器具略去),请回答:
体积。装置如图所示(夹持器具略去),请回答:
①使丫形管中的残余清液与锌粒反应的正确操作是将
②平视读数前应依次进行的两步操作是
您最近一年使用:0次
7 . 实验室用图所示装置制备KClO溶液,并通过KClO溶液与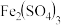 溶液的反应制备高效水处理剂高铁酸钾
溶液的反应制备高效水处理剂高铁酸钾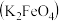 。
。

(1) ,其中铁元素的化合价为
,其中铁元素的化合价为_______ 。
(2)B装置的作用是_______ 。
(3)写出装置A中制备 的化学方程式:
的化学方程式:_______ 。
(4)装置D中发生的离子反应方程式_______ 。
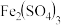 溶液的反应制备高效水处理剂高铁酸钾
溶液的反应制备高效水处理剂高铁酸钾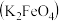 。
。
(1)
 ,其中铁元素的化合价为
,其中铁元素的化合价为(2)B装置的作用是
(3)写出装置A中制备
 的化学方程式:
的化学方程式:(4)装置D中发生的离子反应方程式
您最近一年使用:0次
名校
解题方法
8 . 高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2 +3Cl-+5H2O。请回答以下问题:
+3Cl-+5H2O。请回答以下问题:
(1)该反应中发生氧化反应的离子是___________ (填离子符号)。
(2)若该反应恰好转移了3mol电子时,生成H2O的质量为___________ g
(3)84消毒液的主要成分为NaClO,洁厕灵的主要成分是稀盐酸,该两种商品同时使用容易发生氯气中毒事件,请用离子方程式分析原因___________ 。。
(4)氯气作为传统的自来水消毒剂,实验室制氯气的化学方程式为___________ 。
 +3Cl-+5H2O。请回答以下问题:
+3Cl-+5H2O。请回答以下问题:(1)该反应中发生氧化反应的离子是
(2)若该反应恰好转移了3mol电子时,生成H2O的质量为
(3)84消毒液的主要成分为NaClO,洁厕灵的主要成分是稀盐酸,该两种商品同时使用容易发生氯气中毒事件,请用离子方程式分析原因
(4)氯气作为传统的自来水消毒剂,实验室制氯气的化学方程式为
您最近一年使用:0次
9 . 某学习小组探究潮湿的Cl2与Na2CO3反应的产物,进行如下实验:

请回答:
(1)仪器X的名称是:___________ 。试剂Y是___________ 。
(2)装置E的作用是:___________ 。
(3)请写出装置A中的化学方程式,并用单线桥法表示电子转移的方向和数目___________ 。
(4)装置C中潮湿的Cl2与Na2CO3以等物质的量反应,生成NaHCO3、气体Cl2O和另一种盐,试写出该反应化学方程式:___________ 。
(5)若将上述装置中的C、D、E部分换成下图所述装置,其中I与III是干燥的有色布条,E中盛装NaOH溶液,请回答下列问题:
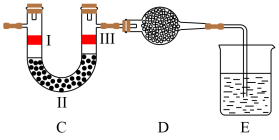
①装置C的作用是验证氯气是否具有漂白性,则装置C中II的作用是______ 。
②描述I、III处的现象:________ ,从物质性质说明I、III处现象不同的原因:________ 。
③D中应装入的物质是______
a.浓硫酸 b.生石灰 c.NaCl固体 d.NaOH固体

请回答:
(1)仪器X的名称是:
(2)装置E的作用是:
(3)请写出装置A中的化学方程式,并用单线桥法表示电子转移的方向和数目
(4)装置C中潮湿的Cl2与Na2CO3以等物质的量反应,生成NaHCO3、气体Cl2O和另一种盐,试写出该反应化学方程式:
(5)若将上述装置中的C、D、E部分换成下图所述装置,其中I与III是干燥的有色布条,E中盛装NaOH溶液,请回答下列问题:

①装置C的作用是验证氯气是否具有漂白性,则装置C中II的作用是
②描述I、III处的现象:
③D中应装入的物质是
a.浓硫酸 b.生石灰 c.NaCl固体 d.NaOH固体
您最近一年使用:0次
名校
解题方法
10 . AlCl3是一种催化剂,某校学习小组用下面装置制备少量AlCl3。已知:AlCl3遇到空气中的水蒸气时能剧烈反应生成Al(OH)3和HCl;AlCl3在180℃时升华。根据要求完成下列问题:
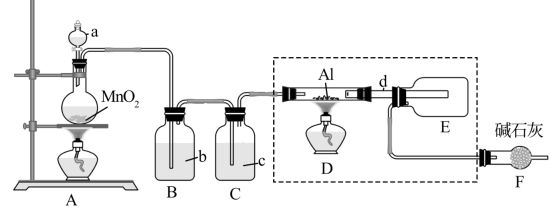
(1)A装置中反应的离子方程式为____ 。
(2)试剂b为____ 。
(3)所用d导管较粗的原因是____ 。
(4)F装置的作用为____ 。

(1)A装置中反应的离子方程式为
(2)试剂b为
(3)所用d导管较粗的原因是
(4)F装置的作用为
您最近一年使用:0次



