名校
解题方法
1 . 最新研究表明,有毒气体H2S具有参与调节神经信号传递、舒张血管减轻高血压的功能。
(1)下列事实中,可以用来比较H2S与H2SO3的酸性强弱的是______ (填标号)。
A.H2S的还原性强于H2SO3
B.0.10 mol·L-1的H2S和H2SO3的pH分别为4.5和2.1
C.H2S不能与NaHCO3溶液反应,而H2SO3可以
D.等浓度的两种溶液pH值: NaHS > NaHSO3
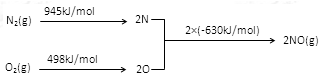
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知(1)式和(5)式的热化学方程式分别为___________ 、________________ ,制得等量H2所需能量系统I是系统II的_______ 倍。
(3)H2S与CO2在高温下发生反应: H2S(g)+CO2(g) COS(g) +H2O(g)△H >0;保持T1温度,将0.20mol CO2与0.80mol H2S充入2.5L的空钢瓶中,反应平衡后COS的物质的量分数为0.02
COS(g) +H2O(g)△H >0;保持T1温度,将0.20mol CO2与0.80mol H2S充入2.5L的空钢瓶中,反应平衡后COS的物质的量分数为0.02
①H2S的平衡转化率a1=_______ %,反应平衡常数K=______________ 。
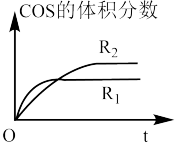
②在不同条件下发生上述反应,COS的体积分数随时间(t)的变化如图所示,根据图象可以判断曲线R1、R2对应的下列反应条件中不同的是____________ (填字母序号)CO2的转化率a2__ a1,(填”>”或“<”)
A.压强B.温度C.催化剂
(4)反应开始,保持T1温度,2L钢瓶中充入0.08molCO2、0.40molH2S、0.02molCOS和0.02molH2O,则此时V正___ V逆(填”>”或“<”)判断依据是___________________________ 。
(1)下列事实中,可以用来比较H2S与H2SO3的酸性强弱的是
A.H2S的还原性强于H2SO3
B.0.10 mol·L-1的H2S和H2SO3的pH分别为4.5和2.1
C.H2S不能与NaHCO3溶液反应,而H2SO3可以
D.等浓度的两种溶液pH值: NaHS > NaHSO3
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知(1)式和(5)式的热化学方程式分别为
(3)H2S与CO2在高温下发生反应: H2S(g)+CO2(g)
 COS(g) +H2O(g)△H >0;保持T1温度,将0.20mol CO2与0.80mol H2S充入2.5L的空钢瓶中,反应平衡后COS的物质的量分数为0.02
COS(g) +H2O(g)△H >0;保持T1温度,将0.20mol CO2与0.80mol H2S充入2.5L的空钢瓶中,反应平衡后COS的物质的量分数为0.02①H2S的平衡转化率a1=
②在不同条件下发生上述反应,COS的体积分数随时间(t)的变化如图所示,根据图象可以判断曲线R1、R2对应的下列反应条件中不同的是
A.压强B.温度C.催化剂

(4)反应开始,保持T1温度,2L钢瓶中充入0.08molCO2、0.40molH2S、0.02molCOS和0.02molH2O,则此时V正
您最近一年使用:0次
2017-12-31更新
|
196次组卷
|
2卷引用:山西省祁县中学2018届高三12月月考化学试题
名校
2 . 已知热化学方程式:2H2(g)+O2(g) =2H2O(l) ∆H= -571.6 kJ·mol-1,2CH3OH(l)+3O2(g) =2CO2(g)+4H2O(l) ∆H= -1452 kJ·mol-1,H+(aq)+OH-(aq) =H2O(l) ∆H= -57.3 kJ·mol-1。据此判断下列说法正确的是
| A.CH3OH的燃烧热∆H为-1452 kJ·mol-1 |
| B.2H2(g)+O2(g) =2H2O(g) ∆H > -571.6 kJ·mol-1 |
| C.CH3COOH(aq)+NaOH(aq)=H2O(l)+CH3COONa(aq) ∆H= -57.3 kJ·mol-1 |
| D.2CH3OH(l)+O2(g)=2CO2(g)+4H2(g) ∆H= -880.4 kJ·mol-1 |
您最近一年使用:0次
2017-12-02更新
|
492次组卷
|
11卷引用:山西省晋中市平遥县第二中学2019-2020学年高二12月月考化学试题
山西省晋中市平遥县第二中学2019-2020学年高二12月月考化学试题2016届广东省华南师大附中等四校高三上期末联考理综化学试卷2016届江西省赣州市十三县高三下期中理综化学试卷广东省广东实验中学2017-2018学年高二上学期期中考试化学试题【全国百强校】山西省山西大学附属中学2018-2019学年高二上学期期中考试化学试题河南省周口中英文学校2019-2020学年高二上学期期中考试化学试题安徽省滁州市定远县民族中学2019-2020学年高二上学期期中考试化学试题安徽省滁州市定远县育才学校2019-2020学年高二(普通班)上学期第三次月考化学试题安徽省滁州市定远县育才学校2019-2020学年高二(实验班)上学期第三次月考化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——弱电解质的电离及影响因素(强化练习)广东实验中学2022-2023学年高二上学期期中考试化学试题
名校
3 . 羰基硫(COS)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染。
(1)羰基硫的水解反应和氢解反应是两种常用的脱硫方法:
水解反应:COS(g)+ H2O(g) H2S(g) +CO2(g) △H=-34 kJ·mol1
H2S(g) +CO2(g) △H=-34 kJ·mol1
氢解反应:COS(g) +H2(g) H2S(g)+CO(g) △H=+7 kJ·mol1。
H2S(g)+CO(g) △H=+7 kJ·mol1。
已知:2H2(g) +O2(g)=== 2H2O(g) △H=-484 kJ·mol1。
写出表示CO燃烧热的热化学方程式:______________ 。
(2)氢解反应达到平衡后,保持体系的温度和总压强不变,通入适量的He,正反应速率______ (填“增大”“减小”或“不变”,下同),COS 的转化率_______ 。
(3)某温度下,向体积为2L的恒容密闭容器中通入2molCOS(g)和4molH2O(g),发生水解反应,5 min后反应达到平衡,测得COS(g)的转化率为75%。
回答下列问题:
①反应从起始至5 min 内,v(H2S)=_______ mol·L-1·min-1。
②该温度下,上述水解反应的平衡常数K=____________ 。
(1)羰基硫的水解反应和氢解反应是两种常用的脱硫方法:
水解反应:COS(g)+ H2O(g)
 H2S(g) +CO2(g) △H=-34 kJ·mol1
H2S(g) +CO2(g) △H=-34 kJ·mol1氢解反应:COS(g) +H2(g)
 H2S(g)+CO(g) △H=+7 kJ·mol1。
H2S(g)+CO(g) △H=+7 kJ·mol1。已知:2H2(g) +O2(g)=== 2H2O(g) △H=-484 kJ·mol1。
写出表示CO燃烧热的热化学方程式:
(2)氢解反应达到平衡后,保持体系的温度和总压强不变,通入适量的He,正反应速率
(3)某温度下,向体积为2L的恒容密闭容器中通入2molCOS(g)和4molH2O(g),发生水解反应,5 min后反应达到平衡,测得COS(g)的转化率为75%。
回答下列问题:
①反应从起始至5 min 内,v(H2S)=
②该温度下,上述水解反应的平衡常数K=
您最近一年使用:0次
2017-11-19更新
|
315次组卷
|
5卷引用:山西省祁县第二中学2019-2020学年高二10月月考化学试题
名校
解题方法
4 . 雾霾天气肆虐给人类健康带来了严重影响.燃煤和汽车尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO 2CO2(g)+N2(g) △H<O
2CO2(g)+N2(g) △H<O
①反应的速率时间图像如图1所示.若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如图2所示.以下说法正确的是(填对应字母)__________
B.b1<b2
C.t1>t2
D.图2中阴影部分面积更大
E.图1中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是(填代号)__________
已知:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
2NO2(g) N2O4(g)△H=﹣56.9kJ/mol H2O(g)=H2O(l)△H=﹣44.0kJ/mol
N2O4(g)△H=﹣56.9kJ/mol H2O(g)=H2O(l)△H=﹣44.0kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:__________ .
(3)CH4和H2O(g)在催化剂表面发生反应CH4+H2O⇌CO+3H2,该反应在不同温度下的化学平衡常数如表:
①该反应是__________ 反应(填“吸热”或“放热”).
②T℃时,向1L密闭容器中投入l mol CH4和l mol H2O(g),平衡时c(CH4)=0.5mol/L,该温度下反应CH4+H2O CO+3H2的平衡常数K=
CO+3H2的平衡常数K=__________ ;
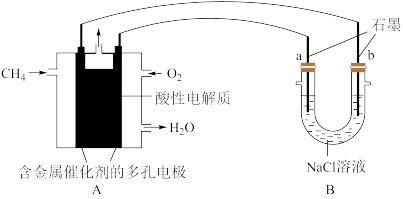
(4)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解100ml1mol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24L(设电解后溶液体积不变)。__________
②电解后溶液的pH=__________ (忽略氯气与氢氧化钠溶液反应)
③阳极产生气体的体积在标准状况下是__________ L。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO
 2CO2(g)+N2(g) △H<O
2CO2(g)+N2(g) △H<O①反应的速率时间图像如图1所示.若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如图2所示.以下说法正确的是(填对应字母)

B.b1<b2
C.t1>t2
D.图2中阴影部分面积更大
E.图1中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是(填代号)
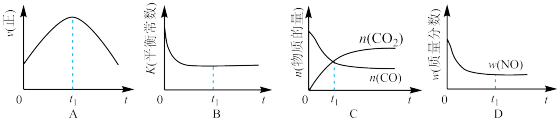
已知:CH4(g)+2NO2(g)
 N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol2NO2(g)
 N2O4(g)△H=﹣56.9kJ/mol H2O(g)=H2O(l)△H=﹣44.0kJ/mol
N2O4(g)△H=﹣56.9kJ/mol H2O(g)=H2O(l)△H=﹣44.0kJ/mol写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:
(3)CH4和H2O(g)在催化剂表面发生反应CH4+H2O⇌CO+3H2,该反应在不同温度下的化学平衡常数如表:
| 温度/℃ | 800 | 1000 | 1200 | 1400 |
| 平衡常数 | 0.45 | 1.92 | 276.5 | 1771.5 |
②T℃时,向1L密闭容器中投入l mol CH4和l mol H2O(g),平衡时c(CH4)=0.5mol/L,该温度下反应CH4+H2O
 CO+3H2的平衡常数K=
CO+3H2的平衡常数K=(4)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解100ml1mol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24L(设电解后溶液体积不变)。
②电解后溶液的pH=
③阳极产生气体的体积在标准状况下是
您最近一年使用:0次
2017-02-17更新
|
377次组卷
|
7卷引用:2016届山西省祁县中学高三5月月考理综化学试卷
5 . 为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物含量显得尤为重要。
(1)一定条件下,将2moLNO与2molO2置于恒容密闭容器中发生反应2NO(g)+O2(g)⇌2NO2(g),下列各项能说明反应达到平衡状态的是_____________ ;
a.体系压强保持不变
b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变
d.每消耗1molO2同时生成2molNO2
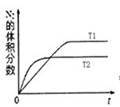
(2)汽车内燃机工作时会引起N2和O2的反应:N2+O2═2NO,是导致汽车尾气中含有NO的原因之一;在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如图所示,根据图象判断反应N2(g)+O2(g)═2NO(g)的△H__________ 0(填>或<)。
(3)NOx是汽车尾气中的主要污染物之一。汽车发动机工作时会引起N2和O2反应,其能量变化如图所示,写出该反应的热化学方程式_____________________ ;
(1)一定条件下,将2moLNO与2molO2置于恒容密闭容器中发生反应2NO(g)+O2(g)⇌2NO2(g),下列各项能说明反应达到平衡状态的是
a.体系压强保持不变
b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变
d.每消耗1molO2同时生成2molNO2
(2)汽车内燃机工作时会引起N2和O2的反应:N2+O2═2NO,是导致汽车尾气中含有NO的原因之一;在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如图所示,根据图象判断反应N2(g)+O2(g)═2NO(g)的△H

(3)NOx是汽车尾气中的主要污染物之一。汽车发动机工作时会引起N2和O2反应,其能量变化如图所示,写出该反应的热化学方程式

您最近一年使用:0次
6 . 已知298K,1.01×105Pa条件下:2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1;
CO(g)+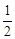 O2(g)=CO2(g) △H=-282.9kJ·mol-1则该条件下CO(g)+H2O(g) = H2(g)+CO2(g)的反应热是
O2(g)=CO2(g) △H=-282.9kJ·mol-1则该条件下CO(g)+H2O(g) = H2(g)+CO2(g)的反应热是
CO(g)+
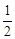 O2(g)=CO2(g) △H=-282.9kJ·mol-1则该条件下CO(g)+H2O(g) = H2(g)+CO2(g)的反应热是
O2(g)=CO2(g) △H=-282.9kJ·mol-1则该条件下CO(g)+H2O(g) = H2(g)+CO2(g)的反应热是| A.- 41.1 kJ·mol-1 | B.+ 200.7 kJ·mol-1 |
| C.- 766.5 kJ·mol-1 | D.+ 41.1 kJ·mol-1 |
您最近一年使用:0次
2016-12-09更新
|
133次组卷
|
2卷引用:山西省祁县第二中学2019-2020学年高二10月月考化学试题
真题
名校
7 . 氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
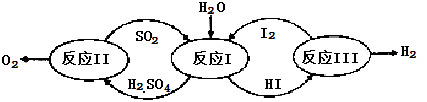
(1)反应Ⅰ的化学方程式是___________ 。
(2)反应Ⅰ得到的产物用I2进行分离。该产物的溶液在过量I2的存在下会分成两层——含低浓度I2的H2SO4层和高浓度的I2的HI层。
①根据上述事实,下列说法正确的是___________ (选填序号)。
a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
②辨别两层溶液的方法是___________ 。
③经检测,H2SO4层中c(H+):c(SO42-)=2.06:1。其比值大于2的原因是___________ 。
(3)反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550kJ/mol
它由两步反应组成:i.H2SO4(l)=SO3(g) +H2O(g) △H=+177kJ/mol
ii.SO3(g)分解。
L(L1、L2),X可分别代表压强或温度。下图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。
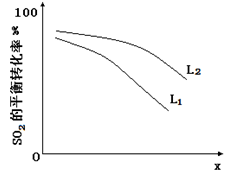
①X代表的物理量是_________________ 。
②判断L1、L2的大小关系,并简述理由:_________________ 。

(1)反应Ⅰ的化学方程式是
(2)反应Ⅰ得到的产物用I2进行分离。该产物的溶液在过量I2的存在下会分成两层——含低浓度I2的H2SO4层和高浓度的I2的HI层。
①根据上述事实,下列说法正确的是
a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
②辨别两层溶液的方法是
③经检测,H2SO4层中c(H+):c(SO42-)=2.06:1。其比值大于2的原因是
(3)反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550kJ/mol
它由两步反应组成:i.H2SO4(l)=SO3(g) +H2O(g) △H=+177kJ/mol
ii.SO3(g)分解。
L(L1、L2),X可分别代表压强或温度。下图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。

①X代表的物理量是
②判断L1、L2的大小关系,并简述理由:
您最近一年使用:0次
2016-12-09更新
|
2433次组卷
|
3卷引用:2016届山西省平遥中学高三第二轮训练三化学试卷
名校
8 . 根据碘与氢气反应的热化学方程式 (i)I2(g)+H2(g) 2HI(g) △H=-9.48kJ/mol ,(ii) I2(s)+H2(g)
2HI(g) △H=-9.48kJ/mol ,(ii) I2(s)+H2(g) 2HI(g) △H=+26.48kJ/mol,下列判断正确的是
2HI(g) △H=+26.48kJ/mol,下列判断正确的是
 2HI(g) △H=-9.48kJ/mol ,(ii) I2(s)+H2(g)
2HI(g) △H=-9.48kJ/mol ,(ii) I2(s)+H2(g) 2HI(g) △H=+26.48kJ/mol,下列判断正确的是
2HI(g) △H=+26.48kJ/mol,下列判断正确的是| A.254g I2(g)中通入2g H2(g),反应放热9.48 kJ |
| B.1 mol固态碘与1mol气态碘所含的能量相差l7.00 kJ |
| C.反应(i)的产物比反应(ii)的产物稳定 |
| D.反应(i) 拆开1mol I-I键与1mol H-H键需要的总能量小于拆开2mol H-I键需要的总能量 |
您最近一年使用:0次
2016-09-18更新
|
318次组卷
|
7卷引用:山西省晋中市和诚中学2019-2020学年高一3月月考化学试题



