名校
1 . 捕集CO2的技术对解决全球温室效应意义重大。目前国际空间站处理CO2的一个重要方法是将CO2还原,涉及的化学反应如下:CO2(g)+4H2(g)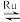 CH4(g)+2H2O(g)+Q(Q>0)
CH4(g)+2H2O(g)+Q(Q>0)
(1)该反应的平衡常数表达式为_______ 。如果改变某种条件,平衡向正反应方向移动,则平衡常数_______ (填写编号)。
a.一定增大 b.一定减小 c.可能增大 d.可能减小 e.可能不变
(2)向2L某密闭容器充入1molCO2和4molH2,一定条件下发生上述反应。5min末测得气体的物质的量减少了20%,则0~5min内CO2的平均反应速率为_______ 。
(3)CO2还可应用于纯碱工业。侯氏制碱的过程中,向饱和的氨化食盐水中通入足量CO2的生产环节又被称为“碳酸化”。碳酸化时产生的现象是_______ 。碳酸化过程中,溶液中c(CO )的变化情况为
)的变化情况为_______ 。
(4)侯氏制碱法析出副产品氯化铵后的溶液中,含有的主要离子有Na+、Cl-、_______ 。检验滤液中Cl-离子的实验操作:_______ 。
(5)侯氏制碱原料中的氨气是用如下反应N2(g)+3H2(g) 2NH3(g)+Q(Q>0)制得,若按n(N2):n(H2)=1:3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。下列说法正确的是
2NH3(g)+Q(Q>0)制得,若按n(N2):n(H2)=1:3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。下列说法正确的是_______ (填字母)。

a.曲线a、b、c对应的温度是由低到高
b.加入催化剂能加快化学反应速率和提高H2的转化率
c.图中Q、M、N点的平衡常数:K(N)>K(Q)=K(M)
d.M点对应H2的转化率为75%
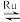 CH4(g)+2H2O(g)+Q(Q>0)
CH4(g)+2H2O(g)+Q(Q>0)(1)该反应的平衡常数表达式为
a.一定增大 b.一定减小 c.可能增大 d.可能减小 e.可能不变
(2)向2L某密闭容器充入1molCO2和4molH2,一定条件下发生上述反应。5min末测得气体的物质的量减少了20%,则0~5min内CO2的平均反应速率为
(3)CO2还可应用于纯碱工业。侯氏制碱的过程中,向饱和的氨化食盐水中通入足量CO2的生产环节又被称为“碳酸化”。碳酸化时产生的现象是
 )的变化情况为
)的变化情况为(4)侯氏制碱法析出副产品氯化铵后的溶液中,含有的主要离子有Na+、Cl-、
(5)侯氏制碱原料中的氨气是用如下反应N2(g)+3H2(g)
 2NH3(g)+Q(Q>0)制得,若按n(N2):n(H2)=1:3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。下列说法正确的是
2NH3(g)+Q(Q>0)制得,若按n(N2):n(H2)=1:3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。下列说法正确的是
a.曲线a、b、c对应的温度是由低到高
b.加入催化剂能加快化学反应速率和提高H2的转化率
c.图中Q、M、N点的平衡常数:K(N)>K(Q)=K(M)
d.M点对应H2的转化率为75%
您最近一年使用:0次
2022高三·全国·专题练习
2 . 捕集CO2的技术对解决全球温室效应意义重大。目前国际空间站处理CO2的一个重要方法是将CO2还原,涉及的化学反应如下:CO2(g)+4H2(g)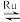 CH4(g)+2H2O(g)+Q(Q>0)
CH4(g)+2H2O(g)+Q(Q>0)
(1)该反应的平衡常数表达式为_______ 。如果改变某种条件,平衡向正反应方向移动,则平衡常数_______ (填写编号)。
a.一定增大 b.一定减小 c.可能增大 d.可能减小 e.可能不变
(2)向2L某密闭容器充入1molCO2和4molH2,一定条件下发生上述反应。5min末测得气体的物质的量减少了20%,则0~5min内CO2的平均反应速率为_______ 。
(3)CO2还可应用于纯碱工业。侯氏制碱的过程中,向饱和的氨化食盐水中通入足量CO2的生产环节又被称为“碳酸化”。碳酸化时产生的现象是_______ 。碳酸化过程中,溶液中c(CO )的变化情况为
)的变化情况为_______ 。
(4)侯氏制碱原料中的氨气是用如下反应N2(g)+3H2(g) 2NH3(g)+Q(Q>0)制得,若按n(N2):n(H2)=1:3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。下列说法正确的是
2NH3(g)+Q(Q>0)制得,若按n(N2):n(H2)=1:3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。下列说法正确的是_______ (填字母)。

a.曲线a、b、c对应的温度是由低到高
b.加入催化剂能加快化学反应速率和提高H2的转化率
c.图中Q、M、N点的平衡常数:K(N)>K(Q)=K(M)
d.M点对应H2的转化率为75%
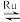 CH4(g)+2H2O(g)+Q(Q>0)
CH4(g)+2H2O(g)+Q(Q>0)(1)该反应的平衡常数表达式为
a.一定增大 b.一定减小 c.可能增大 d.可能减小 e.可能不变
(2)向2L某密闭容器充入1molCO2和4molH2,一定条件下发生上述反应。5min末测得气体的物质的量减少了20%,则0~5min内CO2的平均反应速率为
(3)CO2还可应用于纯碱工业。侯氏制碱的过程中,向饱和的氨化食盐水中通入足量CO2的生产环节又被称为“碳酸化”。碳酸化时产生的现象是
 )的变化情况为
)的变化情况为(4)侯氏制碱原料中的氨气是用如下反应N2(g)+3H2(g)
 2NH3(g)+Q(Q>0)制得,若按n(N2):n(H2)=1:3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。下列说法正确的是
2NH3(g)+Q(Q>0)制得,若按n(N2):n(H2)=1:3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。下列说法正确的是
a.曲线a、b、c对应的温度是由低到高
b.加入催化剂能加快化学反应速率和提高H2的转化率
c.图中Q、M、N点的平衡常数:K(N)>K(Q)=K(M)
d.M点对应H2的转化率为75%
您最近一年使用:0次
解题方法
3 . “绿水青山就是金山银山”,运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)汽车是近代重要的交通运输工具,随着汽车量的激增,汽车尾气造成的环境污染也日益严重。汽车尾气中的有害成分主要有CO、NO、SO2、颗粒物和臭氧等。
①汽车尾气中NO生成过程中的能量变化如图所示。1 mol N2和1 mol O2完全反应生成NO会_______ (填“吸收”或“放出”)_______ kJ能量。
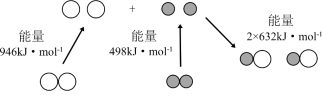
②一种新型催化剂用于NO和CO的反应:NO+2CO2 CO2+N2为了测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表:
CO2+N2为了测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表:
前2 s内的平均反应速率v(N2)=_______ 。(保留小数点后一位)
③在容积固定的绝热容器中发生反应2NO+2CO 2CO2+N2,下列能说明该反应已达到平衡状态的是
2CO2+N2,下列能说明该反应已达到平衡状态的是_______ (填标号)
A.容器内混合气体温度不再变化 B.容器内的气体压强保持不变
C.2v逆(NO)=v正(N2) D.容器内混合气体密度保持不变
(2)煤燃烧排放的烟气中含有SO2和NO2,会形成酸雨,污染大气。
①NaClO2溶液在碱性条件下可对烟气进行脱硫、脱硝,效果非常好。完成下列对烟气脱氮过程的离子方程式:_______
_______ +_______NO+__________=_______Cl-+_______
+_______NO+__________=_______Cl-+_______ +______________。
+______________。
②针对含SO2的工业废气可以采用“钙基固硫法”。例如将生石灰与含硫的煤混合后再燃烧,可以将SO2最终转化为CaSO4,请写出生石灰将SO2转化为CaSO4的反应的化学方程式:_______
③将SO2转化为重要的化工原料H2SO4的原理示意图如图。
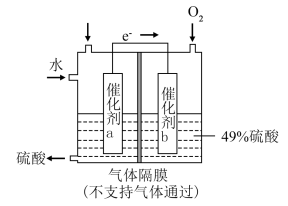
催化剂a表面的电极反应式为_______ 。若得到的硫酸质量分数仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为_______ 。
(1)汽车是近代重要的交通运输工具,随着汽车量的激增,汽车尾气造成的环境污染也日益严重。汽车尾气中的有害成分主要有CO、NO、SO2、颗粒物和臭氧等。
①汽车尾气中NO生成过程中的能量变化如图所示。1 mol N2和1 mol O2完全反应生成NO会

②一种新型催化剂用于NO和CO的反应:NO+2CO2
 CO2+N2为了测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表:
CO2+N2为了测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10-4 mol·L-1) | 10 | 4.5 | 2.5 | 1.5 | 1.0 | 1.0 |
| c(CO)/(10-3 mol·L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
前2 s内的平均反应速率v(N2)=
③在容积固定的绝热容器中发生反应2NO+2CO
 2CO2+N2,下列能说明该反应已达到平衡状态的是
2CO2+N2,下列能说明该反应已达到平衡状态的是A.容器内混合气体温度不再变化 B.容器内的气体压强保持不变
C.2v逆(NO)=v正(N2) D.容器内混合气体密度保持不变
(2)煤燃烧排放的烟气中含有SO2和NO2,会形成酸雨,污染大气。
①NaClO2溶液在碱性条件下可对烟气进行脱硫、脱硝,效果非常好。完成下列对烟气脱氮过程的离子方程式:
_______
 +_______NO+__________=_______Cl-+_______
+_______NO+__________=_______Cl-+_______ +______________。
+______________。②针对含SO2的工业废气可以采用“钙基固硫法”。例如将生石灰与含硫的煤混合后再燃烧,可以将SO2最终转化为CaSO4,请写出生石灰将SO2转化为CaSO4的反应的化学方程式:
③将SO2转化为重要的化工原料H2SO4的原理示意图如图。

催化剂a表面的电极反应式为
您最近一年使用:0次
名校
解题方法
4 . “绿水青山就是金山银山”,运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)汽车是近代重要的交通运输工具,随着汽车量的激增,汽车尾气造成的环境污染也日益严重,汽车尾气中的有害成分主要有CO、NO、SO2、颗粒物和臭氧等。
①汽车尾气中NO生成过程中的能量变化如图所示,1molN2和1molO2完全反应生成NO会_____ (填“吸收”或“放出”)_____ kJ能量。
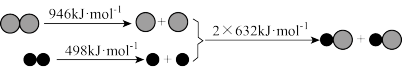
②一种新型催化剂用于汽车尾气NO和CO的反应:2NO+2CO 2CO2+N2,为测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2,为测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
前2s内的平均反应速率v(N2)=____ 。为了进一步提高尾气处理的效率,缩短达到化学反应平衡所需要的时间,你认为还可以尝试哪些方法:_____ (写出一种即可)。
③在容积固定的绝热容器中发生反应2NO+2CO 2CO2+N2,下列能说明该反应已达到平衡状态的是
2CO2+N2,下列能说明该反应已达到平衡状态的是_____ (填标号)。
A.容器内混合气体温度不再变化 B.容器内的气体压强保持不变
C.2v逆(NO)=v正(N2) D.容器内混合气体密度保持不变
(2)煤燃烧排放的烟气中含有SO2和NO2,会污染大气,形成酸雨。
①针对含SO2的工业废气可以采用“钙基固硫法”。例如将生石灰与含硫的煤混合后再燃烧,可以将SO2最终转化为CaSO4,请写出生石灰将SO2转化为CaSO4的反应的化学方程式:_____ 。
②将SO2转化为重要的化工原料H2SO4的原理示意图如图,催化剂a表面的电极反应式为_____ 。若得到的硫酸质量分数仍为49%,则理论上参加反应的SO2与加入的H2O的物质的量之比为_____ 。

(1)汽车是近代重要的交通运输工具,随着汽车量的激增,汽车尾气造成的环境污染也日益严重,汽车尾气中的有害成分主要有CO、NO、SO2、颗粒物和臭氧等。
①汽车尾气中NO生成过程中的能量变化如图所示,1molN2和1molO2完全反应生成NO会
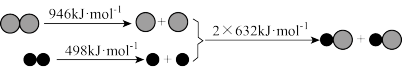
②一种新型催化剂用于汽车尾气NO和CO的反应:2NO+2CO
 2CO2+N2,为测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2,为测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(×10-4mol·L-1) | 10 | 4.5 | 2.5 | 1.5 | 1.0 | 1.0 |
| c(CO)/(×10-3mol·L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
前2s内的平均反应速率v(N2)=
③在容积固定的绝热容器中发生反应2NO+2CO
 2CO2+N2,下列能说明该反应已达到平衡状态的是
2CO2+N2,下列能说明该反应已达到平衡状态的是A.容器内混合气体温度不再变化 B.容器内的气体压强保持不变
C.2v逆(NO)=v正(N2) D.容器内混合气体密度保持不变
(2)煤燃烧排放的烟气中含有SO2和NO2,会污染大气,形成酸雨。
①针对含SO2的工业废气可以采用“钙基固硫法”。例如将生石灰与含硫的煤混合后再燃烧,可以将SO2最终转化为CaSO4,请写出生石灰将SO2转化为CaSO4的反应的化学方程式:
②将SO2转化为重要的化工原料H2SO4的原理示意图如图,催化剂a表面的电极反应式为

您最近一年使用:0次
5 . 在一定温度下,将2mol A和2molB 两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(气)+B(气)⇌xC(气)+2D(气),2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于_______ ;
(2)B的平衡浓度为_______ ;
(3)A的转化率为_______ ;
(4)生成D的反应速率为_______ ;
(5)如果增大反应体系的压强,则平衡体系中C的质量分数_______ (填增大、减小或不变);
(6)该温度下的平衡常数为_______ ;如果上述反应在相同条件下从逆反应开始进行,开始加入C和D各4/3mol,要使平衡时各物质的质量分数与原平衡时完全相等,则还应加入_______ 物质_______ mol。
(1)x值等于
(2)B的平衡浓度为
(3)A的转化率为
(4)生成D的反应速率为
(5)如果增大反应体系的压强,则平衡体系中C的质量分数
(6)该温度下的平衡常数为
您最近一年使用:0次
2022-08-22更新
|
39次组卷
|
2卷引用:宁夏吴忠市吴忠中学2021-2022学年高二上学期月考化学试题
解题方法
6 . 填空。
(1)一定温度下,在1 L密闭容器内进行某化学反应,气体X、Y的物质的量随反应时间变化的曲线如图所示
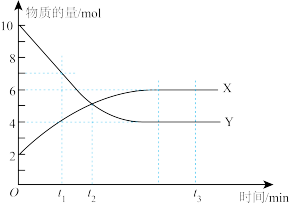
①写出该反应的化学方程式:_______
②在t1、t2和t3三个时刻中,反应程度最大的是_______ (填“t1”“t2”或“t3”)。
③平衡时X的体积分数为:_______
(2)一定温度下,将一定量的 和
和 充入固定容积催化剂的密闭容器中进行反应:
充入固定容积催化剂的密闭容器中进行反应: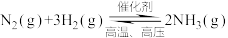 。
。
①下列描述能说明该可逆反应达到化学平衡状态的有_______ (填序号)。
A.容器内的压强不变 B.容器内气体的密度不变
C. D.
D. 的质量分数不再改变
的质量分数不再改变
E.相同时间内有3 mol H-H键断裂,有6 mol N-H键形成
②若起始时向容器中充入 的
的 和
和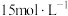 的
的 ,10 min时测得容器内
,10 min时测得容器内 的浓度为
的浓度为 。10 min内用
。10 min内用 表示的反应速率为
表示的反应速率为_______ ;此时 的转化率为
的转化率为_______ 。
(1)一定温度下,在1 L密闭容器内进行某化学反应,气体X、Y的物质的量随反应时间变化的曲线如图所示

①写出该反应的化学方程式:
②在t1、t2和t3三个时刻中,反应程度最大的是
③平衡时X的体积分数为:
(2)一定温度下,将一定量的
 和
和 充入固定容积催化剂的密闭容器中进行反应:
充入固定容积催化剂的密闭容器中进行反应: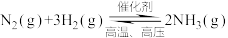 。
。①下列描述能说明该可逆反应达到化学平衡状态的有
A.容器内的压强不变 B.容器内气体的密度不变
C.
 D.
D. 的质量分数不再改变
的质量分数不再改变E.相同时间内有3 mol H-H键断裂,有6 mol N-H键形成
②若起始时向容器中充入
 的
的 和
和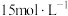 的
的 ,10 min时测得容器内
,10 min时测得容器内 的浓度为
的浓度为 。10 min内用
。10 min内用 表示的反应速率为
表示的反应速率为 的转化率为
的转化率为
您最近一年使用:0次
2022-08-15更新
|
208次组卷
|
2卷引用:吉林省通化市部分重点中学校2021-2022学年高一下学期期末联考化学试题
解题方法
7 . Ⅰ、
(1)已知:
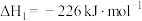
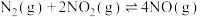

则CO与NO反应生成 气体和
气体和 气体的热化学方程式为
气体的热化学方程式为___________ 。
Ⅱ、一定温度下,在体积为2L的密闭容器中,充入1mol 和3mol
和3mol 发生如下反应:
发生如下反应: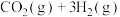
 。经测得
。经测得 和
和 (g)的物质的量随时间变化如图所示。
(g)的物质的量随时间变化如图所示。
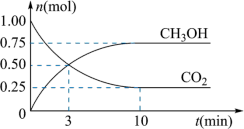
(2)从反应开始到平衡,需要的时间___________ ,在这段时间内, 的平均反应速率
的平均反应速率
___________ 。
(3)达到平衡时, 的转化率为
的转化率为___________ (用百分数表示);此温度下该反应的平衡常数K=___________ (可用分数表示)。
(4)下列措施不能提高反应速率的是___________。
(5)下列叙述中不能说明上述反应达到平衡状态的是___________ 。
A.混合气体的平均相对分子质量保持不变
B.混合气体的压强不随时间的变化而变化
C. 在混合气体中的质量分数保持不变
在混合气体中的质量分数保持不变
D.反应中 与
与 的物质的量之比为1∶1
的物质的量之比为1∶1
E.单位时间内每消耗1mol 同时生成1mo
同时生成1mo
(1)已知:

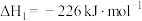
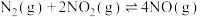

则CO与NO反应生成
 气体和
气体和 气体的热化学方程式为
气体的热化学方程式为Ⅱ、一定温度下,在体积为2L的密闭容器中,充入1mol
 和3mol
和3mol 发生如下反应:
发生如下反应: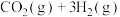
 。经测得
。经测得 和
和 (g)的物质的量随时间变化如图所示。
(g)的物质的量随时间变化如图所示。
(2)从反应开始到平衡,需要的时间
 的平均反应速率
的平均反应速率
(3)达到平衡时,
 的转化率为
的转化率为(4)下列措施不能提高反应速率的是___________。
| A.升高温度 | B.加入适当催化剂 |
| C.缩小体积,增大压强 | D.恒温、恒压下通入氦气 |
A.混合气体的平均相对分子质量保持不变
B.混合气体的压强不随时间的变化而变化
C.
 在混合气体中的质量分数保持不变
在混合气体中的质量分数保持不变D.反应中
 与
与 的物质的量之比为1∶1
的物质的量之比为1∶1E.单位时间内每消耗1mol
 同时生成1mo
同时生成1mo
您最近一年使用:0次
名校
解题方法
8 . “绿水青山就是金山银山”,运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)汽车是近代重要的交通运输工具,随着汽车量的激增,汽车尾气造成的环境污染也日益严重,汽车尾气中的有害成分主要有 、
、 、
、 、颗粒物和臭氧等。
、颗粒物和臭氧等。
①汽车尾气中 生成过程中的能量变化如图所示,1mol
生成过程中的能量变化如图所示,1mol 和1mol
和1mol 完全反应生成
完全反应生成 会
会_______ (填“吸收”或“放出”)_______ kJ能量。

②一种新型催化剂用于 和
和 的反应:
的反应: ,为测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的
,为测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的 和
和 浓度如下表:
浓度如下表:
前2s内的平均反应速率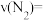
_______ 。
③在容积固定的绝热容器中发生反应 ,下列能说明该反应已达到平衡状态的是
,下列能说明该反应已达到平衡状态的是_______ (填标号)。
A.容器内混合气体温度不再变化 B.容器内的气体压强保持不变
C.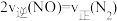 D.容器内混合气体密度保持不变
D.容器内混合气体密度保持不变
(2)煤燃烧排放的烟气中含有 和
和 ,会污染大气,形成酸雨。
,会污染大气,形成酸雨。
①针对含 的工业废气可以采用“钙基固硫法”。例如将生石灰与含硫的煤混合后再燃烧,可以将
的工业废气可以采用“钙基固硫法”。例如将生石灰与含硫的煤混合后再燃烧,可以将 最终转化为
最终转化为 ,请写出生石灰将
,请写出生石灰将 转化为
转化为 的反应的化学方程式:
的反应的化学方程式:_______ 。
②将 转化为重要的化工原料
转化为重要的化工原料 的原理示意图如图。催化剂a表面的电极反应式为
的原理示意图如图。催化剂a表面的电极反应式为_______ 。若得到的硫酸质量分数仍为49%,则理论上参加反应的 与加入的
与加入的 的物质的量之比为
的物质的量之比为_______ 。

(1)汽车是近代重要的交通运输工具,随着汽车量的激增,汽车尾气造成的环境污染也日益严重,汽车尾气中的有害成分主要有
 、
、 、
、 、颗粒物和臭氧等。
、颗粒物和臭氧等。①汽车尾气中
 生成过程中的能量变化如图所示,1mol
生成过程中的能量变化如图所示,1mol 和1mol
和1mol 完全反应生成
完全反应生成 会
会
②一种新型催化剂用于
 和
和 的反应:
的反应: ,为测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的
,为测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的 和
和 浓度如下表:
浓度如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
 | 10 | 4.5 | 2.5 | 1.5 | 1.0 | 1.0 |
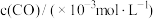 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
前2s内的平均反应速率
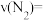
③在容积固定的绝热容器中发生反应
 ,下列能说明该反应已达到平衡状态的是
,下列能说明该反应已达到平衡状态的是A.容器内混合气体温度不再变化 B.容器内的气体压强保持不变
C.
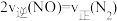 D.容器内混合气体密度保持不变
D.容器内混合气体密度保持不变(2)煤燃烧排放的烟气中含有
 和
和 ,会污染大气,形成酸雨。
,会污染大气,形成酸雨。①针对含
 的工业废气可以采用“钙基固硫法”。例如将生石灰与含硫的煤混合后再燃烧,可以将
的工业废气可以采用“钙基固硫法”。例如将生石灰与含硫的煤混合后再燃烧,可以将 最终转化为
最终转化为 ,请写出生石灰将
,请写出生石灰将 转化为
转化为 的反应的化学方程式:
的反应的化学方程式:②将
 转化为重要的化工原料
转化为重要的化工原料 的原理示意图如图。催化剂a表面的电极反应式为
的原理示意图如图。催化剂a表面的电极反应式为 与加入的
与加入的 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
9 . 合成氨是人类科学技术发展史上的一项重大成就。实验室利用如右图所示装置及药品制取氨气:_____________ 。
(2)下列装置中,可用于收集氨的是_________ (填标号)。______________ 。
(4)在一定条件下,将2molN2和6molH2在体积恒为5L的密闭容器中混合,发生如下反应:N2(g)+3H2(g) 2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:
2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:
①2min内该反应的平均反应速率v(N2)=______ mol/(L·min)
②一段时间后反应达到平衡,密闭容器中混合气体的压强比反应前减少了25%,计算此时容器中NH3的浓度为____________ mol/L。
③能说明该反应已经达到平衡状态的是____________ 。
a.气体的密度保持不变 b.NH3的含量保持不变
c.N2和H2的物质的量之比为1:3 d.N2的转化率不再发生改变
(5)工业上通常用氨转化法处理含NO、NO2等氮氧化物的尾气:已知8 mol氨恰好能将含NO和NO2共7mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为_____ 。
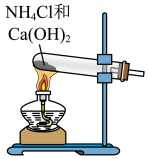
(2)下列装置中,可用于收集氨的是
a. 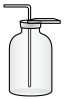 b.
b. 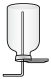 c.
c. 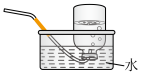
(4)在一定条件下,将2molN2和6molH2在体积恒为5L的密闭容器中混合,发生如下反应:N2(g)+3H2(g)
 2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:
2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:①2min内该反应的平均反应速率v(N2)=
②一段时间后反应达到平衡,密闭容器中混合气体的压强比反应前减少了25%,计算此时容器中NH3的浓度为
③能说明该反应已经达到平衡状态的是
a.气体的密度保持不变 b.NH3的含量保持不变
c.N2和H2的物质的量之比为1:3 d.N2的转化率不再发生改变
(5)工业上通常用氨转化法处理含NO、NO2等氮氧化物的尾气:已知8 mol氨恰好能将含NO和NO2共7mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
您最近一年使用:0次
10 . 将CO或CO2转化为高附加值化学品是颇具前景的合成路线。
(1)工业上用CO2和H2反应合成二甲醚。
已知:
 ;
;

 。
。
写出 和
和 转化为
转化为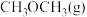 和
和 的热化学方程式:
的热化学方程式:_______________ ,该反应在________ (填“高温”或“低温”)条件下能自发进行。
(2)CO2催化加氢合成乙醇的反应原理为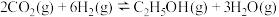
 ,设m为起始时的投料比,即
,设m为起始时的投料比,即 。
。________________ 。
②图1右图表示在总压为5MPa的恒压条件下,且m=3时,平衡状态下各物质的物质的量分数与温度的关系,则曲线d代表的物质为________ (填化学式)。
(3)一种利用焦炉气中的H2和工业废气捕获的CO2生产绿色燃料甲醇的原理为 、
、 。
。
在研究该反应历程时发现,反应气中水蒸气含量会影响CH3OH的产率。为了研究水分子对该反应机制的内在影响,科学家利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响,如图3所示(吸附在催化剂表面上的物种用*标注)。________________ 。
②资料显示:水也可以使催化剂活化点位减少。结合资料、上图及学过的知识推测,在反应气中添加水蒸气将如何影响甲醇产率及产生这种影响的原因:________________ (任答两点)。
(4)一定条件下,利用CO2和H2还可制得甲烷: ,主要副反应为
,主要副反应为 。一定温度下,向恒容密闭容器中充入CO2和H2(物质的量之比为1:4)发生反应,容器内气体的压强随时间的变化如表所示:
。一定温度下,向恒容密闭容器中充入CO2和H2(物质的量之比为1:4)发生反应,容器内气体的压强随时间的变化如表所示:
①用单位时间内气体分压的变化表示反应 的速率,则前120min内CH4的平均反应速率
的速率,则前120min内CH4的平均反应速率
________ 。
②该温度下,平衡时CO的体积分数为8%,反应 的平衡常数
的平衡常数
________ ( 为以分压表示的平衡常数,保留小数点后2位)。
为以分压表示的平衡常数,保留小数点后2位)。
(1)工业上用CO2和H2反应合成二甲醚。
已知:

 ;
;
 。
。写出
 和
和 转化为
转化为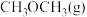 和
和 的热化学方程式:
的热化学方程式:(2)CO2催化加氢合成乙醇的反应原理为
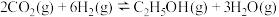
 ,设m为起始时的投料比,即
,设m为起始时的投料比,即 。
。
②图1右图表示在总压为5MPa的恒压条件下,且m=3时,平衡状态下各物质的物质的量分数与温度的关系,则曲线d代表的物质为
(3)一种利用焦炉气中的H2和工业废气捕获的CO2生产绿色燃料甲醇的原理为
 、
、 。
。在研究该反应历程时发现,反应气中水蒸气含量会影响CH3OH的产率。为了研究水分子对该反应机制的内在影响,科学家利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响,如图3所示(吸附在催化剂表面上的物种用*标注)。

②资料显示:水也可以使催化剂活化点位减少。结合资料、上图及学过的知识推测,在反应气中添加水蒸气将如何影响甲醇产率及产生这种影响的原因:
(4)一定条件下,利用CO2和H2还可制得甲烷:
 ,主要副反应为
,主要副反应为 。一定温度下,向恒容密闭容器中充入CO2和H2(物质的量之比为1:4)发生反应,容器内气体的压强随时间的变化如表所示:
。一定温度下,向恒容密闭容器中充入CO2和H2(物质的量之比为1:4)发生反应,容器内气体的压强随时间的变化如表所示:时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
压强/kPa | 100 | 93.8 | 88.0 | 83.4 | 79.4 | 75.0 | 75.0 |
 的速率,则前120min内CH4的平均反应速率
的速率,则前120min内CH4的平均反应速率
②该温度下,平衡时CO的体积分数为8%,反应
 的平衡常数
的平衡常数
 为以分压表示的平衡常数,保留小数点后2位)。
为以分压表示的平衡常数,保留小数点后2位)。
您最近一年使用:0次



