1 . 2molSO2和1molO2在一定条件反应:2SO2(g)+O2(g)⇌2SO3(g)△H<0。若恒温恒容条件下SO2的转化率为a%;恒温恒压条件下SO2的转化率为b%;恒容绝热条件下SO2的转化率为c%;则它们之间的关系是
| A.a% > b%> c% | B.b%> a% >c% | C.a% >c% > b% | D.b%> c% >a% |
您最近一年使用:0次
名校
2 . 在一定温度下的密闭容器中发生反应: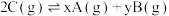 ,平衡时测得A的浓度为0.50mol/L。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30mol/L。下列有关判断不正确的是
,平衡时测得A的浓度为0.50mol/L。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30mol/L。下列有关判断不正确的是
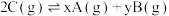 ,平衡时测得A的浓度为0.50mol/L。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30mol/L。下列有关判断不正确的是
,平衡时测得A的浓度为0.50mol/L。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30mol/L。下列有关判断不正确的是A.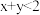 | B.平衡向正反应方向移动 |
| C.C的转化率增大 | D.B的体积分数增大 |
您最近一年使用:0次
2022-10-29更新
|
283次组卷
|
3卷引用:广东省江门市蓬江区棠下中学2022-2023学年高二上学期第一次月考化学试题
3 . 相同温度下,体积相等的两个恒容密闭容器中发生如下反应:N2(g)+3H2(g)  2NH3(g) ΔH=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表所示:
2NH3(g) ΔH=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表所示:
下列叙述错误的是
 2NH3(g) ΔH=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表所示:
2NH3(g) ΔH=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表所示:| 容器编号 | 起始时各物质物质的量/mol | 到达平衡时能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:27.78 kJ |
| ② | 0 | 0 | 2 | 吸收热量:Q kJ |
| A.平衡时,容器①中N2的转化率为30% |
| B.平衡后,向容器②再充入N2,氨气的体积分数一定增大 |
| C.容器①达到平衡时,混合气体的密度是同温同压下H2密度的5倍 |
| D.Q = 64.82 |
您最近一年使用:0次
4 . 推进能源绿色转型,实现碳达峰、碳中和,事关经济社会发展全局。CO2甲烷化及甲烷重整制甲醇是能源综合利用领域的研究热点。回答下列问题:
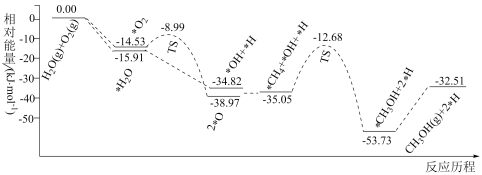
(1)已知CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面可合成甲醇:CH4(g)+ O2(g)=CH3OH(g) △H,反应的部分历程如图所示(吸附在催化剂表面的物种用“*”标注,TS代表过渡态)。下列说法正确的是
O2(g)=CH3OH(g) △H,反应的部分历程如图所示(吸附在催化剂表面的物种用“*”标注,TS代表过渡态)。下列说法正确的是_____ (填标号)。
(2)催化剂的选择是CO2甲烷化的核心,金属Ni或Ni-CeO2均可作为催化剂。
①基态Ni原子的核外电子排布式为_____ 。
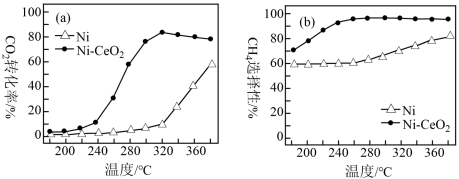
②在上述两种催化剂的条件下反应相同时间,测得CO2转化率和CH4选择性随温度的变化如图所示。高于320℃,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是____ 。对比上述两种催化剂的催化性能,工业上应选择的催化剂和温度分别是____ 。
(3)一定条件下,发生反应CO(g)+3H2(g) CH4(g)+H2O(g) △H=-198kJ•mol-1,测CO的平衡转化率与温度、起始投料比m[m=
CH4(g)+H2O(g) △H=-198kJ•mol-1,测CO的平衡转化率与温度、起始投料比m[m=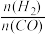 ]的关系如图所示。已知v正=k正•c(CO)•c3(H2),v逆=k逆•c(CH4)•c(H2O) (k正、k逆为速率常数,只与温度有关)。
]的关系如图所示。已知v正=k正•c(CO)•c3(H2),v逆=k逆•c(CH4)•c(H2O) (k正、k逆为速率常数,只与温度有关)。

①图中m1、m2、m3由大到小的顺序为_____ 。
②向一体积为2L的恒容密闭容器中充入1molCO和3molH2,在一定温度下,经5s达到平衡,此时CO的转化率为50%。0~5s内,v(H2)=____ mol•L-1•s-1。平衡时k正:k逆=____ ,达到平衡后,升高温度,k正:k逆_____ (填“增大”、“减小”或“不变”)。
(4)微生物电化学产甲烷法的装置如图所示。b电极的电极反应式为____ 。

(1)已知CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面可合成甲醇:CH4(g)+
 O2(g)=CH3OH(g) △H,反应的部分历程如图所示(吸附在催化剂表面的物种用“*”标注,TS代表过渡态)。下列说法正确的是
O2(g)=CH3OH(g) △H,反应的部分历程如图所示(吸附在催化剂表面的物种用“*”标注,TS代表过渡态)。下列说法正确的是
| A.该反应的△H=-32.5kJ•mol-1 |
| B.H2O(g)比O2(g)更容易吸附在催化剂表面 |
| C.该反应过程中只涉及σ键的断裂与形成 |
| D.图中慢反应的化学方程式为*CH4+*OH=*CH3OH+*H |
①基态Ni原子的核外电子排布式为
②在上述两种催化剂的条件下反应相同时间,测得CO2转化率和CH4选择性随温度的变化如图所示。高于320℃,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是

(3)一定条件下,发生反应CO(g)+3H2(g)
 CH4(g)+H2O(g) △H=-198kJ•mol-1,测CO的平衡转化率与温度、起始投料比m[m=
CH4(g)+H2O(g) △H=-198kJ•mol-1,测CO的平衡转化率与温度、起始投料比m[m=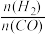 ]的关系如图所示。已知v正=k正•c(CO)•c3(H2),v逆=k逆•c(CH4)•c(H2O) (k正、k逆为速率常数,只与温度有关)。
]的关系如图所示。已知v正=k正•c(CO)•c3(H2),v逆=k逆•c(CH4)•c(H2O) (k正、k逆为速率常数,只与温度有关)。
①图中m1、m2、m3由大到小的顺序为
②向一体积为2L的恒容密闭容器中充入1molCO和3molH2,在一定温度下,经5s达到平衡,此时CO的转化率为50%。0~5s内,v(H2)=
(4)微生物电化学产甲烷法的装置如图所示。b电极的电极反应式为

您最近一年使用:0次
名校
5 . 在双碳目标驱动下,大批量氢燃料客车在2022年北京冬奥会上投入使用。氢源的获取和利用成为科学研究热点。回答下列问题:
Ⅰ.氢源的获取:电解液氨制氢
氨分子中具有较高的含氢量,因此是制氢的优选原料。现以液氨为原料,使用 非水电解质电解制氢。(已知:电解过程中电解液内含氮微粒只有
非水电解质电解制氢。(已知:电解过程中电解液内含氮微粒只有 、
、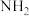 和
和 )
)
(1)产生 的电极反应式为
的电极反应式为______ 。
Ⅱ.氢源的利用: 还原
还原 制甲醇
制甲醇
(2)800℃时, 还原
还原 反应的热化学方程式及其平衡常数如下:
反应的热化学方程式及其平衡常数如下:
反应1:
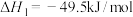

反应2: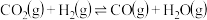

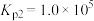
反应3: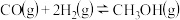

______ 
(3)800℃时,正反应进行的程度“反应2”______ “反应1”(选填“>”或“<”),判断依据是______ 。
(4)反应1在一定条件下建立平衡,关于反应1的相关描述正确的是______。
(5)某温度下,向2L恒容密闭容器中充入0.5mol 和0.9mol
和0.9mol 发生反应1和反应2,经过5min达到平衡状态,反应过程中
发生反应1和反应2,经过5min达到平衡状态,反应过程中 和
和 的物质的量随时间变化情况如下图所示:
的物质的量随时间变化情况如下图所示:
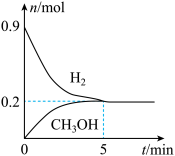
平衡时, 的转化率为
的转化率为______ ,该温度下,反应2的化学平衡常数
______ 。
(6) 用途广泛,写出基于其物理性质的一种用途:
用途广泛,写出基于其物理性质的一种用途:______ 。
Ⅰ.氢源的获取:电解液氨制氢
氨分子中具有较高的含氢量,因此是制氢的优选原料。现以液氨为原料,使用
 非水电解质电解制氢。(已知:电解过程中电解液内含氮微粒只有
非水电解质电解制氢。(已知:电解过程中电解液内含氮微粒只有 、
、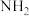 和
和 )
)(1)产生
 的电极反应式为
的电极反应式为Ⅱ.氢源的利用:
 还原
还原 制甲醇
制甲醇(2)800℃时,
 还原
还原 反应的热化学方程式及其平衡常数如下:
反应的热化学方程式及其平衡常数如下:反应1:

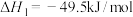

反应2:
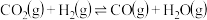

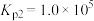
反应3:
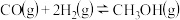


(3)800℃时,正反应进行的程度“反应2”
(4)反应1在一定条件下建立平衡,关于反应1的相关描述正确的是______。
| A.使用高效催化剂可降低反应的活化能,增大活化分子百分数,加快化学反应速率 |
| B.该反应的反应物总能量小于生成物总能量 |
| C.容器内气体的平均相对分子质量不再改变说明反应达到了平衡 |
D.增大压强,反应1的化学平衡常数 变小 变小 |
 和0.9mol
和0.9mol 发生反应1和反应2,经过5min达到平衡状态,反应过程中
发生反应1和反应2,经过5min达到平衡状态,反应过程中 和
和 的物质的量随时间变化情况如下图所示:
的物质的量随时间变化情况如下图所示:
平衡时,
 的转化率为
的转化率为
(6)
 用途广泛,写出基于其物理性质的一种用途:
用途广泛,写出基于其物理性质的一种用途:
您最近一年使用:0次
名校
6 . 在容积为2 L的恒容密闭容器中充入P(g)和Q(g),发生反应P(g)+2Q(g)⇌3R(g)+4S(s) ΔH。所得数据如下表:
下列说法正确的是
| 组号 | 温度/℃ | 起始量/mol | 平衡量/mol | ||
| n(P) | n(Q) | n(R) | n(S) | ||
| ① | 500 | 0.10 | 0.80 | 0.24 | 0.32 |
| ② | 500 | 0.20 | 1.60 | x | 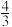 x x |
| ③ | 700 | 0.10 | 0.30 | 0.18 | 0.24 |
| A.该反应的ΔH>0 | B.反应达到平衡后增大压强,平衡逆向移动 |
| C.②中反应的平衡常数K=6.0 | D.根据题目信息不能确定x的值 |
您最近一年使用:0次
2022-09-24更新
|
529次组卷
|
3卷引用:山东省威海乳山市银滩高级中学2022-2023学年高二9月月考化学试题
名校
7 . 如图所示,三个烧瓶中分别充满NO2气体并分别装在盛有水的三个烧杯中,在①烧杯中加入CaO,在②烧杯中不加其他任何物质,在③烧杯中加入NH4Cl晶体,发现①中红棕色变深,③中红棕色变浅。已知:2NO2(红棕色) N2O4(无色),下列叙述正确的是
N2O4(无色),下列叙述正确的是
 N2O4(无色),下列叙述正确的是
N2O4(无色),下列叙述正确的是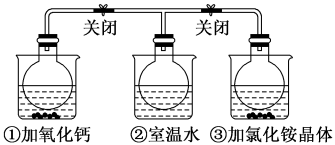
A.2NO2 N2O4是吸热反应 N2O4是吸热反应 |
| B.NH4Cl溶于水时吸收热量 |
| C.①烧瓶中平衡时混合气体的平均相对分子质量增大 |
| D.③烧瓶中气体的压强增大 |
您最近一年使用:0次
2022-08-28更新
|
1133次组卷
|
23卷引用:新疆生产建设兵团第二中学2017-2018学年高二上学期第四次月考(期末)化学试题
新疆生产建设兵团第二中学2017-2018学年高二上学期第四次月考(期末)化学试题新疆自治区生产建设兵团第二中学2018-2019学年高二第一次月考化学试题四川省泸州市泸县第二中学2019-2020学年高二下学期第一次在线月考化学试题黑龙江省大庆市第四中学2019-2020学年高二上学期第一次检测化学试题安徽省蚌埠田家炳中学2020-2021学年高二10月月考化学试题福建省三明第一中学2021-2022学年高二上学期第一次月考化学试题福建省莆田市擢英中学2021-2022学年高二上学期第一次月考化学试卷(已下线)2010年北京市八一中学高二第二学期期末考试化学试卷2018版化学(苏教版)高考总复习专题七课时跟踪训练--化学平衡的移动【全国百强校】辽宁省鞍山市第一中学2018-2019学年高二下学期开学考试化学试题陕西省延安市第一中学2019-2020学年高二上学期期中考试化学试题(已下线)专题7.2 化学平衡状态 化学平衡移动(练)-《2020年高考一轮复习讲练测》云南省普洱市江城县第一中学2019—2020学年高二上学期期末考试化学试题(已下线)2.3.2+影响化学平衡状态的因素-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)江西省上饶市2020-2021学年高二上学期期末教学质量测试化学试题江西省赣州市第一中学2020-2021学年高二下学期开学测试化学试题河南省信阳高级中学2020-2021学年高二下学期回顾测试化学试题(已下线)2.2.2 浓度商、温度对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期中考试化学试题广东省深圳市宝安区宝安中学2022-2023学年高一上学期期中考试化学试题新疆奇台县第一中学2022-2023学年高二上学期期中考试化学试题山东省淄博市部分学校联考2022-2023学年高一下学期4月期中考试化学试题(已下线)选择题11-15
名校
8 . 在恒温恒压下,向密闭容器中充入4molSO2和2molO2,发生如下反应:2SO2(g)+O2(g)  2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ。则下列分析正确的是
2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ。则下列分析正确的是
 2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ。则下列分析正确的是
2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ。则下列分析正确的是| A.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于QkJ |
| B.2min后,向容器中再通入一定量的SO3气体,重新达到平衡时,SO2的含量变小 |
| C.若把条件“恒温恒压”改为“恒压绝热”,则平衡后n(SO3)大于1.4mol |
| D.若反应开始时容器体积为2L,则v(SO3)=0.7mol·L-1·min-1 |
您最近一年使用:0次
2022-08-24更新
|
1015次组卷
|
3卷引用:浙江省舟山市舟山中学2021-2022学年高一下学期阶段性检测化学试题
名校
解题方法
9 . 以CO和CO2为原料合成乙烯、二甲醚(CH3OCH3)等有机物,一直是当前化学领域研究的热点。回答下列问题:
(1)已知相关物质能量变化示意图如下:
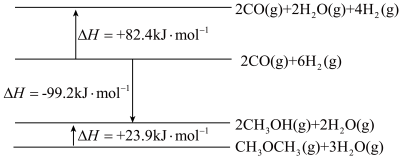
①写出由CO(g)和H2(g)反应生成CH3OCH3(g)和H2O(g)的热化学方程式:_______ 。
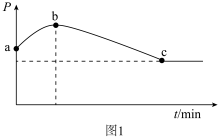
②在一绝热的恒容密闭容器中,通入CO和H2(物质的量之比1 :2)发生反应2CO(g)+4H2(g) C2H4(g) +2H2O(g) ΔH<0,反应过程中容器内压强(p)与时间(t)变化如图1所示,随着反应进行,a~b段压强增大的原因是
C2H4(g) +2H2O(g) ΔH<0,反应过程中容器内压强(p)与时间(t)变化如图1所示,随着反应进行,a~b段压强增大的原因是_______ 。
③CO2与H2催化重整制备CH3OCH3的过程中存在反应:
Ⅰ.2CO2(g) + 6H2(g) CH3OCH3(g)+3H2O(g);
CH3OCH3(g)+3H2O(g);
Ⅱ.CO2(g) +H2(g) CO(g) + H2O(g)。
CO(g) + H2O(g)。
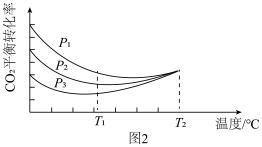
向密闭容器中以物质的量之比为1:3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图2所示。p1、p2、p3由大小的顺序为_______ ;T2℃时主要发生反应_______ (填“Ⅰ”或“Ⅱ”),平衡转化率随温度变化先降后升的原因为_______ 。
(2)一定温度和压强为3. 3p MPa条件下,将CO和H2按物质的量之比为2: 3通入密闭弹性容器中发生催化反应,假设只发生反应:3CO(g) + 3H2 (g) CH3OCH3(g)+CO2(g) 、2CO(g) + 4H2(g)
CH3OCH3(g)+CO2(g) 、2CO(g) + 4H2(g)  C2H4(g) + 2H2O(g)。平衡时,CO平衡转化率为60%,C2H4选择性为50%(C2H4的选择性=
C2H4(g) + 2H2O(g)。平衡时,CO平衡转化率为60%,C2H4选择性为50%(C2H4的选择性=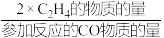 )。该温度下。反应C2H4(g)+ 2H2O(g)
)。该温度下。反应C2H4(g)+ 2H2O(g)  2CO(g) +4H2(g)的Kp=
2CO(g) +4H2(g)的Kp=_______ MPa3(用含字母p的代数式表示,已知Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替),若要提高C2H4的选择性,则应考虑的因素是_______ 。
(1)已知相关物质能量变化示意图如下:

①写出由CO(g)和H2(g)反应生成CH3OCH3(g)和H2O(g)的热化学方程式:
②在一绝热的恒容密闭容器中,通入CO和H2(物质的量之比1 :2)发生反应2CO(g)+4H2(g)
 C2H4(g) +2H2O(g) ΔH<0,反应过程中容器内压强(p)与时间(t)变化如图1所示,随着反应进行,a~b段压强增大的原因是
C2H4(g) +2H2O(g) ΔH<0,反应过程中容器内压强(p)与时间(t)变化如图1所示,随着反应进行,a~b段压强增大的原因是
③CO2与H2催化重整制备CH3OCH3的过程中存在反应:
Ⅰ.2CO2(g) + 6H2(g)
 CH3OCH3(g)+3H2O(g);
CH3OCH3(g)+3H2O(g);Ⅱ.CO2(g) +H2(g)
 CO(g) + H2O(g)。
CO(g) + H2O(g)。向密闭容器中以物质的量之比为1:3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图2所示。p1、p2、p3由大小的顺序为

(2)一定温度和压强为3. 3p MPa条件下,将CO和H2按物质的量之比为2: 3通入密闭弹性容器中发生催化反应,假设只发生反应:3CO(g) + 3H2 (g)
 CH3OCH3(g)+CO2(g) 、2CO(g) + 4H2(g)
CH3OCH3(g)+CO2(g) 、2CO(g) + 4H2(g)  C2H4(g) + 2H2O(g)。平衡时,CO平衡转化率为60%,C2H4选择性为50%(C2H4的选择性=
C2H4(g) + 2H2O(g)。平衡时,CO平衡转化率为60%,C2H4选择性为50%(C2H4的选择性=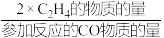 )。该温度下。反应C2H4(g)+ 2H2O(g)
)。该温度下。反应C2H4(g)+ 2H2O(g)  2CO(g) +4H2(g)的Kp=
2CO(g) +4H2(g)的Kp=
您最近一年使用:0次
2022-07-29更新
|
289次组卷
|
3卷引用:辽宁省朝阳市凌源市实验中学2022-2023学年高二上学期12月月考化学试题
名校
解题方法
10 . 工业上利用硫(S8)与 为原料制备
为原料制备 。450℃以上,发生反应Ⅰ:
。450℃以上,发生反应Ⅰ: ;通常在600℃以上发生反应Ⅱ:
;通常在600℃以上发生反应Ⅱ: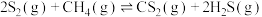 。一定条件下,
。一定条件下, 分解产生
分解产生 的体积分数、
的体积分数、 与
与 反应中
反应中 的平衡转化率与温度的关系如图所示。下列说法一定正确的是
的平衡转化率与温度的关系如图所示。下列说法一定正确的是

 为原料制备
为原料制备 。450℃以上,发生反应Ⅰ:
。450℃以上,发生反应Ⅰ: ;通常在600℃以上发生反应Ⅱ:
;通常在600℃以上发生反应Ⅱ: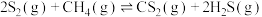 。一定条件下,
。一定条件下, 分解产生
分解产生 的体积分数、
的体积分数、 与
与 反应中
反应中 的平衡转化率与温度的关系如图所示。下列说法一定正确的是
的平衡转化率与温度的关系如图所示。下列说法一定正确的是
| A.反应Ⅱ的正反应为吸热反应 |
B.在恒温密闭容器中,反应相同时间,温度越低, 的转化率越大 的转化率越大 |
C.发生反应Ⅱ温度不低于600℃的原因是:此温度 平衡转化率已很高;低于此温度, 平衡转化率已很高;低于此温度, 浓度小,反应速率慢 浓度小,反应速率慢 |
D.某温度下若 完全分解成 完全分解成 ,在密闭容器中, ,在密闭容器中, 开始反应,当 开始反应,当 体积分数为10%时, 体积分数为10%时, 转化率为43% 转化率为43% |
您最近一年使用:0次
2022-07-03更新
|
626次组卷
|
4卷引用:湖南省长沙市第一中学2021-2022学年高三下学期月考(八)化学试题



