2024高三下·全国·专题练习
1 . 用硫酸浸取镍钴矿时,提高浸取速率的方法为___________ (答出一条即可)。
您最近一年使用:0次
名校
解题方法
2 . 下列说法不正确的是
A.将 溶液滴入 溶液滴入 溶液中,同时会有气体和沉淀生成 溶液中,同时会有气体和沉淀生成 |
| B.可用红外光谱仪来区分石英玻璃和水晶 |
C.向硫酸铜溶液中滴加过量氨水,形成深蓝色的溶液,是由于生成了 配离子 配离子 |
D.大理石与盐酸反应制取 时,将块状大理石改为粉末状,对增大反应速率有明显效果 时,将块状大理石改为粉末状,对增大反应速率有明显效果 |
您最近一年使用:0次
2024-02-29更新
|
143次组卷
|
3卷引用:河北正定中学本部2023-2024学年高二上学期期末考试化学试题
名校
解题方法
3 . 反应C(s)+H2O(g)  CO(g)+H2(g)在一体积可变的容器中进行,则下列条件的改变使其反应速率增大的是
CO(g)+H2(g)在一体积可变的容器中进行,则下列条件的改变使其反应速率增大的是
 CO(g)+H2(g)在一体积可变的容器中进行,则下列条件的改变使其反应速率增大的是
CO(g)+H2(g)在一体积可变的容器中进行,则下列条件的改变使其反应速率增大的是| A.降低温度 | B.将容器的体积缩小一半 |
| C.将容器的体积拉大到原来的2倍 | D.增加C的量 |
您最近一年使用:0次
2024-02-26更新
|
789次组卷
|
4卷引用:河北省沧州市盐山中学2023-2024学年高一下学期开学化学试题
4 . 宏观辨识与微观探析是化学学科核心素养之一。下列对应离子方程式书写错误的是
A.硫代硫酸钠溶液中滴入稀硫酸: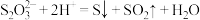 |
B.将碘盐(含 )加入滴加淀粉碘化钾的醋酸溶液中: )加入滴加淀粉碘化钾的醋酸溶液中: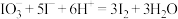 |
C.向烧碱溶液中加入一小段铝片: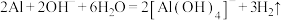 |
D.等浓度 和 和 溶液等体积混合: 溶液等体积混合: |
您最近一年使用:0次
2024-02-24更新
|
67次组卷
|
2卷引用:湖北省新高考联考协作体2023-2024学年高二下学期2月收心考试化学试题
23-24高一下·全国·课后作业
名校
5 . 为研究不同状态 块状、粉末状
块状、粉末状 碳酸钙固体与盐酸反应的反应速率,某同学通过实验测定数据得出如图所示的曲线。下列有关说法中正确的
碳酸钙固体与盐酸反应的反应速率,某同学通过实验测定数据得出如图所示的曲线。下列有关说法中正确的
 块状、粉末状
块状、粉末状 碳酸钙固体与盐酸反应的反应速率,某同学通过实验测定数据得出如图所示的曲线。下列有关说法中正确的
碳酸钙固体与盐酸反应的反应速率,某同学通过实验测定数据得出如图所示的曲线。下列有关说法中正确的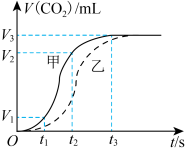
| A.曲线乙表示的是粉末状碳酸钙固体与盐酸反应 |
| B.随着反应进行,盐酸浓度降低,反应速率不断降低 |
C.若用单位时间内 的体积变化来表示该反应的速率,则甲线中 的体积变化来表示该反应的速率,则甲线中 时间内平均反应速率为 时间内平均反应速率为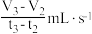 |
D.两次实验,粉末状固体最终生成的 的量更多 的量更多 |
您最近一年使用:0次
2024-02-24更新
|
455次组卷
|
3卷引用:6.2.1化学反应的速率课后作业提高篇
(已下线)6.2.1化学反应的速率课后作业提高篇新疆克孜勒苏柯尔克孜自治州第二中学2022-2023学年高一下学期期末考试化学试题广东省广州市广东番禺中学2023-2024学年高一下学期期中考试化学试题
名校
6 .  盐酸溶液与过量锌粉反应,在一定温度下,为了减缓反应进行的速率,又不影响生成氢气的总量,可向反应物中加入适量的
盐酸溶液与过量锌粉反应,在一定温度下,为了减缓反应进行的速率,又不影响生成氢气的总量,可向反应物中加入适量的
 盐酸溶液与过量锌粉反应,在一定温度下,为了减缓反应进行的速率,又不影响生成氢气的总量,可向反应物中加入适量的
盐酸溶液与过量锌粉反应,在一定温度下,为了减缓反应进行的速率,又不影响生成氢气的总量,可向反应物中加入适量的| A.碳酸钠溶液 | B. 溶液 溶液 | C. 溶液 溶液 | D. 的硫酸溶液 的硫酸溶液 |
您最近一年使用:0次
名校
解题方法
7 . Ⅰ.完成下列问题
(1)列事实或做法与化学反应速率无关的是___________
(2)下列事实能用勒夏特列原理解释的是_______
(3)反应3A(g) 2B(g)+C(g)(ΔH<0)的反应速率随时间变化如图所示,在t1、t3、t4、t5时刻都只有一种因素发生改变。下列判断正确的是_______
2B(g)+C(g)(ΔH<0)的反应速率随时间变化如图所示,在t1、t3、t4、t5时刻都只有一种因素发生改变。下列判断正确的是_______

Ⅱ.氮氧化物(NOx)的任意排放会造成酸雨、光化学烟雾等环境污染问题,其与悬浮在大气中的海盐粒子相互作用时,发生反应:4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)。
2NaNO3(s)+2NO(g)+Cl2(g)。
(4)该反应的平衡常数表达式K=___________
(5)若反应在恒容密闭容器中进行,能说明该反应已达到平衡状态的是___________ (选填编号)。
a.v(NO2)=2v(NO) b.NO2和NO的物质的量之和保持不变
c.混合气体密度保持不变 d.c(NO2)∶c(NO)∶c(Cl2)=4∶2∶1
Ⅲ.上述反应可以视作分两步进行:
(ⅰ)……
(ⅱ)2ClNO(g) 2NO(g)+Cl2(g);ΔH>0
2NO(g)+Cl2(g);ΔH>0
(6)反应ⅰ的化学方程式可能是___________ ;反应ⅱ中反应物化学键总能量___________ 生成物化学键总能量(填“高于”“低于”或“等于”)。
(7)保持恒温条件,将2molClNO充入不同容积的密闭容器中进行反应ⅱ,充分反应达到平衡后,反应物的转化率与容器容积及不同温度的关系如图所示:

①图中T1、T2的关系为T1___________ T2(填“>”“<”或“=”);A、B、C各自对应化学平衡常数大小关系是___________ 。
②若从起始到处于A点状态共经过10min,该时间段内化学反应速率v(NO)=___________ 。
Ⅳ.工业中利用新型催化剂M催化氨气与NO反应生成N2,从而去除NO的影响:4NH3(g)+6NO(g) 5N2(g)+6H2O(g);ΔH=-2070kJ·mol-1,相同时间内,NO的去除率随反应温度的变化曲线如图所示。
5N2(g)+6H2O(g);ΔH=-2070kJ·mol-1,相同时间内,NO的去除率随反应温度的变化曲线如图所示。
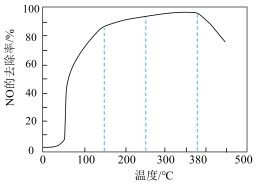
(8)在50~150℃范围内随着温度的升高,NO的去除率上升的原因可能是(任写一点):_________ 。
(1)列事实或做法与化学反应速率无关的是___________
| A.将食物存放在温度低的地方 | B.用铁作催化剂合成氨 |
| C.将煤块粉碎后燃烧 | D.用浓硝酸和铜反应制备NO2气体 |
(2)下列事实能用勒夏特列原理解释的是_______
| A.NO2气体受压缩后,颜色先变深后变浅 |
B.对2HI(g) H2(g)+I2(g)平衡体系加压,颜色迅速变深 H2(g)+I2(g)平衡体系加压,颜色迅速变深 |
| C.接触法制硫酸中,采用500℃高温条件下制备SO3 |
| D.配制硫酸亚铁溶液时,常加入少量铁屑防止氧化 |
(3)反应3A(g)
 2B(g)+C(g)(ΔH<0)的反应速率随时间变化如图所示,在t1、t3、t4、t5时刻都只有一种因素发生改变。下列判断正确的是_______
2B(g)+C(g)(ΔH<0)的反应速率随时间变化如图所示,在t1、t3、t4、t5时刻都只有一种因素发生改变。下列判断正确的是_______
| A.t6~t7阶段,C的百分含量最大 | B.t2~t3阶段,A的转化率最小 |
| C.t3时,改变因素一定是使用了催化剂 | D.t5时,改变因素一定是升高了温度 |
Ⅱ.氮氧化物(NOx)的任意排放会造成酸雨、光化学烟雾等环境污染问题,其与悬浮在大气中的海盐粒子相互作用时,发生反应:4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g)。
2NaNO3(s)+2NO(g)+Cl2(g)。(4)该反应的平衡常数表达式K=
(5)若反应在恒容密闭容器中进行,能说明该反应已达到平衡状态的是
a.v(NO2)=2v(NO) b.NO2和NO的物质的量之和保持不变
c.混合气体密度保持不变 d.c(NO2)∶c(NO)∶c(Cl2)=4∶2∶1
Ⅲ.上述反应可以视作分两步进行:
(ⅰ)……
(ⅱ)2ClNO(g)
 2NO(g)+Cl2(g);ΔH>0
2NO(g)+Cl2(g);ΔH>0(6)反应ⅰ的化学方程式可能是
(7)保持恒温条件,将2molClNO充入不同容积的密闭容器中进行反应ⅱ,充分反应达到平衡后,反应物的转化率与容器容积及不同温度的关系如图所示:

①图中T1、T2的关系为T1
②若从起始到处于A点状态共经过10min,该时间段内化学反应速率v(NO)=
Ⅳ.工业中利用新型催化剂M催化氨气与NO反应生成N2,从而去除NO的影响:4NH3(g)+6NO(g)
 5N2(g)+6H2O(g);ΔH=-2070kJ·mol-1,相同时间内,NO的去除率随反应温度的变化曲线如图所示。
5N2(g)+6H2O(g);ΔH=-2070kJ·mol-1,相同时间内,NO的去除率随反应温度的变化曲线如图所示。
(8)在50~150℃范围内随着温度的升高,NO的去除率上升的原因可能是(任写一点):
您最近一年使用:0次
8 . 一定条件下在容积不变的容器中充入 和
和 发生如下反应:
发生如下反应: ,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得
,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得 与时间的关系如图所示。已知:
与时间的关系如图所示。已知:

ⅰ.起始投料比 均为2:3;
均为2:3;
ⅱ.比表面积:单位质量的物质具有的总面积。
下列说法不正确的是
 和
和 发生如下反应:
发生如下反应: ,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得
,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得 与时间的关系如图所示。已知:
与时间的关系如图所示。已知:
ⅰ.起始投料比
 均为2:3;
均为2:3;ⅱ.比表面积:单位质量的物质具有的总面积。
下列说法不正确的是
| A.Ⅰ、Ⅱ曲线证明催化剂比表面积对上述反应有影响 |
B.Ⅱ中 的平衡转化率为50% 的平衡转化率为50% |
C.在Ⅲ的条件下,该反应的平衡常数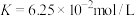 |
D. min,Ⅲ中平均反应速率 min,Ⅲ中平均反应速率 |
您最近一年使用:0次
名校
9 . 在硫酸工业中,使 氧化为
氧化为 的反应为
的反应为
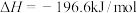 。下表列出了恒容密闭容器中,在不同温度和压强下,反应达到平衡时
。下表列出了恒容密闭容器中,在不同温度和压强下,反应达到平衡时 的转化率。下列说法错误的是
的转化率。下列说法错误的是
 氧化为
氧化为 的反应为
的反应为
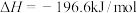 。下表列出了恒容密闭容器中,在不同温度和压强下,反应达到平衡时
。下表列出了恒容密闭容器中,在不同温度和压强下,反应达到平衡时 的转化率。下列说法错误的是
的转化率。下列说法错误的是平衡时 | |||||
0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
450℃ | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
500℃ | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
A.通入适当过量的氧气,既有利于提高反应速率,又有利于增大 的转化率 的转化率 |
B.尾气中的 需要回收循环利用,防止污染环境并提高原料的利用率 需要回收循环利用,防止污染环境并提高原料的利用率 |
| C.在实际生产中,应选择的条件是450℃,10MPa |
| D.在实际生产中,选定的温度为400-500℃,主要原因是考虑催化剂的活性最佳 |
您最近一年使用:0次
2024-02-08更新
|
130次组卷
|
2卷引用:辽宁省锦州市2023-2024学年高二上学期1月期末化学试题
解题方法
10 . 碱式碳酸铜可用作有机催化剂。工业上以辉铜矿(主要成分为 ,含
,含 及少量
及少量 )为原料制备碱式碳酸铜,工业流程如下:
)为原料制备碱式碳酸铜,工业流程如下:
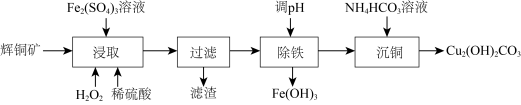
(1)滤渣可能含S、___________ (填化学式)。
(2)①“浸取”时能提高辉铜矿Cu浸取率的措施有___________ (填2条)。
②某小组测得Cu浸取率随 浓度及温度影响的变化曲线如下:
浓度及温度影响的变化曲线如下:

a.由图一可知 适宜的浓度范围为
适宜的浓度范围为___________ ;由图一中的a点分析,浸取时 也起到了氧化辉铜矿的作用,该反应的离子方程式为
也起到了氧化辉铜矿的作用,该反应的离子方程式为___________ 。
b.图二中高于85℃时Cu浸取率下降的原因是___________ 。
(3)“除铁”步骤调pH可加入试剂___________ (填选项字母);
a.氨气 b. c.
c. d.
d.
(4)常温下,“过滤”后的滤液中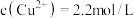 ,则“除铁”步骤调pH应小于
,则“除铁”步骤调pH应小于___________ 。[常温下, ]。
]。
 ,含
,含 及少量
及少量 )为原料制备碱式碳酸铜,工业流程如下:
)为原料制备碱式碳酸铜,工业流程如下:
(1)滤渣可能含S、
(2)①“浸取”时能提高辉铜矿Cu浸取率的措施有
②某小组测得Cu浸取率随
 浓度及温度影响的变化曲线如下:
浓度及温度影响的变化曲线如下:
a.由图一可知
 适宜的浓度范围为
适宜的浓度范围为 也起到了氧化辉铜矿的作用,该反应的离子方程式为
也起到了氧化辉铜矿的作用,该反应的离子方程式为b.图二中高于85℃时Cu浸取率下降的原因是
(3)“除铁”步骤调pH可加入试剂
a.氨气 b.
 c.
c. d.
d.
(4)常温下,“过滤”后的滤液中
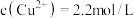 ,则“除铁”步骤调pH应小于
,则“除铁”步骤调pH应小于 ]。
]。
您最近一年使用:0次



