名校
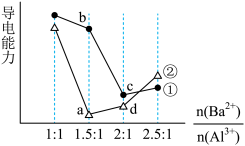
1 . 向两份20 ml 0.1 mol/LBa(OH)2溶液中各加入定量的KAl(SO4)2和Al2(SO4)3溶液的导电性随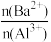 (混合前)的变化关系如图所示,下列分析不正确的是
(混合前)的变化关系如图所示,下列分析不正确的是
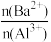 (混合前)的变化关系如图所示,下列分析不正确的是
(混合前)的变化关系如图所示,下列分析不正确的是
| A.a点溶液的pH值约为7 | B.b点溶液中大量存在的阳离子有Al3+和Ba2+ |
| C.c、d两点溶液中OH-均已完全反应 | D.②代表加入Al2(SO4)3的变化曲线 |
您最近一年使用:0次
2023-01-05更新
|
984次组卷
|
3卷引用:河南省鹤壁市高中2022-2023学年高二下学期精英对抗赛化学试题
名校
解题方法
2 . “84消毒液”广泛应用于杀菌消毒,其有效成分是 。实验小组制备消毒液,并利用其性质探究制备碘水的方法。
。实验小组制备消毒液,并利用其性质探究制备碘水的方法。
资料:i. 的电离常数为
的电离常数为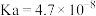 ;
; 的电离常数为
的电离常数为 、
、
ii.碘的化合物主要以 和
和 的形式存在,
的形式存在, 。
。
iii.碘单质能与 反应:
反应: (
( 低浓度时显黄色,高浓度时为棕色)。
低浓度时显黄色,高浓度时为棕色)。
I.制备消毒液(夹持装置略)

(1)制备 的离子反应方程式
的离子反应方程式_______ 。
(2)结合资料i,写出D中反应的化学方程式_______ 。
II.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
(3)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设1成立,实验a的操作及现象是_______ 。
假设2:过量的 将反应生成的
将反应生成的 氧化为
氧化为 。
。
设计实验b证实了假设2成立。 氧化
氧化 生成
生成 的离子方程式是
的离子方程式是_______ 。
(4)某小组检验烧杯3所得溶液中含 :取烧杯3所得无色溶液少许,加入稀硫酸酸化的
:取烧杯3所得无色溶液少许,加入稀硫酸酸化的 溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在
溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在 ,说明理由
,说明理由_______ 。
(5)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据_______ 。
(6)对比不同方案的实验现象,得出制取碘水的最佳方法要关注的因素是_______ 。
 。实验小组制备消毒液,并利用其性质探究制备碘水的方法。
。实验小组制备消毒液,并利用其性质探究制备碘水的方法。资料:i.
 的电离常数为
的电离常数为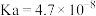 ;
; 的电离常数为
的电离常数为 、
、
ii.碘的化合物主要以
 和
和 的形式存在,
的形式存在, 。
。iii.碘单质能与
 反应:
反应: (
( 低浓度时显黄色,高浓度时为棕色)。
低浓度时显黄色,高浓度时为棕色)。I.制备消毒液(夹持装置略)

(1)制备
 的离子反应方程式
的离子反应方程式(2)结合资料i,写出D中反应的化学方程式
II.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
| 方案 | 操作 | 现象 | 反应后加淀粉溶液 |
| 1 | 烧杯1溶液中加入9g 固体 固体 | 溶液为橙黄色 | …… |
| 2 | 烧杯2溶液中加入9g 固体,再加入1 固体,再加入1 盐酸10mL 盐酸10mL | 溶液颜色快速加深,呈紫红色 | 变蓝 |
| 3 | 烧杯3溶液中加入少量 固体(小于0.5g) 固体(小于0.5g) | 振荡后溶液保持无色 | 不变蓝 |
假设1:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设1成立,实验a的操作及现象是
假设2:过量的
 将反应生成的
将反应生成的 氧化为
氧化为 。
。设计实验b证实了假设2成立。
 氧化
氧化 生成
生成 的离子方程式是
的离子方程式是(4)某小组检验烧杯3所得溶液中含
 :取烧杯3所得无色溶液少许,加入稀硫酸酸化的
:取烧杯3所得无色溶液少许,加入稀硫酸酸化的 溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在
溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在 ,说明理由
,说明理由(5)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据
(6)对比不同方案的实验现象,得出制取碘水的最佳方法要关注的因素是
您最近一年使用:0次
2022-12-30更新
|
1184次组卷
|
4卷引用:河南省鹤壁市高中2022-2023学年高二下学期精英对抗赛化学试题
名校
解题方法
3 . 钠是一种非常活泼、具有广泛应用的金属。请回答:
(1)将一小块金属钠投入水中,发生反应的离子方程式是_______ ;可观察到的实验现象是_______ (填字母序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动 d.有嘶嘶声
(2)钠在空气中的燃烧产物Na2O2可用于呼吸面具或潜水艇中氧气的来源,11.6gCO2和H2O的混合物与足量Na2O2充分反应后,固体质量增加了3.6 g,则生成标准状况下O2的体积_______ L;原混合气体的中CO2和H2O的分子数比为_______ 。
(3)下列实验方案中,不能测定Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是_______
(1)将一小块金属钠投入水中,发生反应的离子方程式是
a.钠沉到水底 b.钠熔成小球 c.小球四处游动 d.有嘶嘶声
(2)钠在空气中的燃烧产物Na2O2可用于呼吸面具或潜水艇中氧气的来源,11.6gCO2和H2O的混合物与足量Na2O2充分反应后,固体质量增加了3.6 g,则生成标准状况下O2的体积
(3)下列实验方案中,不能测定Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是_______
| A.取a g混合物充分加热,质量减少b g |
| B.取a g混合物与足量NaOH溶液充分反应,得到b g溶液 |
| C.取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到b g固体 |
| D.取a g混合物与足量稀硫酸反应,逸出气体经干燥后用碱石灰吸收,质量增加b g |
您最近一年使用:0次
2022-11-29更新
|
538次组卷
|
2卷引用:湖南省邵阳市第二中学2023-2024学年高一上学期基础知识竞赛化学试题
4 . 点击化学及其应用
2001年诺贝尔化学奖获得者K.B.Sharpless教授发现,在亚铜的催化下,末端炔烃可以高区域选择性地与叠氮化合物发生高效的点击(Click)反应,类似炔烃与叠氮化合物发生了1,3-偶极环加成反应。这一反应目前已经应用于生物化学等交叉领域,Sharpless教授也因此获得了2022年度诺贝尔化学奖。
Click反应示例:
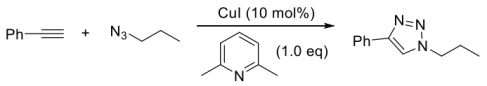
科学家以环己烯为原料,经过多步转化和click反应合成化合物E,请按要求回答下面的问题。在四氢呋喃溶剂中,环己烯与NBS(N-溴代丁二酰亚胺)反应生成关键中间体A,A与水发生反应生成化合物B化合物B经过碳酸钾处理可以高产率合成化合物C,化合物C也可以通过环己烯与间氯过氧苯甲酸反应直接制得;化合物C与叠氮化钠反应可以合成D,D与苯乙炔在碱的存在下及碘化亚铜的催化下发生Click反应生成E。
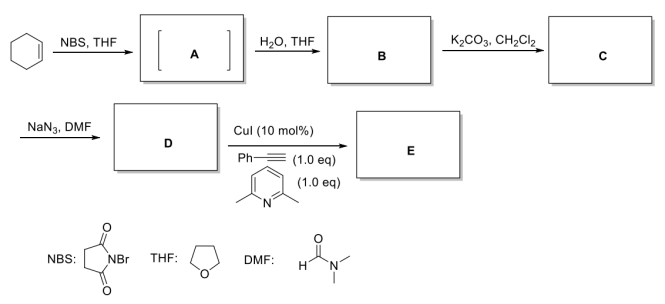
请给出关键中间体A,产物B、C、D、E的结构式,请用楔形式标注产物中的立体化学_____ 、_____ 、_____ 、_____ 、_____ 。
2001年诺贝尔化学奖获得者K.B.Sharpless教授发现,在亚铜的催化下,末端炔烃可以高区域选择性地与叠氮化合物发生高效的点击(Click)反应,类似炔烃与叠氮化合物发生了1,3-偶极环加成反应。这一反应目前已经应用于生物化学等交叉领域,Sharpless教授也因此获得了2022年度诺贝尔化学奖。
Click反应示例:

科学家以环己烯为原料,经过多步转化和click反应合成化合物E,请按要求回答下面的问题。在四氢呋喃溶剂中,环己烯与NBS(N-溴代丁二酰亚胺)反应生成关键中间体A,A与水发生反应生成化合物B化合物B经过碳酸钾处理可以高产率合成化合物C,化合物C也可以通过环己烯与间氯过氧苯甲酸反应直接制得;化合物C与叠氮化钠反应可以合成D,D与苯乙炔在碱的存在下及碘化亚铜的催化下发生Click反应生成E。

请给出关键中间体A,产物B、C、D、E的结构式,请用楔形式标注产物中的立体化学
您最近一年使用:0次
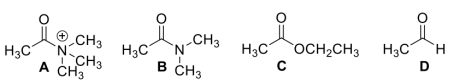
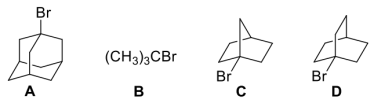
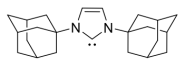
5 . 反应活性与电子效应
(1)将下列过氧化物按照与环己烯发生环氧化反应的活性由高到低排序_____ 。_____ 。_____ 。_____ 。_____ 。
(1)将下列过氧化物按照与环己烯发生环氧化反应的活性由高到低排序


您最近一年使用:0次
6 . 白钨矿晶体结构
白钨矿是钨的重要矿物。其晶胞参数为a=b=523.9pm,c=1137.8pm,α=β=γ=90°。晶体结构如图1所示,隐去氧离子后的晶胞如图2所示,请根据所学知识,回答下列问题。

(1)请给出白钨矿的化学式_____ 。
(2)已知晶胞中的各离子都只有一种化学环境,请给出各离子的配位数_____ 。
(3)请写出晶胞中所有钙离子与钨离子的原子坐标_____ 。
(4)请计算白钨矿的密度_____ 。
白钨矿是钨的重要矿物。其晶胞参数为a=b=523.9pm,c=1137.8pm,α=β=γ=90°。晶体结构如图1所示,隐去氧离子后的晶胞如图2所示,请根据所学知识,回答下列问题。

(1)请给出白钨矿的化学式
(2)已知晶胞中的各离子都只有一种化学环境,请给出各离子的配位数
(3)请写出晶胞中所有钙离子与钨离子的原子坐标
(4)请计算白钨矿的密度
您最近一年使用:0次
7 . S2F10的分子结构问题
分子构型对其性质有着显著的影响。对无机物来说,其结构通常可以通过红外光谱拟合或气态电子衍射得到。请根据所学知识,回答下列问题。
(1)为了拟合红外光谱,需要先拟定分子的可能构型。运用VSEPR理论,请给出SF 离子可能的构型
离子可能的构型_____ 。与理想多面体相比,你预计SF 离子的实际结构将会发生怎样的变形?请解释理由
离子的实际结构将会发生怎样的变形?请解释理由_____ 。
(2)电子衍射结果表明,S2F10中存在S-S键。请画出其最稳定的结构_____ 。
(3)已知S2F10中,赤道面上的S-F键长为157.4pm,S-S键长为227.4pm,请根据你在上一问中所画的结构,计算不同S原子上F原子之间的最短间距_____ ,并与F原子的范德华半径147pm比较。通常情况下,F原子的范德华半径与共价半径谁更大_____ ?
(4)请写出S2F10分子所具有的对称元素(仅考虑旋转轴、对称面与对称中心)_____ 。
(5)将S2F10与N2F4混合后,可以制得一种具有单根S-N键的化合物,与许多高价氟化物不同,它对水是稳定的。请画出这种化合物的结构,并解释其对水的稳定性_____ 。
分子构型对其性质有着显著的影响。对无机物来说,其结构通常可以通过红外光谱拟合或气态电子衍射得到。请根据所学知识,回答下列问题。
(1)为了拟合红外光谱,需要先拟定分子的可能构型。运用VSEPR理论,请给出SF
 离子可能的构型
离子可能的构型 离子的实际结构将会发生怎样的变形?请解释理由
离子的实际结构将会发生怎样的变形?请解释理由(2)电子衍射结果表明,S2F10中存在S-S键。请画出其最稳定的结构
(3)已知S2F10中,赤道面上的S-F键长为157.4pm,S-S键长为227.4pm,请根据你在上一问中所画的结构,计算不同S原子上F原子之间的最短间距
(4)请写出S2F10分子所具有的对称元素(仅考虑旋转轴、对称面与对称中心)
(5)将S2F10与N2F4混合后,可以制得一种具有单根S-N键的化合物,与许多高价氟化物不同,它对水是稳定的。请画出这种化合物的结构,并解释其对水的稳定性
您最近一年使用:0次
解题方法
8 . 稀有气体的性质与应用
稀有气体在大功率激光、特殊的光学玻璃等领域具有重大应用前景。Xe的氟化物中XeF2是最有前途的氟化剂,其与氟磺酸(FSO3H)反应产生游离基A(反应一),A双聚成含有非极性键的极性分子B;XeF2水溶液作为强氧化剂可以用来测定I-的含量,在弱酸性介质中氧化I-为IO (反应二);计算表明,Xe的电离能(12.13eV)比O2的电离能(12.2eV)更低,据此,研究者试图通过O2BF4与Xe反应来制备XeBF4,然而得到的白色固体C中氟含量为28.63%,低于目标产物中氟含量(反应三);XeOBF4同路易斯酸SbF5以1∶2反应生成离子化合物D(反应四)。
(反应二);计算表明,Xe的电离能(12.13eV)比O2的电离能(12.2eV)更低,据此,研究者试图通过O2BF4与Xe反应来制备XeBF4,然而得到的白色固体C中氟含量为28.63%,低于目标产物中氟含量(反应三);XeOBF4同路易斯酸SbF5以1∶2反应生成离子化合物D(反应四)。
(1)写出反应一、二、三的方程式_____ 、_____ 、_____ 。
(2)画出B的立体结构_____ 。
(3)画出C的立体结构,在结构中标出中心原子的杂化方式_____ 。
(4)画出D的立体结构_____ 。
稀有气体在大功率激光、特殊的光学玻璃等领域具有重大应用前景。Xe的氟化物中XeF2是最有前途的氟化剂,其与氟磺酸(FSO3H)反应产生游离基A(反应一),A双聚成含有非极性键的极性分子B;XeF2水溶液作为强氧化剂可以用来测定I-的含量,在弱酸性介质中氧化I-为IO
 (反应二);计算表明,Xe的电离能(12.13eV)比O2的电离能(12.2eV)更低,据此,研究者试图通过O2BF4与Xe反应来制备XeBF4,然而得到的白色固体C中氟含量为28.63%,低于目标产物中氟含量(反应三);XeOBF4同路易斯酸SbF5以1∶2反应生成离子化合物D(反应四)。
(反应二);计算表明,Xe的电离能(12.13eV)比O2的电离能(12.2eV)更低,据此,研究者试图通过O2BF4与Xe反应来制备XeBF4,然而得到的白色固体C中氟含量为28.63%,低于目标产物中氟含量(反应三);XeOBF4同路易斯酸SbF5以1∶2反应生成离子化合物D(反应四)。(1)写出反应一、二、三的方程式
(2)画出B的立体结构
(3)画出C的立体结构,在结构中标出中心原子的杂化方式
(4)画出D的立体结构
您最近一年使用:0次
9 . 完成下列问题
(1)下列四个合成反应路线的设计哪些是错误的?(请写出错误路线的编号) 和
和 从大到小排序:
从大到小排序:_________


_________ _________ _________ _________ _________
(1)下列四个合成反应路线的设计哪些是错误的?(请写出错误路线的编号)
①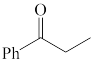

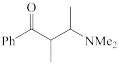
②


③

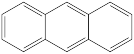
④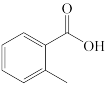


 和
和 从大到小排序:
从大到小排序:



(a)  (b)
(b) 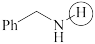 (c)
(c) 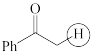 (d)
(d) 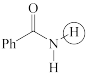 (e)
(e) 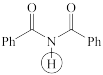
A. B.
B. C.
C.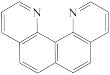 D.
D.
A.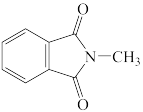 B.
B. C.
C. D.
D.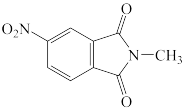
A. 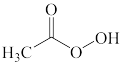 B.
B. 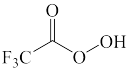 C.
C. 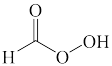 D.
D.  E.
E.  F.
F. 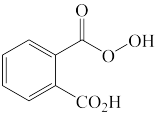
①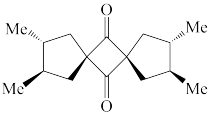 ②
② ③
③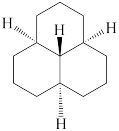 ④
④ ⑤
⑤
⑥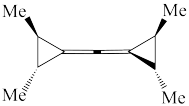 ⑦
⑦ ⑧
⑧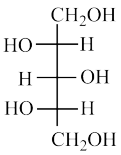 ⑨
⑨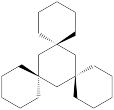 ⑩
⑩
您最近一年使用:0次
10 . 抗肿瘤药Pelitinib的合成
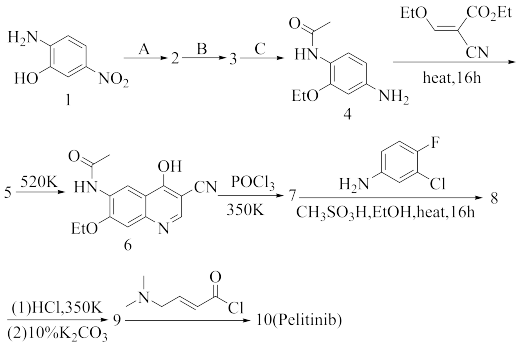
(1)写出上述各步合成反应产物2,3,5,7,8,9,10的结构简式、步骤A,B,C所需的试剂及必要的反应条件_______ 。
(2)化合物4在加热回流条件下与2-氰基-3-乙氧基丙烯酸乙酯反应经中间体5a转化为5,化合物5在250℃条件下经6a,6b中间体得到6:

画出中间体5a,6a,6b的结构简式_______ 。

(1)写出上述各步合成反应产物2,3,5,7,8,9,10的结构简式、步骤A,B,C所需的试剂及必要的反应条件
(2)化合物4在加热回流条件下与2-氰基-3-乙氧基丙烯酸乙酯反应经中间体5a转化为5,化合物5在250℃条件下经6a,6b中间体得到6:

画出中间体5a,6a,6b的结构简式
您最近一年使用:0次



