名校
1 . 下列有关性质的比较,不能用元素周期律解释的是
| A.酸性:H2SO4>H3PO4 | B.非金属性:N>P |
| C.氧化性:O2>S | D.高温时的还原性:C>Si |
您最近一年使用:0次
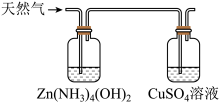
2 . 天然气中常混有 ,现用如下方法测定天然气中
,现用如下方法测定天然气中 的含量。反应中涉及的方程式有:
的含量。反应中涉及的方程式有:
①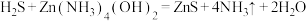
②
③
(1)反应①中, 体现
体现_______ (选填“酸性”“氧化性”或“还原性”)。
采用以下方法测定 的含量。
的含量。
步骤I:将1L天然气中的 溶于水并进行反应①,配制成500mL溶液。
溶于水并进行反应①,配制成500mL溶液。
步骤II:加入0.001mol的I2(过量)使ZnS完全转化为ZnI2,加入淀粉溶液作为指示剂,用0.1mol·L-1的 滴定过量的I2,做几组平行实验,平均消耗15.00mL。
滴定过量的I2,做几组平行实验,平均消耗15.00mL。
(2)①滴定达到终点的现象为:溶液由_______ 色变_______ 色,且半分钟不恢复原色。
②根据条件计算天然气中H2S的含量为_______ mg·L-1。
③若在步骤I收集H2S的过程中,有少量硫化氢进入 溶液中,则测得H2S的含量
溶液中,则测得H2S的含量_______ (选填“偏高”“偏低”或“无影响”)。
(3)假设在反应②中,碘单质全部转化为易溶于水的ZnI2,如何检验体系中的I-_______ 。
(4)利用硫碘循环处理H2S的方法如图所示:
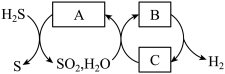
写出上述流程中A、B、C的化学式。
A:_______ ;B:_______ ;C:_______ 。
 ,现用如下方法测定天然气中
,现用如下方法测定天然气中 的含量。反应中涉及的方程式有:
的含量。反应中涉及的方程式有:①
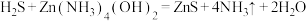
②

③

(1)反应①中,
 体现
体现采用以下方法测定
 的含量。
的含量。步骤I:将1L天然气中的
 溶于水并进行反应①,配制成500mL溶液。
溶于水并进行反应①,配制成500mL溶液。
步骤II:加入0.001mol的I2(过量)使ZnS完全转化为ZnI2,加入淀粉溶液作为指示剂,用0.1mol·L-1的
 滴定过量的I2,做几组平行实验,平均消耗15.00mL。
滴定过量的I2,做几组平行实验,平均消耗15.00mL。(2)①滴定达到终点的现象为:溶液由
②根据条件计算天然气中H2S的含量为
③若在步骤I收集H2S的过程中,有少量硫化氢进入
 溶液中,则测得H2S的含量
溶液中,则测得H2S的含量(3)假设在反应②中,碘单质全部转化为易溶于水的ZnI2,如何检验体系中的I-
(4)利用硫碘循环处理H2S的方法如图所示:

写出上述流程中A、B、C的化学式。
A:
您最近一年使用:0次
名校
解题方法
3 . 下列实验操作能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 向足量酸性KMnO4溶液中滴加少量FeCl2溶液,振荡 | 验证Fe2+具有还原性 |
| B | 用洁净的铂丝蘸取KCl溶液在酒精灯外焰上灼烧 | 观察钾元素的焰色 |
| C | 向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡 | 验证Br2的氧化性强于I2 |
| D | 用玻璃棒蘸取饱和氯水点在pH试纸上,待变色后与标准比色卡对照 | 测定饱和氯水的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-19更新
|
377次组卷
|
3卷引用:安徽省宣城市2022-2023学年高一上学期期末调研考试化学试题
4 . SO2是重要的化工原料,回收利用SO2既能减少大气污染,又能充分利用资源。
(1)向食品中添加适量的SO2可以起到的作用:①杀菌;②漂白;③抗氧化,则葡萄酒中添加适量的SO2的作用是___________ 。(填序号)
(2)SO2性质多变,若将SO2气体通入H2S溶液中,能观察到的现象为___________ ,该反应中SO2表现出___________ 性;
(3)若将SO2气体通入酸性高锰酸钾溶液中,发生反应的离子方程式为___________ ,该反应中SO2表现出___________ 性。
(4)同时向BaCl2溶液中通入NH3和SO2有白色沉淀产生,产生沉淀的化学式___________ 。SO2通入Na2CO3溶液中有CO2生成,说明H2SO3具有___________ (填“酸性”、“氧化性”、“还原性”或“漂白性”,下同),SO2通入品红溶液中,品红溶液褪色,说明SO2具有___________ 。
(1)向食品中添加适量的SO2可以起到的作用:①杀菌;②漂白;③抗氧化,则葡萄酒中添加适量的SO2的作用是
(2)SO2性质多变,若将SO2气体通入H2S溶液中,能观察到的现象为
(3)若将SO2气体通入酸性高锰酸钾溶液中,发生反应的离子方程式为
(4)同时向BaCl2溶液中通入NH3和SO2有白色沉淀产生,产生沉淀的化学式
您最近一年使用:0次
名校
解题方法
5 . 根据元素周期律,下列关于物质的性质比较正确的是
A.酸性: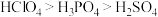 | B.简单气态氢化物稳定性: |
C.氧化性: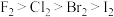 | D.碱性: |
您最近一年使用:0次
2023-08-23更新
|
723次组卷
|
6卷引用:云南省保山市高(完)中C、D类学校2022-2023学年高二上学期10月份联考化学试题
解题方法
6 . 下列关于 的说法中不正确的是
的说法中不正确的是
 的说法中不正确的是
的说法中不正确的是A. 有刺激性气味,有毒 有刺激性气味,有毒 |
| B.既有氧化性又有还原性 |
| C.能使酸性高锰酸钾溶液褪色,体现漂白性 |
| D.可按照食品添加剂使用标准用作食品的添加剂 |
您最近一年使用:0次
2022-12-20更新
|
76次组卷
|
2卷引用:云南省昆明长鸿实验中学2021-2022学年高一下学期3月月考化学试题
解题方法
7 . 回答下列问题:
(1)H2O2水溶液称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口,对下列两个涉及H2O2的反应,填写下列空白:
A.
B.
① H2O2仅体现氧化性的反应是_______ (填代号,下同);
② H2O2仅体现还原性的是_______ 。
(2)在一定条件下,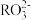 与Cl2反应如下:
与Cl2反应如下: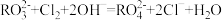 由以上反应可知上述过程中
由以上反应可知上述过程中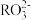 被
被_______ (填“氧化”或“还原”),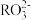 中元素R的化合价是
中元素R的化合价是_______ 。
(3)已知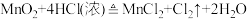
①当产生标准状况下11.2L的氯气时,被氧化的HCl的物质的量是_______ ;转移电子的数目是_______ 。
②浓盐酸所表现出的性质是_______ 。
a. 还原性 b. 酸性 c. 氧化性
(1)H2O2水溶液称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口,对下列两个涉及H2O2的反应,填写下列空白:
A.

B.

① H2O2仅体现氧化性的反应是
② H2O2仅体现还原性的是
(2)在一定条件下,
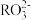 与Cl2反应如下:
与Cl2反应如下: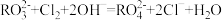 由以上反应可知上述过程中
由以上反应可知上述过程中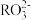 被
被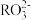 中元素R的化合价是
中元素R的化合价是(3)已知
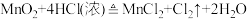
①当产生标准状况下11.2L的氯气时,被氧化的HCl的物质的量是
②浓盐酸所表现出的性质是
a. 还原性 b. 酸性 c. 氧化性
您最近一年使用:0次
8 . 在实验室和生活中高铁酸钾都是一种应用十分广泛的盐类,如下有几种制备方式,
湿法: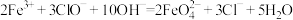
干法:
电解法:
下列选项中说法正确的是
湿法:
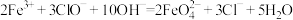
干法:

电解法:

下列选项中说法正确的是
| A.实验室中常用钾盐而不是钠盐原因是钠盐易风化导致固体结块 |
| B.物质的氧化性和还原性在水溶液中和非水体系中不一定相同 |
| C.坤cà和Nilky两人根据元素和化合物知识做出推断,坤ca:高铁酸钾在生活中可用于杀菌因为具有强氧化性;Nilky:高铁酸钾不可用作净水剂,因为高铁酸根不能水解生成胶体 |
| D.高铁酸根在酸性或中性溶液中分解,将生成气体收集在试管中,点燃的小木条靠近可以听到轻微的爆鸣声,且该气体在能源方面有很广泛的发展前景,常用于作清洁能源 |
您最近一年使用:0次
名校
解题方法
9 . 下列各组性质的比较中正确的是
A.酸性: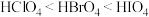 | B.稳定性: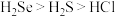 |
C.碱性: | D.氧化性: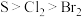 |
您最近一年使用:0次
10 . 室温下,下列实验探究方案不能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向较浓的FeCl2溶液中滴入少量酸性KMnO4溶液,观察KMnO4溶液紫色是否褪去 | Fe2+具有还原性 |
| B | Na2O2用棉花包裹放在石棉网上,向棉花上滴几滴水,观察棉花是否燃烧 | Na2O2与H2O反应放热 |
| C | 向2mL1mol•L-1CH3COOH溶液中滴加1mol•L-1Na2CO3溶液,观察是否产生气泡 | 比较Ka(CH3COOH)和Ka1(H2CO3)的大小 |
| D | 向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 | Br2的氧化性强于I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-08更新
|
693次组卷
|
6卷引用:江苏省苏州中学、淮阴中学、姜堰中学、海门中学四校2023届高三上学期期中联考化学试题



