1 . 以银锰精矿(主要含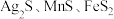 )和氧化锰矿(主要含
)和氧化锰矿(主要含 )为原料联合提取银、锰及
)为原料联合提取银、锰及 的一种流程示意图如下:
的一种流程示意图如下: 的氧化性强于
的氧化性强于 。
。
(1)“浸锰渣”含有S和 ,写出“浸锰”过程中,二氧化锰和硫化锰反应的化学方程式:
,写出“浸锰”过程中,二氧化锰和硫化锰反应的化学方程式:_______ 。
(2)“除杂”时,若溶液中 ,欲使溶液中
,欲使溶液中 浓度小于
浓度小于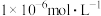 ,需控制的
,需控制的 范围为
范围为_______ (已知:室温下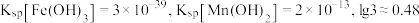 )。
)。
(3)沉锰过程在 为7.0条件下充分进行,反应温度对锰沉淀率的影响关系如图所示。沉锰反应中,锰沉淀率在
为7.0条件下充分进行,反应温度对锰沉淀率的影响关系如图所示。沉锰反应中,锰沉淀率在 左右达最大的原因是
左右达最大的原因是_______ 。 晶体的晶胞示意图如图1,晶胞的俯视图和正视图如图2。
晶体的晶胞示意图如图1,晶胞的俯视图和正视图如图2。_______  (用含有a、b及
(用含有a、b及 的代数式表示)。
的代数式表示)。
(5)“浸银”时,使用过量 和
和 混合液作为浸出剂,将
混合液作为浸出剂,将 中的银以
中的银以 形式浸出并生成S。写出“浸银”反应的离子方程式:
形式浸出并生成S。写出“浸银”反应的离子方程式:_______ 。“沉银”过程中需要过量的铁粉作为还原剂,“沉银”后的滤液中,主要含有的阳离子有_______ 。
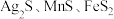 )和氧化锰矿(主要含
)和氧化锰矿(主要含 )为原料联合提取银、锰及
)为原料联合提取银、锰及 的一种流程示意图如下:
的一种流程示意图如下: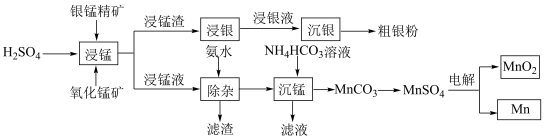
 的氧化性强于
的氧化性强于 。
。(1)“浸锰渣”含有S和
 ,写出“浸锰”过程中,二氧化锰和硫化锰反应的化学方程式:
,写出“浸锰”过程中,二氧化锰和硫化锰反应的化学方程式:(2)“除杂”时,若溶液中
 ,欲使溶液中
,欲使溶液中 浓度小于
浓度小于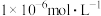 ,需控制的
,需控制的 范围为
范围为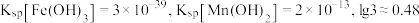 )。
)。(3)沉锰过程在
 为7.0条件下充分进行,反应温度对锰沉淀率的影响关系如图所示。沉锰反应中,锰沉淀率在
为7.0条件下充分进行,反应温度对锰沉淀率的影响关系如图所示。沉锰反应中,锰沉淀率在 左右达最大的原因是
左右达最大的原因是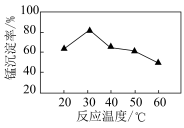
 晶体的晶胞示意图如图1,晶胞的俯视图和正视图如图2。
晶体的晶胞示意图如图1,晶胞的俯视图和正视图如图2。
①图1中“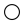 ”代表的是
”代表的是 ”或“O”),对应图2中的
”或“O”),对应图2中的
 (用含有a、b及
(用含有a、b及 的代数式表示)。
的代数式表示)。(5)“浸银”时,使用过量
 和
和 混合液作为浸出剂,将
混合液作为浸出剂,将 中的银以
中的银以 形式浸出并生成S。写出“浸银”反应的离子方程式:
形式浸出并生成S。写出“浸银”反应的离子方程式:
您最近一年使用:0次
解题方法
2 . 有机物 是治疗良性前列腺增生的药物,其一种合成路线如下:
是治疗良性前列腺增生的药物,其一种合成路线如下:
(1)已知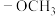 为取代基团(甲氧基),
为取代基团(甲氧基), 的化学名称为
的化学名称为___________ 。
(2) 过程中,先生成中间体
过程中,先生成中间体 (分子式为
(分子式为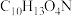 ),然后发生消去反应生成
),然后发生消去反应生成 。写出
。写出 的结构简式:
的结构简式:___________ 。
(3)写出 的化学方程式:
的化学方程式:___________ ,该反应类型为___________ 。
(4)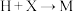 的另一产物为
的另一产物为 ,
, 的结构简式为
的结构简式为___________ 。
(5)满足下列条件的 的二取代芳香族同分异构体的结构简式为
的二取代芳香族同分异构体的结构简式为___________ 。
①与 溶液发生显色反应;
溶液发生显色反应;
②能发生银镜反应;
③核磁共振氢谱有5组峰,且峰面积之比为6:2:2:1:1
(6)参照C→D→E官能团转化信息,设计以苯甲醇为原料,制备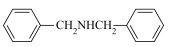 的合成路线:
的合成路线:___________ 。(其他无机试剂任选)。
 是治疗良性前列腺增生的药物,其一种合成路线如下:
是治疗良性前列腺增生的药物,其一种合成路线如下: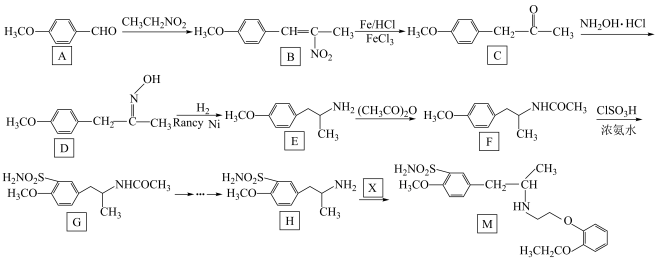
(1)已知
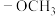 为取代基团(甲氧基),
为取代基团(甲氧基), 的化学名称为
的化学名称为(2)
 过程中,先生成中间体
过程中,先生成中间体 (分子式为
(分子式为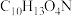 ),然后发生消去反应生成
),然后发生消去反应生成 。写出
。写出 的结构简式:
的结构简式:(3)写出
 的化学方程式:
的化学方程式:(4)
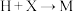 的另一产物为
的另一产物为 ,
, 的结构简式为
的结构简式为(5)满足下列条件的
 的二取代芳香族同分异构体的结构简式为
的二取代芳香族同分异构体的结构简式为①与
 溶液发生显色反应;
溶液发生显色反应;②能发生银镜反应;
③核磁共振氢谱有5组峰,且峰面积之比为6:2:2:1:1
(6)参照C→D→E官能团转化信息,设计以苯甲醇为原料,制备
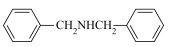 的合成路线:
的合成路线:
您最近一年使用:0次
3 . 草酸钴是制作氧化钴和金属钴的原料。一种利用含钴废料(主要成分为 ,含少量
,含少量 、
、 、CaO、MgO、碳及有机物等)制取
、CaO、MgO、碳及有机物等)制取 的工艺流程如图:
的工艺流程如图:____________ 。
(2)“碱浸”过程中浸出液主要成分是____________ 。
(3)“钴浸出”过程中,不能用盐酸代替硫酸,因为 与盐酸反应生成
与盐酸反应生成 污染环境,该反应的离子方程式为
污染环境,该反应的离子方程式为____________ , 的作用是
的作用是____________ 。
(4)“净化除杂1”过程中,先在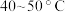 加入
加入 ,再升温至
,再升温至 ,加入
,加入 溶液,调pH至4.5。滤渣1的主要成分是
溶液,调pH至4.5。滤渣1的主要成分是____________ 金属离子与 反应的离子方程式为
反应的离子方程式为____________ 。
(5)“净化除杂2”过程中,加入NaF以除去原溶液中 (浓度为
(浓度为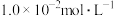 )和
)和 ,若控制溶液中
,若控制溶液中 ,则
,则 的去除率准确值为
的去除率准确值为______ 。[已知某温度下, ]
]
 ,含少量
,含少量 、
、 、CaO、MgO、碳及有机物等)制取
、CaO、MgO、碳及有机物等)制取 的工艺流程如图:
的工艺流程如图:
(2)“碱浸”过程中浸出液主要成分是
(3)“钴浸出”过程中,不能用盐酸代替硫酸,因为
 与盐酸反应生成
与盐酸反应生成 污染环境,该反应的离子方程式为
污染环境,该反应的离子方程式为 的作用是
的作用是(4)“净化除杂1”过程中,先在
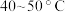 加入
加入 ,再升温至
,再升温至 ,加入
,加入 溶液,调pH至4.5。滤渣1的主要成分是
溶液,调pH至4.5。滤渣1的主要成分是 反应的离子方程式为
反应的离子方程式为(5)“净化除杂2”过程中,加入NaF以除去原溶液中
 (浓度为
(浓度为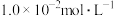 )和
)和 ,若控制溶液中
,若控制溶液中 ,则
,则 的去除率准确值为
的去除率准确值为 ]
]
您最近一年使用:0次
4 .  (丙烯)是重要基本有机原料。
(丙烯)是重要基本有机原料。 (丙烷)催化脱氢制
(丙烷)催化脱氢制 过程如下:
过程如下:
Ⅰ.主反应: ;
;
Ⅱ.副反应: 。
。
回答下列问题:
(1)已知断裂 下列化学键所需能量如下表:
下列化学键所需能量如下表:
上述主反应的
___________  。
。
(2)一定条件下, 催化脱氢制
催化脱氢制 发生上述Ⅰ、Ⅱ反应,
发生上述Ⅰ、Ⅱ反应, 和
和 的平衡体积分数与温度、压强的关系如图1所示(图中压强分别为
的平衡体积分数与温度、压强的关系如图1所示(图中压强分别为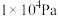 和
和 )。
)。 时,图中表示
时,图中表示 和
和 积分数变化的曲线分别为
积分数变化的曲线分别为___________ 、___________ 。
②提高 催化脱氢制
催化脱氢制 的反应平衡转化率的方法是
的反应平衡转化率的方法是___________ (任写一种)。
(3)在压力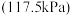 恒定,以
恒定,以 作为稀释气,不同水烃比
作为稀释气,不同水烃比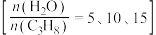 时,
时, 催化脱氢制备
催化脱氢制备 反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图2所示。
反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图2所示。 平衡转化率相同时,水烃比越高,对应的反应温度越
平衡转化率相同时,水烃比越高,对应的反应温度越___________ (填“高”或“低”)。
②相同温度下,水烃比远大于15:1时,丙烷的消耗速率明显下降,可能的原因是:
ⅰ.丙烷的浓度过低;
ⅱ.___________ 。
③M点对应条件下,若 的选择性为
的选择性为 ,则反应Ⅰ的分压平衡常数
,则反应Ⅰ的分压平衡常数 为
为___________ kPa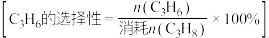 。
。
(4)利用 的弱氧化性,科研人员开发了
的弱氧化性,科研人员开发了 氧化脱氢制
氧化脱氢制 的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图3所示。
的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图3所示。___________ 。
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是___________ 。
(5)研究表明, 氧化脱氢制
氧化脱氢制 的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni组成的
的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni组成的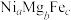 的立方晶胞结构如图4所示。已知晶胞的边长为
的立方晶胞结构如图4所示。已知晶胞的边长为 ,设
,设 为阿伏加德罗常数的值。该晶体密度是
为阿伏加德罗常数的值。该晶体密度是___________  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
 (丙烯)是重要基本有机原料。
(丙烯)是重要基本有机原料。 (丙烷)催化脱氢制
(丙烷)催化脱氢制 过程如下:
过程如下:Ⅰ.主反应:
 ;
;Ⅱ.副反应:
 。
。回答下列问题:
(1)已知断裂
 下列化学键所需能量如下表:
下列化学键所需能量如下表:| 化学键 |  |  |  |
能量 | 436.0 | 413.4 | 344.7 |

 。
。(2)一定条件下,
 催化脱氢制
催化脱氢制 发生上述Ⅰ、Ⅱ反应,
发生上述Ⅰ、Ⅱ反应, 和
和 的平衡体积分数与温度、压强的关系如图1所示(图中压强分别为
的平衡体积分数与温度、压强的关系如图1所示(图中压强分别为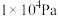 和
和 )。
)。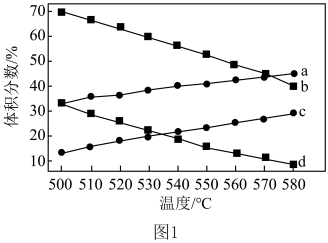
 时,图中表示
时,图中表示 和
和 积分数变化的曲线分别为
积分数变化的曲线分别为②提高
 催化脱氢制
催化脱氢制 的反应平衡转化率的方法是
的反应平衡转化率的方法是(3)在压力
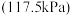 恒定,以
恒定,以 作为稀释气,不同水烃比
作为稀释气,不同水烃比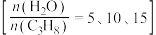 时,
时, 催化脱氢制备
催化脱氢制备 反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图2所示。
反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图2所示。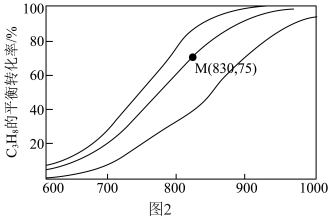
 平衡转化率相同时,水烃比越高,对应的反应温度越
平衡转化率相同时,水烃比越高,对应的反应温度越②相同温度下,水烃比远大于15:1时,丙烷的消耗速率明显下降,可能的原因是:
ⅰ.丙烷的浓度过低;
ⅱ.
③M点对应条件下,若
 的选择性为
的选择性为 ,则反应Ⅰ的分压平衡常数
,则反应Ⅰ的分压平衡常数 为
为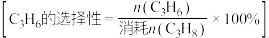 。
。(4)利用
 的弱氧化性,科研人员开发了
的弱氧化性,科研人员开发了 氧化脱氢制
氧化脱氢制 的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图3所示。
的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图3所示。
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是
(5)研究表明,
 氧化脱氢制
氧化脱氢制 的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni组成的
的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni组成的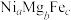 的立方晶胞结构如图4所示。已知晶胞的边长为
的立方晶胞结构如图4所示。已知晶胞的边长为 ,设
,设 为阿伏加德罗常数的值。该晶体密度是
为阿伏加德罗常数的值。该晶体密度是 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解题方法
5 . 实验室用苯和液溴制取溴苯并验证其反应类型的实验装置图(夹持装置略)及有关数据如下,按下列步骤回答有关问题。
_______ 。
(2)在a中加入15mL无水苯和少量铁屑,在b中小心加入4mL液态溴,向a中滴入液溴,有白雾生成,a中发生反应的化学方程式为_______ 。
(3)d中CCl4的作用是_______ ;e中出现_______ ,则说明苯与液溴发生了取代反应。
(4)充分反应后,经过下列步骤分离提纯。
①反应后a瓶中的溴苯因溶有溴而显褐色,提纯溴苯的过程中,除去溴苯中的溴依次用水、_______ 溶液、水洗涤。
②向分离出的粗溴苯中加入少量无水氯化钙,静置、过滤。加入氯化钙的目的是_______ 。
③已知苯与溴还可能发生副反应生成对二溴苯(沸点 和邻二溴苯(沸点
和邻二溴苯(沸点 要进一步提纯,再进行
要进一步提纯,再进行_______ (填操作名称)即可得到较纯净的溴苯,该过程中为了受热均匀和易于控制温度,可采用_______ (填“水浴”或“油浴”)加热。
| 苯 | 溴 | 溴苯 | |
| 密度/(g·cm⁻³) | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解性 | 微溶 | 微溶 | 微溶 |

(2)在a中加入15mL无水苯和少量铁屑,在b中小心加入4mL液态溴,向a中滴入液溴,有白雾生成,a中发生反应的化学方程式为
(3)d中CCl4的作用是
(4)充分反应后,经过下列步骤分离提纯。
①反应后a瓶中的溴苯因溶有溴而显褐色,提纯溴苯的过程中,除去溴苯中的溴依次用水、
②向分离出的粗溴苯中加入少量无水氯化钙,静置、过滤。加入氯化钙的目的是
③已知苯与溴还可能发生副反应生成对二溴苯(沸点
 和邻二溴苯(沸点
和邻二溴苯(沸点 要进一步提纯,再进行
要进一步提纯,再进行
您最近一年使用:0次
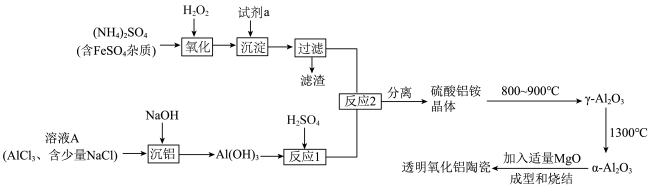
6 . 透明氧化铝陶瓷被认为是最具潜力的材料之一,制备透明氧化铝陶瓷的一种方法的流程如图所示:
(1)试剂a应选用___________ (填名称), 的电子式为
的电子式为___________ 。
(2)“反应1”的离子方程式为___________ 。
(3)检验上述流程中“过滤”后杂质已除尽的方法是___________ 。
(4)“沉铝”时,欲使 恰好完全转化为
恰好完全转化为 沉淀,应控制pH的范围是
沉淀,应控制pH的范围是___________ {已知:溶液中 、
、 浓度小于
浓度小于 认为
认为 沉淀完全,
沉淀完全,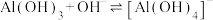 ,
,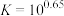 ,
,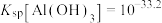 }。
}。
(5)硫酸铝铵晶体[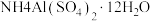 ]是一种重要的分析试剂,向硫酸铝铵溶液中加入同浓度的
]是一种重要的分析试剂,向硫酸铝铵溶液中加入同浓度的 溶液,沉淀质量最大时,反应的总离子方程式为
溶液,沉淀质量最大时,反应的总离子方程式为___________ 。
(6)硫酸铝铵晶体加热到800~900℃得到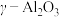 ,加热过程中固体质量随温度的变化如图所示。则633℃时剩余固体成分的化学式为
,加热过程中固体质量随温度的变化如图所示。则633℃时剩余固体成分的化学式为___________ 。___________ 特性;用它制造刚玉球磨机,是利用它的___________ 特性。
(1)试剂a应选用
 的电子式为
的电子式为(2)“反应1”的离子方程式为
(3)检验上述流程中“过滤”后杂质已除尽的方法是
(4)“沉铝”时,欲使
 恰好完全转化为
恰好完全转化为 沉淀,应控制pH的范围是
沉淀,应控制pH的范围是 、
、 浓度小于
浓度小于 认为
认为 沉淀完全,
沉淀完全,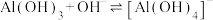 ,
,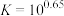 ,
,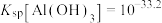 }。
}。(5)硫酸铝铵晶体[
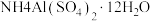 ]是一种重要的分析试剂,向硫酸铝铵溶液中加入同浓度的
]是一种重要的分析试剂,向硫酸铝铵溶液中加入同浓度的 溶液,沉淀质量最大时,反应的总离子方程式为
溶液,沉淀质量最大时,反应的总离子方程式为(6)硫酸铝铵晶体加热到800~900℃得到
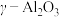 ,加热过程中固体质量随温度的变化如图所示。则633℃时剩余固体成分的化学式为
,加热过程中固体质量随温度的变化如图所示。则633℃时剩余固体成分的化学式为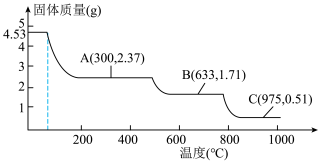
您最近一年使用:0次
2024-05-12更新
|
159次组卷
|
2卷引用:2024届河南省九师联盟2023-2024学年高三下学期4月联考理综试题-高中化学
名校
解题方法
7 . 甲烷是重要的燃料和化工原料,一种利用CO2制备CH4的反应为CO2(g)+4H2(g) CH4(g)+2H2O(g)。T℃下,在2L的恒容密闭容器中通入2molCO2和2molH2,发生上述反应,容器内两种气体的物质的量随时间变化的关系如图所示。回答下列问题:
CH4(g)+2H2O(g)。T℃下,在2L的恒容密闭容器中通入2molCO2和2molH2,发生上述反应,容器内两种气体的物质的量随时间变化的关系如图所示。回答下列问题:___________ ;5~10min内,用H2O(g)表示的平均反应速率v(H2O)=___________ mol/(L·min);下列措施能加快上述反应的正反应速率的是___________ (填标号)。
A.升高温度 B.通入He C.通入CO2 D.分离出CH4
(2)下列情况能说明上述反应已达到平衡状态的是___________ (填标号);反应达到平衡时,H2的转化率为___________ ,平衡时的压强与初始压强的比值为___________ (填最简整数比)。
a.混合气体的密度不再改变
b.n(CO2)∶n(H2)的值不再改变
c.CO2、H2、CH4、H2O同时存在
d.c(CH4):c(H2O)的值不再改变
e.消耗22gCO2的同时生成18gH2O
f.断裂1个H-H键的同时断裂1个C-H键
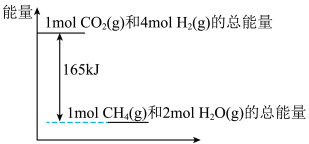
(3)T℃时,上述反应中相关物质的能量如图所示,若该条件下,反应放出33kJ能量,则共消耗___________ L(换算成标准状况下)H2,生成___________ gCH4。
 CH4(g)+2H2O(g)。T℃下,在2L的恒容密闭容器中通入2molCO2和2molH2,发生上述反应,容器内两种气体的物质的量随时间变化的关系如图所示。回答下列问题:
CH4(g)+2H2O(g)。T℃下,在2L的恒容密闭容器中通入2molCO2和2molH2,发生上述反应,容器内两种气体的物质的量随时间变化的关系如图所示。回答下列问题: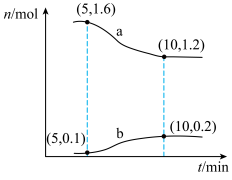
A.升高温度 B.通入He C.通入CO2 D.分离出CH4
(2)下列情况能说明上述反应已达到平衡状态的是
a.混合气体的密度不再改变
b.n(CO2)∶n(H2)的值不再改变
c.CO2、H2、CH4、H2O同时存在
d.c(CH4):c(H2O)的值不再改变
e.消耗22gCO2的同时生成18gH2O
f.断裂1个H-H键的同时断裂1个C-H键
(3)T℃时,上述反应中相关物质的能量如图所示,若该条件下,反应放出33kJ能量,则共消耗
您最近一年使用:0次
2024-05-10更新
|
334次组卷
|
3卷引用:河北省石家庄市第十五中学2023-2024学年高一下学期期中考试化学试题
河北省石家庄市第十五中学2023-2024学年高一下学期期中考试化学试题河南省驻马店市新蔡县第一高级中学2023-2024学年高一下学期5月月考化学试题(已下线)期末检测卷02-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)
名校
解题方法
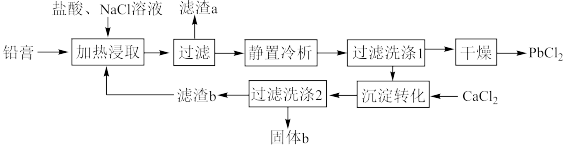
8 . 铅酸蓄电池是全球使用最广泛的化学电源,废铅酸蓄电池铅膏湿法回收铅的工艺研究是当前再生铅回收的重要研究方向,一种利用铅酸蓄电池中铅膏(主要成分为PbSO4、PbO,还含有一些不与流程中试剂反应的物质)制备PbCl2的工艺流程如图所示。请回答下列问题:
②铅酸蓄电池放电时的反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O;
③PbSO4与PbCl2均能与Cl-反应生成[PbCln](n-2)-,[PbCln](n-2)-冷析时转化为PbCl2。
(1)铅酸蓄电池需先放电后再进行“加热浸取”,铅酸蓄电池放电时的负极为___________ (填“Pb”或“PbO2”),正极的电极反应式为___________ ;写出提高“加热浸取”速率的一种方法:___________ 。
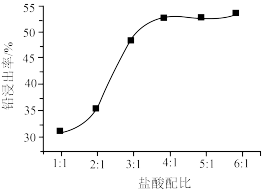
(2)PbO2与盐酸在“加热浸取”时会发生反应生成一种有毒气体和PbCl2,该反应的化学方程式为___________ ;盐酸配比(盐酸配比是指盐酸实际用量与理论用量之比)对铅浸出率的影响如图所示,则工业上一般选择的盐酸配比为___________ ,选择该配比的原因是___________ 。___________ ;“过滤洗涤1”时,可以用___________ (填标号)检验PbCl2是否洗涤干净;“沉淀转化”的目的是降低滤液b中 的浓度,则生成的固体b的主要成分为
的浓度,则生成的固体b的主要成分为___________ (填化学式)。
A.稀硝酸、AgNO3溶液 B.稀硫酸、AgNO3溶液
C.稀硫酸、BaCl2溶液 D.稀盐酸、BaCl2溶液
②铅酸蓄电池放电时的反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O;
③PbSO4与PbCl2均能与Cl-反应生成[PbCln](n-2)-,[PbCln](n-2)-冷析时转化为PbCl2。
(1)铅酸蓄电池需先放电后再进行“加热浸取”,铅酸蓄电池放电时的负极为
(2)PbO2与盐酸在“加热浸取”时会发生反应生成一种有毒气体和PbCl2,该反应的化学方程式为
 的浓度,则生成的固体b的主要成分为
的浓度,则生成的固体b的主要成分为A.稀硝酸、AgNO3溶液 B.稀硫酸、AgNO3溶液
C.稀硫酸、BaCl2溶液 D.稀盐酸、BaCl2溶液
您最近一年使用:0次
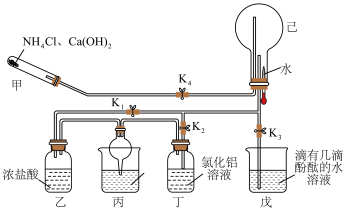
9 . 某化学兴趣小组在教师的指导下,利用如图所示装置(夹持和加热装置已省略)和试剂进行NH3的制备及性质探究的一体化实验。请回答下列问题:___________ ;乙处瓶内观察到的现象为___________ ;丙处烧杯中的试剂为稀硫酸,丙处球形干燥管的作用是___________ 。
(2)一段时间后关闭K1,打开K2,丁处瓶内发生反应的离子方程式为___________ ;继续反应一段时间后,关闭K2、K4,打开K3,挤压胶头滴管,己处圆底烧瓶内能观察到的现象为___________ 。
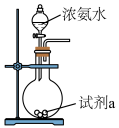
(3)甲装置可以用如图所示装置代替,试剂a可选择___________ (填试剂名称)。氨的催化氧化是工业制硝酸的基础,氨与氧气在催化剂作用下发生反应生成氮的氧化物时,氧化剂和还原剂的物质的量之比为___________ 。
(2)一段时间后关闭K1,打开K2,丁处瓶内发生反应的离子方程式为
(3)甲装置可以用如图所示装置代替,试剂a可选择
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
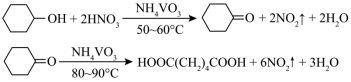
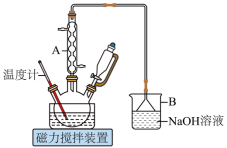
10 . 1,6己二酸是常用的化工原料,在高分子材料、医药、润滑剂的制造等方面都有重要作用。实验室利用图中的装置(夹持装置已省略),以环己醇和硝酸为反应物制备1,6己二酸。反应原理为:
实验步骤如下:
Ⅰ.向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),向恒压滴液漏斗中加入6mL环己醇
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕
Ⅲ.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品
Ⅳ.1,6-己二酸粗产品的提纯
(1)将步骤Ⅲ补充完整:_______ 。步骤Ⅳ提纯方法的名称为_______ 。如图为1,6己二酸在水中的溶解度曲线,80℃时1,6-己二酸水溶液的密度为ρg·mL-1;该溶液的物质的量浓度为_______ 。
| 试剂 | 相对分子质量 | 密度/(g·mL-1) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 环己醇 | 100 | 0.962 | 25.9 | 161.8 | 可溶于水、乙醇、乙醚 |
| 1,6-己二酸 | 146 | 1.360 | 152 | 330.5 | 微溶于冷水,易溶于乙醇 |
| NH4VO3 | 117 | 2.326 | 210(分解) | — | 微溶于冷水,易溶于热水 |
Ⅰ.向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),向恒压滴液漏斗中加入6mL环己醇
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕
Ⅲ.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品
Ⅳ.1,6-己二酸粗产品的提纯
(1)将步骤Ⅲ补充完整:

| A.46.07% | B.57.08% | C.63.03% | D.74.61% |
您最近一年使用:0次



