名校
1 . 化学创造美好生活。下列说法错误的是
A. 可用作葡萄酒的抗氧化剂 可用作葡萄酒的抗氧化剂 |
| B.泡沫灭火器的瓶身内装有硫酸铝溶液和碳酸钠溶液 |
| C.过氧化钠可用作呼吸面罩或潜水艇的供氧剂 |
| D.维生素C与补铁口服液一起服用可促进人体对铁元素的吸收 |
您最近一年使用:0次
2023-08-27更新
|
106次组卷
|
2卷引用:吉林省四平市第一高级中学2023-2024学年高三上学期10月月考化学试题
名校
解题方法
2 . 海水是一个巨大的化学资源宝库。请回答下列问题:
Ⅰ.从海带中提取碘单质
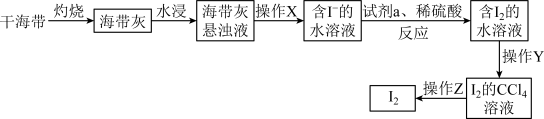
(1)“灼烧”过程需要用到的仪器为酒精灯、三脚架、泥三角、_____ ,“操作X”的名称为_____ 。
(2)若试剂 选择
选择 ,试剂
,试剂 参与反应的离子方程式为
参与反应的离子方程式为_____ ,氧化性:
_____ (填“>”或“<”) 。
。
(3)“操作Y”为萃取分液,萃取后分液时,转移 的
的 溶液至烧杯中的操作是
溶液至烧杯中的操作是_____ 。
Ⅱ.海水提溴:海水→海水淡化→ 氧化→空气吹出→吸收→……→液溴
氧化→空气吹出→吸收→……→液溴
(4)“空气吹出”体现了溴的_____ 性,该步骤的目的是_____ 。
(5)若“吸收”步骤使用浓的 溶液,则反应后产物有
溶液,则反应后产物有 、
、 ,该过程发生反应的离子方程式为
,该过程发生反应的离子方程式为_____ 。若反应后得到 、
、 、
、 的混合溶液,经测定,
的混合溶液,经测定,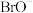 与
与 的物质的量之比为
的物质的量之比为 ,则
,则 与
与 反应时,被还原的溴元素和被氧化的溴元素的物质的量之比
反应时,被还原的溴元素和被氧化的溴元素的物质的量之比_____ 。
Ⅰ.从海带中提取碘单质

(1)“灼烧”过程需要用到的仪器为酒精灯、三脚架、泥三角、
(2)若试剂
 选择
选择 ,试剂
,试剂 参与反应的离子方程式为
参与反应的离子方程式为
 。
。(3)“操作Y”为萃取分液,萃取后分液时,转移
 的
的 溶液至烧杯中的操作是
溶液至烧杯中的操作是Ⅱ.海水提溴:海水→海水淡化→
 氧化→空气吹出→吸收→……→液溴
氧化→空气吹出→吸收→……→液溴(4)“空气吹出”体现了溴的
(5)若“吸收”步骤使用浓的
 溶液,则反应后产物有
溶液,则反应后产物有 、
、 ,该过程发生反应的离子方程式为
,该过程发生反应的离子方程式为 、
、 、
、 的混合溶液,经测定,
的混合溶液,经测定,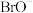 与
与 的物质的量之比为
的物质的量之比为 ,则
,则 与
与 反应时,被还原的溴元素和被氧化的溴元素的物质的量之比
反应时,被还原的溴元素和被氧化的溴元素的物质的量之比
您最近一年使用:0次
解题方法
3 . 复兴号高铁车体材质用到锰元素,锰及其化合物用途广泛。以菱锰矿(主要成分为MnCO3,还含有铁、镍、钴的碳酸盐以及SiO2杂质)为原料生产金属锰和高品位MnCO3的工艺流程如图:

(1)“溶浸”过程中,若其他条件不变,采取下列措施能提高浸出率的有________ (填序号)。
A.适当升高溶浸温度 B.适当加快搅拌速度 C.适当缩短溶浸时间
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为___________ 。

(3)残余在滤渣1中需要回收循环利用的MnO2,可加入葡萄糖和硫酸溶液处理,氧化产物为CO2.写出对应的离子方程式___________ 。
(4)“除杂”步骤所得滤渣2的主要成分除了CoS、NiS以外,还有___________ (填化学式)。
(5)写出“沉锰”的原理为___________ (用离子方程式表示);“沉锰”的关键操作是将反应终点pH控制在7附近,原因是___________ 。
(6)由锰、镍、镓制备的磁性形状记忆型合金中,基态Mn原子的价层电子排布图为___________ ,晶胞结构如图,立方晶胞的边长为 a nm,则该晶体的密度为___________ g•cm-3(NA表示阿伏加德罗常数)。


(1)“溶浸”过程中,若其他条件不变,采取下列措施能提高浸出率的有
A.适当升高溶浸温度 B.适当加快搅拌速度 C.适当缩短溶浸时间
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为

(3)残余在滤渣1中需要回收循环利用的MnO2,可加入葡萄糖和硫酸溶液处理,氧化产物为CO2.写出对应的离子方程式
(4)“除杂”步骤所得滤渣2的主要成分除了CoS、NiS以外,还有
(5)写出“沉锰”的原理为
(6)由锰、镍、镓制备的磁性形状记忆型合金中,基态Mn原子的价层电子排布图为

您最近一年使用:0次
名校
4 . 抗坏血酸(维生素C)是一种重要的抗氧化剂,关于抗坏血酸及其氧化产物的说法不正确的是
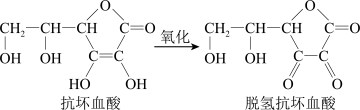
| A.抗坏血酸具有还原性 |
B.抗坏血酸及其氧化产物均能与 反应 反应 |
| C.抗坏血酸是一种安全的食品添加剂 |
D.氧化 抗坏血酸生成脱氢抗坏血酸需要 抗坏血酸生成脱氢抗坏血酸需要 |
您最近一年使用:0次
真题
名校
5 . 化学烫发巧妙利用了头发中蛋白质发生化学反应实现对头发的“定型”,其变化过程示意图如下。下列说法不正确 的是

| A.药剂A具有还原性 |
B.①→②过程若有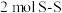 键断裂,则转移 键断裂,则转移 电子 电子 |
C.②→③过程若药剂B是 ,其还原产物为 ,其还原产物为 |
D.化学烫发通过改变头发中某些蛋白质中 键位置来实现头发的定型 键位置来实现头发的定型 |
您最近一年使用:0次
2023-06-21更新
|
5313次组卷
|
21卷引用:吉林省长春外国语学校2022-2023学年高二下学期7月期末考试化学试题
吉林省长春外国语学校2022-2023学年高二下学期7月期末考试化学试题2023年高考浙江卷化学真题(6月)(已下线)2023年高考浙江卷化学真题(6月)变式题(选择题6-10)(已下线)考点05 氧化还原反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)2.4.3氨基酸和蛋白质(课中)-鲁科版选择性必修3山西省阳泉市第一中学校2023-2024学年高二上学期开学考试化学试题新疆石河子第一中学2023-2024学年高三上学期第二次月考化学试题北京理工大学附属中学2023-2024学年高三上学期10月月考化学试题福建泉州培元中学2023-2024学年上学期高三10月月考化学试题(已下线)第5讲 生物大分子 合成高分子湖南省常德市汉寿县第一中学2023-2024学年高三上学期10月月考化学试题海南省海口市琼山华侨中学2023-2024学年高三上学期第二次月考化学试题浙江省湖州市吴兴高级中学2023-2024学年高一上学期12月月考化学试题浙江省宁波市鄞州中学(宁波鄞州蓝青高级中学)2023-2024学年高一上学期12月月考化学学科试题云南省宣威市第六中学2023-2024学年高二上学期11月月考化学试题广东省深圳实验学校高中部2023-2024学年高一上学期第二阶段考试化学试题 江西省宜春市百树学校2023-2024学年高三上学期11月期中考试化学试卷北京市第二中学2023-2024学年高三下学期三模化学试题宁夏回族自治区银川一中2024届高三下学期考前热身训练化学试卷2北京市第二中学2023-2024学年高三下学期模拟测试化学试题 (已下线)第04讲 氧化还原反应的基本概念和规律(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
6 .  是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某
是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某 (Ⅱ)催化剂(用
(Ⅱ)催化剂(用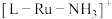 表示)能高效电催化氧化
表示)能高效电催化氧化 合成
合成 ,其反应机理如图所示。
,其反应机理如图所示。
 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某
是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某 (Ⅱ)催化剂(用
(Ⅱ)催化剂(用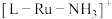 表示)能高效电催化氧化
表示)能高效电催化氧化 合成
合成 ,其反应机理如图所示。
,其反应机理如图所示。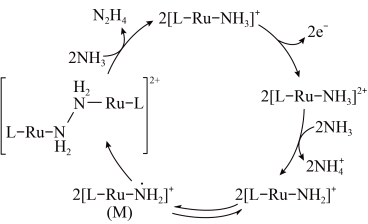
A. (Ⅱ)被氧化至 (Ⅱ)被氧化至 (Ⅲ)后,配体 (Ⅲ)后,配体 失去质子能力增强 失去质子能力增强 |
B.M中 的化合价为 的化合价为 |
| C.该过程有非极性键的形成 |
D.该过程的总反应式: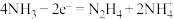 |
您最近一年使用:0次
2023-06-16更新
|
9743次组卷
|
18卷引用:吉林省长春外国语学校2023-2024学年高三上学期开学考试化学试题
吉林省长春外国语学校2023-2024学年高三上学期开学考试化学试题2023年高考湖南卷化学真题(已下线)专题10 物质的反应及转化(已下线)专题10 物质的反应及转化(已下线)专题10 物质的反应及转化(已下线)第3讲 氧化还原反应(已下线)2023年湖南卷高考真题变式题(选择题11-14)浙江省名校协作体2023-2024学年高三上学期开学适应性考试化学试题河北省石家庄市正定中学2022- 2023学年高二下学期期末考试化学试题(已下线)专题09 化学反应中的热效应与反应机理-2023年高考化学真题题源解密(全国通用)(已下线)考点1 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)湖北省华中师范大学第一附属中学2023-2024学年高二上学期10月月考化学试题陕西省西安中学2023-2024学年高三(实验版)上学期12月练考理科综合试题(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题02 化学反应速率-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)江西省宜春市丰城市第九中学2023-2024学年高一上学期1月期末化学试题(已下线)专题05 化学反应与能量(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)浙江省杭州市西湖高级中学2024届高三下学期5月模拟预测化学试题
7 . 某工厂采用如下工艺处理镍钴矿硫酸浸取液(含 和
和 )。实现镍、钴、镁元素的回收。
)。实现镍、钴、镁元素的回收。
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为_______ (答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸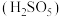 ,
, 中过氧键的数目为
中过氧键的数目为_______ 。
(3)“氧化”中,用石灰乳调节 ,
, 被
被 氧化为
氧化为 ,该反应的离子方程式为
,该反应的离子方程式为_______ ( 的电离第一步完全,第二步微弱);滤渣的成分为
的电离第一步完全,第二步微弱);滤渣的成分为 、
、_______ (填化学式)。
(4)“氧化”中保持空气通入速率不变, (Ⅱ)氧化率与时间的关系如下。
(Ⅱ)氧化率与时间的关系如下。 体积分数为
体积分数为_______ 时, (Ⅱ)氧化速率最大;继续增大
(Ⅱ)氧化速率最大;继续增大 体积分数时,
体积分数时, (Ⅱ)氧化速率减小的原因是
(Ⅱ)氧化速率减小的原因是_______ 。
 (Ⅱ)在空气中可被氧化成
(Ⅱ)在空气中可被氧化成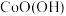 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(6)“沉镁”中为使 沉淀完全
沉淀完全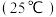 ,需控制
,需控制 不低于
不低于_______ (精确至0.1)。
 和
和 )。实现镍、钴、镁元素的回收。
)。实现镍、钴、镁元素的回收。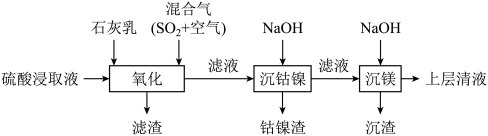
| 物质 |  | 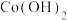 |  |  |
 |  |  |  | 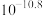 |
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸
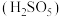 ,
, 中过氧键的数目为
中过氧键的数目为(3)“氧化”中,用石灰乳调节
 ,
, 被
被 氧化为
氧化为 ,该反应的离子方程式为
,该反应的离子方程式为 的电离第一步完全,第二步微弱);滤渣的成分为
的电离第一步完全,第二步微弱);滤渣的成分为 、
、(4)“氧化”中保持空气通入速率不变,
 (Ⅱ)氧化率与时间的关系如下。
(Ⅱ)氧化率与时间的关系如下。 体积分数为
体积分数为 (Ⅱ)氧化速率最大;继续增大
(Ⅱ)氧化速率最大;继续增大 体积分数时,
体积分数时, (Ⅱ)氧化速率减小的原因是
(Ⅱ)氧化速率减小的原因是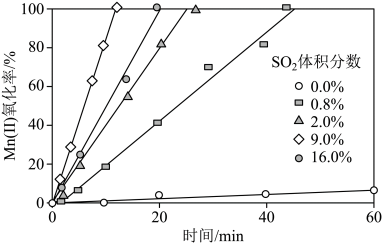
 (Ⅱ)在空气中可被氧化成
(Ⅱ)在空气中可被氧化成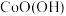 ,该反应的化学方程式为
,该反应的化学方程式为(6)“沉镁”中为使
 沉淀完全
沉淀完全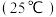 ,需控制
,需控制 不低于
不低于
您最近一年使用:0次
2023-06-13更新
|
12474次组卷
|
20卷引用:吉林省通化市梅河口市第五中学2023-2024学年高二上学期1月期末化学试题
吉林省通化市梅河口市第五中学2023-2024学年高二上学期1月期末化学试题2023年高考辽宁卷化学真题(已下线)T16-工业流程题(已下线)2023年高考化学真题完全解读(辽宁卷)(已下线)专题18 工艺流程题(已下线)2023年高考山东卷化学真题变式题(工业流程题)(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)江苏省华罗庚中学2023-2024学年高三夏令营学习能力测试化学试题山西省三重教育联盟2023-2024学年高三上学期9月联考化学试题四川省成都市第七中学2023-2024学年高三上学期入学考试理综化学试题(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)江苏省镇江市丹阳市吕叔湘中学2023-2024学年高三上学期10月月考化学试题辽宁省葫芦岛市第一高级中学2023-2024学年高二上学期化学期末复习提升卷福建泉州科技中学2022-2023学年高二下学期期末考化学试题甘肃省白银市会宁县第四中学2023-2024学年高三上学期第三次月考化学试题(已下线)测试辽宁化学 请勿下载
名校
解题方法
8 . 近日,中国科学院化学物理研究所李灿院士团队揭示催化剂(Co3O4)上催化水氧化产氧历程如图所示(注明: s、ms、μs表示秒、毫秒、微秒)。下列叙述错误的是
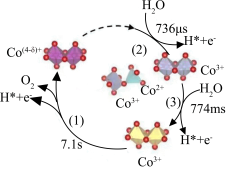

| A.第(1)步反应为总反应的控速反应 |
| B.Co原子价电子排布式为3d74s2,位于周期表中第四周期第Ⅷ族 |
| C.从总反应看,每生成标况22. 4LO2必转移3mol 电子 |
| D.该反应过程中三步都断裂了极性键 |
您最近一年使用:0次
名校
9 . 现有下列七种物质:① ②过氧化钠③氧化铁④
②过氧化钠③氧化铁④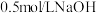 溶液⑤碳酸氢钠⑥
溶液⑤碳酸氢钠⑥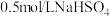 溶液⑦次氯酸钠。请根据上述物质回答下列问题:
溶液⑦次氯酸钠。请根据上述物质回答下列问题:
(1)在上述物质中属于电解质的有______________ (填①~⑦序号)
(2)含有 氧原子的②与足量①反应,产生气体在标准状况下的体积为
氧原子的②与足量①反应,产生气体在标准状况下的体积为_______ L。
(3)写出③物质的一种用途_____________________ 。
(4)某同学帮助水质检测站配制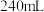 ④溶液以备使用。
④溶液以备使用。
①该同学应用托盘天平称取NaOH固体_______ g。
②配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、_______ 。
③定容时仰视刻度线,则所配制的溶液的浓度会_______ (填“偏高”、“偏低”、“不变”)。
(5)⑤⑥两种溶液混合可以发生反应,离子方程式为_____________________
(6)废水脱氮工艺有一种方法是在废水中加入过量⑦使 完全转化为
完全转化为 ,此方法可用离子方程式表示为:
,此方法可用离子方程式表示为: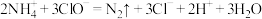 。用单线桥法在离子方程式上标出电子转移的方向和数目
。用单线桥法在离子方程式上标出电子转移的方向和数目_______ ;该反应中氧化剂与还原剂的物质的量之比为_______ 。
 ②过氧化钠③氧化铁④
②过氧化钠③氧化铁④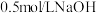 溶液⑤碳酸氢钠⑥
溶液⑤碳酸氢钠⑥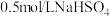 溶液⑦次氯酸钠。请根据上述物质回答下列问题:
溶液⑦次氯酸钠。请根据上述物质回答下列问题:(1)在上述物质中属于电解质的有
(2)含有
 氧原子的②与足量①反应,产生气体在标准状况下的体积为
氧原子的②与足量①反应,产生气体在标准状况下的体积为(3)写出③物质的一种用途
(4)某同学帮助水质检测站配制
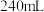 ④溶液以备使用。
④溶液以备使用。①该同学应用托盘天平称取NaOH固体
②配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、
③定容时仰视刻度线,则所配制的溶液的浓度会
(5)⑤⑥两种溶液混合可以发生反应,离子方程式为
(6)废水脱氮工艺有一种方法是在废水中加入过量⑦使
 完全转化为
完全转化为 ,此方法可用离子方程式表示为:
,此方法可用离子方程式表示为: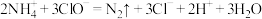 。用单线桥法在离子方程式上标出电子转移的方向和数目
。用单线桥法在离子方程式上标出电子转移的方向和数目
您最近一年使用:0次
2023-03-27更新
|
467次组卷
|
4卷引用:吉林省辽源市田家炳高中友好学校七十六届期末联考2023-2024学年高一上学期1月期末化学试题
吉林省辽源市田家炳高中友好学校七十六届期末联考2023-2024学年高一上学期1月期末化学试题辽宁省沈阳市五校协作体2022-2023学年高一上学期期末考试化学试题 (已下线)专题03 氧化还原反应-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)河南省南阳市社旗县第一高级中学2023-2024学年高三上学期1月月考化学试题
名校
解题方法
10 . 为探究“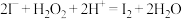 ”碘离子氧化过程进行如下实验.
”碘离子氧化过程进行如下实验.
下列说法不正确的是
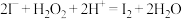 ”碘离子氧化过程进行如下实验.
”碘离子氧化过程进行如下实验.编号 | 1 | 2 |
实验内容 |
|
|
实验现象 | 随着液体不断滴入,产生大量气体;溶液变黄并不断加深至棕黄色后又变浅 | 随着液体不断滴入,溶液变黄,摇匀后又褪色,不断重复直至析出紫色沉淀 |
A.实验1中溶液变浅是因为 |
B.实验2中出现紫色沉淀是因为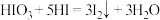 |
C.实验1中产生大量气体的原因是 被氧化的过程大量放热 被氧化的过程大量放热 |
| D.实验2相较于实验1,可节约H2O2用量且有利于反应终点观察 |
您最近一年使用:0次
2023-03-08更新
|
801次组卷
|
3卷引用:2024届吉林省延边州高三教学质量检测(一模)化学试题





