名校
解题方法
1 . 乙醇是燃料,也是重要的有机化工原料,二氧化碳加氢还原制乙醇已成为研究热点,相关的反应如下:
反应i:
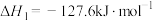
反应ii: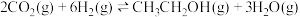
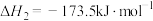
反应iii: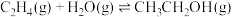
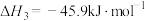
请回答下列问题:
(1)已知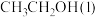 的燃烧热(
的燃烧热( )为
)为 ,表示
,表示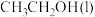 燃烧热的热化学方程式为
燃烧热的热化学方程式为________ 。
(2)在一定温度下,向2L恒容密闭容器中充入 和
和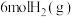 ,在某催化剂作用下发生上述反应,测得含碳元素物质占比[如
,在某催化剂作用下发生上述反应,测得含碳元素物质占比[如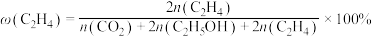 ]与时间的关系如图所示。
]与时间的关系如图所示。
①表示乙烯占比的曲线是________ (填“a”“b”或“c”)。
②若选择对反应i催化效果更好的催化剂,则A点可能移向________ (填“E”“E点上方”或“E点下方”)。
③已知C点、D点均为平衡点,则反应iii的平衡常数K=________ (保留小数点后一位)。
④设反应i和反应ii的化学平衡常数分别为 、
、 ,适当升温后,
,适当升温后,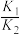
________ (填“增大”“减小”或“无法判断”),理由是________ 。
(3)近日,中国科学技术大学某课题组以Pd掺杂的 原子层为原型,在温和条件下,通过
原子层为原型,在温和条件下,通过 光还原合成乙酸,获得选择性近100%的好成绩。草酸钴是制备钻的氧化物的重要原料,二水合草酸钴(
光还原合成乙酸,获得选择性近100%的好成绩。草酸钴是制备钻的氧化物的重要原料,二水合草酸钴( )(
)(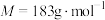 )在空气中受热时固体质量随温度变化的曲线如图所示。
)在空气中受热时固体质量随温度变化的曲线如图所示。________ ,CD段发生反应的化学方程式为________ 。
反应i:

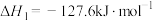
反应ii:
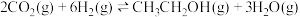
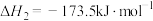
反应iii:
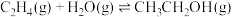
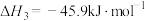
请回答下列问题:
(1)已知
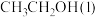 的燃烧热(
的燃烧热( )为
)为 ,表示
,表示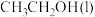 燃烧热的热化学方程式为
燃烧热的热化学方程式为(2)在一定温度下,向2L恒容密闭容器中充入
 和
和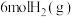 ,在某催化剂作用下发生上述反应,测得含碳元素物质占比[如
,在某催化剂作用下发生上述反应,测得含碳元素物质占比[如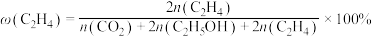 ]与时间的关系如图所示。
]与时间的关系如图所示。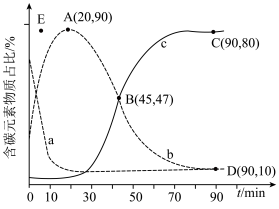
①表示乙烯占比的曲线是
②若选择对反应i催化效果更好的催化剂,则A点可能移向
③已知C点、D点均为平衡点,则反应iii的平衡常数K=
④设反应i和反应ii的化学平衡常数分别为
 、
、 ,适当升温后,
,适当升温后,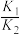
(3)近日,中国科学技术大学某课题组以Pd掺杂的
 原子层为原型,在温和条件下,通过
原子层为原型,在温和条件下,通过 光还原合成乙酸,获得选择性近100%的好成绩。草酸钴是制备钻的氧化物的重要原料,二水合草酸钴(
光还原合成乙酸,获得选择性近100%的好成绩。草酸钴是制备钻的氧化物的重要原料,二水合草酸钴( )(
)(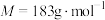 )在空气中受热时固体质量随温度变化的曲线如图所示。
)在空气中受热时固体质量随温度变化的曲线如图所示。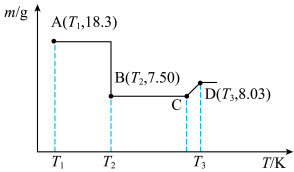
您最近一年使用:0次
2 . 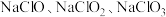 等含氯化合物在生活中有着重要应用。
等含氯化合物在生活中有着重要应用。
(1) 的制备。将
的制备。将 通入
通入 溶液中反应生成
溶液中反应生成 ,该反应为放热反应,温度过高会有副产物
,该反应为放热反应,温度过高会有副产物 生成。
生成。
①提高单位时间内 的产率,可以采取的可行措施为
的产率,可以采取的可行措施为______ 序号)。
A.适当减缓通入 速率 B.充分搅拌浆料 C.加水稀释
速率 B.充分搅拌浆料 C.加水稀释 溶液
溶液
②反应结束后,测得溶液中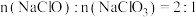 ,则该反应的化学方程式为
,则该反应的化学方程式为______ ;
③用 溶液吸收硝酸尾气,可提高尾气中
溶液吸收硝酸尾气,可提高尾气中 的去除率。其他条件相同,
的去除率。其他条件相同, 转化为
转化为 的转化率随
的转化率随 溶液初始
溶液初始 (用稀盐酸调节)的变化如图所示。
(用稀盐酸调节)的变化如图所示。 溶液的初始
溶液的初始 越小,
越小, 转化率越高的原因是
转化率越高的原因是______ ; 的制备。
的制备。 是一种高效的消毒剂,其生产工艺流程如下。
是一种高效的消毒剂,其生产工艺流程如下。 和
和 中
中 的化合价分别为
的化合价分别为______ 、______ ;
②“吸收”时, 不能用
不能用 代替的理由是
代替的理由是______ ;
③实验室可以利用 与
与 反应可以制得
反应可以制得 。若生成
。若生成 ,反应中转移的电子数为
,反应中转移的电子数为______ 。
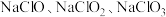 等含氯化合物在生活中有着重要应用。
等含氯化合物在生活中有着重要应用。(1)
 的制备。将
的制备。将 通入
通入 溶液中反应生成
溶液中反应生成 ,该反应为放热反应,温度过高会有副产物
,该反应为放热反应,温度过高会有副产物 生成。
生成。①提高单位时间内
 的产率,可以采取的可行措施为
的产率,可以采取的可行措施为A.适当减缓通入
 速率 B.充分搅拌浆料 C.加水稀释
速率 B.充分搅拌浆料 C.加水稀释 溶液
溶液②反应结束后,测得溶液中
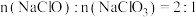 ,则该反应的化学方程式为
,则该反应的化学方程式为③用
 溶液吸收硝酸尾气,可提高尾气中
溶液吸收硝酸尾气,可提高尾气中 的去除率。其他条件相同,
的去除率。其他条件相同, 转化为
转化为 的转化率随
的转化率随 溶液初始
溶液初始 (用稀盐酸调节)的变化如图所示。
(用稀盐酸调节)的变化如图所示。 溶液的初始
溶液的初始 越小,
越小, 转化率越高的原因是
转化率越高的原因是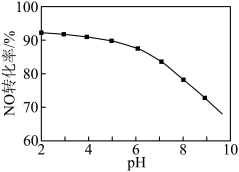
 的制备。
的制备。 是一种高效的消毒剂,其生产工艺流程如下。
是一种高效的消毒剂,其生产工艺流程如下。
 和
和 中
中 的化合价分别为
的化合价分别为②“吸收”时,
 不能用
不能用 代替的理由是
代替的理由是③实验室可以利用
 与
与 反应可以制得
反应可以制得 。若生成
。若生成 ,反应中转移的电子数为
,反应中转移的电子数为
您最近一年使用:0次
2024-05-29更新
|
130次组卷
|
2卷引用:江苏省连云港市东海县2023-2024学年高一下学期期中考试化学试题
3 . 肼 常用作火箭燃料,燃烧
常用作火箭燃料,燃烧 肼生成液态水时放出
肼生成液态水时放出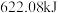 热量,可由
热量,可由 与
与 反应制备;下列变化的方程式表示正确的是
反应制备;下列变化的方程式表示正确的是
 常用作火箭燃料,燃烧
常用作火箭燃料,燃烧 肼生成液态水时放出
肼生成液态水时放出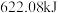 热量,可由
热量,可由 与
与 反应制备;下列变化的方程式表示正确的是
反应制备;下列变化的方程式表示正确的是A.次氯酸在水中的电离: |
B. 与 与 反应制备肼: 反应制备肼: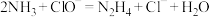 |
C.肼的燃烧: |
D. 与 与 的水溶液反应制备硒: 的水溶液反应制备硒: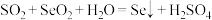 |
您最近一年使用:0次
4 . 乙二胺四乙酸铁钠(化学式 )是一种重要补铁剂,某小组以铁屑为原料制备
)是一种重要补铁剂,某小组以铁屑为原料制备 并测定其含量。
并测定其含量。
已知:① 是一种配合物,微溶于乙醇,
是一种配合物,微溶于乙醇, 时水中的溶解度为
时水中的溶解度为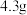 。
。
②乙二胺四乙酸( ,用
,用 表示)是一种弱酸。
表示)是一种弱酸。
Ⅰ.制备
实验室用铁屑制备 的主要流程如下:
的主要流程如下:___________
A.升高温度 B.加快搅拌速率 C.缩短浸取时间
(2)向酸浸所得滤液中通入足量 ,过程中浓度减少的离子有
,过程中浓度减少的离子有___________ (填离子符号)。
(3)“制备”步骤,向氧化所得的 溶液中加入一定量
溶液中加入一定量
 ,控制反应温度为
,控制反应温度为 ,加入
,加入 溶液调节
溶液调节 为5,搅拌,直到溶液中出现少量浑浊。其中发生的反应为
为5,搅拌,直到溶液中出现少量浑浊。其中发生的反应为 。
。
①从反应后的混合物中获得较高产率的 粗品的实验操作是,
粗品的实验操作是,___________ ,过滤,水洗,干燥。检验 是否洗净的试剂是
是否洗净的试剂是___________
②保持其他条件不变,乙二胺四乙酸铁钠的产率随反应液 的变化如图1所示。
的变化如图1所示。 过低或过高产品产率均减小的主要原因是
过低或过高产品产率均减小的主要原因是___________ 。
样品中乙二胺四乙酸铁钠纯度可用 标准溶液滴定。原理是在
标准溶液滴定。原理是在 为
为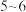 发生反应:
发生反应: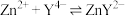 ,二甲酚橙作指示剂,滴定终点时溶液由紫红色变黄色。
,二甲酚橙作指示剂,滴定终点时溶液由紫红色变黄色。
(4)补充完整实验方案:准确称取 样品,溶于一定量的蒸馏水,加入掩蔽剂排除
样品,溶于一定量的蒸馏水,加入掩蔽剂排除 干扰,得到待测溶液
干扰,得到待测溶液 ,将溶液
,将溶液 完全转移到
完全转移到 容量瓶中定容;按规定操作分别将
容量瓶中定容;按规定操作分别将 标准溶液和待测溶液
标准溶液和待测溶液 装入如图2所示的滴定管中:
装入如图2所示的滴定管中:___________ 。
 )是一种重要补铁剂,某小组以铁屑为原料制备
)是一种重要补铁剂,某小组以铁屑为原料制备 并测定其含量。
并测定其含量。已知:①
 是一种配合物,微溶于乙醇,
是一种配合物,微溶于乙醇, 时水中的溶解度为
时水中的溶解度为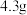 。
。②乙二胺四乙酸(
 ,用
,用 表示)是一种弱酸。
表示)是一种弱酸。Ⅰ.制备

实验室用铁屑制备
 的主要流程如下:
的主要流程如下:
A.升高温度 B.加快搅拌速率 C.缩短浸取时间
(2)向酸浸所得滤液中通入足量
 ,过程中浓度减少的离子有
,过程中浓度减少的离子有(3)“制备”步骤,向氧化所得的
 溶液中加入一定量
溶液中加入一定量
 ,控制反应温度为
,控制反应温度为 ,加入
,加入 溶液调节
溶液调节 为5,搅拌,直到溶液中出现少量浑浊。其中发生的反应为
为5,搅拌,直到溶液中出现少量浑浊。其中发生的反应为 。
。①从反应后的混合物中获得较高产率的
 粗品的实验操作是,
粗品的实验操作是, 是否洗净的试剂是
是否洗净的试剂是②保持其他条件不变,乙二胺四乙酸铁钠的产率随反应液
 的变化如图1所示。
的变化如图1所示。 过低或过高产品产率均减小的主要原因是
过低或过高产品产率均减小的主要原因是
样品中乙二胺四乙酸铁钠纯度可用
 标准溶液滴定。原理是在
标准溶液滴定。原理是在 为
为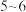 发生反应:
发生反应: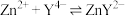 ,二甲酚橙作指示剂,滴定终点时溶液由紫红色变黄色。
,二甲酚橙作指示剂,滴定终点时溶液由紫红色变黄色。(4)补充完整实验方案:准确称取
 样品,溶于一定量的蒸馏水,加入掩蔽剂排除
样品,溶于一定量的蒸馏水,加入掩蔽剂排除 干扰,得到待测溶液
干扰,得到待测溶液 ,将溶液
,将溶液 完全转移到
完全转移到 容量瓶中定容;按规定操作分别将
容量瓶中定容;按规定操作分别将 标准溶液和待测溶液
标准溶液和待测溶液 装入如图2所示的滴定管中:
装入如图2所示的滴定管中:
您最近一年使用:0次
解题方法
5 . 用软锰矿( ,含
,含 、
、 杂质)和方铅矿(PbS含少量FeS)为原料制备电极材料
杂质)和方铅矿(PbS含少量FeS)为原料制备电极材料 的工艺流程如下:
的工艺流程如下: ,
,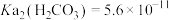 ,
,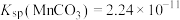
有关离子沉淀时的pH:
回答下列问题:
(1)“滤渣1”除了S、 外,还有
外,还有___________ (填化学式)。
(2)“试剂a”可以选用___________ (填标号),“除杂”应调pH范围是___________ 。
A.NaClO B. C.
C. D.NaOH
D.NaOH
(3)“沉锰”时发生反应的离子方程式为___________ 。
(4)“沉锰”后上层清液中
___________ 。
(5)“焙烧”时发生反应的化学方程式为___________ 。
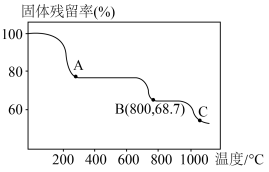
(6)碳酸锰在空气中加热,固体残留率随温度变化如图。碳酸锰在300℃时已完全脱碳,则B点对应的物质的化学式为___________ 。
 ,含
,含 、
、 杂质)和方铅矿(PbS含少量FeS)为原料制备电极材料
杂质)和方铅矿(PbS含少量FeS)为原料制备电极材料 的工艺流程如下:
的工艺流程如下: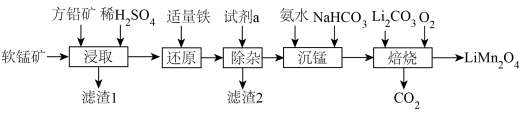
 ,
,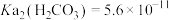 ,
,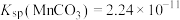
有关离子沉淀时的pH:
 |  |  |  | |
| 开始沉淀时 | 8.3 | 7.6 | 2.7 | 3.0 |
| 沉淀完全时 | 9.8 | 9.6 | 3.7 | 4.7 |
(1)“滤渣1”除了S、
 外,还有
外,还有(2)“试剂a”可以选用
A.NaClO B.
 C.
C. D.NaOH
D.NaOH(3)“沉锰”时发生反应的离子方程式为
(4)“沉锰”后上层清液中

(5)“焙烧”时发生反应的化学方程式为
(6)碳酸锰在空气中加热,固体残留率随温度变化如图。碳酸锰在300℃时已完全脱碳,则B点对应的物质的化学式为
您最近一年使用:0次
2024-05-28更新
|
253次组卷
|
2卷引用:江苏省部分学校2024届高三下学期高考模拟化学试题
名校
6 . 二氧化铈( )是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含
)是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备
等)为原料制备 ,其工艺流程如图所示:
,其工艺流程如图所示:
(1)“焙烧”时,通入空气的主要目的是_________________ 。
(2)滤渣的主要成分是___________________ (填化学式)。
(3)“还原、脱氟”时,先加入硫脲(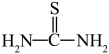 ),目的是将溶液中的
),目的是将溶液中的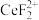 还原为
还原为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:_________________ [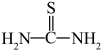 被氧化为
被氧化为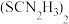 ,生成物还有HF和
,生成物还有HF和 ]。
]。
(4)“沉铈”时反应的离子方程式为__________________ 。若用 溶液代替
溶液代替 溶液,产生的后果是
溶液,产生的后果是________________ 。
(5)若常温下,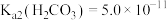 ,
,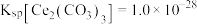 ,
, 恰好沉淀完全
恰好沉淀完全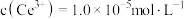 ,此时测得溶液的
,此时测得溶液的 ,则溶液中
,则溶液中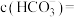
_____________  。
。
(6)二氧化铈作为一种SCR脱硝催化剂,能在 和
和 之间改变氧化状态,将
之间改变氧化状态,将 氧化为
氧化为 ,并引起氧空位的形成,得到新的铈氧化物
,并引起氧空位的形成,得到新的铈氧化物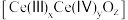 。铈氧化物发生的可能变化如图所示。当
。铈氧化物发生的可能变化如图所示。当
 氧化标准状况下
氧化标准状况下 NO后,生成新的铈氧化物中x、y、z的最简整数比为
NO后,生成新的铈氧化物中x、y、z的最简整数比为____________ 。
 )是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含
)是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备
等)为原料制备 ,其工艺流程如图所示:
,其工艺流程如图所示: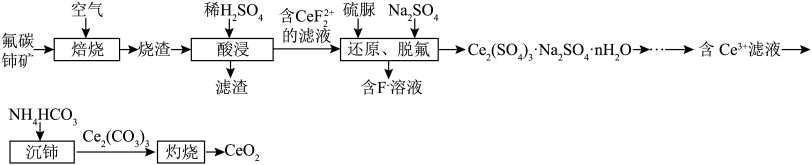
(1)“焙烧”时,通入空气的主要目的是
(2)滤渣的主要成分是
(3)“还原、脱氟”时,先加入硫脲(
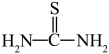 ),目的是将溶液中的
),目的是将溶液中的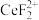 还原为
还原为 ,写出该反应的离子方程式:
,写出该反应的离子方程式: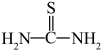 被氧化为
被氧化为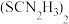 ,生成物还有HF和
,生成物还有HF和 ]。
]。(4)“沉铈”时反应的离子方程式为
 溶液代替
溶液代替 溶液,产生的后果是
溶液,产生的后果是(5)若常温下,
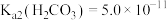 ,
,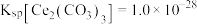 ,
, 恰好沉淀完全
恰好沉淀完全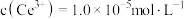 ,此时测得溶液的
,此时测得溶液的 ,则溶液中
,则溶液中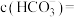
 。
。(6)二氧化铈作为一种SCR脱硝催化剂,能在
 和
和 之间改变氧化状态,将
之间改变氧化状态,将 氧化为
氧化为 ,并引起氧空位的形成,得到新的铈氧化物
,并引起氧空位的形成,得到新的铈氧化物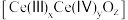 。铈氧化物发生的可能变化如图所示。当
。铈氧化物发生的可能变化如图所示。当
 氧化标准状况下
氧化标准状况下 NO后,生成新的铈氧化物中x、y、z的最简整数比为
NO后,生成新的铈氧化物中x、y、z的最简整数比为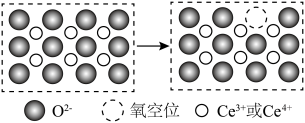
您最近一年使用:0次
2024-05-27更新
|
128次组卷
|
3卷引用:江苏省部分学校2024届高三下学期全真模拟测化学试卷
解题方法
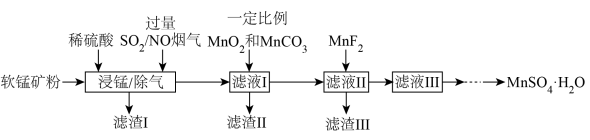
7 . 燃煤烟气中含有大量 和NO。某实验室模拟“软锰矿浆同步脱硫脱硝技术”并制备
和NO。某实验室模拟“软锰矿浆同步脱硫脱硝技术”并制备 ,部分流程如下。
,部分流程如下。
已知:①软锰矿(主要成分为 ,另含有少量
,另含有少量 、CaO、
、CaO、 等杂质)。
等杂质)。
② ;
;
③
 发生的主要化学方程式为
发生的主要化学方程式为________ 。
②滤渣Ⅰ的主要成分为________ 。(写化学式)
(2)“除气”过程,烟气中混入一定量 可提高NO脱除率,其可能的原因是:
可提高NO脱除率,其可能的原因是:________ 。
(3)“滤液Ⅰ”中加入等物质的量 和
和 ,反应的离子方程式为:
,反应的离子方程式为:________ 。
(4)“滤液Ⅱ”中用 可除去
可除去 ,结合反应方程式和定量计算说明原因
,结合反应方程式和定量计算说明原因________ 。(当反应平衡常数大于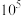 时,可认为反应完全)。
时,可认为反应完全)。
(5)“滤液Ⅲ”可制得 。已知:
。已知:
①在烟气吸收过程中,除生成 外,还容易产生连二硫酸锰(
外,还容易产生连二硫酸锰( ),当温度
),当温度
超过35℃, 会快速分解为
会快速分解为 和
和 。
。
②部分锰盐在不同温度下的溶解度和析出晶体的组成如图。 的实验方案为:
的实验方案为:________ 。(须使用的试剂为: L NaOH溶液,无水乙醇)
L NaOH溶液,无水乙醇)
 和NO。某实验室模拟“软锰矿浆同步脱硫脱硝技术”并制备
和NO。某实验室模拟“软锰矿浆同步脱硫脱硝技术”并制备 ,部分流程如下。
,部分流程如下。已知:①软锰矿(主要成分为
 ,另含有少量
,另含有少量 、CaO、
、CaO、 等杂质)。
等杂质)。②
 ;
;
③

 发生的主要化学方程式为
发生的主要化学方程式为②滤渣Ⅰ的主要成分为
(2)“除气”过程,烟气中混入一定量
 可提高NO脱除率,其可能的原因是:
可提高NO脱除率,其可能的原因是:(3)“滤液Ⅰ”中加入等物质的量
 和
和 ,反应的离子方程式为:
,反应的离子方程式为:(4)“滤液Ⅱ”中用
 可除去
可除去 ,结合反应方程式和定量计算说明原因
,结合反应方程式和定量计算说明原因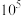 时,可认为反应完全)。
时,可认为反应完全)。(5)“滤液Ⅲ”可制得
 。已知:
。已知:①在烟气吸收过程中,除生成
 外,还容易产生连二硫酸锰(
外,还容易产生连二硫酸锰( ),当温度
),当温度超过35℃,
 会快速分解为
会快速分解为 和
和 。
。②部分锰盐在不同温度下的溶解度和析出晶体的组成如图。

 的实验方案为:
的实验方案为: L NaOH溶液,无水乙醇)
L NaOH溶液,无水乙醇)
您最近一年使用:0次
8 . 已知 晶体在加热条件下发生如下反应:
晶体在加热条件下发生如下反应: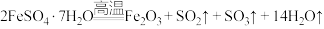 (已知:
(已知: 和
和 的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
 晶体在加热条件下发生如下反应:
晶体在加热条件下发生如下反应: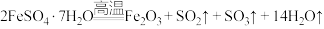 (已知:
(已知: 和
和 的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
| A.仪器的连接顺序为a、f(或g)、g(或f)、h、i、d、e、b |
B.装置C中的X溶液为 溶液 溶液 |
| C.装置B的作用为处理尾气 |
D.反应中每生成 ,转移2mol电子 ,转移2mol电子 |
您最近一年使用:0次
解题方法
9 . 某化学兴趣小组为探究 的性质,按下图装置进行实验。回答下列问题:
的性质,按下图装置进行实验。回答下列问题:_______ ,A中发生反应的化学方程式为_______ 。
(2)B中出现淡黄色沉淀,则证明 具有
具有______ 性,发生反应的化学方程式为______ 。
(3)装置B、C、D中能够证明 具有还原性的是
具有还原性的是____ (填字母),观察到的现象为____ 。
(4)当反应进行一段时间后,装置E中最终生成少量红色沉淀,为确定红色沉淀的成分,进行以下实验:_______ (填“只有Cu”“只有 ”或“Cu和
”或“Cu和 的混合物”);E中出现少量红色沉淀的总反应的离子方程式为
的混合物”);E中出现少量红色沉淀的总反应的离子方程式为_______ 。
(5)在三颈烧瓶中加入 溶液和
溶液和 溶液,在加热条件下通入
溶液,在加热条件下通入 充分反应生成
充分反应生成 ,将含
,将含 的溶液进行结晶,可得到
的溶液进行结晶,可得到 晶体样品。用
晶体样品。用 溶液测定样品的纯度,步骤如下:称取5.00g样品,用蒸馏水溶解,配成100mL样品溶液。取
溶液测定样品的纯度,步骤如下:称取5.00g样品,用蒸馏水溶解,配成100mL样品溶液。取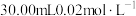 的
的 溶液,用稀硫酸酸化后加入过量KI溶液,然后滴加样品溶液至溶液呈淡黄绿色,再加入淀粉溶液作指示剂,继续滴加样品溶液,蓝色恰好完全消失时,共消耗样品溶液20.00mL。
溶液,用稀硫酸酸化后加入过量KI溶液,然后滴加样品溶液至溶液呈淡黄绿色,再加入淀粉溶液作指示剂,继续滴加样品溶液,蓝色恰好完全消失时,共消耗样品溶液20.00mL。
已知实验过程中发生的反应的计算关系式为: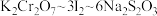 。则该样品的纯度为
。则该样品的纯度为_______ %(保留三位有效数字)。
 的性质,按下图装置进行实验。回答下列问题:
的性质,按下图装置进行实验。回答下列问题: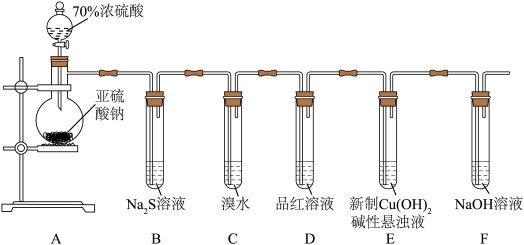
(2)B中出现淡黄色沉淀,则证明
 具有
具有(3)装置B、C、D中能够证明
 具有还原性的是
具有还原性的是(4)当反应进行一段时间后,装置E中最终生成少量红色沉淀,为确定红色沉淀的成分,进行以下实验:

 ”或“Cu和
”或“Cu和 的混合物”);E中出现少量红色沉淀的总反应的离子方程式为
的混合物”);E中出现少量红色沉淀的总反应的离子方程式为(5)在三颈烧瓶中加入
 溶液和
溶液和 溶液,在加热条件下通入
溶液,在加热条件下通入 充分反应生成
充分反应生成 ,将含
,将含 的溶液进行结晶,可得到
的溶液进行结晶,可得到 晶体样品。用
晶体样品。用 溶液测定样品的纯度,步骤如下:称取5.00g样品,用蒸馏水溶解,配成100mL样品溶液。取
溶液测定样品的纯度,步骤如下:称取5.00g样品,用蒸馏水溶解,配成100mL样品溶液。取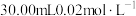 的
的 溶液,用稀硫酸酸化后加入过量KI溶液,然后滴加样品溶液至溶液呈淡黄绿色,再加入淀粉溶液作指示剂,继续滴加样品溶液,蓝色恰好完全消失时,共消耗样品溶液20.00mL。
溶液,用稀硫酸酸化后加入过量KI溶液,然后滴加样品溶液至溶液呈淡黄绿色,再加入淀粉溶液作指示剂,继续滴加样品溶液,蓝色恰好完全消失时,共消耗样品溶液20.00mL。已知实验过程中发生的反应的计算关系式为:
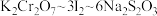 。则该样品的纯度为
。则该样品的纯度为
您最近一年使用:0次
解题方法
10 . “价—类”二维图是学习元素化合物的一种好方法。硫或氮及其化合物的部分“价—类”二维图如图所示,回答下列问题: ,写出F和G的稀溶液反应生成H的化学方程式(还原产物为+2价氧化物):
,写出F和G的稀溶液反应生成H的化学方程式(还原产物为+2价氧化物):_______ 。
(2)若B为 ,则下列关于氨气的性质和用途描述正确的是_______(填字母)。
,则下列关于氨气的性质和用途描述正确的是_______(填字母)。
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸( ),该反应的化学方程式为
),该反应的化学方程式为_______ ;某厂废液中含有2%~5%的 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为
转化为 的是
的是_______ (填字母)。
A.NaOH B. C.
C. D.浓硫酸
D.浓硫酸
(4)D可以是 ,已知同温同压下,同体积的
,已知同温同压下,同体积的 与
与 (蒸气)的质量比为7:64,则x=
(蒸气)的质量比为7:64,则x=_____ 。
(5) 在空气中易变质,写出检验
在空气中易变质,写出检验 发生变质的实验方法:
发生变质的实验方法:_______ 。
(6)常温下,G的浓溶液可以用干燥的铁或铝制容器盛装,原因是_______ 。
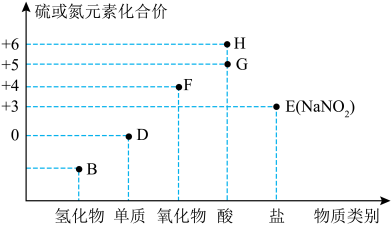
 ,写出F和G的稀溶液反应生成H的化学方程式(还原产物为+2价氧化物):
,写出F和G的稀溶液反应生成H的化学方程式(还原产物为+2价氧化物):(2)若B为
 ,则下列关于氨气的性质和用途描述正确的是_______(填字母)。
,则下列关于氨气的性质和用途描述正确的是_______(填字母)。| A.氨气易液化;液氨可用作制冷剂 | B.可用排水法收集氨气 |
| C.氨气是一种无色、无味的气体 | D.向氨水中滴加酚酞,溶液变红 |
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(
 ),该反应的化学方程式为
),该反应的化学方程式为 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为
转化为 的是
的是A.NaOH B.
 C.
C. D.浓硫酸
D.浓硫酸(4)D可以是
 ,已知同温同压下,同体积的
,已知同温同压下,同体积的 与
与 (蒸气)的质量比为7:64,则x=
(蒸气)的质量比为7:64,则x=(5)
 在空气中易变质,写出检验
在空气中易变质,写出检验 发生变质的实验方法:
发生变质的实验方法:(6)常温下,G的浓溶液可以用干燥的铁或铝制容器盛装,原因是
您最近一年使用:0次



