解题方法
1 . 氯化亚铜(化学式可表示为CuCl)常用作有机合成工业中的催化剂,微溶于水、不溶于乙醇,在潮湿空气中易水解、易被氧化。某学习小组用工业废渣(主要成分为Cu2S和Fe2O3)制取CuCl并同时得到电路板蚀刻液,实验步骤如图:
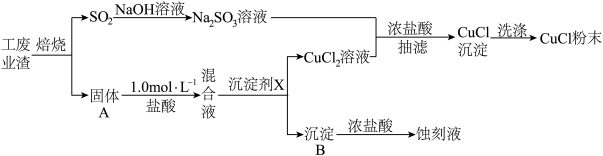
已知:
根据以上信息回答下列问题:
(1)写出焙烧过程中产生SO2的化学方程式:______ ;实验室中常用亚硫酸钠固体与70%的浓硫酸制备二氧化硫,若要达到控制反应速率的目的,图中可选用的装置是_____ (填标号)。
A.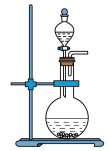 B.
B.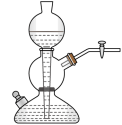 C.
C.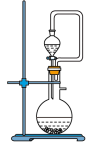 D.
D.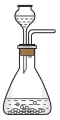
(2)混合液中加入的沉淀剂X可为______ ;(填化学式),调节溶液的pH至______ ,过滤得到CuCl2溶液。
(3)①向Na2SO3溶液中逐滴加入CuCl2溶液,再加入少量浓盐酸,混匀后倾倒出清液,抽滤、洗涤、干燥获得CuCl产品,该反应的离子方程式为______ 。
②抽滤也称减压过滤,请选择合适的仪器并组装抽滤的装置从溶液中得到CuCl产品,装置连接顺序为_____→_____→E→_____(填标号)。______
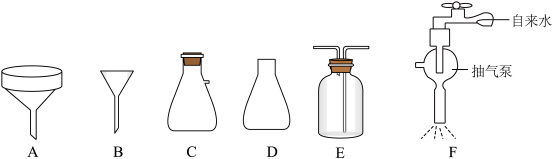
下列有关抽滤的说法错误的是_____ (填标号)。
A.原理为利用抽气泵使抽滤瓶中的压强降低,以达到固液分离的目的
B.过滤速度快,可得到较干燥的沉淀
C.实验结束后,先关抽气泵,后拔开抽滤瓶接管
③抽滤过程中先用“去氧水”作洗涤剂洗涤产品,然后立即用无水酒精洗涤,并在70℃真空下干燥2h,冷却后密封包装,密封包装的原因是______ 。
(4)实验测得氯化亚铜蒸气的相对分子质量为199,则氯化亚铜的分子式为_____ ;氯化亚铜定量吸收CO后形成配合物Cu2(CO)2Cl2·2H2O(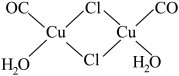 ),则Cu2(CO)2Cl2·2H2O中的配位体为
),则Cu2(CO)2Cl2·2H2O中的配位体为_____ (填化学式)。

已知:
| 金属阳离子 | 开始沉淀的pH | 完全沉淀的pH |
| Cu2+ | 4.8 | 6.4 |
| Fe3+ | 2.7 | 3.7 |
(1)写出焙烧过程中产生SO2的化学方程式:
A.
 B.
B. C.
C. D.
D.
(2)混合液中加入的沉淀剂X可为
(3)①向Na2SO3溶液中逐滴加入CuCl2溶液,再加入少量浓盐酸,混匀后倾倒出清液,抽滤、洗涤、干燥获得CuCl产品,该反应的离子方程式为
②抽滤也称减压过滤,请选择合适的仪器并组装抽滤的装置从溶液中得到CuCl产品,装置连接顺序为_____→_____→E→_____(填标号)。

下列有关抽滤的说法错误的是
A.原理为利用抽气泵使抽滤瓶中的压强降低,以达到固液分离的目的
B.过滤速度快,可得到较干燥的沉淀
C.实验结束后,先关抽气泵,后拔开抽滤瓶接管
③抽滤过程中先用“去氧水”作洗涤剂洗涤产品,然后立即用无水酒精洗涤,并在70℃真空下干燥2h,冷却后密封包装,密封包装的原因是
(4)实验测得氯化亚铜蒸气的相对分子质量为199,则氯化亚铜的分子式为
 ),则Cu2(CO)2Cl2·2H2O中的配位体为
),则Cu2(CO)2Cl2·2H2O中的配位体为
您最近一年使用:0次
2023-03-16更新
|
661次组卷
|
5卷引用:广西壮族自治区玉林市2022-2023学年高二下学期期中考试化学试题
广西壮族自治区玉林市2022-2023学年高二下学期期中考试化学试题河北省邯郸市2023届高三一模考试化学试题(已下线)2022年天津市普通高中学业水平等级性考试化学试题变式题(实验综合题)(已下线)专题16 实验题(已下线)工业流程题
名校
2 . 含氯消毒剂为疫情防控提供了强有力的物质支撑。
(1) 、
、 、
、 、NaClO常被用作消毒剂,上述物质消毒效率(以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)最高的是
、NaClO常被用作消毒剂,上述物质消毒效率(以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)最高的是________ (填标号)
a. b.
b. c.
c. d.NaClO
d.NaClO
(2)工业上常用反应: 来制备
来制备 ,则X的化学式为
,则X的化学式为________ ,每生成 ,反应中转移电子的数目为
,反应中转移电子的数目为________ 。
(3)如图为某消毒液产品参数的一部分:
①若此消毒液未变质,则消毒液中NaClO的质量分数为________ 。
②某实验需用240mL上述消毒液,现用NaClO固体配制,如图所示的仪器中肯定不需要的是________ (填序号),还需用到的玻璃仪器是________ (填仪器名称)。________ 。
a.溶解后未经冷却就移液
b.转移时没有洗涤烧杯内壁和玻璃棒
c.定容时俯视刻度线
d.定容摇匀后发现溶液液面低于刻度线,再补加蒸馏水至刻度线
e.用托盘天平(未使用游码)称量时“左码右物”
(1)
 、
、 、
、 、NaClO常被用作消毒剂,上述物质消毒效率(以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)最高的是
、NaClO常被用作消毒剂,上述物质消毒效率(以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)最高的是a.
 b.
b. c.
c. d.NaClO
d.NaClO(2)工业上常用反应:
 来制备
来制备 ,则X的化学式为
,则X的化学式为 ,反应中转移电子的数目为
,反应中转移电子的数目为(3)如图为某消毒液产品参数的一部分:
| 密度:1.25g·cm-3 主要成分:NaClO 浓度:c(NaClO)=5.0mol·L-1 注意事项:密封保存,易吸收空气中CO2变质 |
②某实验需用240mL上述消毒液,现用NaClO固体配制,如图所示的仪器中肯定不需要的是
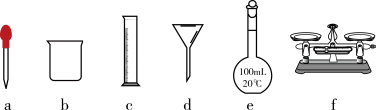
a.溶解后未经冷却就移液
b.转移时没有洗涤烧杯内壁和玻璃棒
c.定容时俯视刻度线
d.定容摇匀后发现溶液液面低于刻度线,再补加蒸馏水至刻度线
e.用托盘天平(未使用游码)称量时“左码右物”
您最近一年使用:0次
2023-03-10更新
|
427次组卷
|
6卷引用:广西柳州高级中学2023-2024学年高一上学期寒假月考化学试卷3
广西柳州高级中学2023-2024学年高一上学期寒假月考化学试卷3山东省济宁市2022-2023学年高一上学期期末考试化学试题山东省济宁市2022-2023学年高一下学期开学考试(上学期期末)化学试题山东省济宁市2022-2023学年高一上学期2月期末化学试题(已下线)专题05 物质的量-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)山东省聊城市临清市第一中学2023-2024学年高一上学期期末模拟考试化学试题
名校
解题方法
3 . 查阅资料知:Bi位于周期表的第ⅤA族, 是难溶于水的盐,有强氧化性;溶液中
是难溶于水的盐,有强氧化性;溶液中 较稳定,无色;某实验小组探究含锰物质的化学性质,有关实验操作和现象如下:
较稳定,无色;某实验小组探究含锰物质的化学性质,有关实验操作和现象如下:
①向稀硫酸酸化的 溶液中加入适量
溶液中加入适量 ,溶液变为紫红色
,溶液变为紫红色
②继续滴加适量的 ,溶液紫红色恰好褪去,并有无色气泡产生
,溶液紫红色恰好褪去,并有无色气泡产生
③再向反应液中加入适量的 固体恰好反应完全,溶液又变为紫红色
固体恰好反应完全,溶液又变为紫红色
发生的反应为: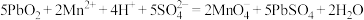
④继续向③的反应液中滴加浓盐酸,有黄绿色气体生成
下列有关说法正确的是
 是难溶于水的盐,有强氧化性;溶液中
是难溶于水的盐,有强氧化性;溶液中 较稳定,无色;某实验小组探究含锰物质的化学性质,有关实验操作和现象如下:
较稳定,无色;某实验小组探究含锰物质的化学性质,有关实验操作和现象如下:①向稀硫酸酸化的
 溶液中加入适量
溶液中加入适量 ,溶液变为紫红色
,溶液变为紫红色②继续滴加适量的
 ,溶液紫红色恰好褪去,并有无色气泡产生
,溶液紫红色恰好褪去,并有无色气泡产生③再向反应液中加入适量的
 固体恰好反应完全,溶液又变为紫红色
固体恰好反应完全,溶液又变为紫红色发生的反应为:
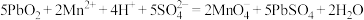
④继续向③的反应液中滴加浓盐酸,有黄绿色气体生成
下列有关说法正确的是
A. 可与浓盐酸发生反应生成相应的最高价含氧酸 可与浓盐酸发生反应生成相应的最高价含氧酸 |
B.根据上述现象可知氧化性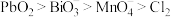 |
C.分别用 和 和 氧化 氧化 制取 制取 ,二者转移电子数不同 ,二者转移电子数不同 |
D.①中发生的反应方程式为: |
您最近一年使用:0次
2023-03-10更新
|
743次组卷
|
9卷引用:广西柳州高级中学2023-2024学年高一上学期寒假月考化学试卷3
广西柳州高级中学2023-2024学年高一上学期寒假月考化学试卷3山东省济宁市2022-2023学年高一上学期期末考试化学试题山东省济宁市2022-2023学年高一下学期开学考试(上学期期末)化学试题山东省济宁市2022-2023学年高一上学期2月期末化学试题山西省晋城市第一中学校2022-2023学年高一下学期4月期中考试化学试题湖北省武昌实验中学2023-2024学年高一上学期10月月考化学试题(已下线)专项02 离子反应和氧化还原反应的应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)山东省青岛市即墨区第一中学2023-2024学年高一上学期第二次阶段检测化学试题江西省三市八校联盟2023-2024学年高一上学期期中联考化学试卷
名校
4 . 从“烂版液”(含有 、
、 和
和 )中回收铜,并制备
)中回收铜,并制备 的实验流程如图所示。
的实验流程如图所示。
 、
、 和
和 )中回收铜,并制备
)中回收铜,并制备 的实验流程如图所示。
的实验流程如图所示。
A.制备 至少需要 至少需要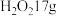 |
| B.步骤1中所用到的玻璃仪器有烧杯、漏斗、玻璃棒 |
C.步骤Ⅲ中 的作用,与 的作用,与 和高锰酸钾反应中的作用相同 和高锰酸钾反应中的作用相同 |
D.将5~6滴饱和 溶液滴入约40mL沸水中形成的分散系,可产生丁达尔效应 溶液滴入约40mL沸水中形成的分散系,可产生丁达尔效应 |
您最近一年使用:0次
2023-03-10更新
|
340次组卷
|
4卷引用:广西柳州高级中学2023-2024学年高一上学期寒假月考化学试卷3
5 . 利用熔融碱焙烧工艺可从铬渣(Al、Al2O3、Cr2O3等)中浸出铬和铝,实现铬和铝的再生利用。其工艺流程如下:
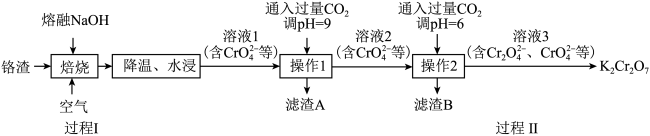
(1)为加快“水浸”速率,可采取的措施为
(2)操作1中通入过量
 调节pH,写出反应的离子方程式
调节pH,写出反应的离子方程式(3)过程Ⅰ中焙烧生成Na2CrO4的化学方程式为
(4)K2Cr2O7不同温度下溶解度(g/100gH2O)如下表:
| 化合物名称 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ |
| K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 |
结合表中数据分析,过程得到K2Cr2O7粗品的操作是:向滤液3中加入稀盐酸和氯化钾后,
(5)实验室通常用氧化还原滴定测定K2Cr2O7产品纯度:氧化还原滴定与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。
①用
②排出碱式滴定管中气泡的方法应采用如图操作中的
A. B.
B.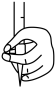 C.
C. D.
D.
③某小组在滴定开始和结束时,装有标准液的滴定管液面如图所示,则本次滴定所消耗标准液的体积为

④若滴定前滴定管尖嘴有气泡,滴定后气泡消失,则会使测定结果
您最近一年使用:0次
2023-03-05更新
|
252次组卷
|
2卷引用:广西南宁市2022-2023学年高二上学期期末教学质量调研化学试题
解题方法
6 . 下列说法不正确的是
| A.燃烧一定要有氧气参加 | B.石墨和金刚石互为同素异形体 |
| C.在实验室中,常将Na保存在煤油中 | D.铝合金具有较强的抗腐蚀能力 |
您最近一年使用:0次
名校
解题方法
7 . 高铁酸钾( ,
, g/mol)是一种高效多功能的绿色消毒剂,在新冠疫情期间大显身手。
g/mol)是一种高效多功能的绿色消毒剂,在新冠疫情期间大显身手。
【查阅资料】 为紫色固体,易溶于水,微溶于KOH溶液,不溶于乙醇;具有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生
为紫色固体,易溶于水,微溶于KOH溶液,不溶于乙醇;具有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生 。
。
I.湿法制备 (夹持装置略)
(夹持装置略)_______ mL浓溶液,量取所用量筒的规格是_______ (填“10mL”“25mL”或“50mL”)。若所配制的稀溶液浓度偏大,则可能的原因是_______ (填字母)。
A.配制前,容量瓶中有少量蒸馏水 B.量取浓溶液时,仰视液面
C.未经冷却,立即转移至容量瓶定容 D.定容时,仰视液面
(2)A中发生反应的化学方程式是_______ 。
(3)下列试剂中,装置B的X溶液可以选用的是_______(填字母)。
(4)C中得到紫色固体和溶液,生成 的化学方程式是
的化学方程式是_______ 。
II.干法制备高铁酸钾分两步进行
(5)第一步反应为: ,该反应氧化剂和还原剂的物质的量之比为
,该反应氧化剂和还原剂的物质的量之比为_______ ;
第二步反应为:
(6)实验室用100mL 2.00
 溶液发生上述反应,产品经干燥后得到纯品35.0g,则
溶液发生上述反应,产品经干燥后得到纯品35.0g,则 的产率为
的产率为_______ (保留一位小数)。
 ,
, g/mol)是一种高效多功能的绿色消毒剂,在新冠疫情期间大显身手。
g/mol)是一种高效多功能的绿色消毒剂,在新冠疫情期间大显身手。【查阅资料】
 为紫色固体,易溶于水,微溶于KOH溶液,不溶于乙醇;具有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生
为紫色固体,易溶于水,微溶于KOH溶液,不溶于乙醇;具有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生 。
。I.湿法制备
 (夹持装置略)
(夹持装置略)
A.配制前,容量瓶中有少量蒸馏水 B.量取浓溶液时,仰视液面
C.未经冷却,立即转移至容量瓶定容 D.定容时,仰视液面
(2)A中发生反应的化学方程式是
(3)下列试剂中,装置B的X溶液可以选用的是_______(填字母)。
| A.饱和食盐水 | B.浓盐酸 | C.氢氧化钠溶液 | D.饱和 溶液 溶液 |
 的化学方程式是
的化学方程式是II.干法制备高铁酸钾分两步进行
(5)第一步反应为:
 ,该反应氧化剂和还原剂的物质的量之比为
,该反应氧化剂和还原剂的物质的量之比为第二步反应为:

(6)实验室用100mL 2.00

 溶液发生上述反应,产品经干燥后得到纯品35.0g,则
溶液发生上述反应,产品经干燥后得到纯品35.0g,则 的产率为
的产率为
您最近一年使用:0次
2023-02-11更新
|
116次组卷
|
2卷引用:广西柳州高级中学2023-2024学年高一上学期寒假月考四化学试题
8 . 科学家研究发现 分子在半导体光催化的作用下可被捕获转化为
分子在半导体光催化的作用下可被捕获转化为 (过程如图所示)。下列说法
(过程如图所示)。下列说法不正确 的是
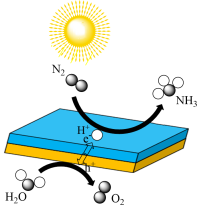
 分子在半导体光催化的作用下可被捕获转化为
分子在半导体光催化的作用下可被捕获转化为 (过程如图所示)。下列说法
(过程如图所示)。下列说法
A. 分子中 分子中 原子杂化方式为 原子杂化方式为 |
B. 和 和 的空间结构相同 的空间结构相同 |
C.反应的化学方程式: |
| D.该过程可以实现太阳能向化学能的转化 |
您最近一年使用:0次
2022-12-29更新
|
148次组卷
|
2卷引用:广西钦州市第四中学2022-2023学年高二下学期2月考试化学试题
解题方法
9 . 新冠疫情的发生,消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,而氯气是制取消毒液的重要原料之一。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式___________________________________ ,若收集到标准状况下3.36LCl2,则被氧化的HCl的物质的量为_____________ mol。
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式_______________________________________ ,若要制取1.5L 2 mol/L的84消毒液,则需要标准状况下___________ L 氯气。
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因__________________________________ (用化学方程式表示), 该反应中氧化剂是______________ 。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因
您最近一年使用:0次
名校
解题方法
10 . 甲、乙、丙、丁、戊几种中学常见的物质在常温有如下转化关系,在转化过程中,乙与KHCO3按等物质的量1:1混合,并且恰好完全反应。

(1)若甲是一种金属单质,其焰色与丁的焰色一样均为黄色,则物质丁的俗名为:_________ 。反应①的化学方程式为: _________ 。
(2)若甲是一种黄绿色的气体单质,丁为一种盐,则物质丙的化学式为_________ 。反应②的离子方程式为:_________ 。
(3)若甲是一种氧化物,丙可以使带火星的木条复燃,戊的焰色为黄色,则物质甲的化学式为:_________ 。反应②的离子方程式为:_________ 。

(1)若甲是一种金属单质,其焰色与丁的焰色一样均为黄色,则物质丁的俗名为:
(2)若甲是一种黄绿色的气体单质,丁为一种盐,则物质丙的化学式为
(3)若甲是一种氧化物,丙可以使带火星的木条复燃,戊的焰色为黄色,则物质甲的化学式为:
您最近一年使用:0次



