1 . 研究表明 与
与 在
在 存在下发生反应,反应的能量变化与反应进程的关系如图所示,设
存在下发生反应,反应的能量变化与反应进程的关系如图所示,设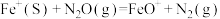
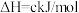 ,下列说法错误的是
,下列说法错误的是
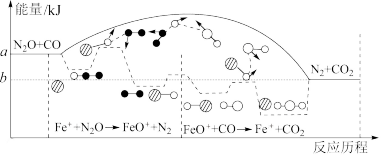
 与
与 在
在 存在下发生反应,反应的能量变化与反应进程的关系如图所示,设
存在下发生反应,反应的能量变化与反应进程的关系如图所示,设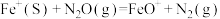
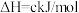 ,下列说法错误的是
,下列说法错误的是
A.  |
B. 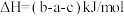 |
C.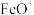 能降低该反应的活化能 能降低该反应的活化能 |
| D.反应物总键能小于生成物总键能 |
您最近一年使用:0次
名校
2 . 下列说法或表示方法中正确的是
| A.同温同压下,H2(g)+Cl2(g) = 2HCl(g)在光照和点燃条件下的ΔH相同 |
| B.使用催化剂能降低反应的活化能,所以也能改变反应的ΔH。 |
| C.甲烷的燃烧热为-890.3KJ/mol,则其热化学方程式为CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) ΔH= - 890.3kJ/mol, |
| D.稀的强酸和稀的强碱溶液反应的热化学方程式均为:H+ +OH- = H2O ΔH= -57.3kJ·mol-1 |
您最近一年使用:0次
2021-10-13更新
|
304次组卷
|
6卷引用:黑龙江省牡丹江市第三中学2021-2022学年高二上学期期中考试化学(理)试题
3 . 大气污染是中国第一大环境污染问题,氮和硫的氧化物排放是造成大气污染的原因之一,研究它们的反应机理,对于消除环境污染有重要意义。
(1)汽车尾气中的 由如下反应产生:
由如下反应产生:

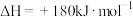
已知:
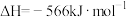
则

___________ 
(2) 反应过程中能量变化如图所示。在
反应过程中能量变化如图所示。在 存在时,该反应的机理为:
存在时,该反应的机理为:
第一步: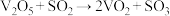 (快) 第二步:
(快) 第二步: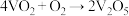 (慢)
(慢)
下列说法正确的是___________(填序号)。
(3) 在一定条件下可发生分解反应:
在一定条件下可发生分解反应: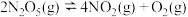 ,某温度下向恒容密闭容器中加入一定量
,某温度下向恒容密闭容器中加入一定量 ,测得
,测得 浓度随时间的变化如表所示:
浓度随时间的变化如表所示:
①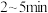 内用
内用 表示的该反应的平均反应速率为
表示的该反应的平均反应速率为___________ 。
②一定温度下,在恒容密闭容器中充入一定量 进行该反应,能判断反应已达到化学平衡状态的是
进行该反应,能判断反应已达到化学平衡状态的是___________ 。
A. 和
和 的浓度比保持不变 B.容器中压强不再变化
的浓度比保持不变 B.容器中压强不再变化
C.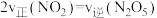 D.气体的密度保持不变
D.气体的密度保持不变
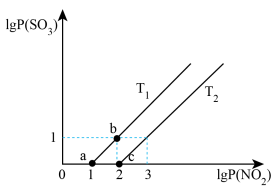
(4)某小组研究某恒容密闭容器中,在不同温度下,氮硫的氧化物之间的转化情况如图所示,已知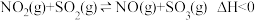 ,实验初始时体系中的
,实验初始时体系中的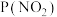 和
和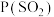 相等、
相等、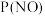 和
和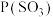 相等,其中P表示各气体的分压。
相等,其中P表示各气体的分压。
①
___________  (填“>”“<”或者“=”);温度为
(填“>”“<”或者“=”);温度为 时化学平衡常数
时化学平衡常数
___________ 。
②由平衡状态a到b,改变的条件是___________ 。
(1)汽车尾气中的
 由如下反应产生:
由如下反应产生:
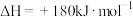
已知:

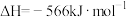
则



(2)
 反应过程中能量变化如图所示。在
反应过程中能量变化如图所示。在 存在时,该反应的机理为:
存在时,该反应的机理为:第一步:
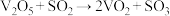 (快) 第二步:
(快) 第二步: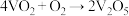 (慢)
(慢)下列说法正确的是___________(填序号)。

| A.反应速率主要取决于第一步 | B. 是该反应的催化剂 是该反应的催化剂 |
C.逆反应的活化能大于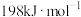 | D.增大 的浓度可显著提高反应速率 的浓度可显著提高反应速率 |
 在一定条件下可发生分解反应:
在一定条件下可发生分解反应: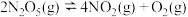 ,某温度下向恒容密闭容器中加入一定量
,某温度下向恒容密闭容器中加入一定量 ,测得
,测得 浓度随时间的变化如表所示:
浓度随时间的变化如表所示: | 0 | 1 | 2 | 3 | 4 | 5 |
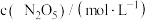 | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
①
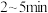 内用
内用 表示的该反应的平均反应速率为
表示的该反应的平均反应速率为②一定温度下,在恒容密闭容器中充入一定量
 进行该反应,能判断反应已达到化学平衡状态的是
进行该反应,能判断反应已达到化学平衡状态的是A.
 和
和 的浓度比保持不变 B.容器中压强不再变化
的浓度比保持不变 B.容器中压强不再变化C.
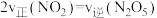 D.气体的密度保持不变
D.气体的密度保持不变(4)某小组研究某恒容密闭容器中,在不同温度下,氮硫的氧化物之间的转化情况如图所示,已知
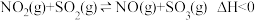 ,实验初始时体系中的
,实验初始时体系中的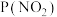 和
和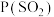 相等、
相等、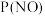 和
和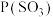 相等,其中P表示各气体的分压。
相等,其中P表示各气体的分压。
①

 (填“>”“<”或者“=”);温度为
(填“>”“<”或者“=”);温度为 时化学平衡常数
时化学平衡常数
②由平衡状态a到b,改变的条件是
您最近一年使用:0次
2021-10-11更新
|
395次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2021-2022学年高三上学期期中考试化学试题
名校
解题方法
4 . Ⅰ.完成下列填空
(1)已知在25℃、101kPa下,1g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7kJ的热量,试写出乙醇燃烧热的热化学方程式___________
(2)已知:C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5kJ/mol
2H2+O2(g)=2H2O(l) ΔH2=-517.6kJ/mol
2C2H2+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599.2kJ/mol
计算25℃时,由C(石墨,s)和H2(g)反应生成C2H2(g)的热化学方程式为___________ 。
Ⅱ.分别取50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。
(3)下图装置缺少一种玻璃仪器,该仪器的名称为___________ ;若用铜棒代替该仪器,会导致ΔH计算结果___________ (偏低、偏高或无影响),原因是___________ 。
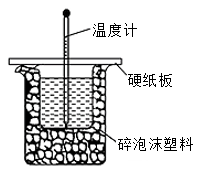
(4)某学生实验记录数据如下:(已知ρ溶液=1g/cm3,c溶液=4.18J/(g·℃)),依据该学生的实验数据计算,该实验测得的中和热为ΔH=___________ 。(保留小数点后1位)
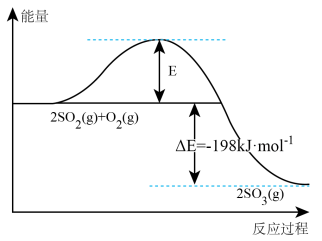
Ⅲ.2SO2(g)+O2(g) 2SO3(g) △H反应过程的能量变化如图所示。已知:1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
2SO3(g) △H反应过程的能量变化如图所示。已知:1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
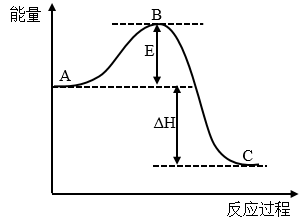
(5)图中A表示___________ 的能量(选用SO2、O2、SO3填空)。E的大小对该反应的反应热___________ (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点___________ (填“升高”还是“降低”),△H___________ (填“变大”、“变小”或“不变”)。
(6)题中反应的中△H=___________ kJ·mol-1。
(1)已知在25℃、101kPa下,1g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7kJ的热量,试写出乙醇燃烧热的热化学方程式
(2)已知:C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5kJ/mol
2H2+O2(g)=2H2O(l) ΔH2=-517.6kJ/mol
2C2H2+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599.2kJ/mol
计算25℃时,由C(石墨,s)和H2(g)反应生成C2H2(g)的热化学方程式为
Ⅱ.分别取50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。
(3)下图装置缺少一种玻璃仪器,该仪器的名称为

(4)某学生实验记录数据如下:(已知ρ溶液=1g/cm3,c溶液=4.18J/(g·℃)),依据该学生的实验数据计算,该实验测得的中和热为ΔH=
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
Ⅲ.2SO2(g)+O2(g)
 2SO3(g) △H反应过程的能量变化如图所示。已知:1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
2SO3(g) △H反应过程的能量变化如图所示。已知:1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
(5)图中A表示
(6)题中反应的中△H=
您最近一年使用:0次
名校
5 . Li/Li2O体系的能量循环图如图所示。下列说法正确的是


| A.△H3<0 | B.△H3+△H4+△H5=△H6 |
| C.△H1>0,△H6>0 | D.△H1+△H2+△H3+△H4+△H5-△H6=0 |
您最近一年使用:0次
名校
6 . 化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)在101kPa时,1.6gCH4完全燃烧生成CO2和液态H2O,放出89.0kJ的热量,CH4的燃烧热为___________ kJ·mol-1,写出CH4燃烧热的热化学方程式:___________ ,89.6LCH4(标况)完全燃烧(产物水为液态)后所产生的热量为___________ kJ
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。已知反应N2(g)+3H2(g) 2NH3(g) ΔH=akJ·mol-1
2NH3(g) ΔH=akJ·mol-1
试根据表中所列键能数据计算a的数值:___________ 。
(3)已知:C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ·mol-1②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599kJ·mol-1③
根据盖斯定律,请写出25℃、101kPa时由C(石墨,s)和H2(g)生成1molC2H2(g)反应的热化学方程式:___________ 。
(4)二甲醚(CH3OCH3)是无色气体,可作为一种新型能源。由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下三个反应:
甲醇合成反应:
①CO(g)+2H2(g)=CH3OH(g) ΔH1=-90.1kJ·mol-1
水煤气变换反应:
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.1kJ·mol-1
二甲醚合成反应:
③2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH4=-24.5kJ·mol-1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为:___________
(1)在101kPa时,1.6gCH4完全燃烧生成CO2和液态H2O,放出89.0kJ的热量,CH4的燃烧热为
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。已知反应N2(g)+3H2(g)
 2NH3(g) ΔH=akJ·mol-1
2NH3(g) ΔH=akJ·mol-1| 化学键 | H-H | N-H | N≡N |
| 键能(kJ·mol-1) | 436 | 391 | 945 |
(3)已知:C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ·mol-1②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599kJ·mol-1③
根据盖斯定律,请写出25℃、101kPa时由C(石墨,s)和H2(g)生成1molC2H2(g)反应的热化学方程式:
(4)二甲醚(CH3OCH3)是无色气体,可作为一种新型能源。由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下三个反应:
甲醇合成反应:
①CO(g)+2H2(g)=CH3OH(g) ΔH1=-90.1kJ·mol-1
水煤气变换反应:
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.1kJ·mol-1
二甲醚合成反应:
③2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH4=-24.5kJ·mol-1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为:
您最近一年使用:0次
2021-10-08更新
|
181次组卷
|
3卷引用:黑龙江省七台河市勃利县高级中学2021-2022学年高三上学期期中考试化学试题
名校
7 . 根据Ca(OH)2/CaO体系的能量循环图:
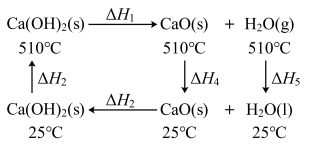
下列说法正确的是

下列说法正确的是
| A.ΔH5>0 | B.ΔH1+ΔH2=0 |
| C.ΔH3=ΔH4+ΔH5 | D.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5=0 |
您最近一年使用:0次
2021-09-15更新
|
617次组卷
|
11卷引用:黑龙江省五校(嫩江市第一中学、嫩江市职业高中、伊拉哈中学、海江中学等)2021-2022学年高二上学期期中联考化学试题
黑龙江省五校(嫩江市第一中学、嫩江市职业高中、伊拉哈中学、海江中学等)2021-2022学年高二上学期期中联考化学试题湖北省武汉市长虹中学2021-2022学年高二上学期10月月考化学试卷浙江省湖州市三贤联盟2021-2022学年高二上学期期中考试化学试题浙江省嘉兴市海盐第二高级中学2021-2022学年高二上学期(10月)阶段检测化学试题河北正定中学2020-2021学年高三上学期第四次半月考化学试题浙江省湖州市长兴县等三县2019-2020学年高二上学期期中考试化学试题 (已下线)专题15 反应热计算的几种类型-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题14 化学反应与热量计算-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)1.1.3能源的充分利用 课前浙江省杭州市四校2023-2024学年高二上学期10月联考化学试题重庆市万州第二高级中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
8 . 下列有关说法正确的是
①太阳光催化分解水制氢:2H2O(1)=2H2(g)+O2(g) ΔH1=+571.6kJ/mol
②碳的“气化”:C(s)+H2O(g)=CO(g)+H2(g) ΔH2=+131.3kJ/mol
③甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH3=+206.1kJ/mol
①太阳光催化分解水制氢:2H2O(1)=2H2(g)+O2(g) ΔH1=+571.6kJ/mol
②碳的“气化”:C(s)+H2O(g)=CO(g)+H2(g) ΔH2=+131.3kJ/mol
③甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH3=+206.1kJ/mol
| A.由反应①可知H2的燃烧热为571.6kJ/mol |
| B.碳的“气化”反应过程熵不变 |
| C.甲烷与水反应制氢过程中使用催化剂,反应的活化能Ea、ΔH3都减小 |
D.反应CH4(g)+ O2(g)=CO(g)+2H2(g)的ΔH4>-79.7kJ/mol O2(g)=CO(g)+2H2(g)的ΔH4>-79.7kJ/mol |
您最近一年使用:0次
2021-09-15更新
|
291次组卷
|
3卷引用:黑龙江省宾县第一中学2021-2022学年高二上学期第一次月考化学试题
9 . 2022年,第24届冬奥会将在中国北京、张家口两地举办。中国绿色碳汇基金会发起“我们的冬奥碳汇林”众筹项目,计划在张家口市崇礼区种植小树。碳汇,是指通过植树造林、森林管理、植被恢复等措施,利用植物光合作用吸收大气中的二氧化碳[6CO2(g)+6H2O(l)→C6H12O6(s)+6CO2(g)],并将其固定在植被和土壤中,从而减少温室气体在大气中浓度的过程、活动或机制。已知利用植物的光合作用每吸收1molCO2需要吸收的能量约为470kJ。请回答下列问题:
(1)碳汇过程中能量的转化形式为___________ 能转化为___________ 能;有资料表明,某块林木通过光合作用大约吸收了1.88×107kJ能量,则吸收的CO2为___________ kg;葡萄糖完全燃烧生成液态水的热化学方程式为___________ 。
(2)工业废气中的CO2可用碱液吸收。已知:
①CO2(g)+2NaOH(aq)=Na2CO3(aq)+H2O(l) =-akJ/mol;
=-akJ/mol;
②CO2(g)+NaOH(aq)=NaHCO3(aq) =-bkJ/mol。
=-bkJ/mol。
反应CO2(g)+H2O(l)+Na2CO3(aq)=2NaHCO3(aq)的 =
=___________ kJ/mol(用含a、b的代数式表示)。
(3)生产液晶显示器的过程中使用的化学清洗剂NF3和CO2一样,也是一种温室气体,其在大气中能够稳定存在数百年。下表是几种化学键的键能:
①关于反应N2(g)+3F2(g)=2NF3(g),下列说法中不正确的是__________ 。
A.过程N2(g)=2N(g)放出能量
B.反应N2(g)+3F2(g)=2NF3(g)放出能量
C.使用催化剂能减小反应的
②NF3对半导体硅进行蚀刻时,在蚀刻物表面不留任何残留物,试写出蚀刻反应方程式___________ 。
(1)碳汇过程中能量的转化形式为
(2)工业废气中的CO2可用碱液吸收。已知:
①CO2(g)+2NaOH(aq)=Na2CO3(aq)+H2O(l)
 =-akJ/mol;
=-akJ/mol;②CO2(g)+NaOH(aq)=NaHCO3(aq)
 =-bkJ/mol。
=-bkJ/mol。反应CO2(g)+H2O(l)+Na2CO3(aq)=2NaHCO3(aq)的
 =
=(3)生产液晶显示器的过程中使用的化学清洗剂NF3和CO2一样,也是一种温室气体,其在大气中能够稳定存在数百年。下表是几种化学键的键能:
| 化学键 | N≡N | F-F | N-F |
| 键能/kJ/mol | 946.0 | 157.0 | 283.0 |
①关于反应N2(g)+3F2(g)=2NF3(g),下列说法中不正确的是
A.过程N2(g)=2N(g)放出能量
B.反应N2(g)+3F2(g)=2NF3(g)放出能量
C.使用催化剂能减小反应的

②NF3对半导体硅进行蚀刻时,在蚀刻物表面不留任何残留物,试写出蚀刻反应方程式
您最近一年使用:0次
2021-09-14更新
|
265次组卷
|
3卷引用:黑龙江省绥化市青冈县第一中学校2021-2022学年高二上学期开学考试化学试题
名校
10 . 如图所示,E1=393.5kJ⋅mol-1,E2=395.4kJ⋅mol-1,下列说法或热化学方程式正确的是
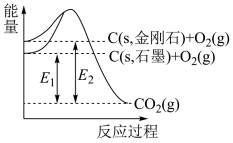

| A.石墨与金刚石之间的转化是物理变化 | B.C(s,石墨)=C(s,金刚石)△H=+1.9kJ⋅mol-1 |
| C.金刚石的稳定性强于石墨 | D.断裂1mol化学键吸收的能量:石墨比金刚石的少 |
您最近一年使用:0次
2021-09-11更新
|
606次组卷
|
7卷引用:黑龙江省哈尔滨市第六中学2021-2022学年高二上学期第一次月考化学试题



