名校
解题方法
1 . 某研究小组为探究弱酸性条件下铁发生电化学腐蚀的类型及腐蚀速率,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞,如图 1 所示。 从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
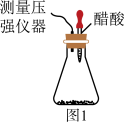
(1)请完成以下实验设计(完成表中空格):
(2)编号①实验测得容器中压强随时间变化如图 2。 t2 时,容器中压强明显小于起始压强, 其原因是铁发生了_____ 腐蚀, 请在图 3 中用箭头标出发生该腐蚀时电子流动方向_____ ;此时,碳粉表面发生了_____ (填“氧化”或“还原”)反应,其电极反应式是_____ 。
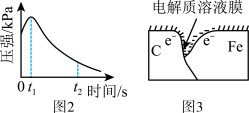
(3)该小组对图 2 中 0~t1 时压强变大的原因提出了如下假设,请你完成假设二:
假设一:发生析氢腐蚀产生了气体;
假设二:_____ 。

(1)请完成以下实验设计(完成表中空格):
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
| ② | 0.5 | 36.0 | ||
| ③ | 碳粉含量的影响 | 0.2 | 2.0 | 90.0 |

(3)该小组对图 2 中 0~t1 时压强变大的原因提出了如下假设,请你完成假设二:
假设一:发生析氢腐蚀产生了气体;
假设二:
您最近一年使用:0次
2020-03-27更新
|
156次组卷
|
2卷引用:山东省泰安市2019-2020学年高二上学期期末考试化学试题
名校
2 . 如图为实验室制溴苯的装置图。完成下列填空:

(1)该反应的化学方程式:___ 。
(2)双球U形管中盛放CCl4的用途:___ 。
(3)A中铁丝的作用:___ 。
(4)分液漏斗中液体滴入A中的实验现象___ 。
(5)若A中混合液倒入冷水,则有黄色液体产生,原因是溴苯中混有___ (填化学式),如何除去该杂质需加入的试剂是___ ,相应操作为___ 。
(6)B试管中若加入硝酸银溶液,则实验现象是:___ 。加入硝酸银溶液的目的是为了检验___ (填化学式)的生成,从而证明该反应为___ (填反应类型)。

(1)该反应的化学方程式:
(2)双球U形管中盛放CCl4的用途:
(3)A中铁丝的作用:
(4)分液漏斗中液体滴入A中的实验现象
(5)若A中混合液倒入冷水,则有黄色液体产生,原因是溴苯中混有
(6)B试管中若加入硝酸银溶液,则实验现象是:
您最近一年使用:0次
14-15高三上·上海浦东新·期末
3 . 欲做实验:氯气与氢气混合后在光照条件下爆鸣。手头没有气体发生器,也不使用加热装置,利用一个“倒Y型”玻璃试管(图)。

(1)该实验的做法是:
在倒Y形管两端底部分别放入一种固体,一端是_______ ,另一端是KMnO4或KClO3;然后在两端同时注入____ 酸,用带导管的塞子将管口塞紧,并将该导管通向盛______ 溶液的容器。临时制取的H2和Cl2即时混合后用闪光灯引爆。
(2)倒Y型试管可用来同时制取两种气体,并便于观察气体在常温下混合后的反应现象。请举一例(用两种气体的分子式表示):______ 与______

(1)该实验的做法是:
在倒Y形管两端底部分别放入一种固体,一端是
(2)倒Y型试管可用来同时制取两种气体,并便于观察气体在常温下混合后的反应现象。请举一例(用两种气体的分子式表示):
您最近一年使用:0次
名校
解题方法
4 . 实验室常用如图所示的两套装置测量所制得气体的体积,下面有关这两套量气装置的使用说明有错误的是
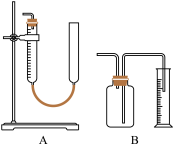

| A.使用A装置量气前,其右管中应充满相应的液体 |
| B.量气前,B装置中广口瓶通常应盛满相应的液体 |
| C.A装置收集完气体后,在读数前应使盛液管内液面与集气管内液面相平 |
| D.A装置是直接测量气体体积,而B装置直接测量的是所排出液体的体积 |
您最近一年使用:0次
2020-03-23更新
|
217次组卷
|
5卷引用:云南省腾冲市第八中学2018-2019学年高一上学期期中考试化学试题
云南省腾冲市第八中学2018-2019学年高一上学期期中考试化学试题(已下线)上海市虹口区2014届高三三模化学试题浙江省温州市龙湾中学2019-2020学年高二下学期第1次居家月考化学试题(已下线)第01讲 化学实验基础知识和技能(精练)——2021年高考化学一轮复习讲练测内蒙古包头市一机一中2021-2022学年高一上学期10月月考化学试题
2014·上海闵行·三模
解题方法
5 . 由于锌的性质与铝相似,也易溶于强碱溶液放出氢气,因此可采用碱溶气体法测定镀锌铁皮锌镀层的厚度,装置如图。下列关于该实验的判断不正确 的是
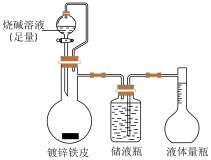

| A.发生的反应是:Zn + 2NaOH = Na2ZnO2 + H2↑ |
| B.反应结束冷却后,要用针筒抽气直至储液瓶中导管内外液面相平 |
| C.若镀锌铁皮的锌镀层中混有金属铝杂质,则会导致测定结果偏小 |
| D.碱溶气体法测定铁皮锌镀层厚度容易判断反应终点,却不及酸溶重量法简便 |
您最近一年使用:0次
2014高二·上海·学业考试
解题方法
6 . 用图所示装置测定镁带样品中单质镁的质量分量(杂质与酸反应不产生气体)。完成下列填空:

(1)用离子方程式表示该实验的反应原理。_______________________
(2)称量镁带所需的定量仪器是________________________________
(3)硫酸必须过量的目的是____________________________________
(4)导管a的作用是____________________________________
(5)取三份镁带样品分别进行实验,所得数据见表:
如果测定结果偏高,可能的原因是____________ 。(选填编号)
a.装置漏气
b.未冷却至室温即读数
c.镁带中含有氧化镁
d.未读数时量气管的液面低于水准管

(1)用离子方程式表示该实验的反应原理。
(2)称量镁带所需的定量仪器是
(3)硫酸必须过量的目的是
(4)导管a的作用是
(5)取三份镁带样品分别进行实验,所得数据见表:
| 实验次数 | 镁带质量(g) | 氢气体积(mL) (已换算成标准状况) |
| 1 | 0.053 | 44.60 |
| 2 | 0.056 | 47.05 |
| 3 | 0.059 | 49.30 |
a.装置漏气
b.未冷却至室温即读数
c.镁带中含有氧化镁
d.未读数时量气管的液面低于水准管
您最近一年使用:0次
解题方法
7 . 在使用下列各实验装置时,不合理的是


| A.装置①用于分离CCl4和H2O的混合物 |
| B.装置②用于收集H2、CO2、Cl2等气体 |
| C.装置③用于吸收NH3或HCl,并防止倒吸 |
| D.装置④用于收集NH3,并吸收多余的NH3 |
您最近一年使用:0次
8 . 为探究铜与稀硝酸反应的气态产物中是否含NO2,进行如下实验.

已知:FeSO4+NO→[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色.
(1)实验前需检验装置的气密性,简述操作__ .
(2)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是__ ;铜片和稀硝酸反应的化学方程式为__ .
(3)洗气瓶中加入KSCN溶液的目的及原理是__ ;本实验只观察到洗气瓶中出现了棕色,写出尾气处理的化学方程式__ .

已知:FeSO4+NO→[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色.
(1)实验前需检验装置的气密性,简述操作
(2)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是
(3)洗气瓶中加入KSCN溶液的目的及原理是
您最近一年使用:0次
9 . (13分)硫酸铜晶体(CuSO4·5H2O)是铜盐中重要的无机化工原料,广泛应用于农业、电镀、饲料添加剂、催化剂、石油、选矿、油漆等行业。
Ⅰ.采用孔雀石[主要成分CuCO3·Cu(OH)2]、硫酸(70%)、氨水为原料制取硫酸铜晶体。其工艺流程如下:
(1)预处理时要用破碎机将孔雀石破碎成粒子直径<1 mm,破碎的目的是____________________ 。
(2)已知氨浸时发生的反应为CuCO3·Cu(OH)2+8NH3·H2O [Cu(NH3)4]2(OH)2CO3+8H2O,蒸氨时得到的固体呈黑色,请写出蒸氨时的反应方程式:
[Cu(NH3)4]2(OH)2CO3+8H2O,蒸氨时得到的固体呈黑色,请写出蒸氨时的反应方程式:______________________ 。
(3)蒸氨出来的气体有污染,需要净化处理,下图装置中合适的为___________ (填标号);经吸收净化所得的溶液用途是_______________ (任写一条)。
(4)操作2为一系列的操作,通过加热浓缩、冷却结晶、___________ 、洗涤、___________ 等操作得到硫酸铜晶体。
Ⅱ.采用金属铜单质制备硫酸铜晶体
(5)教材中用金属铜单质与浓硫酸反应制备硫酸铜,虽然生产工艺简洁,但在实际生产过程中不采用,其原因是______________________ (任写两条)。
(6)某兴趣小组查阅资料得知:Cu+CuCl2 2CuCl,4CuCl+O2+2H2O
2CuCl,4CuCl+O2+2H2O 2[Cu(OH)2·CuCl2],[Cu(OH)2·CuCl2]+H2SO4
2[Cu(OH)2·CuCl2],[Cu(OH)2·CuCl2]+H2SO4 CuSO4+CuCl2+2H2O。现设计如下实验来制备硫酸铜晶体,装置如图:
CuSO4+CuCl2+2H2O。现设计如下实验来制备硫酸铜晶体,装置如图:

向铜和稀硫酸的混合物中加入氯化铜溶液,利用二连球鼓入空气,将铜溶解,当三颈烧瓶中呈乳状浑浊液时,滴加浓硫酸。
①盛装浓硫酸的仪器名称为___________ 。
②装置中加入CuCl2的作用是______________ ;最后可以利用重结晶的方法纯化硫酸铜晶体的原因为______________________ 。
③若开始时加入a g铜粉,含b g氯化铜溶质的氯化铜溶液,最后制得c g CuSO4·5H2O,假设整个过程中杂质不参与反应且不结晶,每步反应都进行得比较完全,则原铜粉的纯度为________ 。
Ⅰ.采用孔雀石[主要成分CuCO3·Cu(OH)2]、硫酸(70%)、氨水为原料制取硫酸铜晶体。其工艺流程如下:

(1)预处理时要用破碎机将孔雀石破碎成粒子直径<1 mm,破碎的目的是
(2)已知氨浸时发生的反应为CuCO3·Cu(OH)2+8NH3·H2O
 [Cu(NH3)4]2(OH)2CO3+8H2O,蒸氨时得到的固体呈黑色,请写出蒸氨时的反应方程式:
[Cu(NH3)4]2(OH)2CO3+8H2O,蒸氨时得到的固体呈黑色,请写出蒸氨时的反应方程式:(3)蒸氨出来的气体有污染,需要净化处理,下图装置中合适的为

(4)操作2为一系列的操作,通过加热浓缩、冷却结晶、
Ⅱ.采用金属铜单质制备硫酸铜晶体
(5)教材中用金属铜单质与浓硫酸反应制备硫酸铜,虽然生产工艺简洁,但在实际生产过程中不采用,其原因是
(6)某兴趣小组查阅资料得知:Cu+CuCl2
 2CuCl,4CuCl+O2+2H2O
2CuCl,4CuCl+O2+2H2O 2[Cu(OH)2·CuCl2],[Cu(OH)2·CuCl2]+H2SO4
2[Cu(OH)2·CuCl2],[Cu(OH)2·CuCl2]+H2SO4 CuSO4+CuCl2+2H2O。现设计如下实验来制备硫酸铜晶体,装置如图:
CuSO4+CuCl2+2H2O。现设计如下实验来制备硫酸铜晶体,装置如图:
向铜和稀硫酸的混合物中加入氯化铜溶液,利用二连球鼓入空气,将铜溶解,当三颈烧瓶中呈乳状浑浊液时,滴加浓硫酸。
①盛装浓硫酸的仪器名称为
②装置中加入CuCl2的作用是
③若开始时加入a g铜粉,含b g氯化铜溶质的氯化铜溶液,最后制得c g CuSO4·5H2O,假设整个过程中杂质不参与反应且不结晶,每步反应都进行得比较完全,则原铜粉的纯度为
您最近一年使用:0次
解题方法
10 . 用下图所示实验装置进行相应实验,能达到实验目的的是


| A.图①所示装置,蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| B.图②所示装置,分离CCl4萃取I2水后的有机层 |
| C.图③所示装置,证明氧化性:Cl2>Br2>I2 |
| D.图④所示装置,除去SO2中混有的少量HCl气体 |
您最近一年使用:0次



