名校
解题方法
1 . 某校化学小组的同学开展了一系列的化学实验活动。

请你参与实验并完成下列问题:
(1)甲同学用图1所示装置,测量锌与硫酸反应速率:把2 g 锌粒放入锥形瓶内,通过分液漏斗加入1 mol·L-1稀硫酸40 mL,收集10 mL气体,通过记录______ 得到反应速率为x mol·(L·min)-1。实验开始时检查该装置气密性的方法是_____ 。
①甲、乙两试管各有两根导管,用橡胶管连接对应接口后,倒置盛稀硫酸的试管,发生反应,放出气体,则固体混合物和稀硫酸应分别置于___ 、__ 仪器中(填仪器编号);
②G管可以用化学实验室里的一种常用仪器来替代,这种仪器的名称是___ ;
③仪器甲、乙接口的连接方式如下:A连接__ ,B连接___ ,C连接___ (填写各接口的编号);
④为提高测量的准确性,收集完气体后,丙装置读数前应进行的操作是____ 。
(3)丙同学与甲同学实验目的相同:用图3装置测定生成的CO2的质量,但该装置存在明显缺陷,从而导致实验误差___ ,请你分析其中使测定结果可能偏大的主要原因___ 。

请你参与实验并完成下列问题:
(1)甲同学用图1所示装置,测量锌与硫酸反应速率:把2 g 锌粒放入锥形瓶内,通过分液漏斗加入1 mol·L-1稀硫酸40 mL,收集10 mL气体,通过记录
①甲、乙两试管各有两根导管,用橡胶管连接对应接口后,倒置盛稀硫酸的试管,发生反应,放出气体,则固体混合物和稀硫酸应分别置于
②G管可以用化学实验室里的一种常用仪器来替代,这种仪器的名称是
③仪器甲、乙接口的连接方式如下:A连接
④为提高测量的准确性,收集完气体后,丙装置读数前应进行的操作是
(3)丙同学与甲同学实验目的相同:用图3装置测定生成的CO2的质量,但该装置存在明显缺陷,从而导致实验误差
您最近一年使用:0次
名校
解题方法
2 . 某同学为了验证难溶的氯化银在水中也存在溶解平衡,设计了如下实验方案:( )
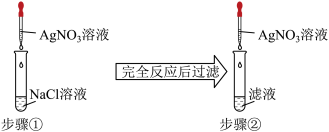

| A.步骤①中应加入过量的AgNO3溶液 |
| B.步骤①中应使NaCl溶液过量 |
| C.步骤②中现象是无沉淀产生 |
| D.步骤②中选用的AgNO3溶液浓度应小于步骤① |
您最近一年使用:0次
2020-04-03更新
|
219次组卷
|
2卷引用:2018年上海市高中学生化学竞赛(“华理一化工杯”)初赛试题
名校
解题方法
3 . 某同学采用BaSO4沉淀重量法测定样品中SO42-的含量时,发现滤液中有少许沉淀,检查滤纸并未破裂,此时他应该( )
| A.将滤液倒回漏斗重新过滤 |
| B.在漏斗中再加一张滤纸,将滤液重新过滤 |
| C.另取一漏斗,将滤液过滤后与原滤纸合并 |
| D.弃去,重新取样分析 |
您最近一年使用:0次
2020-04-03更新
|
141次组卷
|
2卷引用:2018年上海市高中学生化学竞赛(“华理一化工杯”)初赛试题
4 . 已知:连苯三酚的碱性溶液能定量吸收O2,CuCl的盐酸溶液能定量吸收CO,且易被O2氧化。拟设计实验方案,采用上述两种溶液和KOH溶液逐一吸收混合气体(由CO2、CO、N2和O2组成)的相应组分。有关该方案设计,下列说法正确的是
| A.CO的吸收必须在吸收O2后进行,因为CuCl的盐酸溶液会被O2氧化 |
| B.采用上述3种吸收剂,气体被逐一吸收的顺序是O2、CO和CO2 |
| C.其他两种吸收剂不变,O2的吸收剂可以用灼热的铜网替代 |
| D.在3种气体被逐一吸收后,导出的气体为纯净的N2 |
您最近一年使用:0次
10-11高三上·上海嘉定·期末
5 . 实验Ⅰ:证明Na2SiO3具有防火性能。
取两个相同的小木条,分别放入蒸馏水和Na2SiO3饱和溶液中,使之充分吸湿、浸透,取出稍沥干(不再滴液)后同时分别放置在酒精灯的外焰处。观察到的现象如下表:
设计实验①的目的是:___________________________________________ 。
实验Ⅱ:我们知道Na2CO3(aq)存在水解平衡,请你设计一个简单的实验证明之。简述
你的实验方法:_______________________________________________________________ ;要从该溶液中获得纯碱晶体需要的操作分别为______________________________________ 。
实验Ⅲ:探究锌与稀硫酸反应制取H2的速率
(1)可以从不同方面进行设计,请你根据影响反应速率的因素设计出几套探究方案,把其中的两套实验的方案标题写出来:①_____________________ ②_________________
(2)请根据你设计的测定方法,填写需要记录的数据及其单位:
①_____________________________ ,单位___________ ;
②______________________________ 单位___________ .
根据你测定的实验数据,处理后可求得_________ (填化学式)的反应速率,单位是:_______ 。
取两个相同的小木条,分别放入蒸馏水和Na2SiO3饱和溶液中,使之充分吸湿、浸透,取出稍沥干(不再滴液)后同时分别放置在酒精灯的外焰处。观察到的现象如下表:
| 编号 | 实验 | 现象 |
| ① | 放入蒸馏水 | 木条燃烧 |
| ② | 放入饱和Na2SiO3溶液中 | 木条不燃烧 |
设计实验①的目的是:
实验Ⅱ:我们知道Na2CO3(aq)存在水解平衡,请你设计一个简单的实验证明之。简述
你的实验方法:
实验Ⅲ:探究锌与稀硫酸反应制取H2的速率
(1)可以从不同方面进行设计,请你根据影响反应速率的因素设计出几套探究方案,把其中的两套实验的方案标题写出来:①
(2)请根据你设计的测定方法,填写需要记录的数据及其单位:
①
②
根据你测定的实验数据,处理后可求得
您最近一年使用:0次
2010·上海奉贤·二模
解题方法
6 . 下列装置或操作不能 达到实验目的的是( )
A.制少量氨气 |
B.制取干燥氢气 |
C.洗气装置 |
D.检验混合液中的Fe3+和Cu2+  |
您最近一年使用:0次
10-11高三上·上海金山·期末
解题方法
7 . (1)以前实验室制备纯碱(Na2CO3)的主要步骤为:将饱和NaCl溶液倒入烧杯加热,控制30~35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质、抽干,转入蒸发皿中灼烧得Na2CO3固体。四种盐在不同温度下的溶解度表 (g/100g水)
①反应控制在30~35℃,是因为高于35℃NH4HCO3会分解,低于30℃则反应速率降低,为控制此温度范围,通常采取的加热方法为________________ ;
②加料完毕,保温30分钟,目的____________________________ ;
③静置后只析出NaHCO3晶体的原因______________________________ ;
④过滤所得母液中含有NaHCO3、NaCl 、NH4Cl、NH4HCO3,加入适当试剂并作进一步处理,使______ (填化学式)循环使用,回收得到NH4Cl晶体。
(2)我国科学家侯德榜改革国外的纯碱生产工艺,使其更加先进,被称为侯德榜制碱法,生产流程为:

⑤ 沉淀池中反应的化学方程式:____________________________________ ;
⑥检验产品碳酸钠中是否含有氯化钠的操作方法为:________________________ 。
⑦循环(I)中应该加入或通入物质的化学式为_____________ 。
| 温度 溶解度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | — | — | — | — |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | — |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
①反应控制在30~35℃,是因为高于35℃NH4HCO3会分解,低于30℃则反应速率降低,为控制此温度范围,通常采取的加热方法为
②加料完毕,保温30分钟,目的
③静置后只析出NaHCO3晶体的原因
④过滤所得母液中含有NaHCO3、NaCl 、NH4Cl、NH4HCO3,加入适当试剂并作进一步处理,使
(2)我国科学家侯德榜改革国外的纯碱生产工艺,使其更加先进,被称为侯德榜制碱法,生产流程为:

⑤ 沉淀池中反应的化学方程式:
⑥检验产品碳酸钠中是否含有氯化钠的操作方法为:
⑦循环(I)中应该加入或通入物质的化学式为
您最近一年使用:0次
10-11高三上·上海浦东新·期末
解题方法
8 . 现有氧化铜和碳粉组成的混合物,为通过实验确定氧化铜的质量分数,某同学设计的实验方案中装置如下:

分析上述装置,回答下列问题:
(1)本实验中,酒精灯加热也可达到反应所需的温度,改用电热丝加热的优点是有利于____ 。
a.加快反应速率 b.氢气流动
c.加热温度更高 d.精确测定数据
(2)U形管中可以加入的物质是______ 。
a.无水硫酸铜 b.硅胶 c.浓硫酸 d.无水氯化钙
(3)为确保能准确测定到必要的数据,下列步骤按实验操作顺序排列应为:___________________ (填字母)。
a.停止通氢气;b.电热丝通电;c.通入氢气;d.装置气密性检查;e.电热丝停止通电。
(4)为准确测定数据,你认为本装置________ (是/否)完整?若需要改进,请在虚线下面的方框内画出所需添加的装置示意图并注明必要的物质名称___________ 。
(5)实验结束后,该同学交给老师的实验报告主要栏目如图(具体内容已略)。
请你根据实验报告的撰写要求,对此份报告作出评价,若有不完整,请在下面的空格中写出,若已完整,则无需填写___________________________________________________ 。
(6)老师看完实验报告后指出,改变实验原理可以设计出更加简便的实验方案。请你用化学方程式来表示新方案的反应原理,并指出需要测定的数据:
化学方程式___________________________ ;
需要测定的数据_________________________ 。

分析上述装置,回答下列问题:
(1)本实验中,酒精灯加热也可达到反应所需的温度,改用电热丝加热的优点是有利于
a.加快反应速率 b.氢气流动
c.加热温度更高 d.精确测定数据
(2)U形管中可以加入的物质是
a.无水硫酸铜 b.硅胶 c.浓硫酸 d.无水氯化钙
(3)为确保能准确测定到必要的数据,下列步骤按实验操作顺序排列应为:
a.停止通氢气;b.电热丝通电;c.通入氢气;d.装置气密性检查;e.电热丝停止通电。
(4)为准确测定数据,你认为本装置
(5)实验结束后,该同学交给老师的实验报告主要栏目如图(具体内容已略)。
| 实验目的:...... 实验原理:...... 实验仪器和药品:...... 实验装置:...... 实验数据处理:...... 实验误差分析:...... 实验问题讨论:...... |
(6)老师看完实验报告后指出,改变实验原理可以设计出更加简便的实验方案。请你用化学方程式来表示新方案的反应原理,并指出需要测定的数据:
化学方程式
需要测定的数据
您最近一年使用:0次
2012·上海嘉定·二模
解题方法
9 . 已知FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2。某化学兴趣研究小组探究在酒精喷灯加热条件下FeSO4分解的气体产物。已知SO3的熔点是16.8℃,沸点是44.8℃。

(1)装置II的试管中不装任何试剂,其作用是__ 。
(2)装置II的试管浸泡在50℃的水浴中,目的是__ 。
(3)装置III和装置IV的作用是探究本实验气体产物成分。请完成实验设计,填写检验试剂、预期现象与结论。__
(4)装置V的作用是防止尾气污染环境,烧杯中应加入的试剂是__ 。

(1)装置II的试管中不装任何试剂,其作用是
(2)装置II的试管浸泡在50℃的水浴中,目的是
(3)装置III和装置IV的作用是探究本实验气体产物成分。请完成实验设计,填写检验试剂、预期现象与结论。
| 检验试剂 | 预期现象与结论 |
| 装置III的试管中加入__ | 产生白色沉淀,证明气体产物中含有SO3 |
| 装置IV的试管中加入__ | __ |
您最近一年使用:0次
2013·上海闵行·一模
解题方法
10 . 完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是
| A | B | C | D | |
| 实 验 | 用CCl4提取 溴水中的Br2 | 除去乙醇中 的苯酚 | 从KI和I2的固体 混合物中回收I2 | 配制100 mL 0.1mol/L H2SO4溶液 |
| 装 置 或 仪 器 | 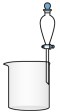 | 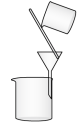 | 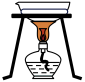 | 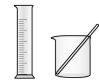 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



