名校
1 . 海洋中蕴含着丰富的资源,海水中Br-的含量约为67 mg/L,海洋植物如海带、海藻中含有丰富的碘元素,以碘离子的形式存在。
I.为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程:___________ 性。
(2)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是___________ (填“甲”或“乙”),理由___________ 。
Ⅱ.实验室里从海藻中提取碘的流程如图:___________ 中进行,其放在三角架上时还需要先放上___________ 。
(4)为寻找氯气的替代品,某同学将O2不断鼓入“含碘离子的溶液”中。请设计实验判断O2能代替氯气。(简要说明所用的试剂、现象和结论)___________
(5)操作②步骤中可供选择的有关试剂是___________ ,该操作步骤的名称为___________ 。
A.酒精 B.四氯化碳 C.醋酸 D.甘油(易溶于水)
(6)实验室中取25mL该含碘离子的溶液,用0.1mol/L的FeCl3溶液测量其中I-的浓度,反应的离子方程式为:I-+Fe3+—I2+Fe2+(未配平),若消耗FeCl3溶液22.5mL,则含碘离子的溶液中I-的浓度为:___________ 。
(7)流程中后期处理用反萃取法:___________ ,操作2的名称为___________ 。
②写出I-、IO 与45%的H2SO4溶液反应的离子方程式:
与45%的H2SO4溶液反应的离子方程式:___________ 。
I.为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程:
甲: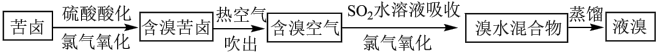
乙: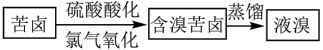
(2)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是
Ⅱ.实验室里从海藻中提取碘的流程如图:
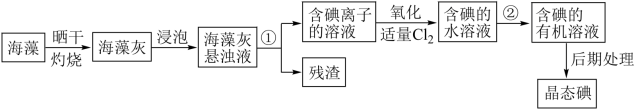
(4)为寻找氯气的替代品,某同学将O2不断鼓入“含碘离子的溶液”中。请设计实验判断O2能代替氯气。(简要说明所用的试剂、现象和结论)
(5)操作②步骤中可供选择的有关试剂是
A.酒精 B.四氯化碳 C.醋酸 D.甘油(易溶于水)
(6)实验室中取25mL该含碘离子的溶液,用0.1mol/L的FeCl3溶液测量其中I-的浓度,反应的离子方程式为:I-+Fe3+—I2+Fe2+(未配平),若消耗FeCl3溶液22.5mL,则含碘离子的溶液中I-的浓度为:
(7)流程中后期处理用反萃取法:

②写出I-、IO
 与45%的H2SO4溶液反应的离子方程式:
与45%的H2SO4溶液反应的离子方程式:
您最近半年使用:0次
名校
解题方法
2 . 中国有广阔的海岸线,建设发展海洋经济、海水的综合利用大有可为。
Ⅰ.海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:___________ 中进行。
(2)操作Ⅰ中具体实验步骤:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.检验分液漏斗旋塞和上口的瓶塞是否漏液;
C.把20mL碘水与5mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
D.倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.将分液漏斗上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
G.从分液漏斗上口倒出上层溶液;
H.静止、分层;
实验步骤的正确顺序为___________ 。
_____→_____→_____→A→H→_____→_____→_____
(3)为寻找氯水的替代品,某同学设计了用 代替氯水。请写出此反应的离子方程式:
代替氯水。请写出此反应的离子方程式:___________ 。
Ⅱ.空气吹出法工艺,是目前“海水提溴”的最主要方法之一,其流程如图所示,试回答下列问题:___________ 。
(5)步骤Ⅱ中涉及的离子方程式如下,请在下面横线上填入适当的化学计量数___________ 。
_____ _____
_____ _____
_____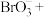 _____
_____ _____
_____
(6)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:___________ 。
Ⅲ.镁及其合金是一种用途很广的金属材料,目前60%的镁是从海水中提取的。主要步骤如下: 转化为
转化为 ,试剂①工业上选用
,试剂①工业上选用___________ (填化学式)。
(8)熔融状态的无水 通电后会产生Mg和
通电后会产生Mg和 ,试写出该反应的化学方程式:
,试写出该反应的化学方程式:___________ 。
Ⅰ.海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:
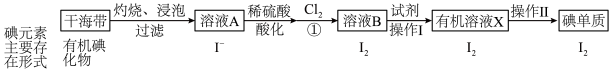
(2)操作Ⅰ中具体实验步骤:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.检验分液漏斗旋塞和上口的瓶塞是否漏液;
C.把20mL碘水与5mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
D.倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.将分液漏斗上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
G.从分液漏斗上口倒出上层溶液;
H.静止、分层;
实验步骤的正确顺序为
_____→_____→_____→A→H→_____→_____→_____
(3)为寻找氯水的替代品,某同学设计了用
 代替氯水。请写出此反应的离子方程式:
代替氯水。请写出此反应的离子方程式:Ⅱ.空气吹出法工艺,是目前“海水提溴”的最主要方法之一,其流程如图所示,试回答下列问题:
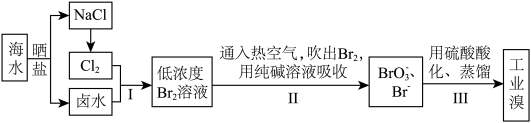
(5)步骤Ⅱ中涉及的离子方程式如下,请在下面横线上填入适当的化学计量数
_____
 _____
_____ _____
_____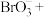 _____
_____ _____
_____
(6)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:
Ⅲ.镁及其合金是一种用途很广的金属材料,目前60%的镁是从海水中提取的。主要步骤如下:
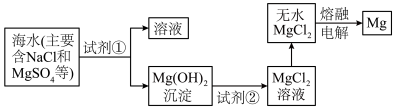
 转化为
转化为 ,试剂①工业上选用
,试剂①工业上选用(8)熔融状态的无水
 通电后会产生Mg和
通电后会产生Mg和 ,试写出该反应的化学方程式:
,试写出该反应的化学方程式:
您最近半年使用:0次
名校
3 . 按要求填空:
(1)现有8个微粒: ;
; ;
;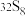 ;
;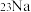 ;
;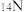 ;
; ;
; ;
; ;
;
表示核素的符号共______ 种;互为同位素的是______ 。
(2)现有以下物质:① ;②
;② ;③NaOH;④
;③NaOH;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ 。
。
其中由离子键和非极性共价键构成的物质是______ (填序号,下同),属于共价化合物的是______ 。
(3)下列变化:①碘升华;②冰融化;③氯化钠溶于水;④氯化氢溶于水;⑤氢氧化钠溶于水。化学键未被破坏的是______ (填序号),仅离子键被破坏的是______ (填序号)。
(4)海带灰中富含以 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如下所示:
的途径如下所示:______ 。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式______ 。反应结束后,再加入 作萃取剂,振荡、静置,该步操作用到的仪器名称为
作萃取剂,振荡、静置,该步操作用到的仪器名称为______ ,可以观察到 层呈
层呈______ 色。
(1)现有8个微粒:
 ;
; ;
;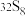 ;
;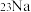 ;
;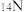 ;
; ;
; ;
; ;
;表示核素的符号共
(2)现有以下物质:①
 ;②
;② ;③NaOH;④
;③NaOH;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ 。
。其中由离子键和非极性共价键构成的物质是
(3)下列变化:①碘升华;②冰融化;③氯化钠溶于水;④氯化氢溶于水;⑤氢氧化钠溶于水。化学键未被破坏的是
(4)海带灰中富含以
 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如下所示:
的途径如下所示:
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
 作萃取剂,振荡、静置,该步操作用到的仪器名称为
作萃取剂,振荡、静置,该步操作用到的仪器名称为 层呈
层呈
您最近半年使用:0次
名校
解题方法
4 . 下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 海带中提取碘单质时,用酒精做萃取剂 | 液体分层,下层溶液为紫红色 | 碘在有机溶剂中溶解度较大 |
| B | 工业上用 与焦炭在高温条件制备粗硅检测 与焦炭在高温条件制备粗硅检测 | 生成可燃性气体,得到黑色固体粗硅 | 非金属性: |
| C | 向 溶液中逐滴加入稀氨水至过量 溶液中逐滴加入稀氨水至过量 | 产生白色沉淀,并逐渐增多,后慢慢溶解 | 碱性: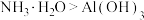 |
| D | 向足量NaBr溶液中通入少量氯气,再加入淀粉KI溶液 | 溶液先变橙色,后变为蓝色 | 氧化性: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
5 . 某同学取干海带经下列加工流程,从中提取I2.下列说法错误的是


| A.操作1中至少包括灼烧、溶解、过滤等主要过程 |
B.试剂a可以是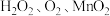 等氧化剂,试剂b可以是 等氧化剂,试剂b可以是 |
| C.操作2和3均需用到分液漏斗,萃取振荡时应将分液漏斗下口向上倾斜,并不时放气 |
D. 可循环利用以有效提高干海带提碘的产率 可循环利用以有效提高干海带提碘的产率 |
您最近半年使用:0次
名校
解题方法
6 . 将碘单质从碘的四氯化碳溶液中提取出来可以采用反萃取法,其流程如图所示,下列说法错误的是

| A.操作①需要用到的玻璃仪器有分液漏斗和烧杯 |
B.加入45%的 溶液,发生反应的离子方程式为 溶液,发生反应的离子方程式为 |
C.往某溶液中加入稀硫酸酸化的 和淀粉的混合溶液后,溶液变蓝,则说明原溶液含有 和淀粉的混合溶液后,溶液变蓝,则说明原溶液含有 |
| D.碘酒可用于伤口消毒,自然界中不存在游离态的碘单质 |
您最近半年使用:0次
名校
7 . 实验室里进行碘的提取,①向盛有KI(aq)的试管中加入少许CCl4后滴加氯水,振荡、静置后,CCl4层变成紫色。②分离出CCl4层,③继续向其中滴加新制氯水,充分振荡,CCl4层会逐渐变浅,最后变成无色。上层水溶液也呈无色。
(1)写出CCl4层由无色变成紫色的化学方程式:_______ 。
(2)分离出CCl4层使用的实验仪器匙:_______ 。
(3)取最终上层水溶液,滴加淀粉溶液,溶液不变蓝,说明:________ 。再经实验测定,最终碘元素以HIO3形式存在,请写出③反应的化学方程式并配平:_______ 。若使用新制氯水和淀粉溶液,请写出检验溶液中含有I-的实验过程:_______ 。
(4)向用硫酸酸化的NaI溶液中中逐滴加入NaBrO3溶液,当加入2.6molNaBrO3时,测得反应后溶液中溴元素和碘元素的存在形式及物质的量如表。
请根据氧化还原反应中化合价升高和降低的总数相等的原则,通过计算判断反应后的溶液中是否存在IO ?
?_______ 。若存在,则IO 的物质的最是多少
的物质的最是多少_______ ?写出计算过程。
(1)写出CCl4层由无色变成紫色的化学方程式:
(2)分离出CCl4层使用的实验仪器匙:
(3)取最终上层水溶液,滴加淀粉溶液,溶液不变蓝,说明:
(4)向用硫酸酸化的NaI溶液中中逐滴加入NaBrO3溶液,当加入2.6molNaBrO3时,测得反应后溶液中溴元素和碘元素的存在形式及物质的量如表。
| 粒子 | I2 | Br2 | IO |
| n/mol | 0.5 | 1.3 | 未知 |
 ?
? 的物质的最是多少
的物质的最是多少
您最近半年使用:0次
8 . 海带中含有丰富的碘,某校化学兴趣小组的同学们设计联合氯碱工业,以海带灰为原料提碘的工艺流程如下:

回答下列问题:
(1)“浸取”操作需要进行2~3次,将所得浸取液合并后进入下一流程,其目的是________ ;请你设计实验证明“浸取"已经进行完全:________ (需要用到的实验药品有:淀粉溶液、硫酸酸化的H2O2溶液,写出具体实验操作和现象)。
(2)“电解”反应的化学方程式为________ 。
(3)“萃取”时,CCl4层的颜色为________ 色;“反萃取”时生成NaI和NaIO3,写出该反应的离子方程式:________ 。
(4)“酸化”后生成含I2的悬浊液,需要经过________ (填操作名称)操作得到I2。
(5)该工艺流程中,除了H2O和NaCl以外,可以循环利用的物质有________ (填化学式)。

回答下列问题:
(1)“浸取”操作需要进行2~3次,将所得浸取液合并后进入下一流程,其目的是
(2)“电解”反应的化学方程式为
(3)“萃取”时,CCl4层的颜色为
(4)“酸化”后生成含I2的悬浊液,需要经过
(5)该工艺流程中,除了H2O和NaCl以外,可以循环利用的物质有
您最近半年使用:0次
解题方法
9 . 海带中含有丰富的碘元素。为从海带中提取单质碘,某研究性学习小组设计并进行以下实验:

提示:苯是有机萃取剂,其密度小于水。
请填写下列空白:
(1)步骤③中过滤操作时,除需要铁架台、烧杯,还需用到的玻璃仪器是_________ 。
(2)步骤中④反应的离子方程式是_________ 。
(3)步骤⑤的实验操作名称分别是_________ 。
(4)步骤⑤中,某学生选择用苯来提取碘单质,有机层在_________ 层(上、下),呈_____________ 色。
(5)步骤⑥为反萃取操作,应先加入 溶液,写出碘单质与
溶液,写出碘单质与  溶液反应的离子方程式
溶液反应的离子方程式_________ 。

提示:苯是有机萃取剂,其密度小于水。
请填写下列空白:
(1)步骤③中过滤操作时,除需要铁架台、烧杯,还需用到的玻璃仪器是
(2)步骤中④反应的离子方程式是
(3)步骤⑤的实验操作名称分别是
(4)步骤⑤中,某学生选择用苯来提取碘单质,有机层在
(5)步骤⑥为反萃取操作,应先加入
 溶液,写出碘单质与
溶液,写出碘单质与  溶液反应的离子方程式
溶液反应的离子方程式
您最近半年使用:0次
名校
解题方法
10 . 某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一)碘含量的测定
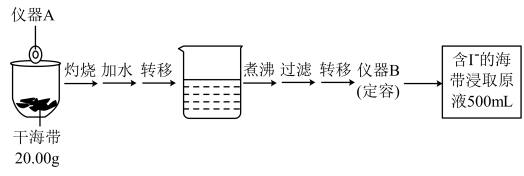
取100.00mL海带浸取原液于锥形瓶中,用 的
的 标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00mL。
标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00mL。
(1)仪器A的名称为_____ ;仪器B的名称为:_____ 。
(2)计算海带中碘的百分含量为_____ %。
实验(二)碘的制取
另取海带浸取原液,甲、乙两种实验方案如下:

已知: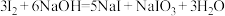 ;酸性条件下,
;酸性条件下, 在水溶液中的溶解度很小。
在水溶液中的溶解度很小。
(3)“适量 ”中能代替
”中能代替 的最佳物质的电子式为
的最佳物质的电子式为_____ 。
(4)下列有关步骤Y的说法,正确的是_____。
(5)方案乙中,上层液体加入 溶液,反应的离子方程式为:
溶液,反应的离子方程式为:_____ ,其中操作Z的名称是_____ 。
实验(一)碘含量的测定

取100.00mL海带浸取原液于锥形瓶中,用
 的
的 标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00mL。
标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00mL。(1)仪器A的名称为
(2)计算海带中碘的百分含量为
实验(二)碘的制取
另取海带浸取原液,甲、乙两种实验方案如下:

已知:
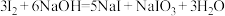 ;酸性条件下,
;酸性条件下, 在水溶液中的溶解度很小。
在水溶液中的溶解度很小。(3)“适量
 ”中能代替
”中能代替 的最佳物质的电子式为
的最佳物质的电子式为(4)下列有关步骤Y的说法,正确的是_____。
A.应控制 溶液的浓度和体积 溶液的浓度和体积 |
| B.将碘转化成离子进入水层 |
| C.主要是除浸取原液中的有机杂质 |
D. 溶液可由乙醇代替 溶液可由乙醇代替 |
(5)方案乙中,上层液体加入
 溶液,反应的离子方程式为:
溶液,反应的离子方程式为:
您最近半年使用:0次



