名校
解题方法
1 . 海洋是最大的资源宝库,可以提取钾、镁、溴、氯、碘等元素。下列说法正确的是
| A.海带中富含碘元素,在海带中以碘单质形式存在 |
| B.空气吹出法提取溴利用了溴的挥发性 |
| C.海带提碘和海水提溴的关键步骤只有氧化,无需富集 |
D.分别向碘水、溴水加入 ,振荡后下层均呈现出紫色 ,振荡后下层均呈现出紫色 |
您最近半年使用:0次
2 . 海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是_______ (填序号)。
(2)海带中含有碘元素。实验室提取碘的步骤如图所示:

①海带灰中含有硫酸镁、碳酸钠等,在实验步骤_______ (填序号)中实现与碘分离。
②写出步骤④反应的离子方程式_______ 。提取碘的过程中,不能选择乙醇代替CCl4提取碘单质的原因_______ 。
(1)无需经过化学变化就能从海水中获得的物质是
| A.食盐 | B.溴 | C.烧碱 | D.纯碱 |

①海带灰中含有硫酸镁、碳酸钠等,在实验步骤
②写出步骤④反应的离子方程式
您最近半年使用:0次
名校
解题方法
3 . 实验室从干海带中提取碘的流程如图所示.下列各操作所使用的装置正确的是
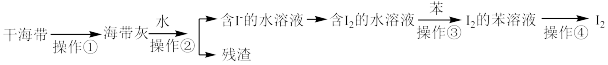
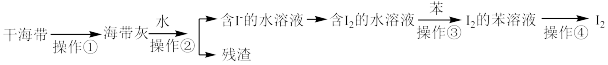
A.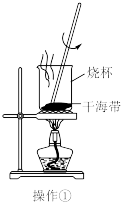 | B. | C. | D. |
您最近半年使用:0次
解题方法
4 . 化学与生活、生产密切相关,下列说法错误的是
| A.使用医用酒精、紫外线杀菌消毒的过程中均涉及蛋白质变性 |
| B.工业上可采用离子交换法提高海带中碘的提取率 |
| C.使用常温下与浓硫酸不反应的铁质容器贮运浓硫酸 |
| D.晨雾中的光束如梦似幻,是丁达尔效应带来的美景 |
您最近半年使用:0次
名校
5 . 从干海带中提取碘的实验流程如下,下列有关说法

| A.氧化过程可以用过氧化氢代替氯水 |
B.试剂X可以选择使用NaOH,发生反应为:3I2 + 6OH- = 5I- + IO +3H2O +3H2O |
| C.萃取时可使用无水乙醇代替CCl4以节约成本 |
| D.操作I需要使用到普通漏斗、烧杯和玻璃棒 |
您最近半年使用:0次
解题方法
6 . 碘元素是人体的必需微量元素之一。某学习小组在实验室进行海带提碘的探究,其流程如下:

上述实验过程中未涉及的操作是

上述实验过程中未涉及的操作是
A.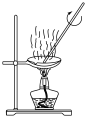 | B.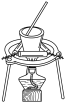 | C.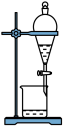 | D.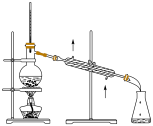 |
您最近半年使用:0次
7 . Ⅰ.海水中的氯化钠被提纯和精制后,可通过电解饱和食盐水制取氯气、氢气和氢氧化钠。实验室电解饱和食盐水所用装置如下图所示:___________ 。
A.试管 B.离心试管 C.U形管 D.Y形试管
②在a的两端滴加酚酞试液,通电后左边电极周围出现红色,写出该电极的电极反应式说明溶液变红的原因___________ 。
(2)通电后试管b中淀粉KI溶液由无色变为蓝色,结合离子方程式说明变化原因。___________ 。
(3)c处出来的气体可以点燃,其燃烧的现象是___________ 。
Ⅱ.地球上99%的溴元素分布在海洋中。空气吹出法工艺是目前“海水提溴”的主要方法之一,工艺流程如下图所示:
(5)上述流程中热空气吹出已经得到了粗溴,为什么还要添加“SO2吸收、氧化、水蒸气吹出”三个步骤,其目的是___________ 。
Ⅲ.海洋中的海带等海藻类植物具有富集碘的能力,工业上获取碘的主要流程如下图所示:
Ⅳ.硫元素和氮元素也存在于海洋中。
(7) 是海洋中硫元素的主要存在形式之一,其存在会干扰海水中Cl-的检验。检验海水中Cl-的方法是
是海洋中硫元素的主要存在形式之一,其存在会干扰海水中Cl-的检验。检验海水中Cl-的方法是___________ 。
(8)氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环起始于氮的固定,过程可用下图表示。下列关于海洋氮循环的说法正确的是___________。
(9)N、O、S三种元素第一电离能由大到小的顺序为___________ 。
A.O > S > N B.S > N > O C.N > O > S D.O > N > S
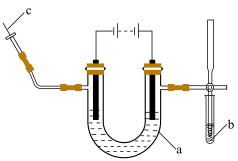
A.试管 B.离心试管 C.U形管 D.Y形试管
②在a的两端滴加酚酞试液,通电后左边电极周围出现红色,写出该电极的电极反应式说明溶液变红的原因
(2)通电后试管b中淀粉KI溶液由无色变为蓝色,结合离子方程式说明变化原因。
(3)c处出来的气体可以点燃,其燃烧的现象是
Ⅱ.地球上99%的溴元素分布在海洋中。空气吹出法工艺是目前“海水提溴”的主要方法之一,工艺流程如下图所示:
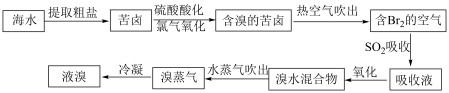
| A.溴离子的还原性 | B.溴单质的还原性 | C.溴的沸点高 | D.HBr极易溶于水 |
(5)上述流程中热空气吹出已经得到了粗溴,为什么还要添加“SO2吸收、氧化、水蒸气吹出”三个步骤,其目的是
Ⅲ.海洋中的海带等海藻类植物具有富集碘的能力,工业上获取碘的主要流程如下图所示:
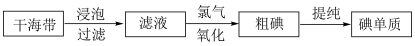
| A.酒精 | B.裂化汽油 | C.四氯化碳 | D.乙酸 |
Ⅳ.硫元素和氮元素也存在于海洋中。
(7)
 是海洋中硫元素的主要存在形式之一,其存在会干扰海水中Cl-的检验。检验海水中Cl-的方法是
是海洋中硫元素的主要存在形式之一,其存在会干扰海水中Cl-的检验。检验海水中Cl-的方法是(8)氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环起始于氮的固定,过程可用下图表示。下列关于海洋氮循环的说法正确的是___________。
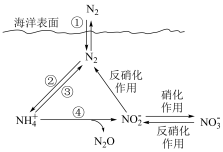
| A.海洋中的氮循环起始于氮的氧化 | B.海洋中的氮循环属于固氮作用的是③ |
| C.海洋中的硝化作用可能有氧气的参与 | D.NH4NO3中只含离子键 |
(9)N、O、S三种元素第一电离能由大到小的顺序为
A.O > S > N B.S > N > O C.N > O > S D.O > N > S
您最近半年使用:0次
名校
解题方法
8 . 海洋中蕴含着丰富的化学元素,是人类资源的宝库。
I.某学校兴趣小组在实验室按如下实验流程提取海带中的碘。

(1)海带灼烧的目的是___________ 。海带灰中含有的其他可溶性无机盐,是在___________ (从以上流程中选填实验操作名称)中实现与碘分离。上述实验流程中不需要用到的仪器是___________ (从下列图中选择,写出名称)。

(2)“氧化”时加入3mol·L-1H2SO4和3%H2O2溶液,发生反应的离子方程式为___________ 。
(3)加碘食盐中的碘以KIO3形式存在,证明食盐中存在IO ,必须使用的物质是
,必须使用的物质是___________ (填序号)。
①pH试纸 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④蒸馏水 ⑤食醋 ⑥醇
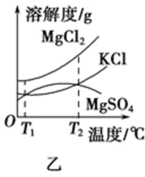
Ⅱ.某学校兴趣小组从海水晒盐后的盐卤(含MgCl2、NaCl、KCl、MgSO4等)中模拟工业生产来提取镁,主要过程如图甲:
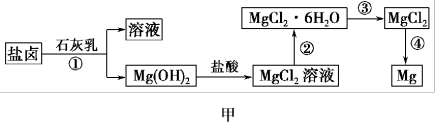
(4)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到T2℃以上,根据溶解度曲线,首先从盐卤中分离出来的晶体是___________ 。步骤③的具体操作为___________ 。
(5)写出步骤④制备金属镁的化学方程式:___________ 。该过程得到的镁蒸气需要在特定的循环中冷却,可选用___________ (填字母)作冷却剂。
A.Ar B.CO2 C.空气 D.O2 E.水蒸气
I.某学校兴趣小组在实验室按如下实验流程提取海带中的碘。

(1)海带灼烧的目的是

(2)“氧化”时加入3mol·L-1H2SO4和3%H2O2溶液,发生反应的离子方程式为
(3)加碘食盐中的碘以KIO3形式存在,证明食盐中存在IO
 ,必须使用的物质是
,必须使用的物质是①pH试纸 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④蒸馏水 ⑤食醋 ⑥醇
Ⅱ.某学校兴趣小组从海水晒盐后的盐卤(含MgCl2、NaCl、KCl、MgSO4等)中模拟工业生产来提取镁,主要过程如图甲:

(4)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到T2℃以上,根据溶解度曲线,首先从盐卤中分离出来的晶体是

(5)写出步骤④制备金属镁的化学方程式:
A.Ar B.CO2 C.空气 D.O2 E.水蒸气
您最近半年使用:0次
9 . 海水的综合利用是当今的热点话题之一。
I.利用海水脱硫可以有效地解决煤燃烧过程中排放的 造成的一系列环境问题。其工艺流程如图所示:
造成的一系列环境问题。其工艺流程如图所示:
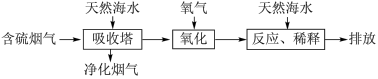
(1)天然海水 吸收含硫的烟气后,会溶有
吸收含硫的烟气后,会溶有 等分子或离子,需要用氧气进行氧化处理,写出
等分子或离子,需要用氧气进行氧化处理,写出 参加反应的离子方程式
参加反应的离子方程式___________ 。
(2)氧化后的海水需要加入 ,与之混合后才能排放。该操作的主要目的是
,与之混合后才能排放。该操作的主要目的是___________ 。
II.从海水中提纯粗盐后的母液中含有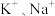 和
和 等阳离子。对母液进行一系列的加工可制得金属镁。
等阳离子。对母液进行一系列的加工可制得金属镁。
(3)从离子反应的角度思考,在母液中加入石灰乳所起的作用是___________ 。
(4)电解熔融的无水氯化镁所得的镁蒸气在特定的环境中冷却后即为固体镁。
___________ (填“能”或“不能”)用作镁蒸气的冷却剂。
III.海带中含有碘元素。从海带中提取碘的实验过程如图:

(5)步骤③会用到下列仪器中的___________(填字母)。
(6)海带灰悬浊液含有 。步骤④的试剂选用
。步骤④的试剂选用 、稀硫酸,发生反应的离子方程式为
、稀硫酸,发生反应的离子方程式为_____ 。
(7)步骤⑤“提取”包含以下四个过程:

过程I使用的 体积明显小于含
体积明显小于含 溶液,即可使
溶液,即可使 几乎完全地转移至
几乎完全地转移至 中,推测
中,推测 在
在________ (填“ ”或“
”或“ ”)中的溶解度更大。
”)中的溶解度更大。
② 与
与 浓溶液反应的离子方程式为
浓溶液反应的离子方程式为___________ 。
③过程I→过程III的目的是___________ 。
I.利用海水脱硫可以有效地解决煤燃烧过程中排放的
 造成的一系列环境问题。其工艺流程如图所示:
造成的一系列环境问题。其工艺流程如图所示:
(1)天然海水
 吸收含硫的烟气后,会溶有
吸收含硫的烟气后,会溶有 等分子或离子,需要用氧气进行氧化处理,写出
等分子或离子,需要用氧气进行氧化处理,写出 参加反应的离子方程式
参加反应的离子方程式(2)氧化后的海水需要加入
 ,与之混合后才能排放。该操作的主要目的是
,与之混合后才能排放。该操作的主要目的是II.从海水中提纯粗盐后的母液中含有
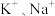 和
和 等阳离子。对母液进行一系列的加工可制得金属镁。
等阳离子。对母液进行一系列的加工可制得金属镁。(3)从离子反应的角度思考,在母液中加入石灰乳所起的作用是
(4)电解熔融的无水氯化镁所得的镁蒸气在特定的环境中冷却后即为固体镁。

III.海带中含有碘元素。从海带中提取碘的实验过程如图:

(5)步骤③会用到下列仪器中的___________(填字母)。
| A.酒精灯 | B.漏斗 | C.试管 | D.玻璃棒 |
(6)海带灰悬浊液含有
 。步骤④的试剂选用
。步骤④的试剂选用 、稀硫酸,发生反应的离子方程式为
、稀硫酸,发生反应的离子方程式为(7)步骤⑤“提取”包含以下四个过程:

过程I使用的
 体积明显小于含
体积明显小于含 溶液,即可使
溶液,即可使 几乎完全地转移至
几乎完全地转移至 中,推测
中,推测 在
在 ”或“
”或“ ”)中的溶解度更大。
”)中的溶解度更大。②
 与
与 浓溶液反应的离子方程式为
浓溶液反应的离子方程式为③过程I→过程III的目的是
您最近半年使用:0次
解题方法
10 . 卤族元素包含F(氟)、Cl(氯)、Br(溴)和I(碘)等元素,卤族元素的单质及其化合物在生产生活中有着重要的应用,人们从自然界中获得卤族单质及基化合物的过程,体现了化学科学在利用自然资源创造新物质中的独特作用,根据所学知识及所给信息,回答下列问题:
(1)写出 的离子结构示意图
的离子结构示意图_______ 。
(2)氯元素存在 、
、 两种核素,由这两种
两种核素,由这两种 、
、 核素构成的氯气单质有
核素构成的氯气单质有_______ 种。
(3)将氯气通入紫色石蕊溶液中,实验的现象是_______ ,结合离子方程式加上必要的文字解释原因_______ 。
(4)从海带中提取碘单质的工艺流程如下,其中海带灰溶于水后碘的存在形成是 。干海带
。干海带 海带灰
海带灰 悬浊液
悬浊液 滤液
滤液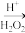 碘水。工艺流程中不会用到的实验仪器有
碘水。工艺流程中不会用到的实验仪器有_______ 。
①酒精灯 ②三脚架 ③泥三角 ④分液漏斗 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒 ⑧量筒 ⑨漏斗
向“滤液”中加入 和
和 发生的离子方程式为
发生的离子方程式为_______ ;检验提取的碘水中含有 的试剂是
的试剂是_______ 。
(5)从海水晒盐后的盐卤(主要含 、
、 、
、 、
、 等)中模拟工业生产来提取镁,主要流程如图:
等)中模拟工业生产来提取镁,主要流程如图:

从流程提取镁的反应①~⑥中,没有涉及到的四种基本反应类型的是_______ 反应。工业上从盐卤中获取 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是_______ 。写出 与盐酸反应的离子方程式
与盐酸反应的离子方程式_______ 。
(1)写出
 的离子结构示意图
的离子结构示意图(2)氯元素存在
 、
、 两种核素,由这两种
两种核素,由这两种 、
、 核素构成的氯气单质有
核素构成的氯气单质有(3)将氯气通入紫色石蕊溶液中,实验的现象是
(4)从海带中提取碘单质的工艺流程如下,其中海带灰溶于水后碘的存在形成是
 。干海带
。干海带 海带灰
海带灰 悬浊液
悬浊液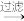 滤液
滤液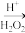 碘水。工艺流程中不会用到的实验仪器有
碘水。工艺流程中不会用到的实验仪器有①酒精灯 ②三脚架 ③泥三角 ④分液漏斗 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒 ⑧量筒 ⑨漏斗
向“滤液”中加入
 和
和 发生的离子方程式为
发生的离子方程式为 的试剂是
的试剂是(5)从海水晒盐后的盐卤(主要含
 、
、 、
、 、
、 等)中模拟工业生产来提取镁,主要流程如图:
等)中模拟工业生产来提取镁,主要流程如图:
从流程提取镁的反应①~⑥中,没有涉及到的四种基本反应类型的是
 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是 与盐酸反应的离子方程式
与盐酸反应的离子方程式
您最近半年使用:0次



