解题方法
1 . 一种自生酸和碱的电化学回收体系,原理如图所示。在Ⅲ室中将 等含磷微粒转化为羟基磷灰石
等含磷微粒转化为羟基磷灰石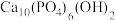 (
(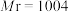 ),同时将
),同时将 转化为
转化为 ,实现废水中的
,实现废水中的 等含磷微粒和
等含磷微粒和 的回收。下列说法
的回收。下列说法不正确 的是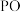 表示
表示 等含磷微粒,
等含磷微粒, 为羟基磷灰石)
为羟基磷灰石)
 等含磷微粒转化为羟基磷灰石
等含磷微粒转化为羟基磷灰石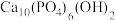 (
(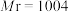 ),同时将
),同时将 转化为
转化为 ,实现废水中的
,实现废水中的 等含磷微粒和
等含磷微粒和 的回收。下列说法
的回收。下列说法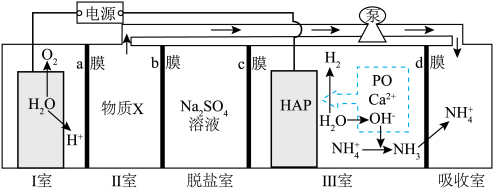
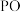 表示
表示 等含磷微粒,
等含磷微粒, 为羟基磷灰石)
为羟基磷灰石)| A.a、c为阳离子交换膜,b为阴离子交换膜 |
B.Ⅲ室可发生反应: |
C.当电路中通过 电子,阴极增重10.04g 电子,阴极增重10.04g |
D.物质X为硫酸溶液,将其泵入吸收室用于吸收 |
您最近一年使用:0次
2 . 中和渣是有色金属冶炼过程中产生的危险废渣。从中和渣(主要含有 和少量
和少量 、
、 、
、 、
、 的氢氧化物)中回收铜、锌等金属的工艺流程如下图:
的氢氧化物)中回收铜、锌等金属的工艺流程如下图: ,几种物质的
,几种物质的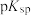 如下表
如下表
②当金属离子浓度小于 时,视为沉淀完全
时,视为沉淀完全
回答下列问题:
(1)“中性浸出”时,采用“中性”的目的是________ 。
(2)“高温高酸浸出”时,“浸渣2”的主要成分为________ 。
(3)“萃铜”时发生反应 ,
,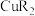 的结构简式如图所示:
的结构简式如图所示: 的价层电子排布图
的价层电子排布图________ 。
②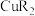 水溶性差的原因是
水溶性差的原因是________ (选填序号)。
a.形成分子内氢键 b.分子结构较稳定 c.亲油基团起主导作用
③萃取剂HR的结构简式为________ 。
(4)“氧化沉淀”时,试剂X用以调节溶液的pH。
①加入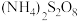 溶液时生成
溶液时生成 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为________ 。
②沉淀后溶液的pH需不低于________ 。
(5)该流程中,可以循环使用的物质有________ 。
(6)某黄铜合金晶胞结构如图,其中A、B的原子坐标均可为 。与Zn原子距离最近且相等的Cu原子有
。与Zn原子距离最近且相等的Cu原子有________ 个,C的原子坐标为________ 。
 和少量
和少量 、
、 、
、 、
、 的氢氧化物)中回收铜、锌等金属的工艺流程如下图:
的氢氧化物)中回收铜、锌等金属的工艺流程如下图: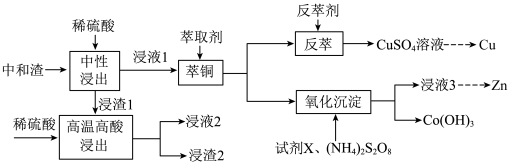
 ,几种物质的
,几种物质的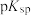 如下表
如下表物质 |
|
|
|
|
|
| 37.4 | 14.6 | 43.7 | 16.9 | 19.6 |
 时,视为沉淀完全
时,视为沉淀完全回答下列问题:
(1)“中性浸出”时,采用“中性”的目的是
(2)“高温高酸浸出”时,“浸渣2”的主要成分为
(3)“萃铜”时发生反应
 ,
,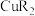 的结构简式如图所示:
的结构简式如图所示: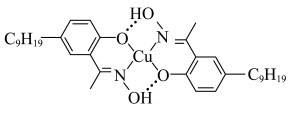
 的价层电子排布图
的价层电子排布图②
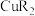 水溶性差的原因是
水溶性差的原因是a.形成分子内氢键 b.分子结构较稳定 c.亲油基团起主导作用
③萃取剂HR的结构简式为
(4)“氧化沉淀”时,试剂X用以调节溶液的pH。
①加入
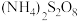 溶液时生成
溶液时生成 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为②沉淀后溶液的pH需不低于
(5)该流程中,可以循环使用的物质有
(6)某黄铜合金晶胞结构如图,其中A、B的原子坐标均可为
 。与Zn原子距离最近且相等的Cu原子有
。与Zn原子距离最近且相等的Cu原子有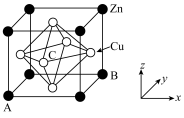
您最近一年使用:0次
3 . 工业生产中采用水解中和法处理含铜废水。常温下,向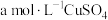 溶液中逐渐加入NaOH固体,发生的反应有:
溶液中逐渐加入NaOH固体,发生的反应有:
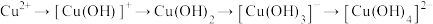
溶液中含铜微粒的分布系数随pH的变化如图所示。
(已知:分布系数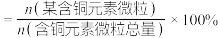 ;忽略加入固体后溶液体积的变化。)
;忽略加入固体后溶液体积的变化。)
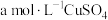 溶液中逐渐加入NaOH固体,发生的反应有:
溶液中逐渐加入NaOH固体,发生的反应有: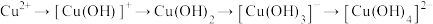
溶液中含铜微粒的分布系数随pH的变化如图所示。
(已知:分布系数
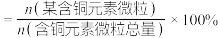 ;忽略加入固体后溶液体积的变化。)
;忽略加入固体后溶液体积的变化。)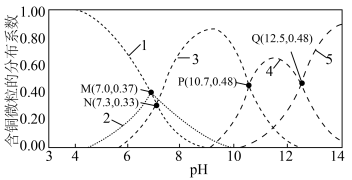
A.曲线4代表的含铜微粒为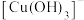 |
B. 时, 时,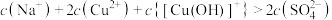 |
C. 的平衡常数为 的平衡常数为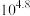 |
D.M点混合溶液中 的浓度为 的浓度为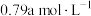 |
您最近一年使用:0次
2024-05-17更新
|
150次组卷
|
2卷引用:2024届福建省三明市高三下学期三模化学试题
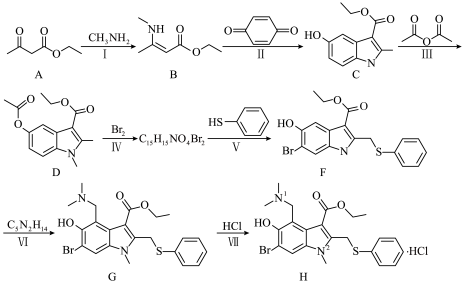
4 . 盐酸阿比朵尔H具有良好的抗病毒活性,其中一种合成路线如图:
(1)A的官能团有酯基和_______ 。
(2)反应I分两步完成,X为中间产物。从电负性视角预测中间产物X,其结构简式为_______ ,第二步反应的类型为_______ 。
(3)反应III的目的是_______ 。
(4)请写出反应IV的化学方程式:_______ 。
(5)反应VI是取代反应,试剂C5N2H14的结构简式为_______ 。
(6)盐酸阿比朵尔H中H+与碱性强的氮原子形成配位键,H+与_______ 号N结合(填“1”或“2”)。
(7)J是B的同分异构体,请写出一种符合下列所有条件的J的结构简式:_______ 。
a.能与金属Na反应产生H2
b.有且仅有两种官能团
c.有1个6元碳环
d.核磁共振氢谱有6组峰,峰面积比为4:4:2:1:1:1
(8)设计以乙烯为原料合成A的路线(用流程图表示,无机试剂任选)_______ 。
(1)A的官能团有酯基和
(2)反应I分两步完成,X为中间产物。从电负性视角预测中间产物X,其结构简式为
(3)反应III的目的是
(4)请写出反应IV的化学方程式:
(5)反应VI是取代反应,试剂C5N2H14的结构简式为
(6)盐酸阿比朵尔H中H+与碱性强的氮原子形成配位键,H+与
(7)J是B的同分异构体,请写出一种符合下列所有条件的J的结构简式:
a.能与金属Na反应产生H2
b.有且仅有两种官能团
c.有1个6元碳环
d.核磁共振氢谱有6组峰,峰面积比为4:4:2:1:1:1
(8)设计以乙烯为原料合成A的路线(用流程图表示,无机试剂任选)
已知: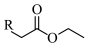 +
+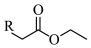
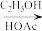
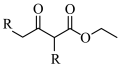 +
+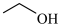
您最近一年使用:0次
5 . 乙醇水蒸气重整制氢是生物质制氢的重要方法,有关反应如下:
ⅰ、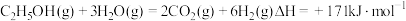 (主反应)
(主反应)
ⅱ、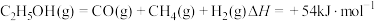
ⅲ、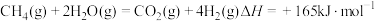
ⅳ、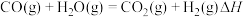
(1)反应ⅳ的
_____  。
。
(2)Akande等研究了以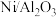 为催化剂的乙醇水蒸气重整反应。下列说法正确的是
为催化剂的乙醇水蒸气重整反应。下列说法正确的是_____ (填序号)。
A.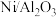 能改变重整反应的历程,因而能改变反应ⅰ的焓变
能改变重整反应的历程,因而能改变反应ⅰ的焓变
B.使用适宜的催化剂提高 的选择性,从而提高
的选择性,从而提高 的平衡产率
的平衡产率
C.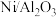 能降低重整反应的活化能,大幅增大反应的速率常数
能降低重整反应的活化能,大幅增大反应的速率常数
(3)在2L刚性容器中,充入 和若干
和若干 ,平衡时产生
,平衡时产生 物质的量与温度、水-乙醇比(水与乙醇物质的量比)的关系如图1所示(曲线上标注的数字为
物质的量与温度、水-乙醇比(水与乙醇物质的量比)的关系如图1所示(曲线上标注的数字为 物质的量/mol)。900K时,
物质的量/mol)。900K时,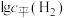 与
与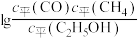 的关系如图2所示。
的关系如图2所示。_____ 。水-乙醇比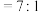 时,产生氢气的量随温度升高的变化趋势是
时,产生氢气的量随温度升高的变化趋势是_____ 。
②降低温度,图2中 点不可能变为
点不可能变为_____ 点(填“A”或“B”)。
③900K,在2L刚性容器中,充入 和
和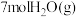 ,以
,以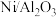 为催化剂,40min达到平衡,测得
为催化剂,40min达到平衡,测得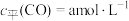 ,且在含碳产物中的体积分数为
,且在含碳产物中的体积分数为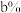 ,则0~40min用
,则0~40min用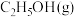 表示的反应速率为
表示的反应速率为_____  (用含a、b的式子表示,下同),
(用含a、b的式子表示,下同),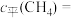
_____  。
。
ⅰ、
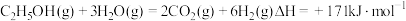 (主反应)
(主反应)ⅱ、
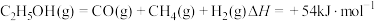
ⅲ、
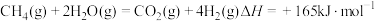
ⅳ、
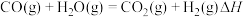
(1)反应ⅳ的

 。
。(2)Akande等研究了以
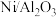 为催化剂的乙醇水蒸气重整反应。下列说法正确的是
为催化剂的乙醇水蒸气重整反应。下列说法正确的是A.
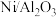 能改变重整反应的历程,因而能改变反应ⅰ的焓变
能改变重整反应的历程,因而能改变反应ⅰ的焓变B.使用适宜的催化剂提高
 的选择性,从而提高
的选择性,从而提高 的平衡产率
的平衡产率C.
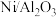 能降低重整反应的活化能,大幅增大反应的速率常数
能降低重整反应的活化能,大幅增大反应的速率常数(3)在2L刚性容器中,充入
 和若干
和若干 ,平衡时产生
,平衡时产生 物质的量与温度、水-乙醇比(水与乙醇物质的量比)的关系如图1所示(曲线上标注的数字为
物质的量与温度、水-乙醇比(水与乙醇物质的量比)的关系如图1所示(曲线上标注的数字为 物质的量/mol)。900K时,
物质的量/mol)。900K时,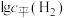 与
与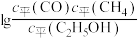 的关系如图2所示。
的关系如图2所示。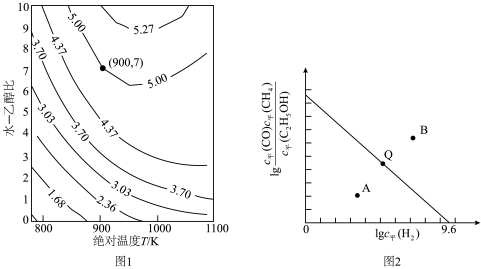
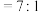 时,产生氢气的量随温度升高的变化趋势是
时,产生氢气的量随温度升高的变化趋势是②降低温度,图2中
 点不可能变为
点不可能变为③900K,在2L刚性容器中,充入
 和
和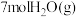 ,以
,以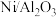 为催化剂,40min达到平衡,测得
为催化剂,40min达到平衡,测得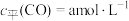 ,且在含碳产物中的体积分数为
,且在含碳产物中的体积分数为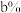 ,则0~40min用
,则0~40min用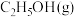 表示的反应速率为
表示的反应速率为 (用含a、b的式子表示,下同),
(用含a、b的式子表示,下同),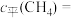
 。
。
您最近一年使用:0次
名校
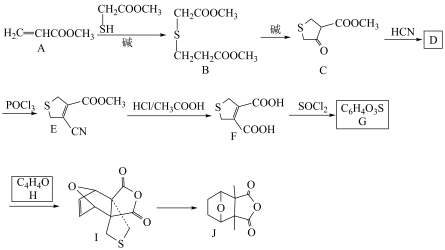
6 . 斑蝥素是斑蝥的有效成分,现代药理研究表明斑蝥素对肝癌、胃癌、肺癌等多种癌症均有抑制作用,斑蝥素的一种合成路线如下(部分试剂和条件略去)。 碳上的
碳上的 键极性增强,易断裂,在碱作用下,与另一分子酯发生酯缩合反应:
键极性增强,易断裂,在碱作用下,与另一分子酯发生酯缩合反应:
(1)A的化学名称是_______________ 。
(2)A→B的反应类型为______________ 。
(3)B→C中,根据酯缩合机理还会生成一种与C互为同分异构体的副产物K,请从极性视角分析生成K更容易原因为______________ 。
(4)已知H为五元环结构,写出H的结构简式_______________ 。
(5)J中含有__________ 个手性碳原子。
(6)写出同时满足下列条件的化合物J的一种同分异构体的结构简式__________ 。
a.含苯环;b.最多能与2倍物质的量的 反应;c.能发生银镜反应;d.不含
反应;c.能发生银镜反应;d.不含 e.
e. 谱表明分子中有4种不同化学环境的氢原子。
谱表明分子中有4种不同化学环境的氢原子。
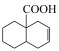
(7)根据上述信息,写出以环己酮和1,3-丁二烯为主要原料制备的合成路线_______________ (用流程图表示,无机试剂任选)。
 碳上的
碳上的 键极性增强,易断裂,在碱作用下,与另一分子酯发生酯缩合反应:
键极性增强,易断裂,在碱作用下,与另一分子酯发生酯缩合反应:
(1)A的化学名称是
(2)A→B的反应类型为
(3)B→C中,根据酯缩合机理还会生成一种与C互为同分异构体的副产物K,请从极性视角分析生成K更容易原因为
(4)已知H为五元环结构,写出H的结构简式
(5)J中含有
(6)写出同时满足下列条件的化合物J的一种同分异构体的结构简式
a.含苯环;b.最多能与2倍物质的量的
 反应;c.能发生银镜反应;d.不含
反应;c.能发生银镜反应;d.不含 e.
e. 谱表明分子中有4种不同化学环境的氢原子。
谱表明分子中有4种不同化学环境的氢原子。(7)根据上述信息,写出以环己酮和1,3-丁二烯为主要原料制备的合成路线
您最近一年使用:0次
2024-05-16更新
|
294次组卷
|
3卷引用:福建省永春一中2023-2024学年高三化学最后一卷试卷
解题方法
7 . 利用 脱除烟气中的
脱除烟气中的 具有重要意义。已知在
具有重要意义。已知在 还原
还原 过程中,会发生如下反应:
过程中,会发生如下反应:
反应i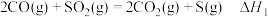
反应ii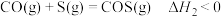
反应iii
回答下列问题:
(1)已知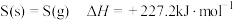 ,
, 和
和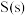 的燃烧热分别为
的燃烧热分别为 、
、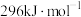 ,则反应i的
,则反应i的 为
为___________  。
。
(2)下列有利于提高反应i中 的平衡转化率的是___________。
的平衡转化率的是___________。
(3)一定条件下,该体系达平衡时各气体物质的量随 进料比的变化如图1所示。
进料比的变化如图1所示。___________ 。
②通入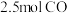 和
和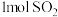 ,达到平衡时
,达到平衡时 ,则反应ii的
,则反应ii的
___________ ( 为物质的量分数,计算结果保留两位小数)。
为物质的量分数,计算结果保留两位小数)。
(4)在刚性容器中,控制反成温度为823K。固定 浓度为
浓度为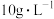 ,
, 进料比分别为
进料比分别为 、
、 、
、 时
时 的转化率随时间变化如图2所示。
的转化率随时间变化如图2所示。 进料比为
进料比为 对应图中曲线
对应图中曲线___________ 。
②反应从开始到A点时间内 的生成速率为
的生成速率为___________ 。
(5)在催化剂作用下, 还原
还原 的部分机理如图3所示(
的部分机理如图3所示( 表示S吸附在催化剂表面)。该反应的催化剂为
表示S吸附在催化剂表面)。该反应的催化剂为___________ ,历程②的方程式为___________ 。
 脱除烟气中的
脱除烟气中的 具有重要意义。已知在
具有重要意义。已知在 还原
还原 过程中,会发生如下反应:
过程中,会发生如下反应:反应i
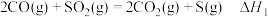
反应ii
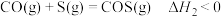
反应iii

回答下列问题:
(1)已知
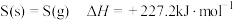 ,
, 和
和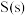 的燃烧热分别为
的燃烧热分别为 、
、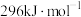 ,则反应i的
,则反应i的 为
为 。
。(2)下列有利于提高反应i中
 的平衡转化率的是___________。
的平衡转化率的是___________。A.恒容时增大 浓度 浓度 | B.降低温度 |
| C.选择合适的催化剂 | D.减小容器的容积 |
(3)一定条件下,该体系达平衡时各气体物质的量随
 进料比的变化如图1所示。
进料比的变化如图1所示。
②通入
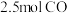 和
和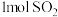 ,达到平衡时
,达到平衡时 ,则反应ii的
,则反应ii的
 为物质的量分数,计算结果保留两位小数)。
为物质的量分数,计算结果保留两位小数)。(4)在刚性容器中,控制反成温度为823K。固定
 浓度为
浓度为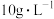 ,
, 进料比分别为
进料比分别为 、
、 、
、 时
时 的转化率随时间变化如图2所示。
的转化率随时间变化如图2所示。
 进料比为
进料比为 对应图中曲线
对应图中曲线②反应从开始到A点时间内
 的生成速率为
的生成速率为(5)在催化剂作用下,
 还原
还原 的部分机理如图3所示(
的部分机理如图3所示( 表示S吸附在催化剂表面)。该反应的催化剂为
表示S吸附在催化剂表面)。该反应的催化剂为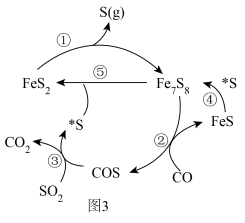
您最近一年使用:0次
解题方法
8 . 科学家通过使用双极膜电渗析法来捕获和转化海水中的CO2,其原理如图。下列说法正确的是

| A.装置运行一段时间后循环液1和循环液2要交替使用 |
| B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜 |
| C.与电源负极相连的电极上的电极反应式为[Fe(CN)6]4--e-=[Fe(CN)6]3- |
| D.该方法可以同时将海水进行淡化 |
您最近一年使用:0次
9 . 已知X,Y,Z、W、Q是前四周期原子序数依次增大的五种元素。Y的基态原子中电子占据三种能级轨道,且每个能级轨道中的电子总数相同;W原子有2个未成对电子;X、Y、W三种元素形成的一种化合物M是新装修居室中常含有的一种有害气体;含Q元素的硫酸盐溶液是制造波尔多液的原料之一。W、Q两种元素形成的化合物的晶胞结构示意图如图,下列说法错误的是

| A.上述元素中,元素第一电离能最大的是Z |
| B.化合物ZX3的沸点比YX4的高 |
C.Z 的空间结构为V形 的空间结构为V形 |
| D.W、Q两种元素形成的化合物的化学式为Q2W |
您最近一年使用:0次
10 . 锆( )是一种重要的战略金属。一种以氧氯化锆(主要含
)是一种重要的战略金属。一种以氧氯化锆(主要含 ,还含有少量
,还含有少量 、
、 等元素)为原料生产金属锆的工艺流程如下:
等元素)为原料生产金属锆的工艺流程如下: 、
、 、
、 ;
;
② 时,
时, ,
, ;
;
③“还原”前后相关物质沸点如下:
回答下列问题:
(1) 是
是 的同族相邻元素,基态
的同族相邻元素,基态 原子的价电子排布式是
原子的价电子排布式是___________ 。
(2) 通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的
通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的 ,再以盐酸酸化得到
,再以盐酸酸化得到 ,写出酸化过程的离子方程式
,写出酸化过程的离子方程式___________ 。
(3)“沉淀”后,废液中 ,则废液中
,则废液中 为
为___________  。
。
(4)“沸腾氯化”时, 转化为
转化为 ,同时生成一种还原性气体,该反应的化学方程式为
,同时生成一种还原性气体,该反应的化学方程式为___________ 。
(5)①气态 通常以二聚体
通常以二聚体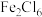 的形式存在,分子结构为
的形式存在,分子结构为 ,二聚体中
,二聚体中 的杂化轨道类型为
的杂化轨道类型为___________ 。 易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为
易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为___________ 。
②“还原”的主要目的是___________ 。
(6)下列金属冶炼方法与本工艺流程中加入 冶炼
冶炼 的方法相似的是___________
的方法相似的是___________
(7)实验室可以用络合滴定法快速测定“酸浸”溶液中锆的含量,步骤如下:___________ ,继续摇动锥形瓶,观察溶液颜色变化。
②已知 与EDTA发生
与EDTA发生 络合反应,则酸浸液中含量(以
络合反应,则酸浸液中含量(以 计)为
计)为___________  。
。
 )是一种重要的战略金属。一种以氧氯化锆(主要含
)是一种重要的战略金属。一种以氧氯化锆(主要含 ,还含有少量
,还含有少量 、
、 等元素)为原料生产金属锆的工艺流程如下:
等元素)为原料生产金属锆的工艺流程如下: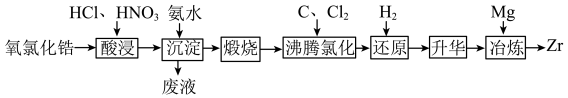
 、
、 、
、 ;
;②
 时,
时, ,
, ;
;③“还原”前后相关物质沸点如下:
| 物质 |  |  |  |  |  |
| 沸点 | 331 | 315 | 1300 | 700 | 1150 |
(1)
 是
是 的同族相邻元素,基态
的同族相邻元素,基态 原子的价电子排布式是
原子的价电子排布式是(2)
 通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的
通常采用“一酸一碱”法生产,主要生产过程为:将锆英砂与氢氧化钠混合熔融得到难溶于水的 ,再以盐酸酸化得到
,再以盐酸酸化得到 ,写出酸化过程的离子方程式
,写出酸化过程的离子方程式(3)“沉淀”后,废液中
 ,则废液中
,则废液中 为
为 。
。(4)“沸腾氯化”时,
 转化为
转化为 ,同时生成一种还原性气体,该反应的化学方程式为
,同时生成一种还原性气体,该反应的化学方程式为(5)①气态
 通常以二聚体
通常以二聚体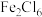 的形式存在,分子结构为
的形式存在,分子结构为 ,二聚体中
,二聚体中 的杂化轨道类型为
的杂化轨道类型为 易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为
易溶于水,也易溶于乙醚等有机溶剂,请判断其晶体类型为②“还原”的主要目的是
(6)下列金属冶炼方法与本工艺流程中加入
 冶炼
冶炼 的方法相似的是___________
的方法相似的是___________| A.高炉炼铁 | B.电解熔融氯化钠制钠 |
| C.铝热反应制锰 | D.氧化汞分解制汞 |
(7)实验室可以用络合滴定法快速测定“酸浸”溶液中锆的含量,步骤如下:

②已知
 与EDTA发生
与EDTA发生 络合反应,则酸浸液中含量(以
络合反应,则酸浸液中含量(以 计)为
计)为 。
。
您最近一年使用:0次







