名校
1 . 高分子M广泛用于牙膏、牙科粘合剂等口腔护理产品,合成路线如图:

| A.试剂a是甲醇,B分子中可能共平面的原子最多8个 |
B.化合物B的核磁共振氢谱有三组峰,峰面积比为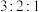 |
| C.用于合成化合物C的原料丁烯二酸可以是顺丁烯二酸,也可以是反丁烯二酸 |
| D.合成M的聚合反应是加聚反应 |
您最近一年使用:0次
2 . 溴及其化合物是重要的化工基础原料,广泛应用于制药、染料、电子、日化等行业。
Ⅰ.用图所示装置A可制取氯气。将纯净的氯气通入装置C的NaBr溶液中可以在实验室制取少量溴单质。_______ 。
(2)为了富集生成的溴单质,用热空气吹出,并在装置D中收集,则装置D中可选用的试剂为_______。
Ⅱ.工业上从海水中提取 过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:
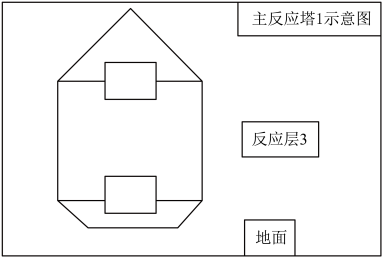
过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:_______ 。主反应塔1中温度保持在82~99℃,减少了水蒸气的用量。从化学性质的角度分析这么做的主要目的有两点:①减少氯气与水的反应,②减少_______ 反应。从经济角度来看这么做还可以减少的_______ 用量。
(4)为了让原料卤水与氯气在主反应塔1中更充分反应,请将正确装置对应的选项填在图中“□”处:_______ 。_______ 。冷凝器需要铺设循环冷却水管道,循环冷却水管道中水流方向是_______ (填“从地面到顶端”或“从顶端到地面”),请说明原因_______ 。
(6)在分离器中经冷凝、分离、纯化后制得精溴。少量氯、溴与混合废气需要经过水蒸气喷射泵喷入气体吸收器。此时,还需进行酸化调节,再经过排水管通入主反应塔1中循环利用。请写出吸收器中酸化调节主要发生的离子反应方程式:_______ 。
Ⅰ.用图所示装置A可制取氯气。将纯净的氯气通入装置C的NaBr溶液中可以在实验室制取少量溴单质。
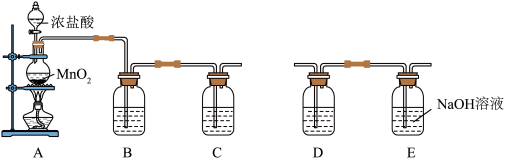
(2)为了富集生成的溴单质,用热空气吹出,并在装置D中收集,则装置D中可选用的试剂为_______。
A. | B.NaOH | C.KI | D. |
Ⅱ.工业上从海水中提取
 过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:
过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:
(4)为了让原料卤水与氯气在主反应塔1中更充分反应,请将正确装置对应的选项填在图中“□”处:

(6)在分离器中经冷凝、分离、纯化后制得精溴。少量氯、溴与混合废气需要经过水蒸气喷射泵喷入气体吸收器。此时,还需进行酸化调节,再经过排水管通入主反应塔1中循环利用。请写出吸收器中酸化调节主要发生的离子反应方程式:
您最近一年使用:0次
3 . 以软锰矿浆(含 及少量
及少量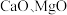 等)吸收烟气中
等)吸收烟气中 并制备高纯
并制备高纯 。
。
(1)吸收 。
。
①将烟气与软锰矿浆在吸收塔中逆流接触,烟气中的 被充分吸收,矿浆中的
被充分吸收,矿浆中的 转化为
转化为 。写出
。写出 与
与 发生反应的化学方程式:
发生反应的化学方程式:_______ 。
②脱硫过程中软锰矿浆的 和
和 吸收率的变化关系如图所示。随着脱硫的进行,软锰矿浆
吸收率的变化关系如图所示。随着脱硫的进行,软锰矿浆 下降,但15小时前
下降,但15小时前 下降缓慢,其主要原因是
下降缓慢,其主要原因是_______ 。 吸收率急剧下降。此时加入菱锰矿
吸收率急剧下降。此时加入菱锰矿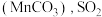 吸收率又可恢复至
吸收率又可恢复至 以上,其原因是
以上,其原因是_______ 。
(2)净化 。
。
①过滤脱硫后的软锰矿浆液,用 沉淀除去所得滤液中的
沉淀除去所得滤液中的 、Mg2+(浓度小于
、Mg2+(浓度小于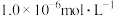 )。此时应控制溶液中
)。此时应控制溶液中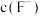 略大于
略大于_______  。(已知:
。(已知: 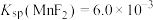 、
、 ,
, 、)
、)
②净化时生成的 沉淀晶胞结构如图所示。在
沉淀晶胞结构如图所示。在 晶胞中
晶胞中 周围距离最近的
周围距离最近的 形成的空隙构型为
形成的空隙构型为_______ 。 。
。
①向反应器中加入 溶液,控制80℃恒温,搅拌下鼓入空气可制得
溶液,控制80℃恒温,搅拌下鼓入空气可制得 。写出生成
。写出生成 的离子方程式:
的离子方程式:_______ 。
②实际生产中,常将 溶液和氨水并流加入反应器。若加入的氨水量不足,产品中会混入
溶液和氨水并流加入反应器。若加入的氨水量不足,产品中会混入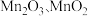 等,其原因是
等,其原因是_______ 。
 及少量
及少量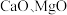 等)吸收烟气中
等)吸收烟气中 并制备高纯
并制备高纯 。
。(1)吸收
 。
。①将烟气与软锰矿浆在吸收塔中逆流接触,烟气中的
 被充分吸收,矿浆中的
被充分吸收,矿浆中的 转化为
转化为 。写出
。写出 与
与 发生反应的化学方程式:
发生反应的化学方程式:②脱硫过程中软锰矿浆的
 和
和 吸收率的变化关系如图所示。随着脱硫的进行,软锰矿浆
吸收率的变化关系如图所示。随着脱硫的进行,软锰矿浆 下降,但15小时前
下降,但15小时前 下降缓慢,其主要原因是
下降缓慢,其主要原因是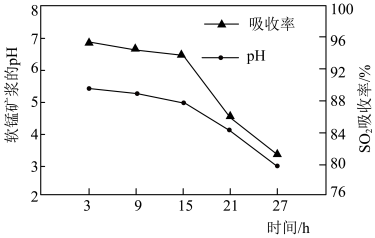
 吸收率急剧下降。此时加入菱锰矿
吸收率急剧下降。此时加入菱锰矿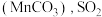 吸收率又可恢复至
吸收率又可恢复至 以上,其原因是
以上,其原因是(2)净化
 。
。①过滤脱硫后的软锰矿浆液,用
 沉淀除去所得滤液中的
沉淀除去所得滤液中的 、Mg2+(浓度小于
、Mg2+(浓度小于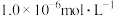 )。此时应控制溶液中
)。此时应控制溶液中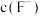 略大于
略大于 。(已知:
。(已知: 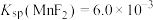 、
、 ,
, 、)
、)②净化时生成的
 沉淀晶胞结构如图所示。在
沉淀晶胞结构如图所示。在 晶胞中
晶胞中 周围距离最近的
周围距离最近的 形成的空隙构型为
形成的空隙构型为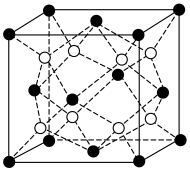
 。
。①向反应器中加入
 溶液,控制80℃恒温,搅拌下鼓入空气可制得
溶液,控制80℃恒温,搅拌下鼓入空气可制得 。写出生成
。写出生成 的离子方程式:
的离子方程式:②实际生产中,常将
 溶液和氨水并流加入反应器。若加入的氨水量不足,产品中会混入
溶液和氨水并流加入反应器。若加入的氨水量不足,产品中会混入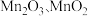 等,其原因是
等,其原因是
您最近一年使用:0次
2024-05-25更新
|
315次组卷
|
2卷引用:福建省泉州中远学校2024届高三下学期5月模拟化学试题
名校
解题方法
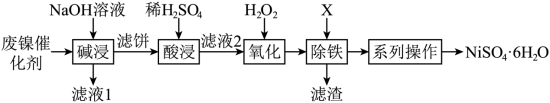
4 . 利用油脂厂废弃镍(Ni)催化剂(主要含有Ni,还含少量Al、Fe、NiO、Al2O3、Fe2O3)制备NiSO4·6H2O的工艺流程如下:
(1)为了加快“碱浸”的速率可以采取的措施是_______ (任写两条)。
(2)向滤液1中通入足量CO2可以将其中的金属元素沉淀,写出该反应的离子反应方程式____ 。
(3)“滤液2” 中含金属阳离子有_______ 。
(4)①“氧化”中反应的离子反应方程式是_______ 。
②“氧化”中可以代替H2O2的最佳物质是_______ (填标号)。
a.Cl2 b.O2 c.Fe
(5)根据除铁及系列操作,回答以下问题:
①已知溶液中存在Fe3++3H2O Fe(OH)3+3H+平衡,X物质可以为下列的
Fe(OH)3+3H+平衡,X物质可以为下列的_______ 。
a.H2SO4 b.NiO c.Ni(OH)2 d.CO2
②边搅拌边向滤液中加入X至pH=4,加热、过滤、洗涤,检验沉淀是否洗涤干净的方法_______ 。
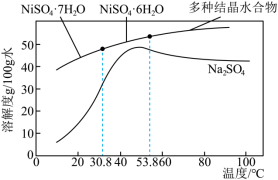
③结晶:将滤液蒸发、降温至稍高于_______ ℃结晶,过滤即获得产品,硫酸镍晶体溶解度曲线图如图所示。
(1)为了加快“碱浸”的速率可以采取的措施是
(2)向滤液1中通入足量CO2可以将其中的金属元素沉淀,写出该反应的离子反应方程式
(3)“滤液2” 中含金属阳离子有
(4)①“氧化”中反应的离子反应方程式是
②“氧化”中可以代替H2O2的最佳物质是
a.Cl2 b.O2 c.Fe
(5)根据除铁及系列操作,回答以下问题:
①已知溶液中存在Fe3++3H2O
 Fe(OH)3+3H+平衡,X物质可以为下列的
Fe(OH)3+3H+平衡,X物质可以为下列的a.H2SO4 b.NiO c.Ni(OH)2 d.CO2
②边搅拌边向滤液中加入X至pH=4,加热、过滤、洗涤,检验沉淀是否洗涤干净的方法
③结晶:将滤液蒸发、降温至稍高于
您最近一年使用:0次
5 . 利用某阳极泥(含 和
和 单质)回收贵金属
单质)回收贵金属 并合成高能量密度材料
并合成高能量密度材料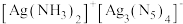 的工艺流程如下。
的工艺流程如下。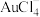 的离子方程式为
的离子方程式为___________ 。
(2)“还原”过程发生反应的化学方程式为___________ 。
(3)溶液中含银微粒的物质的量分数随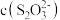 的变化如图。
的变化如图。 ,应调节
,应调节 最佳浓度为
最佳浓度为___________  。
。
②25℃时, 的
的 ,
, 的
的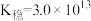 ,
,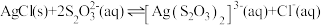 的平衡常数
的平衡常数
___________ 。
(4)“电解”过程生成 的电极反应式为
的电极反应式为___________ 。
(5)“溶解”过程可提高溶解速率的措施有___________ (填1条)。
(6)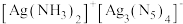 晶体的局部结构如图。
晶体的局部结构如图。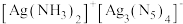 晶体中存在的微粒间作用力有
晶体中存在的微粒间作用力有___________ (填标号)。
A.离子键 B. 键 C.
键 C. 键 D.金属键 E.氢键
键 D.金属键 E.氢键
②晶体中 的杂化轨道类型
的杂化轨道类型___________ (填“相同”或“不同”),依据是___________ 。
 和
和 单质)回收贵金属
单质)回收贵金属 并合成高能量密度材料
并合成高能量密度材料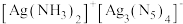 的工艺流程如下。
的工艺流程如下。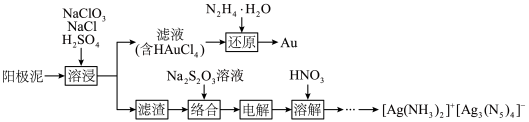
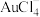 的离子方程式为
的离子方程式为(2)“还原”过程发生反应的化学方程式为
(3)溶液中含银微粒的物质的量分数随
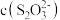 的变化如图。
的变化如图。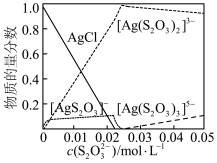
 ,应调节
,应调节 最佳浓度为
最佳浓度为 。
。②25℃时,
 的
的 ,
, 的
的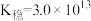 ,
,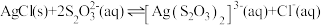 的平衡常数
的平衡常数
(4)“电解”过程生成
 的电极反应式为
的电极反应式为(5)“溶解”过程可提高溶解速率的措施有
(6)
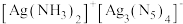 晶体的局部结构如图。
晶体的局部结构如图。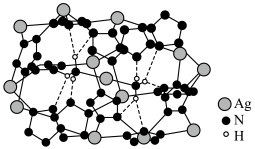
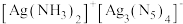 晶体中存在的微粒间作用力有
晶体中存在的微粒间作用力有A.离子键 B.
 键 C.
键 C. 键 D.金属键 E.氢键
键 D.金属键 E.氢键②晶体中
 的杂化轨道类型
的杂化轨道类型
您最近一年使用:0次
名校
6 . 某化学兴趣小组同学进行如下实验:①分别向 溶液和
溶液和 溶液中滴加KSCN溶液,均无明显现象。②向
溶液中滴加KSCN溶液,均无明显现象。②向 和
和 的混合液中滴加少量KSCN溶液,溶液立刻变红,振荡后,红色褪去,产生白色沉淀,继续滴加过量KSCN溶液,红色不再褪去,并产生大量白色沉淀。③过滤②中白色沉淀并洗涤干净,向其中加入过量氨水,白色沉淀溶解得无色溶液,放置过程中,无色溶液变蓝色。已知:CuSCN为白色、难溶性物质;
的混合液中滴加少量KSCN溶液,溶液立刻变红,振荡后,红色褪去,产生白色沉淀,继续滴加过量KSCN溶液,红色不再褪去,并产生大量白色沉淀。③过滤②中白色沉淀并洗涤干净,向其中加入过量氨水,白色沉淀溶解得无色溶液,放置过程中,无色溶液变蓝色。已知:CuSCN为白色、难溶性物质; 为无色离子;
为无色离子; 为深蓝色离子。下列说法不正确的是
为深蓝色离子。下列说法不正确的是
 溶液和
溶液和 溶液中滴加KSCN溶液,均无明显现象。②向
溶液中滴加KSCN溶液,均无明显现象。②向 和
和 的混合液中滴加少量KSCN溶液,溶液立刻变红,振荡后,红色褪去,产生白色沉淀,继续滴加过量KSCN溶液,红色不再褪去,并产生大量白色沉淀。③过滤②中白色沉淀并洗涤干净,向其中加入过量氨水,白色沉淀溶解得无色溶液,放置过程中,无色溶液变蓝色。已知:CuSCN为白色、难溶性物质;
的混合液中滴加少量KSCN溶液,溶液立刻变红,振荡后,红色褪去,产生白色沉淀,继续滴加过量KSCN溶液,红色不再褪去,并产生大量白色沉淀。③过滤②中白色沉淀并洗涤干净,向其中加入过量氨水,白色沉淀溶解得无色溶液,放置过程中,无色溶液变蓝色。已知:CuSCN为白色、难溶性物质; 为无色离子;
为无色离子; 为深蓝色离子。下列说法不正确的是
为深蓝色离子。下列说法不正确的是A.实验①说明 不能与SCN反应生成CuSCN 不能与SCN反应生成CuSCN |
B.实验②中红色褪去的原因是振荡后 降低 降低 |
C.实验③中无色溶液变蓝色的原因是: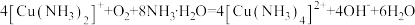 |
D.依据实验①、②、③推测,②中由于生成CuSCN,使 氧化性增强,将 氧化性增强,将 氧化为 氧化为 |
您最近一年使用:0次
名校
解题方法
7 . 宏观辨识和微观探析是化学学科核心素养之一,下列描述物质制备和应用的离子方程式正确的是
A.向 溶液中加入过量氨水: 溶液中加入过量氨水: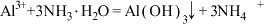 |
B.用纯碱溶液富集海水提溴工艺中 : :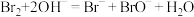 |
C.向 溶液中通入少量 溶液中通入少量 : : |
D.工业上制备粗硅: |
您最近一年使用:0次
8 . 下图是降压药主要成分尼卡地平的一种合成路线。
(1) 的反应类型是
的反应类型是___________ 。
(2)I中含氧官能团的名称是___________ 。 的结构简式是
的结构简式是___________ 。
(5) 的化学反应方程式是
的化学反应方程式是___________ 。
(6)同时符合下列条件的芳香族化合物的结构有___________ 种(不考虑立体异构)。
a.比H多1个碳原子和4个氢原子,且 与
与 不直接相连
不直接相连
b.苯环上只有2个取代基
c. 该物质最多消耗
该物质最多消耗
其中核磁共振氢谱显示5组峰,且峰面积之比为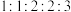 的结构简式为:
的结构简式为:___________ (任写一种)。
(7)参照以上信息,由 甲基丙醛及必备的试剂制备化合物Z的路线如下:
甲基丙醛及必备的试剂制备化合物Z的路线如下: 甲基丙醛分子中2号碳上的H比3号碳上的更活泼,从结构角度解释
甲基丙醛分子中2号碳上的H比3号碳上的更活泼,从结构角度解释___________ 。
②化合物 结构简式是
结构简式是___________ 。
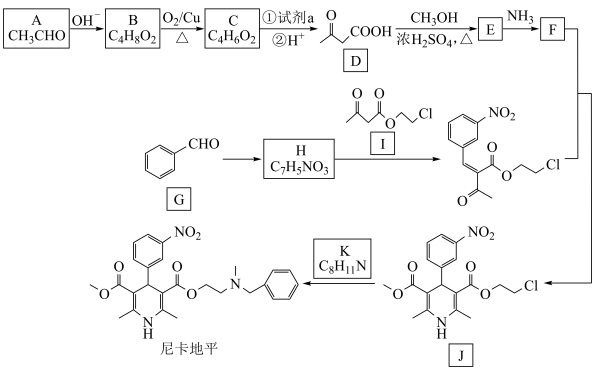
已知:
(1)
 的反应类型是
的反应类型是(2)I中含氧官能团的名称是
(3) 与J合成尼卡地平的过程中会生成
与J合成尼卡地平的过程中会生成 ,合成过程中通常还会加入少量吡啶(
,合成过程中通常还会加入少量吡啶(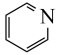 ),主要目的是
),主要目的是
 的结构简式是
的结构简式是(5)
 的化学反应方程式是
的化学反应方程式是(6)同时符合下列条件的芳香族化合物的结构有
a.比H多1个碳原子和4个氢原子,且
 与
与 不直接相连
不直接相连b.苯环上只有2个取代基
c.
 该物质最多消耗
该物质最多消耗
其中核磁共振氢谱显示5组峰,且峰面积之比为
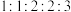 的结构简式为:
的结构简式为:(7)参照以上信息,由
 甲基丙醛及必备的试剂制备化合物Z的路线如下:
甲基丙醛及必备的试剂制备化合物Z的路线如下:
 甲基丙醛分子中2号碳上的H比3号碳上的更活泼,从结构角度解释
甲基丙醛分子中2号碳上的H比3号碳上的更活泼,从结构角度解释②化合物
 结构简式是
结构简式是
您最近一年使用:0次
9 . 向敞口容器中加入一定体积pH=13的84消毒液(NaClO的浓度约为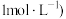 ,不断搅拌,逐滴加入
,不断搅拌,逐滴加入 溶液,溶液pH变化曲线如图1所示(AB段pH快速下降的原因之一是
溶液,溶液pH变化曲线如图1所示(AB段pH快速下降的原因之一是 )。图2表示NaClO溶液中含氯微粒的物质的量分数与pH的关系。
)。图2表示NaClO溶液中含氯微粒的物质的量分数与pH的关系。
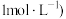 ,不断搅拌,逐滴加入
,不断搅拌,逐滴加入 溶液,溶液pH变化曲线如图1所示(AB段pH快速下降的原因之一是
溶液,溶液pH变化曲线如图1所示(AB段pH快速下降的原因之一是 )。图2表示NaClO溶液中含氯微粒的物质的量分数与pH的关系。
)。图2表示NaClO溶液中含氯微粒的物质的量分数与pH的关系。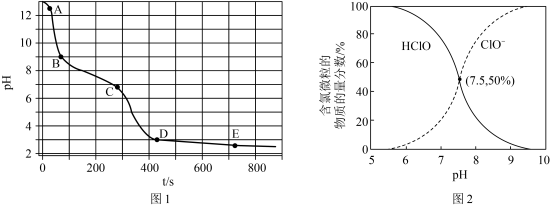
A.原84消毒液中,HClO的含量约为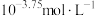 |
B.AB段Fe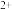 被氧化的反应 被氧化的反应 |
| C.CD段较BC段pH下降快的主要原因是HClO的氧化性强于ClO⁻ |
| D.400s后反应几乎停止 |
您最近一年使用:0次
解题方法
10 . 一种自生酸和碱的电化学回收体系,原理如图所示。在Ⅲ室中将 等含磷微粒转化为羟基磷灰石
等含磷微粒转化为羟基磷灰石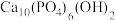 (
(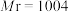 ),同时将
),同时将 转化为
转化为 ,实现废水中的
,实现废水中的 等含磷微粒和
等含磷微粒和 的回收。下列说法
的回收。下列说法不正确 的是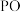 表示
表示 等含磷微粒,
等含磷微粒, 为羟基磷灰石)
为羟基磷灰石)
 等含磷微粒转化为羟基磷灰石
等含磷微粒转化为羟基磷灰石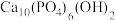 (
(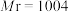 ),同时将
),同时将 转化为
转化为 ,实现废水中的
,实现废水中的 等含磷微粒和
等含磷微粒和 的回收。下列说法
的回收。下列说法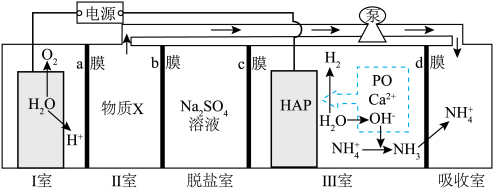
 表示
表示 等含磷微粒,
等含磷微粒, 为羟基磷灰石)
为羟基磷灰石)| A.a、c为阳离子交换膜,b为阴离子交换膜 |
B.Ⅲ室可发生反应: |
C.当电路中通过 电子,阴极增重10.04g 电子,阴极增重10.04g |
D.物质X为硫酸溶液,将其泵入吸收室用于吸收 |
您最近一年使用:0次



