名校
1 . I. 和
和 在工农业、科研等方面应用广泛。
在工农业、科研等方面应用广泛。
(1) (氨硼烷)是具有广泛应用前景的储氢材料。
(氨硼烷)是具有广泛应用前景的储氢材料。
① 中存在配位键,提供空轨道的原子是
中存在配位键,提供空轨道的原子是___________ 。
② 的沸点高于
的沸点高于 的可能原因是
的可能原因是___________ 。
(2)工业合成 时用到含铁催化剂。
时用到含铁催化剂。
① 元素在周期表第
元素在周期表第___________ 族,基态 原子电子的空间运动状态有
原子电子的空间运动状态有___________ 种。
②从结构的角度分析 容易被氧化成
容易被氧化成 的原因是
的原因是___________ 。
(3)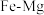 合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时,
合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时, 分子在晶胞的体心和棱的中心位置。
分子在晶胞的体心和棱的中心位置。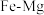 合金中,每个
合金中,每个 原子周围与它最近且相等距离的
原子周围与它最近且相等距离的 原子有
原子有___________ 个。
②要储存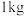
 ,至少需要
,至少需要___________ 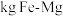 合金。
合金。
II.请回答:
(4)下列说法中正确的有___________ 。
①金属晶体的导电性、导热性均与自由电子有关
②若晶体中有阳离子,必然有阴离子
③分子晶体的熔点一定比金属晶体低
④共价键的强弱决定分子晶体熔、沸点的高低
⑤共价晶体中一定含有共价键
⑥含有离子的晶体一定是离子晶体
⑦硬度由大到小:金刚石>碳化硅>晶体硅
⑧ 和
和 晶体中,阴离子周围紧邻的阳离子数均为8
晶体中,阴离子周围紧邻的阳离子数均为8
 和
和 在工农业、科研等方面应用广泛。
在工农业、科研等方面应用广泛。(1)
 (氨硼烷)是具有广泛应用前景的储氢材料。
(氨硼烷)是具有广泛应用前景的储氢材料。①
 中存在配位键,提供空轨道的原子是
中存在配位键,提供空轨道的原子是②
 的沸点高于
的沸点高于 的可能原因是
的可能原因是(2)工业合成
 时用到含铁催化剂。
时用到含铁催化剂。①
 元素在周期表第
元素在周期表第 原子电子的空间运动状态有
原子电子的空间运动状态有②从结构的角度分析
 容易被氧化成
容易被氧化成 的原因是
的原因是(3)
 合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时,
合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时, 分子在晶胞的体心和棱的中心位置。
分子在晶胞的体心和棱的中心位置。
 合金中,每个
合金中,每个 原子周围与它最近且相等距离的
原子周围与它最近且相等距离的 原子有
原子有②要储存
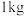
 ,至少需要
,至少需要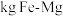 合金。
合金。II.请回答:
(4)下列说法中正确的有
①金属晶体的导电性、导热性均与自由电子有关
②若晶体中有阳离子,必然有阴离子
③分子晶体的熔点一定比金属晶体低
④共价键的强弱决定分子晶体熔、沸点的高低
⑤共价晶体中一定含有共价键
⑥含有离子的晶体一定是离子晶体
⑦硬度由大到小:金刚石>碳化硅>晶体硅
⑧
 和
和 晶体中,阴离子周围紧邻的阳离子数均为8
晶体中,阴离子周围紧邻的阳离子数均为8
您最近一年使用:0次
名校
解题方法
2 . 一氯甲烷等卤代烃跟苯的反应如图所示,(无机小分子产物略去)。下列说法正确的是
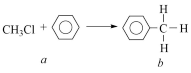
| A.该反应属于化合反应 | B.b的二氯代物有6种结构 |
| C.b分子中共平面的原子最多有8个 | D.C5H11Cl的结构有8种 |
您最近一年使用:0次
名校
解题方法
3 . 化合物J是一种治疗高脂血症的药物,其合成路线如图:______ ,反应H→I的反应类型为______ 。
(2)化合物J中的官能团为______ 。
(3)E→F反应的化学方程式为____________ 。
(4)H的结构简式为______ 。
(5)K是D的同系物,其相对分子质量比D多14,满足下列条件的K的同分异构体共有______ 种(不考虑立体异构)。
①苯环上只有两个侧链
②能与Na反应生成
③能与银氨溶液发生银镜反应
K的所有同分异构体在下列表征仪器中显示的信号(或数据)完全相同的是______ (填字母)。
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
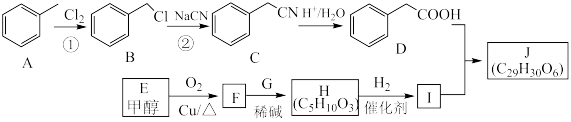
Ⅱ. 。
。
(2)化合物J中的官能团为
(3)E→F反应的化学方程式为
(4)H的结构简式为
(5)K是D的同系物,其相对分子质量比D多14,满足下列条件的K的同分异构体共有
①苯环上只有两个侧链
②能与Na反应生成

③能与银氨溶液发生银镜反应
K的所有同分异构体在下列表征仪器中显示的信号(或数据)完全相同的是
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
您最近一年使用:0次
名校
4 . 二氯化二硫( )可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。
)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。 可通过硫与少量氯气在110~140℃反应制得。
可通过硫与少量氯气在110~140℃反应制得。
(1)有关 的下列说法正确的是 。
的下列说法正确的是 。
(2)选用以下装置制取少量 (加热及夹持装置略):
(加热及夹持装置略):_____________________ 。
②装置连接顺序:A→__________ →D。
③B中玻璃纤维的作用是______________________ 。
④D中的最佳试剂是__________ (选填序号)。
a.碱石灰 b.浓硫酸 c.NaOH溶液 d.无水氯化钙
(3) 遇水会生成
遇水会生成 、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中
、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中 的体积分数。
的体积分数。_________ (填标号);
a. 溶液 b.
溶液 b. 溶液(硫酸酸化) c.氯水
溶液(硫酸酸化) c.氯水
 )可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。
)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。 可通过硫与少量氯气在110~140℃反应制得。
可通过硫与少量氯气在110~140℃反应制得。(1)有关
 的下列说法正确的是 。
的下列说法正确的是 。A. 中S-Cl键的键能大于S-S键的键能 中S-Cl键的键能大于S-S键的键能 | B.固态时 属于原子晶体 属于原子晶体 |
| C.第一电离能、电负性均为:Cl>S | D. 中既有极性键又有非极性键 中既有极性键又有非极性键 |
(2)选用以下装置制取少量
 (加热及夹持装置略):
(加热及夹持装置略):
②装置连接顺序:A→
③B中玻璃纤维的作用是
④D中的最佳试剂是
a.碱石灰 b.浓硫酸 c.NaOH溶液 d.无水氯化钙
(3)
 遇水会生成
遇水会生成 、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中
、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中 的体积分数。
的体积分数。
a.
 溶液 b.
溶液 b. 溶液(硫酸酸化) c.氯水
溶液(硫酸酸化) c.氯水
您最近一年使用:0次
名校
5 . 丙烯可发生如下转化,下列说法不正确的是

| A.丙烯分子中最少有6个原子共平面 |
| B.X具有顺反异构 |
| C.Y与足量NaOH溶液共热可生成1,2-丙二醇 |
D.聚合物Z的链节结构简式为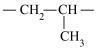 |
您最近一年使用:0次
7日内更新
|
615次组卷
|
2卷引用:2024届辽宁省实验中学高三下学期考前模拟训练(五模)化学试卷
名校
解题方法
6 . 乙醇-水催化重整可获得 。主要发生以下反应:
。主要发生以下反应:
反应Ⅰ:
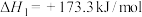
反应Ⅱ:
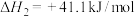
(1)反应Ⅰ自发进行的条件是_______。
(2)500℃时,向体积为VL的恒容密闭容器中充入1mol (g)和3mol
(g)和3mol  (g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%,
(g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%, 的转化率为80%。(CO的选择性=
的转化率为80%。(CO的选择性= )
)
①反应Ⅰ的
_______ (列出计算式即可)。反应Ⅰ的标准平衡常数 ,其中
,其中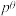 为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。
为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。
②在下图中画出500℃时,乙醇平衡转化率随[ ]变化而变化的情况
]变化而变化的情况_______ 。 的平衡产率与温度、起始时
的平衡产率与温度、起始时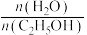 关系如图所示,每条曲线表示
关系如图所示,每条曲线表示 相同的平衡产率。
相同的平衡产率。 的平衡产率:Q点
的平衡产率:Q点_______ N点(填“>”、“=”或“<”);
②M、N两点 的平衡产率相等的原因是
的平衡产率相等的原因是_______ 。
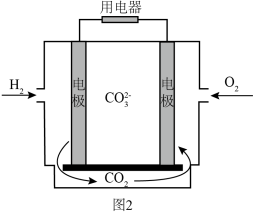
(4)氢气的应用:氢气熔融碳酸盐燃料电池工作原理如图所示。 和
和 经催化重整生成CO和
经催化重整生成CO和 ,CO和
,CO和 全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)
全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)_______ 。
②理论上负极生成的 与正极消耗的
与正极消耗的 的物质的量之比是
的物质的量之比是_______ 。
 。主要发生以下反应:
。主要发生以下反应:反应Ⅰ:

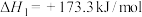
反应Ⅱ:

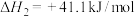
(1)反应Ⅰ自发进行的条件是_______。
| A.低温 | B.高温 | C.低压 | D.高压 |
(2)500℃时,向体积为VL的恒容密闭容器中充入1mol
 (g)和3mol
(g)和3mol  (g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%,
(g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%, 的转化率为80%。(CO的选择性=
的转化率为80%。(CO的选择性= )
)①反应Ⅰ的

 ,其中
,其中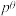 为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。
为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。②在下图中画出500℃时,乙醇平衡转化率随[
 ]变化而变化的情况
]变化而变化的情况
 的平衡产率与温度、起始时
的平衡产率与温度、起始时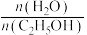 关系如图所示,每条曲线表示
关系如图所示,每条曲线表示 相同的平衡产率。
相同的平衡产率。
 的平衡产率:Q点
的平衡产率:Q点②M、N两点
 的平衡产率相等的原因是
的平衡产率相等的原因是(4)氢气的应用:氢气熔融碳酸盐燃料电池工作原理如图所示。

 和
和 经催化重整生成CO和
经催化重整生成CO和 ,CO和
,CO和 全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)
全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)②理论上负极生成的
 与正极消耗的
与正极消耗的 的物质的量之比是
的物质的量之比是
您最近一年使用:0次
真题
7 . 氢是清洁能源,硼氢化钠( )是一种环境友好的固体储氢材料,其水解生氢反应方程式如下:(除非特别说明,本题中反应条件均为
)是一种环境友好的固体储氢材料,其水解生氢反应方程式如下:(除非特别说明,本题中反应条件均为 ,
, )
)

请回答:
(1)该反应能自发进行的条件是_______。
(2)该反应比较缓慢。忽略体积变化的影响,下列措施中可加快反应速率的是_______。
(3)为加速 水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应开始时生氢速率v与投料比
水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应开始时生氢速率v与投料比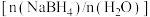 之间的关系,结果如图1所示。请解释ab段变化的原因
之间的关系,结果如图1所示。请解释ab段变化的原因_______ 。_______ 。该电池以 恒定电流工作14分钟,消耗
恒定电流工作14分钟,消耗 体积为
体积为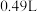 ,故可测得该电池将化学能转化为电能的转化率为
,故可测得该电池将化学能转化为电能的转化率为_______ 。[已知:该条件下 的摩尔体积为
的摩尔体积为 ;电荷量
;电荷量 电流
电流 时间
时间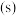 ;
;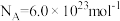 ;
;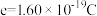 。]
。] )再生为
)再生为 。(已知:
。(已知: 是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比
是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比 计算方法;当
计算方法;当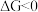 时,反应能自发进行。)
时,反应能自发进行。)
I.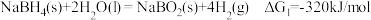
II.
III.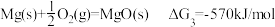
请书写一个方程式表示 再生为
再生为 的一种制备方法,并注明
的一种制备方法,并注明
_______ 。(要求:反应物不超过三种物质;氢原子利用率为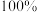 。)
。)
 )是一种环境友好的固体储氢材料,其水解生氢反应方程式如下:(除非特别说明,本题中反应条件均为
)是一种环境友好的固体储氢材料,其水解生氢反应方程式如下:(除非特别说明,本题中反应条件均为 ,
, )
)
请回答:
(1)该反应能自发进行的条件是_______。
| A.高温 | B.低温 | C.任意温度 | D.无法判断 |
| A.升高溶液温度 | B.加入少量异丙胺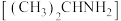 |
C.加入少量固体硼酸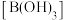 | D.增大体系压强 |
 水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应开始时生氢速率v与投料比
水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应开始时生氢速率v与投料比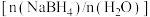 之间的关系,结果如图1所示。请解释ab段变化的原因
之间的关系,结果如图1所示。请解释ab段变化的原因
 恒定电流工作14分钟,消耗
恒定电流工作14分钟,消耗 体积为
体积为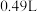 ,故可测得该电池将化学能转化为电能的转化率为
,故可测得该电池将化学能转化为电能的转化率为 的摩尔体积为
的摩尔体积为 ;电荷量
;电荷量 电流
电流 时间
时间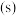 ;
;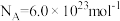 ;
;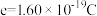 。]
。]
 )再生为
)再生为 。(已知:
。(已知: 是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比
是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比 计算方法;当
计算方法;当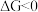 时,反应能自发进行。)
时,反应能自发进行。)I.
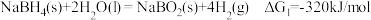
II.

III.
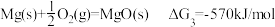
请书写一个方程式表示
 再生为
再生为 的一种制备方法,并注明
的一种制备方法,并注明
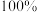 。)
。)
您最近一年使用:0次
名校
8 . 利用 合成甲醇、二甲醚技术是有效利用
合成甲醇、二甲醚技术是有效利用 资源,实现“碳中和”目标的重要途径。
资源,实现“碳中和”目标的重要途径。
(1)开发 直接催化加氢合成二甲醚技术是很好的一个研究方向。
直接催化加氢合成二甲醚技术是很好的一个研究方向。
主反应: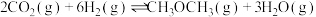

副反应:

①已知25℃和101kPa下,H2(g)、CO(g)的燃烧热 分别为-285.8kJ/mol、-283.0kJ/mol,
分别为-285.8kJ/mol、-283.0kJ/mol,
 ,则
,则
_______ kJ/mol。
②其他条件相同时,反应温度对 平衡转化率影响如图所示。温度低于280℃时,
平衡转化率影响如图所示。温度低于280℃时, 平衡转化率随温度的升高而减小的原因可能是
平衡转化率随温度的升高而减小的原因可能是_______ 。 ,反应平衡时测得
,反应平衡时测得 的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择性
的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择性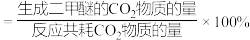 ),则副反应
),则副反应 的
的
_______ (保留两位有效数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)利用 合成甲醇也是有效利用
合成甲醇也是有效利用 资源的重要途径。将原料气
资源的重要途径。将原料气 充入某一恒容密闭容器中,只发生
充入某一恒容密闭容器中,只发生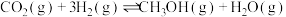
 ,在不同催化剂作用下,反应
,在不同催化剂作用下,反应 时
时 的转化率随温度的变化如图所示。
的转化率随温度的变化如图所示。_______ 。
A.使用催化剂Ⅰ时,d点已达到平衡
B. 的平衡常数大于
的平衡常数大于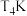 的平衡常数
的平衡常数
C.若a点时, ,则此条件下反应已达到最大限度
,则此条件下反应已达到最大限度
D.c点转化率比a点低的原因一定是催化剂活性降低
②若图中a点时反应已达平衡,现原料气按 充入同一恒容密闭容器中,在催化剂Ⅰ的作用下发生反应。请在图中用实线画出
充入同一恒容密闭容器中,在催化剂Ⅰ的作用下发生反应。请在图中用实线画出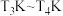 之间
之间 的平衡转化率变化曲线
的平衡转化率变化曲线______ 。
(3)水煤气变换反应的机理被广泛研究,其中有一种为羧基机理,某催化剂催化 (*表示吸附态、
(*表示吸附态、 表示活化能)步骤如下:
表示活化能)步骤如下:
Ⅰ.

Ⅱ._______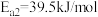
Ⅲ.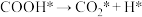

Ⅳ._______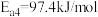
①请补充其中的一个反应式:Ⅱ_______ 。
②反应 的决速步骤是
的决速步骤是_______ (填序号)。
 合成甲醇、二甲醚技术是有效利用
合成甲醇、二甲醚技术是有效利用 资源,实现“碳中和”目标的重要途径。
资源,实现“碳中和”目标的重要途径。(1)开发
 直接催化加氢合成二甲醚技术是很好的一个研究方向。
直接催化加氢合成二甲醚技术是很好的一个研究方向。主反应:
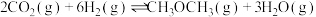

副反应:


①已知25℃和101kPa下,H2(g)、CO(g)的燃烧热
 分别为-285.8kJ/mol、-283.0kJ/mol,
分别为-285.8kJ/mol、-283.0kJ/mol,
 ,则
,则
②其他条件相同时,反应温度对
 平衡转化率影响如图所示。温度低于280℃时,
平衡转化率影响如图所示。温度低于280℃时, 平衡转化率随温度的升高而减小的原因可能是
平衡转化率随温度的升高而减小的原因可能是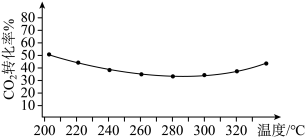
 ,反应平衡时测得
,反应平衡时测得 的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择性
的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择性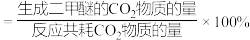 ),则副反应
),则副反应 的
的
(2)利用
 合成甲醇也是有效利用
合成甲醇也是有效利用 资源的重要途径。将原料气
资源的重要途径。将原料气 充入某一恒容密闭容器中,只发生
充入某一恒容密闭容器中,只发生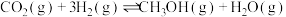
 ,在不同催化剂作用下,反应
,在不同催化剂作用下,反应 时
时 的转化率随温度的变化如图所示。
的转化率随温度的变化如图所示。
A.使用催化剂Ⅰ时,d点已达到平衡
B.
 的平衡常数大于
的平衡常数大于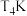 的平衡常数
的平衡常数C.若a点时,
 ,则此条件下反应已达到最大限度
,则此条件下反应已达到最大限度D.c点转化率比a点低的原因一定是催化剂活性降低
②若图中a点时反应已达平衡,现原料气按
 充入同一恒容密闭容器中,在催化剂Ⅰ的作用下发生反应。请在图中用实线画出
充入同一恒容密闭容器中,在催化剂Ⅰ的作用下发生反应。请在图中用实线画出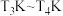 之间
之间 的平衡转化率变化曲线
的平衡转化率变化曲线(3)水煤气变换反应的机理被广泛研究,其中有一种为羧基机理,某催化剂催化
 (*表示吸附态、
(*表示吸附态、 表示活化能)步骤如下:
表示活化能)步骤如下:Ⅰ.


Ⅱ._______
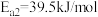
Ⅲ.
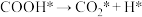

Ⅳ._______
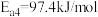
①请补充其中的一个反应式:Ⅱ
②反应
 的决速步骤是
的决速步骤是
您最近一年使用:0次
名校
解题方法
9 . 丙醛工业上主要用于制合成纤维、橡胶促进剂和防老剂等。在铑催化剂作用下与常用乙烯羰基化合成丙醛,涉及的反应如下:
主反应Ⅰ:C2H4(g)+H2(g)+CO(g) CH3CH2CHO(g) ΔH1
CH3CH2CHO(g) ΔH1
副反应Ⅱ:C2H4(g)+H2(g) CH3CH3(g) ΔH2
CH3CH3(g) ΔH2
已知:在一定条件下一氧化碳能与铑催化剂结合生成羰基铑络合物;丙醛选择性:x(CH3CH2CHO)= ×100%。
×100%。
回答下列问题:
(1)反应Ⅰ、Ⅱ以气体分压表示的平衡常数Kp与温度T变化关系如图所示。 CH3CH2CHO(g) ΔH
CH3CH2CHO(g) ΔH________ 0(填“>”、“<”或“=”), 的数值范围是
的数值范围是________ (填标号)。
A.<-1 B.-1~0 C.0~1 D.>1
(2)在T1℃、压强为150kPa条件下,在密闭反应器中,按照投料n(C2H4):n(CO):n(H2)=1:1∶1,发生上述反应,经tmin反应达到平衡,测得p(C2H4)=p(C2H6)=20kPa,则CH3CH2CHO(g)的选择性为________ %(保留小数点后一位),v(CO)=________ kPa/min(用含t的代数式表示),反应Ⅰ的逆反应的Kp=________ 。
(3)在恒压密闭容器中,在一定温度和铙催化剂作用下,发生上述反应,反应相同时间时,测得C2H4的转化率(α)和丙醛选择性随 变化关系如图所示。
变化关系如图所示。________ (填“C2H4的转化率”或“丙醛选择性”);
②当 小于1时,曲线b随
小于1时,曲线b随 的降低而降低的可能原因是
的降低而降低的可能原因是________ 。
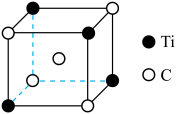
(4)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为______ 。
主反应Ⅰ:C2H4(g)+H2(g)+CO(g)
 CH3CH2CHO(g) ΔH1
CH3CH2CHO(g) ΔH1副反应Ⅱ:C2H4(g)+H2(g)
 CH3CH3(g) ΔH2
CH3CH3(g) ΔH2已知:在一定条件下一氧化碳能与铑催化剂结合生成羰基铑络合物;丙醛选择性:x(CH3CH2CHO)=
 ×100%。
×100%。回答下列问题:
(1)反应Ⅰ、Ⅱ以气体分压表示的平衡常数Kp与温度T变化关系如图所示。

 CH3CH2CHO(g) ΔH
CH3CH2CHO(g) ΔH 的数值范围是
的数值范围是A.<-1 B.-1~0 C.0~1 D.>1
(2)在T1℃、压强为150kPa条件下,在密闭反应器中,按照投料n(C2H4):n(CO):n(H2)=1:1∶1,发生上述反应,经tmin反应达到平衡,测得p(C2H4)=p(C2H6)=20kPa,则CH3CH2CHO(g)的选择性为
(3)在恒压密闭容器中,在一定温度和铙催化剂作用下,发生上述反应,反应相同时间时,测得C2H4的转化率(α)和丙醛选择性随
 变化关系如图所示。
变化关系如图所示。
②当
 小于1时,曲线b随
小于1时,曲线b随 的降低而降低的可能原因是
的降低而降低的可能原因是(4)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为
您最近一年使用:0次
名校
解题方法
10 .  可合成有机试剂DMF,用含金属铱(Ir)的化合物催化,反应机理如下图(其中L表示配体)。下列说法正确的是
可合成有机试剂DMF,用含金属铱(Ir)的化合物催化,反应机理如下图(其中L表示配体)。下列说法正确的是
 可合成有机试剂DMF,用含金属铱(Ir)的化合物催化,反应机理如下图(其中L表示配体)。下列说法正确的是
可合成有机试剂DMF,用含金属铱(Ir)的化合物催化,反应机理如下图(其中L表示配体)。下列说法正确的是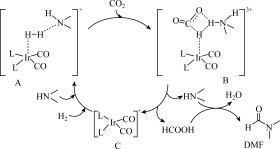
A. 在反应中极性键未被破坏 在反应中极性键未被破坏 |
B.总反应方程式为H2+ +CO2 +CO2  +H2O +H2O |
| C.化合物B是该反应的催化剂 |
| D.流程中生成DMF步骤的反应类型为还原反应 |
您最近一年使用:0次



