名校
1 . 回答下列问题:
(1)同温同压下的两个容积相同的容器中分别装有O2和O3气体,则两瓶气体中原子数之比是_______ 。
(2)下列所给出的几组物质中:标准状况下体积最大的是_______ ;质量最大的是_______ 。(填序号)
①1g H2; ②2.408×1023个CH4;③10.8 g H2O; ④标准状况下6.72 LCO2
(3)与0.2molH3PO4具有相同氢原子数的HNO3的物质的量是_______ mol,具有相同氧原子数的硫酸分子有_______ 个。
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ 。
(5)已知一混合溶液中有Na+、Cl-、SO 、H+、K+,含Na+0.2 mol,SO
、H+、K+,含Na+0.2 mol,SO 0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为
0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为 _______ 。
(1)同温同压下的两个容积相同的容器中分别装有O2和O3气体,则两瓶气体中原子数之比是
(2)下列所给出的几组物质中:标准状况下体积最大的是
①1g H2; ②2.408×1023个CH4;③10.8 g H2O; ④标准状况下6.72 LCO2
(3)与0.2molH3PO4具有相同氢原子数的HNO3的物质的量是
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(5)已知一混合溶液中有Na+、Cl-、SO
 、H+、K+,含Na+0.2 mol,SO
、H+、K+,含Na+0.2 mol,SO 0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为
0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为
您最近一年使用:0次
2022-10-30更新
|
275次组卷
|
2卷引用:安徽省淮北市第一中学2022-2023学年高一上学期期中考试化学试题
名校
2 . 完成下列问题
(1)某温度(t℃)时,水的Kw=10-13,则该温度(填大于、等于或小于)_______ 25℃,将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,
①若所得混合溶液为中性,则a:b=_______ ;
②若所得混合溶液pH=2, 则 a:b=_______ 。
(2)在一定温度下,有a.醋酸 b.盐酸 c.硫酸 三种酸:
①同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小 的顺序是_______ ;(用a、b、c表示,下同)
②若三者c(H+)相同时,酸的物质的量浓度由大到小 的顺序为_______ ;
③将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小 的顺序是_______ 。
(1)某温度(t℃)时,水的Kw=10-13,则该温度(填大于、等于或小于)
①若所得混合溶液为中性,则a:b=
②若所得混合溶液pH=2, 则 a:b=
(2)在一定温度下,有a.醋酸 b.盐酸 c.硫酸 三种酸:
①同体积、同物质的量浓度的三种酸,中和NaOH的能力
②若三者c(H+)相同时,酸的物质的量浓度
③将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)
您最近一年使用:0次
2022-10-28更新
|
575次组卷
|
3卷引用:安徽省合肥庐巢八校2022-2023学年高二上学期12月联考化学试题
3 . 化学计量是研究化学的重要工具。回答下列有关问题:
(1)28g氮气中含有的原子数约为_______ 个,标准状况下的体积为_______ L。
(2)7.8g 固体中含有离子的总物质的量为
固体中含有离子的总物质的量为_______ mol。
(3)在含有 、
、 、
、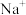 、
、 、
、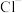 的溶液中,
的溶液中, ,若
,若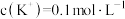 ,则
,则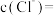
_______  。
。
(4)某气体纯净物在标准状况下的密度为1.25 ,且每个气体分子中含有两个相同原子,则该气体的名称是
,且每个气体分子中含有两个相同原子,则该气体的名称是_______ 。
(5)27g某二价金属氯化物中含有0.4mol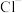 ,则该物质的化学式为
,则该物质的化学式为_______ 。
(6)标准状况下,由CO与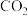 组成的混合气体密度为
组成的混合气体密度为 ,则该混合气体中
,则该混合气体中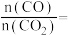
_______ (用含 的分式表示,不需要化简)。
的分式表示,不需要化简)。
(1)28g氮气中含有的原子数约为
(2)7.8g
 固体中含有离子的总物质的量为
固体中含有离子的总物质的量为(3)在含有
 、
、 、
、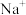 、
、 、
、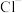 的溶液中,
的溶液中, ,若
,若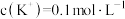 ,则
,则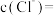
 。
。(4)某气体纯净物在标准状况下的密度为1.25
 ,且每个气体分子中含有两个相同原子,则该气体的名称是
,且每个气体分子中含有两个相同原子,则该气体的名称是(5)27g某二价金属氯化物中含有0.4mol
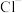 ,则该物质的化学式为
,则该物质的化学式为(6)标准状况下,由CO与
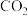 组成的混合气体密度为
组成的混合气体密度为 ,则该混合气体中
,则该混合气体中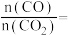
 的分式表示,不需要化简)。
的分式表示,不需要化简)。
您最近一年使用:0次
4 . 把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(1)用单线桥表示反应的电子转移方向和数目:_______ 。
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:_______ 。
(3)若反应中有3.4克氨发生氧化反应,则反应中有生成氮气的质量为_______ 。
(4)高铁酸钠(Na2FeO4)(铁为+6 价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+ NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中 (用化学式表示, 下同),还原产物为_______ ,_______ 元素被氧化。
②配平该反应的方程式并用双线桥在方程式中标出电子转移的情况:_______ 。
(1)用单线桥表示反应的电子转移方向和数目:
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:
(3)若反应中有3.4克氨发生氧化反应,则反应中有生成氮气的质量为
(4)高铁酸钠(Na2FeO4)(铁为+6 价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+ NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中 (用化学式表示, 下同),还原产物为
②配平该反应的方程式并用双线桥在方程式中标出电子转移的情况:
您最近一年使用:0次
名校
解题方法
5 . 已知:2H2(g)+O2(g)=2H2O(1);△H=-571.6 kJ/mol、2CO(g)+O2(g)=2CO2(g);△H=-566 kJ/mol;完全燃烧30 g与H2的相对密度为7.5的水煤气。
(1)求混合气体中各成分的物质的量是多少______ ?
(2)所放出的热量是多少______ ?
(1)求混合气体中各成分的物质的量是多少
(2)所放出的热量是多少
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题:
(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如下:

漂白粉的主要成分是CaCl2和Ca(ClO)2,其中有效成分为Ca(ClO)2,长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式_______ ,_______ 。
(2)若用43.50g二氧化锰与足量浓盐酸(质量分数为63.50%)完全反应,制取氯气。求:
①所得气体的质量为_______ 。
②若将所得气体全部用石灰乳吸收,所制得的漂白粉中所含有效成分的质量为_______ 。
(已知MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O ,本题要求写出计算步骤,答案保留2位小数)
MnCl2+Cl2↑+2H2O ,本题要求写出计算步骤,答案保留2位小数)
(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如下:

漂白粉的主要成分是CaCl2和Ca(ClO)2,其中有效成分为Ca(ClO)2,长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式
(2)若用43.50g二氧化锰与足量浓盐酸(质量分数为63.50%)完全反应,制取氯气。求:
①所得气体的质量为
②若将所得气体全部用石灰乳吸收,所制得的漂白粉中所含有效成分的质量为
(已知MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O ,本题要求写出计算步骤,答案保留2位小数)
MnCl2+Cl2↑+2H2O ,本题要求写出计算步骤,答案保留2位小数)
您最近一年使用:0次
7 . 有 和
和 的混合物共
的混合物共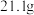 ,将其放入
,将其放入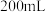 某浓度的盐酸中恰好完全反应。另取等质量该混合物与
某浓度的盐酸中恰好完全反应。另取等质量该混合物与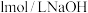 溶液反应,当混合物质量不再减少时,消耗
溶液反应,当混合物质量不再减少时,消耗 溶液
溶液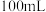 。
。
求:
(1)原混合物中 和
和 的质量各多少克
的质量各多少克_______ ?
(2)盐酸的物质的量浓度为多少_______ ?
 和
和 的混合物共
的混合物共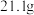 ,将其放入
,将其放入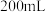 某浓度的盐酸中恰好完全反应。另取等质量该混合物与
某浓度的盐酸中恰好完全反应。另取等质量该混合物与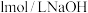 溶液反应,当混合物质量不再减少时,消耗
溶液反应,当混合物质量不再减少时,消耗 溶液
溶液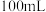 。
。求:
(1)原混合物中
 和
和 的质量各多少克
的质量各多少克(2)盐酸的物质的量浓度为多少
您最近一年使用:0次
解题方法
8 . 某抗酸药的有效成分为碳酸钙。取0.2克药片研碎后加入30 ml 某浓度稀盐酸,恰好完全反应,生成33.6 mL CO2气体(标准状况下)。(假设药片中其他成分不与盐酸反应)。计算:
(1)药片中CaCO3的质量分数_______ 。
(2)所加稀盐酸的物质的量浓度_______ 。
(1)药片中CaCO3的质量分数
(2)所加稀盐酸的物质的量浓度
您最近一年使用:0次
9 . NA为阿伏加德罗常数的值,请完成以下有关计算。
(1)0.05 mol的硫酸钠中含有_______ 个氧原子;其所含Na+与_______ g NaCl中所含有的Na+数目相同。
(2)溶质质量分数为98%、密度为1.84 g·cm-3的某浓硫酸,溶质的物质的量浓度为_______ 。
(3)a个X原子的总质量为b g,则X的相对原子质量可表示为_______ 。
(1)0.05 mol的硫酸钠中含有
(2)溶质质量分数为98%、密度为1.84 g·cm-3的某浓硫酸,溶质的物质的量浓度为
(3)a个X原子的总质量为b g,则X的相对原子质量可表示为
您最近一年使用:0次
解题方法
10 . 一定温度下,在某体积为2L的密闭容器中充入1.5molNO2和2molCO,在一定条件下发生反应:NO2(g)+CO(g) CO2(g)+NO(g),2min时,测得容器中NO的物质的量为0.5mol。
CO2(g)+NO(g),2min时,测得容器中NO的物质的量为0.5mol。
(1)此段时间内,用CO2表示的平均反应速率_______ 。
(2)2min时,CO的转化率_______ 。
(3)平衡时,CO为1mol,求CO2的体积分数_______ 。
 CO2(g)+NO(g),2min时,测得容器中NO的物质的量为0.5mol。
CO2(g)+NO(g),2min时,测得容器中NO的物质的量为0.5mol。(1)此段时间内,用CO2表示的平均反应速率
(2)2min时,CO的转化率
(3)平衡时,CO为1mol,求CO2的体积分数
您最近一年使用:0次



