名校
解题方法
1 . 海洋是资源的宝库,是目前溴和碘的主要来源。海水呈弱碱性,其中溴元素主要以 形式。海水提溴的流程示意图如下:
形式。海水提溴的流程示意图如下:___________ 、___________ 、提取。
2. 可用热空气吹出,其原因是
可用热空气吹出,其原因是___________ 。
3.写出步骤②涉及反应的离子方程式___________ 。该反应说明 的氧化性比
的氧化性比
___________ (填“强”或“弱”)。
4.步骤②需要在酸性条件下进行,原因是什么?___________
5.某小组取含
 的浓缩海水V mL进行实验,最后提取得到
的浓缩海水V mL进行实验,最后提取得到 m g,则该实验中
m g,则该实验中 的产率为
的产率为___________ 。( )
)
 形式。海水提溴的流程示意图如下:
形式。海水提溴的流程示意图如下: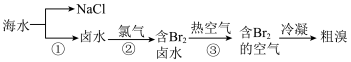
2.
 可用热空气吹出,其原因是
可用热空气吹出,其原因是3.写出步骤②涉及反应的离子方程式
 的氧化性比
的氧化性比
4.步骤②需要在酸性条件下进行,原因是什么?
5.某小组取含

 的浓缩海水V mL进行实验,最后提取得到
的浓缩海水V mL进行实验,最后提取得到 m g,则该实验中
m g,则该实验中 的产率为
的产率为 )
)
您最近一年使用:0次
名校
2 . 人类使用能源的历史可以划分为几个主要阶段:
Ⅰ.柴草时期
(1)大约在180万年前,山西芮城西侯度人发现火并学会利用火。从能量转化的角度看,木材燃烧时化学能主要转化成___________ 能和光能。
Ⅱ.化石能源时期
(2)蒸汽机的发明和广泛应用,标志着煤炭成为主要能源。煤炭中的硫以 的形式存在,用天然气替代煤炭作为燃料能有效减缓
的形式存在,用天然气替代煤炭作为燃料能有效减缓___________ 型酸雨的形成。下列措施不能减少燃煤对大气造成污染的是___________ 。
A.安装除尘脱氨脱硫设备 B.将煤炭气化转化为可燃性气体
C.燃煤工厂烟囱加高 D.开发利用氢能、风能等清洁能源
(3)在明代宋应星所著的《天工开物》中,有关于火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成团。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。):请完成上述火法炼锌反应的化学方程式: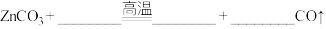 ,用单线桥标出电子转移的方向和数目
,用单线桥标出电子转移的方向和数目___________ 。
(4)炉甘石还含有FeO、 、
、 等杂质,现代以此为原料利用湿法冶炼锌主要分为以下步骤:步骤1:用稀硫酸充分浸取菱锌矿;步骤2:在步骤1的滤液中加入适量
等杂质,现代以此为原料利用湿法冶炼锌主要分为以下步骤:步骤1:用稀硫酸充分浸取菱锌矿;步骤2:在步骤1的滤液中加入适量 除去其中的
除去其中的 ……
……
①步骤1中用稀硫酸浸取后,所得滤渣的主要成分是___________ (填化学式)。
②步骤2中 与
与 反应生成
反应生成 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
Ⅲ.多能源结构时期
在19世纪末期,电力的发现、开发及利用,使人类对化石能源实现了延伸利用,生产出二次能源。随着科技不断发展,可再生能源和清洁能源(绿色能源)将成为新能源的主力军。
(5)某课题小组了解了电池历史后,萌生了自己动手做一个电池的想法,为确保实验顺利进行,下列化学反应可以设计成原电池的是___________
(6)了解了原电池的原理后,该小组收集用品,组装了如下原电池,对该原电池分析正确的是___________
(7)如图所示原电池中,负极材料为___________ 棒(填“Al”或“Mg”),Al电极的反应式为___________ 。
Ⅰ.柴草时期
(1)大约在180万年前,山西芮城西侯度人发现火并学会利用火。从能量转化的角度看,木材燃烧时化学能主要转化成
Ⅱ.化石能源时期
(2)蒸汽机的发明和广泛应用,标志着煤炭成为主要能源。煤炭中的硫以
 的形式存在,用天然气替代煤炭作为燃料能有效减缓
的形式存在,用天然气替代煤炭作为燃料能有效减缓A.安装除尘脱氨脱硫设备 B.将煤炭气化转化为可燃性气体
C.燃煤工厂烟囱加高 D.开发利用氢能、风能等清洁能源
(3)在明代宋应星所著的《天工开物》中,有关于火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成团。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。):请完成上述火法炼锌反应的化学方程式:
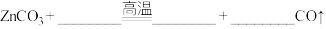 ,用单线桥标出电子转移的方向和数目
,用单线桥标出电子转移的方向和数目(4)炉甘石还含有FeO、
 、
、 等杂质,现代以此为原料利用湿法冶炼锌主要分为以下步骤:步骤1:用稀硫酸充分浸取菱锌矿;步骤2:在步骤1的滤液中加入适量
等杂质,现代以此为原料利用湿法冶炼锌主要分为以下步骤:步骤1:用稀硫酸充分浸取菱锌矿;步骤2:在步骤1的滤液中加入适量 除去其中的
除去其中的 ……
……①步骤1中用稀硫酸浸取后,所得滤渣的主要成分是
②步骤2中
 与
与 反应生成
反应生成 ,写出该反应的离子方程式:
,写出该反应的离子方程式:Ⅲ.多能源结构时期
在19世纪末期,电力的发现、开发及利用,使人类对化石能源实现了延伸利用,生产出二次能源。随着科技不断发展,可再生能源和清洁能源(绿色能源)将成为新能源的主力军。
(5)某课题小组了解了电池历史后,萌生了自己动手做一个电池的想法,为确保实验顺利进行,下列化学反应可以设计成原电池的是___________
A.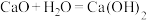 | B. |
C. | D. |
(6)了解了原电池的原理后,该小组收集用品,组装了如下原电池,对该原电池分析正确的是___________

| A.铁环作负极,发生还原反应 |
| B.电池工作时,电子从铁环经LED灯流向铜线 |
| C.电池工作时,铁环变细铜线变粗 |
| D.电池工作结束后柠檬的酸性变强 |
(7)如图所示原电池中,负极材料为

您最近一年使用:0次
3 . 磁铁矿(主要成分是Fe3O4)是炼铁的重要原料,以磁铁矿为原料制取Fe2(SO4)3的反应为4Fe3O4+18SO3+O2 6Fe2(SO4)3
6Fe2(SO4)3
(1)该反应中,氧化剂是___________ ;当1mol O2参与反应时,该反应转移的电子的物质的量___________ mol。
(2)检验Fe2(SO4)3溶液中的Fe3+的方法是___________ 。
 6Fe2(SO4)3
6Fe2(SO4)3(1)该反应中,氧化剂是
(2)检验Fe2(SO4)3溶液中的Fe3+的方法是
您最近一年使用:0次
解题方法
4 .  在一定条件下可被
在一定条件下可被 还原为
还原为 。
。
(1)用电子式表示 的形成过程。
的形成过程。_______ 。
(2)理论上,标准状况下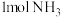 能还原_______
能还原_______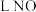 。
。
 在一定条件下可被
在一定条件下可被 还原为
还原为 。
。(1)用电子式表示
 的形成过程。
的形成过程。(2)理论上,标准状况下
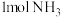 能还原_______
能还原_______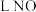 。
。| A.33.6 | B.22.4 | C.14.9 | D.11.2 |
您最近一年使用:0次
解题方法
5 . Ⅰ.氮氧化合物有多种治理或利用的方法。
(1) 被一定量
被一定量 溶液吸收后生成了三种盐,是
溶液吸收后生成了三种盐,是 、
、 与
与___________ 。
(2) ,
, 的
的 。
。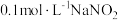 溶液中,下列关系错误的是_______。
溶液中,下列关系错误的是_______。
Ⅱ. 在一定条件下可被还原为
在一定条件下可被还原为 。
。
(3)用电子式表示 的形成过程
的形成过程_________________________________ 。
(4)理论上,标准状况下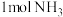 能还原__________
能还原__________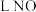 。
。
(1)
 被一定量
被一定量 溶液吸收后生成了三种盐,是
溶液吸收后生成了三种盐,是 、
、 与
与(2)
 ,
, 的
的 。
。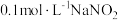 溶液中,下列关系错误的是_______。
溶液中,下列关系错误的是_______。A. | B.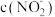 远大于 远大于 |
C. | D.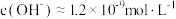 |
Ⅱ.
 在一定条件下可被还原为
在一定条件下可被还原为 。
。(3)用电子式表示
 的形成过程
的形成过程(4)理论上,标准状况下
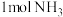 能还原__________
能还原__________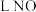 。
。| A.33.6 | B.22.4 | C.14.9 | D.11.2 |
您最近一年使用:0次
名校
解题方法
6 . 海洋中蕴藏着丰富的水资源和卤素资源,具有巨大的开发利用潜力。
(一)海水淡化可用蒸馏法,实验装置如图所示:_______ ,A中除了海水外,还应加入少量_______ 以防暴沸。
(2)图中有两处明显的错误,分别是①_______ ,②_______ 。
(二)从海水中提取溴的工艺流程如图所示:_______ 性,步骤③的离子方程式是_______ 。
(4)不直接用“溴水混合物I”而要用“溴水混合物Ⅱ”进行蒸馏得到液溴,原因是_______ 。
(三)一种利用高分子吸附树脂吸附I2来提取碘元素的工艺流程如图所示:
(四)卤素在性质上存在相似性和递变性。
(6)关于卤素X(X=F、Cl、Br、I)的性质,以下说法正确的是_______。
(7)某实验小组设计了如下装置,验证卤素单质氧化性的递变规律。_______ 。
②若实验操作得当,可证明“氧化性Cl2>Br2>I2”的实验现象是_______ 。
(五)(CN)2和(SCN)2被称为拟卤素,它们的性质与卤素单质相似,已知还原性强弱顺序为I->SCN->CN->Br-。
(8)关于(CN)2的性质推测,不合理的是_______。
(9)向KI、KBr和KSCN的混合溶液中通入一定量的(CN)2后,加热蒸干溶液并充分灼烧,剩余固体的成分不可能是_______。
(一)海水淡化可用蒸馏法,实验装置如图所示:
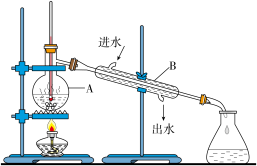
(2)图中有两处明显的错误,分别是①
(二)从海水中提取溴的工艺流程如图所示:
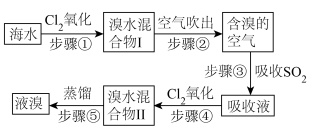
(4)不直接用“溴水混合物I”而要用“溴水混合物Ⅱ”进行蒸馏得到液溴,原因是
(三)一种利用高分子吸附树脂吸附I2来提取碘元素的工艺流程如图所示:
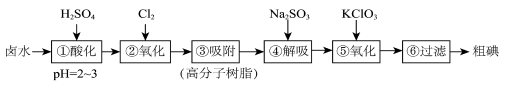
| A.步骤①到④的目的是富集碘元素 |
| B.步骤④是利用氧化还原反应将被吸附的I2洗脱下来 |
| C.若将步骤⑤中的KClO3换成KIO3,产量会提升 |
| D.用酒精洗涤步骤⑥得到的滤渣比用冷水洗涤效果更好 |
(四)卤素在性质上存在相似性和递变性。
(6)关于卤素X(X=F、Cl、Br、I)的性质,以下说法正确的是_______。
| A.X2都可以与水反应生成HX和HXO |
| B.随着X原子核电荷数的增加,X2的熔沸点逐渐升高 |
| C.随着X原子核电荷数的增加,X2与H2化合的程度逐渐减弱 |
| D.随着X原子核电荷数的增加,X-的还原性逐渐减弱 |
(7)某实验小组设计了如下装置,验证卤素单质氧化性的递变规律。
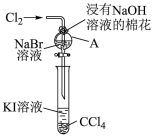
②若实验操作得当,可证明“氧化性Cl2>Br2>I2”的实验现象是
(五)(CN)2和(SCN)2被称为拟卤素,它们的性质与卤素单质相似,已知还原性强弱顺序为I->SCN->CN->Br-。
(8)关于(CN)2的性质推测,不合理的是_______。
| A.(CN)2可以和碱发生反应(CN)2+2OH-=OCN-+CN-+H2O |
| B.NaCN和AgCN都易溶于水 |
| C.CN-可以被Cl2氧化 |
| D.(CN)2可以和活泼金属发生反应 |
(9)向KI、KBr和KSCN的混合溶液中通入一定量的(CN)2后,加热蒸干溶液并充分灼烧,剩余固体的成分不可能是_______。
| A.KI、KBr和KCN | B.KCN和KBr |
| C.KI、KBr、KSCN和KCN | D.KBr、KSCN和KCN |
您最近一年使用:0次
名校
解题方法
7 . ClO2是一种广谱的杀菌剂。它的沸点为11℃,常温下为黄色气体,易分解爆炸,稀释到10%以下时较为安全。该物质易溶于水,某水溶液也具有强氧化性。
(一)工业上制备ClO2的反应为_______NaClO3+_______HCl=_______ClO2↑+_______Cl2↑+_______H2O+_______NaCl
(1)配平上述反应方程式_______ 。
(2)该反应中的还原产物是_______ (写化学式),反应中每生成1molClO2分子,转移电子的数目为_______ 。
(3)ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(ClO )。需要将其转化为Cl-除去,下列试剂能实现其转化过程的是_______(填序号)。
)。需要将其转化为Cl-除去,下列试剂能实现其转化过程的是_______(填序号)。
(二)实验室里可用干燥的氯气与固体亚氯酸钠(NaClO2)制备物质ClO2。_______ 。
(5)试剂X是_______ ,装置B的作用是_______ 。
(6)装置D中冰水的作用是_______ ,通入干燥空气的作用是_______ 。
(7)同学认为该实验装置存在缺陷,应该在D和E之间加入干燥装置,或者将E换成_______ 。
(三)市面上有一种用于消毒的含氯泡腾片,有效成分为NaClO2、NaHSO4和NaHCO3,能快速溶于水并产生大量气泡,同时得到ClO2的溶液。
(8)在上述过程中,产生大量气泡的反应的离子方程式为_______ 。
(9)已知上述过程中生成物质ClO2的反应属于歧化反应,另一个产物为NaCl,请配平这个反应并标出电子转移的方向和数目_______ 。
_______ClO +_______H+=_______Cl-+_______ClO2+_______
+_______H+=_______Cl-+_______ClO2+_______
(一)工业上制备ClO2的反应为_______NaClO3+_______HCl=_______ClO2↑+_______Cl2↑+_______H2O+_______NaCl
(1)配平上述反应方程式
(2)该反应中的还原产物是
(3)ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(ClO
 )。需要将其转化为Cl-除去,下列试剂能实现其转化过程的是_______(填序号)。
)。需要将其转化为Cl-除去,下列试剂能实现其转化过程的是_______(填序号)。| A.O2 | B.FeCl2 | C.KI | D.KMnO4 |
(二)实验室里可用干燥的氯气与固体亚氯酸钠(NaClO2)制备物质ClO2。

(5)试剂X是
(6)装置D中冰水的作用是
(7)同学认为该实验装置存在缺陷,应该在D和E之间加入干燥装置,或者将E换成
(三)市面上有一种用于消毒的含氯泡腾片,有效成分为NaClO2、NaHSO4和NaHCO3,能快速溶于水并产生大量气泡,同时得到ClO2的溶液。
(8)在上述过程中,产生大量气泡的反应的离子方程式为
(9)已知上述过程中生成物质ClO2的反应属于歧化反应,另一个产物为NaCl,请配平这个反应并标出电子转移的方向和数目
_______ClO
 +_______H+=_______Cl-+_______ClO2+_______
+_______H+=_______Cl-+_______ClO2+_______
您最近一年使用:0次
名校
8 . 下图为硫及其化合物在自然界中的部分转化关系。
(2)下列关于SO2的说法正确的是___________。
(3)工业上常用SO2漂白纸浆,时间久了,纸会发黄。简述原因:___________ 。
(4)请写出过程①发生反应的化学方程式,并标出电子转移的方向和数目:___________ 。
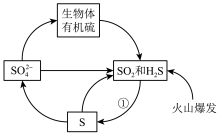
| A.硫元素只有被氧化的过程 |
| B.硫元素只有被还原的过程 |
| C.自然界中硫既有游离态也有化合态 |
| D.自然界中硫只有化合态 |
(2)下列关于SO2的说法正确的是___________。
| A.SO2可用向上排气法收集 |
| B.SO2有毒,不能用作食品加工 |
| C.SO2与H2O反应生成不稳定的H2SO3 |
| D.SO2气体通入BaCl2溶液中产生白色沉淀 |
(3)工业上常用SO2漂白纸浆,时间久了,纸会发黄。简述原因:
(4)请写出过程①发生反应的化学方程式,并标出电子转移的方向和数目:
您最近一年使用:0次
名校
解题方法
9 .  与水反应的化学方程式如下:
与水反应的化学方程式如下: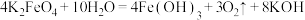 该反应消耗2mol
该反应消耗2mol  时,转移的电子数为
时,转移的电子数为_______  个。若消毒净化1L水投放5mg
个。若消毒净化1L水投放5mg  即可达到卫生标准,则某次消毒净化1980L水时按照标准投入
即可达到卫生标准,则某次消毒净化1980L水时按照标准投入 后,产生的KOH质量为
后,产生的KOH质量为_____ g。
 与水反应的化学方程式如下:
与水反应的化学方程式如下: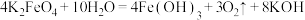 该反应消耗2mol
该反应消耗2mol  时,转移的电子数为
时,转移的电子数为 个。若消毒净化1L水投放5mg
个。若消毒净化1L水投放5mg  即可达到卫生标准,则某次消毒净化1980L水时按照标准投入
即可达到卫生标准,则某次消毒净化1980L水时按照标准投入 后,产生的KOH质量为
后,产生的KOH质量为
您最近一年使用:0次
名校
解题方法
10 . NaH是一种生氢剂,它的电子式为___ ,1mol NaH与水充分反应能生成___ mol  。
。
 。
。
您最近一年使用:0次



