名校
解题方法
1 .  在化学工业中主要用作橡胶和颜料的添加剂,医药上用于制软膏、橡皮膏等。工业上可由菱锌矿(主要成分为
在化学工业中主要用作橡胶和颜料的添加剂,医药上用于制软膏、橡皮膏等。工业上可由菱锌矿(主要成分为 ,还含有
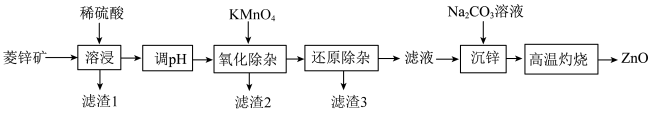
,还含有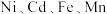 等元素)制备。工艺如图所示:
等元素)制备。工艺如图所示:
相关金属离子 形成氢氧化物沉淀的
形成氢氧化物沉淀的 范围如表:
范围如表:
已知:①“溶浸”后的溶液中金属离子主要有: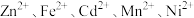 。
。
②弱酸性溶液中 能将
能将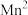 氧化生成
氧化生成 。
。
③氧化性顺序: 。
。
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为___________ , 溶于氨水生成
溶于氨水生成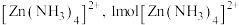 含有
含有___________  键。
键。
(2)“调 ”是向“溶浸”后的溶液中加入少量
”是向“溶浸”后的溶液中加入少量___________ (填化学式)调节至弱酸性(pH为5.5)。此时溶液中 的最大浓度是
的最大浓度是___________ 。
(3)加 “氧化除杂”发生反应的离子方程式分别是
“氧化除杂”发生反应的离子方程式分别是 和
和___________ 。
(4)“还原除杂”除去的离子是___________ 。
(5)生成碱式碳酸锌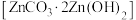 沉淀,写出该步骤的离子方程式
沉淀,写出该步骤的离子方程式___________ 。碱式碳酸锌灼烧后得到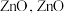 的一种晶体的晶胞是立方晶胞(如图所示),其中与锌原子距离最近的氧原子数有
的一种晶体的晶胞是立方晶胞(如图所示),其中与锌原子距离最近的氧原子数有___________ 个,请在图中画出该晶胞沿 轴方向的平面投影图
轴方向的平面投影图___________ 。

 在化学工业中主要用作橡胶和颜料的添加剂,医药上用于制软膏、橡皮膏等。工业上可由菱锌矿(主要成分为
在化学工业中主要用作橡胶和颜料的添加剂,医药上用于制软膏、橡皮膏等。工业上可由菱锌矿(主要成分为 ,还含有
,还含有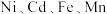 等元素)制备。工艺如图所示:
等元素)制备。工艺如图所示:
相关金属离子
 形成氢氧化物沉淀的
形成氢氧化物沉淀的 范围如表:
范围如表:| 金属离子 |  |  |  |  |  |  |
开始沉淀的 | 1.5 | 6.3 | 6.0 | 7.4 | 8.1 | 6.9 |
沉淀完全的 | 2.8 | 8.3 | 8.0 | 9.4 | 10.1 | 8.9 |
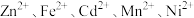 。
。②弱酸性溶液中
 能将
能将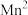 氧化生成
氧化生成 。
。③氧化性顺序:
 。
。(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为 溶于氨水生成
溶于氨水生成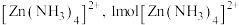 含有
含有 键。
键。(2)“调
 ”是向“溶浸”后的溶液中加入少量
”是向“溶浸”后的溶液中加入少量 的最大浓度是
的最大浓度是(3)加
 “氧化除杂”发生反应的离子方程式分别是
“氧化除杂”发生反应的离子方程式分别是 和
和(4)“还原除杂”除去的离子是
(5)生成碱式碳酸锌
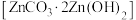 沉淀,写出该步骤的离子方程式
沉淀,写出该步骤的离子方程式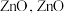 的一种晶体的晶胞是立方晶胞(如图所示),其中与锌原子距离最近的氧原子数有
的一种晶体的晶胞是立方晶胞(如图所示),其中与锌原子距离最近的氧原子数有 轴方向的平面投影图
轴方向的平面投影图
您最近一年使用:0次
2024-02-23更新
|
493次组卷
|
2卷引用:湖南省长沙市雅礼中学2023-2024学年高三上学期一模化学试题
名校
2 . I.铝土矿是工业上制备金属铝的主要原料,其主要成分是 ,同时还含有
,同时还含有 、
、 。工业上可使用碱浸法提取铝土矿中的
。工业上可使用碱浸法提取铝土矿中的 ,其工业流程如图所示。根据图示信息,请回答下列问题:
,其工业流程如图所示。根据图示信息,请回答下列问题:_______ ,滤渣B的主要成分是_______ (填化学式)。
(2)实验室中进行煅烧时最适合用来盛放 固体的实验仪器名称是
固体的实验仪器名称是_______ 。
(3)用 与C、
与C、 在高温条件下反应可制取
在高温条件下反应可制取 ,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是
,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是_______ 。
Ⅱ.高铁酸钾( )具有极强的氧化性和优良的絮凝功能,是一种绿色环保多功能型水处理剂。下图是生产高铁酸钾的一种工艺流程:
)具有极强的氧化性和优良的絮凝功能,是一种绿色环保多功能型水处理剂。下图是生产高铁酸钾的一种工艺流程: 的部分性质如下:
的部分性质如下:
(4)写出①中发生的离子方程式:_______ 。
(5)②中加入NaOH固体的目的是_______ (填字母序号)
A.加入NaOH固体做氧化剂
B.为后续反应提供碱性环境
C.NaOH固体溶解时会放出较多的热量,有利于后续生成
(6)完成④中反应的离子方程式:_______ 。
(7)⑥中洗涤时,洗涤剂最好选用_______(填字母序号)。
(8)现取洗涤并干燥后 样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为
样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为_______ 。(计算结果保留到0.1%)
 ,同时还含有
,同时还含有 、
、 。工业上可使用碱浸法提取铝土矿中的
。工业上可使用碱浸法提取铝土矿中的 ,其工业流程如图所示。根据图示信息,请回答下列问题:
,其工业流程如图所示。根据图示信息,请回答下列问题: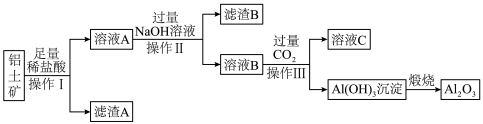
(2)实验室中进行煅烧时最适合用来盛放
 固体的实验仪器名称是
固体的实验仪器名称是(3)用
 与C、
与C、 在高温条件下反应可制取
在高温条件下反应可制取 ,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是
,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是Ⅱ.高铁酸钾(
 )具有极强的氧化性和优良的絮凝功能,是一种绿色环保多功能型水处理剂。下图是生产高铁酸钾的一种工艺流程:
)具有极强的氧化性和优良的絮凝功能,是一种绿色环保多功能型水处理剂。下图是生产高铁酸钾的一种工艺流程: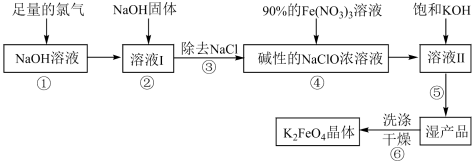
 的部分性质如下:
的部分性质如下:溶解性 | 溶于水,微溶于浓KOH溶液,难溶于有机物 |
稳定性 | 温度为0~5℃或强碱性溶液中能稳定存在;酸性或中性溶液中Fe变为+3价并放出 |
(4)写出①中发生的离子方程式:
(5)②中加入NaOH固体的目的是
A.加入NaOH固体做氧化剂
B.为后续反应提供碱性环境
C.NaOH固体溶解时会放出较多的热量,有利于后续生成

(6)完成④中反应的离子方程式:
(7)⑥中洗涤时,洗涤剂最好选用_______(填字母序号)。
A. | B.KOH溶液 | C.异丙醇 | D. 溶液 溶液 |
(8)现取洗涤并干燥后
 样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为
样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为
您最近一年使用:0次
2024-02-20更新
|
196次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高一下学期选科适应性检测化学试卷
名校
3 . 连二亚硫酸钠 也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取
也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取 。
。
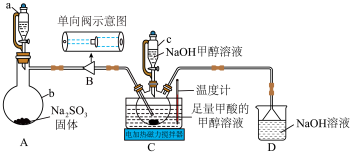
回答下列问题:
(1)仪器a的名称是___________ 。
(2)单向阀的作用是___________ ,制备保险粉前先打开仪器a的活塞的目的是___________ 。
(3)已知三颈烧瓶中的甲酸转化为 ,写出生成
,写出生成 的化学方程式:
的化学方程式:___________ 。
(4) 是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:
是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:___________ 。
(5) 固体隔绝空气加热使之完全分解得到固体产物
固体隔绝空气加热使之完全分解得到固体产物 、
、 和
和 气体,设计实验方案检验产物中含有的
气体,设计实验方案检验产物中含有的 :
:___________ (写出实验操作、现象及结论)。
(6)称取粗产品 加水溶解,用NaOH溶液碱化后,加入一定量的
加水溶解,用NaOH溶液碱化后,加入一定量的 溶液恰好完全反应
溶液恰好完全反应 ,将溶液中生成的纳米级的银粉干燥后称重,得到
,将溶液中生成的纳米级的银粉干燥后称重,得到 银,则粗产品中连二亚硫酸钠的纯度为
银,则粗产品中连二亚硫酸钠的纯度为___________ (用含 、
、 的表达式)。
的表达式)。
 也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取
也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取 。
。
回答下列问题:
(1)仪器a的名称是
(2)单向阀的作用是
(3)已知三颈烧瓶中的甲酸转化为
 ,写出生成
,写出生成 的化学方程式:
的化学方程式:(4)
 是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:
是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:(5)
 固体隔绝空气加热使之完全分解得到固体产物
固体隔绝空气加热使之完全分解得到固体产物 、
、 和
和 气体,设计实验方案检验产物中含有的
气体,设计实验方案检验产物中含有的 :
:(6)称取粗产品
 加水溶解,用NaOH溶液碱化后,加入一定量的
加水溶解,用NaOH溶液碱化后,加入一定量的 溶液恰好完全反应
溶液恰好完全反应 ,将溶液中生成的纳米级的银粉干燥后称重,得到
,将溶液中生成的纳米级的银粉干燥后称重,得到 银,则粗产品中连二亚硫酸钠的纯度为
银,则粗产品中连二亚硫酸钠的纯度为 、
、 的表达式)。
的表达式)。
您最近一年使用:0次
名校
解题方法
4 . 某小组利用如图所示装置制备并收集TiCl4(夹持装置略去),并测定由TiCl4制备的纳米xTiO2•yH2O的组成。
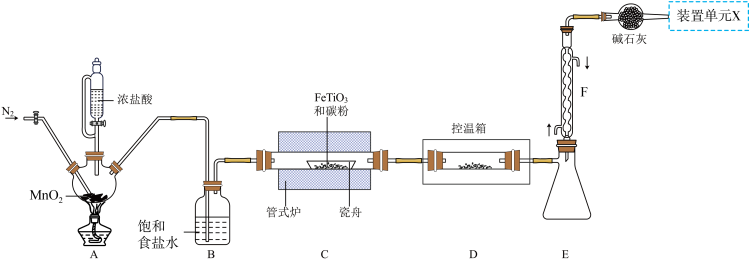
已知:
I. TiCl4高温时能与O2反应,极易水解,能溶于CCl4;
Ⅱ.瓷舟中主反应生成TiCl4、FeCl3(容易二聚成Fe2Cl6)和一种氧化物(有毒气体),还有少量副产物CCL4;
Ⅲ.相关物质的熔沸点如表:
(1)TiCl4摩尔质量大于FeCl3,但沸点却低于FeCl3的原因是_______ 。
(2)写出A中反应的化学方程式_______ ;上述装置存在一处缺陷,会导致TiCl4产率降低,改进的方法是_______ 。
(3)将管式炉加热至900℃时,瓷舟中主要反应的化学方程式为_______ 。
(4)装置E、F的作用为_______ 。
(5)设计实验测定纳米xTiO2•yH2O组成。
已知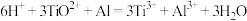 ,
,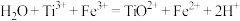
(可选试剂:水、稀硫酸、稀硝酸、氢氧化钠溶液、Al粉、0.1000 的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)
的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)
①取样称重:称取4.675g样品。②酸溶:用足量稀硫酸溶解。
③还原:加入过量Al粉还原至Al粉不再溶解,过滤取滤液定容。定容为500mL,取20.00mL。
④滴定:用0.1000 的NH4Fe(SO4)2标准溶液滴定,标准溶液装在
的NH4Fe(SO4)2标准溶液滴定,标准溶液装在_______ 滴定管(填“酸式”、“碱式”),用_______ 做指示剂,平均消耗标准溶液20.00mL,则xTiO2•yH2O的化学式为_______ 。

已知:
I. TiCl4高温时能与O2反应,极易水解,能溶于CCl4;
Ⅱ.瓷舟中主反应生成TiCl4、FeCl3(容易二聚成Fe2Cl6)和一种氧化物(有毒气体),还有少量副产物CCL4;
Ⅲ.相关物质的熔沸点如表:
TiCl4 | FeCl3 | CCl4 | |
熔点/℃ |
| 306 |
|
沸点/℃ | 136.4 | 315 | 76.8 |
(1)TiCl4摩尔质量大于FeCl3,但沸点却低于FeCl3的原因是
(2)写出A中反应的化学方程式
(3)将管式炉加热至900℃时,瓷舟中主要反应的化学方程式为
(4)装置E、F的作用为
(5)设计实验测定纳米xTiO2•yH2O组成。
已知
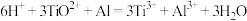 ,
,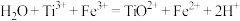
(可选试剂:水、稀硫酸、稀硝酸、氢氧化钠溶液、Al粉、0.1000
 的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)
的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)①取样称重:称取4.675g样品。②酸溶:用足量稀硫酸溶解。
③还原:加入过量Al粉还原至Al粉不再溶解,过滤取滤液定容。定容为500mL,取20.00mL。
④滴定:用0.1000
 的NH4Fe(SO4)2标准溶液滴定,标准溶液装在
的NH4Fe(SO4)2标准溶液滴定,标准溶液装在
您最近一年使用:0次
2024-02-19更新
|
911次组卷
|
3卷引用:湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题
湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题(已下线)2024届广东省华南师范大学附属中学 广雅中学 深圳中学 广东实验中学高三上学期四校联考化学试题广东省云浮市云安区云安中学2023-2024学年高三下学期3月考试化学试题
名校
5 . 用低品铜矿(主要含 、
、 )制备
)制备 的一种工艺流程如下:
的一种工艺流程如下:
 、
、 )制备
)制备 的一种工艺流程如下:
的一种工艺流程如下: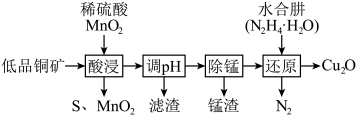
A.“酸浸”过程中 发生反应的离子方程式为 发生反应的离子方程式为 |
B.“调 ”的目的是除去溶液中的 ”的目的是除去溶液中的 |
C.使用 溶液“除锰”时,锰渣中可能会含有少量 溶液“除锰”时,锰渣中可能会含有少量 |
| D.“还原”过程中参与反应的氧化剂和还原剂的物质的量之比为2:1 |
您最近一年使用:0次
2024-02-17更新
|
209次组卷
|
3卷引用:湖南省常德市汉寿县第一中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
6 . 过氧化尿素[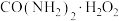 ,无毒无味的白色粉末,易溶于水,水溶液离解为尿素和
,无毒无味的白色粉末,易溶于水,水溶液离解为尿素和 ,45℃以上能分解]是一种新型精细化工产品,也是一种新型的固体消毒剂和氧化剂,其合成原理如下:
,45℃以上能分解]是一种新型精细化工产品,也是一种新型的固体消毒剂和氧化剂,其合成原理如下: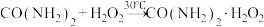 ,实验过程:在三口烧瓶(实验装置如图所示)中加入一定比例的双氧水、尿素和稳定剂,搅拌,固体溶解后,升温至30℃,反应40min,加入包膜剂,继续搅拌10min。然后降温至0℃,结晶3h后,抽滤,将滤饼置于烘箱中,50℃下烘干2h,得到最终的过氧化尿素产品。
,实验过程:在三口烧瓶(实验装置如图所示)中加入一定比例的双氧水、尿素和稳定剂,搅拌,固体溶解后,升温至30℃,反应40min,加入包膜剂,继续搅拌10min。然后降温至0℃,结晶3h后,抽滤,将滤饼置于烘箱中,50℃下烘干2h,得到最终的过氧化尿素产品。
(1)仪器A的名称是___________ 。
(2)过氧化尿素是过氧化氢和尿素的加合产物,二者之间通过___________ (填“配位键”或“氢键”)相结合。
(3)从抽滤后的母液中分离出 和尿素,可采用的操作是___________(填字母)。
和尿素,可采用的操作是___________(填字母)。
(4)过氧化尿素的纯度与干燥温度的关系如图所示:___________ 。
(5)为测定产品中活性氧的含量,称取干燥样品4.000 g,溶解,在250 mL容量瓶中定容,准确量取25 mL于锥形瓶中,加入2 mL 6.0 mol⋅L-1硫酸,然后用0.1000 mol⋅L-1的KMnO4标准溶液滴定,滴定终点时,消耗KMnO4溶液16.00mL(已知KMnO4溶液与尿素不反应)。
①写出用KMnO4标准溶液滴定时反应的离子方程式:___________ 。
②本实验KMnO4溶液滴定过程中操作滴定管的图示正确的是___________ (填字母)。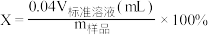 ,根据滴定结果,可确定产品中活性氧的含量为
,根据滴定结果,可确定产品中活性氧的含量为___________ %。
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量___________ (填“偏高”“偏低”或“不变”)。
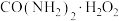 ,无毒无味的白色粉末,易溶于水,水溶液离解为尿素和
,无毒无味的白色粉末,易溶于水,水溶液离解为尿素和 ,45℃以上能分解]是一种新型精细化工产品,也是一种新型的固体消毒剂和氧化剂,其合成原理如下:
,45℃以上能分解]是一种新型精细化工产品,也是一种新型的固体消毒剂和氧化剂,其合成原理如下: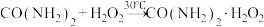 ,实验过程:在三口烧瓶(实验装置如图所示)中加入一定比例的双氧水、尿素和稳定剂,搅拌,固体溶解后,升温至30℃,反应40min,加入包膜剂,继续搅拌10min。然后降温至0℃,结晶3h后,抽滤,将滤饼置于烘箱中,50℃下烘干2h,得到最终的过氧化尿素产品。
,实验过程:在三口烧瓶(实验装置如图所示)中加入一定比例的双氧水、尿素和稳定剂,搅拌,固体溶解后,升温至30℃,反应40min,加入包膜剂,继续搅拌10min。然后降温至0℃,结晶3h后,抽滤,将滤饼置于烘箱中,50℃下烘干2h,得到最终的过氧化尿素产品。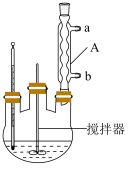
(1)仪器A的名称是
(2)过氧化尿素是过氧化氢和尿素的加合产物,二者之间通过
(3)从抽滤后的母液中分离出
 和尿素,可采用的操作是___________(填字母)。
和尿素,可采用的操作是___________(填字母)。| A.盐析、过滤 | B.减压蒸馏、结晶 | C.分液、过滤 | D.减压蒸馏、萃取 |
(4)过氧化尿素的纯度与干燥温度的关系如图所示:
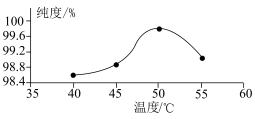
(5)为测定产品中活性氧的含量,称取干燥样品4.000 g,溶解,在250 mL容量瓶中定容,准确量取25 mL于锥形瓶中,加入2 mL 6.0 mol⋅L-1硫酸,然后用0.1000 mol⋅L-1的KMnO4标准溶液滴定,滴定终点时,消耗KMnO4溶液16.00mL(已知KMnO4溶液与尿素不反应)。
①写出用KMnO4标准溶液滴定时反应的离子方程式:
②本实验KMnO4溶液滴定过程中操作滴定管的图示正确的是
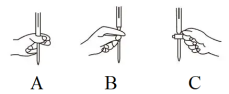
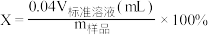 ,根据滴定结果,可确定产品中活性氧的含量为
,根据滴定结果,可确定产品中活性氧的含量为④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量
您最近一年使用:0次
2024-02-01更新
|
302次组卷
|
3卷引用:2024届湖南省衡阳市第八中学高三下学期模拟预测化学试题
名校
解题方法
7 . 草酸是一种用途广泛的二元有机中强酸,某同学通过查阅资料设计了如图所示的装置(夹持仪器省略)制备一定量的草酸晶体(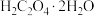 ),并验证其具有的某些性质。回答下列问题:
),并验证其具有的某些性质。回答下列问题:___________ 。
(2)装置B的作用是___________ ,若实验中使用酒精溶液代替食盐水,并且利用酸性 溶液检验有乙炔生成,则气体通过B后应先通入到盛有
溶液检验有乙炔生成,则气体通过B后应先通入到盛有___________ 的洗气瓶,最后通入到酸性 溶液中。
溶液中。
(3)草酸在装置C中生成,反应的化学方程式为___________ ,装置D的作用是___________ 。
(4)待反应结束后,从C中分离出草酸晶体,然后用 的酸性
的酸性 溶液进行滴定以测定其纯度。
溶液进行滴定以测定其纯度。
①称量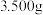 草酸晶体配制
草酸晶体配制 溶液,下列配制操作中错误的是
溶液,下列配制操作中错误的是___________ (填标号)。 溶液的体积如表所示,其中第一次实验滴定后的液面位置如图所示:
溶液的体积如表所示,其中第一次实验滴定后的液面位置如图所示:
则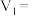
___________  ,样品中草酸晶体的质量分数为
,样品中草酸晶体的质量分数为___________  (保留一位小数)。
(保留一位小数)。
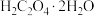 ),并验证其具有的某些性质。回答下列问题:
),并验证其具有的某些性质。回答下列问题: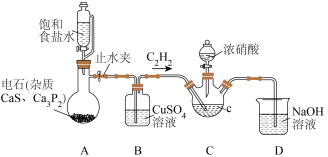
(2)装置B的作用是
 溶液检验有乙炔生成,则气体通过B后应先通入到盛有
溶液检验有乙炔生成,则气体通过B后应先通入到盛有 溶液中。
溶液中。(3)草酸在装置C中生成,反应的化学方程式为
(4)待反应结束后,从C中分离出草酸晶体,然后用
 的酸性
的酸性 溶液进行滴定以测定其纯度。
溶液进行滴定以测定其纯度。①称量
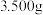 草酸晶体配制
草酸晶体配制 溶液,下列配制操作中错误的是
溶液,下列配制操作中错误的是a.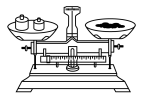 b.
b.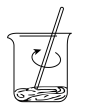 c.
c.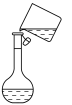 d.
d.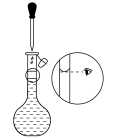
 溶液的体积如表所示,其中第一次实验滴定后的液面位置如图所示:
溶液的体积如表所示,其中第一次实验滴定后的液面位置如图所示: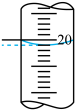
| 滴定次数 | 待测溶液体积 | 标准溶液的体积 | ||
| 滴定前刻度 | 滴定后刻度 | 溶液的体积 | ||
| 第一次 | 20.00 | 0.20 |  | |
| 第二次 | 20.00 | 2.56 | 28.40 | |
| 第三次 | 20.00 | 0.22 | 20.32 | |
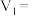
 ,样品中草酸晶体的质量分数为
,样品中草酸晶体的质量分数为 (保留一位小数)。
(保留一位小数)。
您最近一年使用:0次
8 . 全球能源结构正在向多元、清洁、低碳转型。太阳能的利用是热门研究方向之一,例如,可以利用太阳能将水转化为 ,某种光分解水的过程如图所示,下列说法不正确的是
,某种光分解水的过程如图所示,下列说法不正确的是
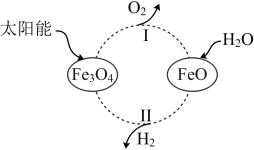
 ,某种光分解水的过程如图所示,下列说法不正确的是
,某种光分解水的过程如图所示,下列说法不正确的是
A.该转化发生的总反应为 |
B.该转化过程中循环利用的物质有 |
C.过程Ⅰ中每产生 ,同时产生 ,同时产生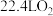 |
D.过程Ⅱ中生成 和 和 的物质的量之比为 的物质的量之比为 |
您最近一年使用:0次
9 . 根据所学知识,进行作答
(1)2023年第19届杭州亚运会场馆实现 覆盖,制作
覆盖,制作 芯片的材料为
芯片的材料为 (氮化镓),镓原子结构示意图为
(氮化镓),镓原子结构示意图为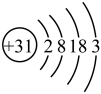 ,镓元素在元素周期表中的位置
,镓元素在元素周期表中的位置___________ 。
(2)2023年10月26日神舟十七号飞船成功对接太空站,为使宇航员有良好的生存环境,飞船中装有盛 颗粒的供氧装置。
颗粒的供氧装置。
① 中的氧元素的化合价为
中的氧元素的化合价为___________ 价。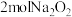 与水完全反应时,生成的氧气在标准状况下体积为
与水完全反应时,生成的氧气在标准状况下体积为___________ L。
②如用 (超氧化钾)代替
(超氧化钾)代替 ,也能达到同样的目的。写出
,也能达到同样的目的。写出 与
与 反应的化学方程式
反应的化学方程式___________ 。
(3)2023年12月18日甘肃省发生地震灾害,受灾废墟需喷洒大量84消毒液的稀溶液进行消毒。84消毒液可由 与
与 溶液反应制得,其主要成分为
溶液反应制得,其主要成分为 。
。
①资料(3)涉及的物质中,属于碱的是___________ (填化学式,下同);属于盐的是___________ 。
②“84消毒液”与稀盐酸混合使用可增强其漂白效果,原因是___________ (用离子方程式表示),但“84消毒液”却不能与“洁厕灵”(浓盐酸)混合使用,原因是___________ (用离子方程式表示)。
(1)2023年第19届杭州亚运会场馆实现
 覆盖,制作
覆盖,制作 芯片的材料为
芯片的材料为 (氮化镓),镓原子结构示意图为
(氮化镓),镓原子结构示意图为 ,镓元素在元素周期表中的位置
,镓元素在元素周期表中的位置(2)2023年10月26日神舟十七号飞船成功对接太空站,为使宇航员有良好的生存环境,飞船中装有盛
 颗粒的供氧装置。
颗粒的供氧装置。①
 中的氧元素的化合价为
中的氧元素的化合价为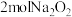 与水完全反应时,生成的氧气在标准状况下体积为
与水完全反应时,生成的氧气在标准状况下体积为②如用
 (超氧化钾)代替
(超氧化钾)代替 ,也能达到同样的目的。写出
,也能达到同样的目的。写出 与
与 反应的化学方程式
反应的化学方程式(3)2023年12月18日甘肃省发生地震灾害,受灾废墟需喷洒大量84消毒液的稀溶液进行消毒。84消毒液可由
 与
与 溶液反应制得,其主要成分为
溶液反应制得,其主要成分为 。
。①资料(3)涉及的物质中,属于碱的是
②“84消毒液”与稀盐酸混合使用可增强其漂白效果,原因是
您最近一年使用:0次
名校
解题方法
10 . 金属镓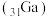 应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。镓与铝是同主族元素,性质相似。
应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。镓与铝是同主族元素,性质相似。
(1)铝原子核外共有___________ 种不同能量的电子。用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如: 。常温下
。常温下 的金属性比
的金属性比 的金属性
的金属性___________ (选填“强”、“弱”)。利用上述方法可制取 的主要原因是
的主要原因是___________ 。
A.高温时 的活泼性大于
的活泼性大于 B.高温有利于
B.高温有利于 分解
分解
C.高温时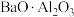 比
比 稳定 D.Ba的沸点比
稳定 D.Ba的沸点比 的低
的低
(2)下列有关镓和镓的化合物的说法正确的是___________。
(3)GaAs是共价化合物,一种重要的半导体材料。As与 同周期,As与
同周期,As与 同主族。
同主族。
①下列事实不能用元素周期律解释的是___________ (填字母)。
a.䂸性: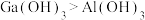
b.非金属性:
c.酸性: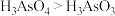
②GaAs中,As元素化合价为-3价,用原子结构理论解释As元素显负价的原因___________ 。
③废弃含 半导体材料可以用浓硝酸溶解
半导体材料可以用浓硝酸溶解 ,生成
,生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
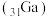 应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。镓与铝是同主族元素,性质相似。
应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。镓与铝是同主族元素,性质相似。(1)铝原子核外共有
 。常温下
。常温下 的金属性比
的金属性比 的金属性
的金属性 的主要原因是
的主要原因是A.高温时
 的活泼性大于
的活泼性大于 B.高温有利于
B.高温有利于 分解
分解C.高温时
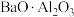 比
比 稳定 D.Ba的沸点比
稳定 D.Ba的沸点比 的低
的低(2)下列有关镓和镓的化合物的说法正确的是___________。
A.基态Ga原子价层电子的轨道表示式: |
B.常温下, 可与水剧烈反应放出氢气 可与水剧烈反应放出氢气 |
C.一定条件下, 可与 可与 反应生成盐 反应生成盐 |
D.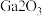 可由 可由 受热分解得到 受热分解得到 |
(3)GaAs是共价化合物,一种重要的半导体材料。As与
 同周期,As与
同周期,As与 同主族。
同主族。①下列事实不能用元素周期律解释的是
a.䂸性:
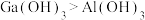
b.非金属性:

c.酸性:
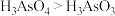
②GaAs中,As元素化合价为-3价,用原子结构理论解释As元素显负价的原因
③废弃含
 半导体材料可以用浓硝酸溶解
半导体材料可以用浓硝酸溶解 ,生成
,生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式
您最近一年使用:0次

 23.2
23.2

