名校
1 . 自古至今,铁及其化合物在人类生产生活中的使用发挥了巨大的作用。
(1)古代中国四大发明之一的司南是由天然磁石制成的,其主要成分是__________ (填化学式)。
(2)工业上,可利用硫酸亚铁溶液和氧气在催化剂条件下制作铁黄(FeOOH),一种不溶于水的黄色固体,写出该反应的离子方程式:______________________________ 。
(3)从某工业废渣wg(主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工艺流程如图(部分操作和条件略):

已知:二氧化硅不溶于硫酸。
①滤渣的主要成分为__________ (填化学式)。
②写出步骤Ⅴ的化学方程式:______________________________ 。
③请写出验证硫酸亚铁溶液中是否存在 的实验方法:
的实验方法:______________________________ 。
④若提取过程中铁元素的损耗忽略不计,最终获得ng的氧化铁。则废渣中铁元素的质量分数为__________ 。
(1)古代中国四大发明之一的司南是由天然磁石制成的,其主要成分是
(2)工业上,可利用硫酸亚铁溶液和氧气在催化剂条件下制作铁黄(FeOOH),一种不溶于水的黄色固体,写出该反应的离子方程式:
(3)从某工业废渣wg(主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工艺流程如图(部分操作和条件略):

已知:二氧化硅不溶于硫酸。
①滤渣的主要成分为
②写出步骤Ⅴ的化学方程式:
③请写出验证硫酸亚铁溶液中是否存在
 的实验方法:
的实验方法:④若提取过程中铁元素的损耗忽略不计,最终获得ng的氧化铁。则废渣中铁元素的质量分数为
您最近半年使用:0次
名校
2 . 下列除杂方案正确的是(括号内为除杂剂)
A. 溶液中混有 溶液中混有 (Fe粉) (Fe粉) |
B.NaOH溶液中混有 ( ( ) ) |
C. 中混有HCl气体(饱和 中混有HCl气体(饱和 溶液) 溶液) |
D. 中混有 中混有 (Cu粉) (Cu粉) |
您最近半年使用:0次
解题方法
3 . 硫酸亚铁晶体( )在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
请回答下列问题:

(1)向步骤①的滤液中滴加KSCN溶液后变为红色,则该滤液中含________ (填离子符号),检验滤液中还存在 的方法为
的方法为________ (说明试剂、现象)。
(2)步骤②加入过量 的目的是
的目的是________ 。
(3)步骤③中反应的离子方程式________ 。
(4)步骤④中一系列处理的操作步骤包括:过滤、________ 、灼烧、________ 、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为________ g。
 )在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:请回答下列问题:

(1)向步骤①的滤液中滴加KSCN溶液后变为红色,则该滤液中含
 的方法为
的方法为(2)步骤②加入过量
 的目的是
的目的是(3)步骤③中反应的离子方程式
(4)步骤④中一系列处理的操作步骤包括:过滤、
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为
您最近半年使用:0次
4 . 至今为止,铁是人类冶炼和使用最多的金属。铁及其化合物在生产生活中,乃至国防建设等都发挥着重要作用。某校化学社成员对铁的部分重要化合物进行了系列实验。
Ⅰ.四氧化三铁的光热效应在热量感应、电磁波吸收和纳米材料加热方面具有广泛的应用。例如,在医学领域中,可以利用四氧化三铁的光热效应进行热疗,用于治疗肿瘤等疾病。该校化学社成员利用如图所示装置进行了“铁与水蒸气反应”的实验制备 ,请回答下列问题:
,请回答下列问题:
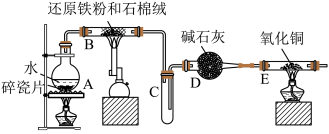
(1)装有碱石灰的仪器D的名称是________ ;装置A的作用是________ 。
(2)装置B中发生反应的化学方程式是________ 。
(3)实验结束后,某成员甲同学认为可以用磁铁吸引产物来确定产物中有未反应的铁粉,有另一成员乙同学认为用此方法判断不妥,你觉得乙同学的依据是________ 。
Ⅱ.氯化铁主要用于金属蚀刻,污水处理。该校化学社成员将Ⅰ中得到的产物溶于稀盐酸中得到溶液a,向溶液a中通入氯气后用此溶液制备 晶体。
晶体。
(4)检验溶液a中是否含 的具体操作及现象为
的具体操作及现象为________ 。
Ⅲ.胶体可以吸附水中悬浮颗粒并沉降而常用来作净水剂。该校化学社成员将得到的 晶体配成饱和溶液,进行实验室制备氢氧化铁胶体实验。
晶体配成饱和溶液,进行实验室制备氢氧化铁胶体实验。
(5)制备方法:在小烧杯中加入50mL蒸馏水,加热至沸腾,向沸水中加入5~6滴饱和 溶液,继续煮沸至液体呈红褐色,停止加热,即可得到
溶液,继续煮沸至液体呈红褐色,停止加热,即可得到 胶体,其反应的化学方程式为
胶体,其反应的化学方程式为________ 。鉴别 胶体和
胶体和 溶液除了观察颜色外,最好的方法是通过
溶液除了观察颜色外,最好的方法是通过________ 判断。
(6)高铁酸钠溶液杀灭病菌后也可以得到氢氧化铁胶体,进而起到净水的作用。其化学反应主要为 (未配平),
(未配平), 的化学式为
的化学式为________ ,请写出配平的化学方程式:________ 。
Ⅰ.四氧化三铁的光热效应在热量感应、电磁波吸收和纳米材料加热方面具有广泛的应用。例如,在医学领域中,可以利用四氧化三铁的光热效应进行热疗,用于治疗肿瘤等疾病。该校化学社成员利用如图所示装置进行了“铁与水蒸气反应”的实验制备
 ,请回答下列问题:
,请回答下列问题:
(1)装有碱石灰的仪器D的名称是
(2)装置B中发生反应的化学方程式是
(3)实验结束后,某成员甲同学认为可以用磁铁吸引产物来确定产物中有未反应的铁粉,有另一成员乙同学认为用此方法判断不妥,你觉得乙同学的依据是
Ⅱ.氯化铁主要用于金属蚀刻,污水处理。该校化学社成员将Ⅰ中得到的产物溶于稀盐酸中得到溶液a,向溶液a中通入氯气后用此溶液制备
 晶体。
晶体。(4)检验溶液a中是否含
 的具体操作及现象为
的具体操作及现象为Ⅲ.胶体可以吸附水中悬浮颗粒并沉降而常用来作净水剂。该校化学社成员将得到的
 晶体配成饱和溶液,进行实验室制备氢氧化铁胶体实验。
晶体配成饱和溶液,进行实验室制备氢氧化铁胶体实验。(5)制备方法:在小烧杯中加入50mL蒸馏水,加热至沸腾,向沸水中加入5~6滴饱和
 溶液,继续煮沸至液体呈红褐色,停止加热,即可得到
溶液,继续煮沸至液体呈红褐色,停止加热,即可得到 胶体,其反应的化学方程式为
胶体,其反应的化学方程式为 胶体和
胶体和 溶液除了观察颜色外,最好的方法是通过
溶液除了观察颜色外,最好的方法是通过(6)高铁酸钠溶液杀灭病菌后也可以得到氢氧化铁胶体,进而起到净水的作用。其化学反应主要为
 (未配平),
(未配平), 的化学式为
的化学式为
您最近半年使用:0次
5 . 物质的分类对化学的学习和研究非常重要,物质的结构、性质和用途是对物质进行分类的重要依据,下列有关常见的几种金属氧化物的性质和用途的说法不正确的是
| A.CaO可用作干燥剂 |
B. 和MgO的熔点都很高,可用作耐火材料 和MgO的熔点都很高,可用作耐火材料 |
C. 是一种红棕色粉末,用于制作红色油漆和涂料 是一种红棕色粉末,用于制作红色油漆和涂料 |
D. 和足量HI溶液发生反应得到的溶液可以使KSCN溶液变红 和足量HI溶液发生反应得到的溶液可以使KSCN溶液变红 |
您最近半年使用:0次
名校
解题方法
6 . 下列离子方程式错误的是
A.用过量氨水吸收少量 气体: 气体: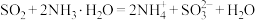 |
B.用 溶液腐蚀覆铜板: 溶液腐蚀覆铜板: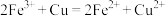 |
C.NaClO溶液中通入少量 气体: 气体: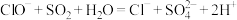 |
D.向硫酸酸化的 溶液中滴加少量双氧水: 溶液中滴加少量双氧水: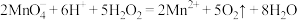 |
您最近半年使用:0次
7 . 下列物质性质与用途具有对应关系的是
A. 具有漂白性,可以使含酚酞的 具有漂白性,可以使含酚酞的 溶液褪色 溶液褪色 |
B. 具有还原性,可以做燃料电池的负极气体 具有还原性,可以做燃料电池的负极气体 |
C. 溶液显酸性,可用于刻蚀铜电路板 溶液显酸性,可用于刻蚀铜电路板 |
| D.铝的化学性质活泼,常温下可用铝制容器盛装稀硝酸 |
您最近半年使用:0次
解题方法
8 . 已知有以下物质相互转化
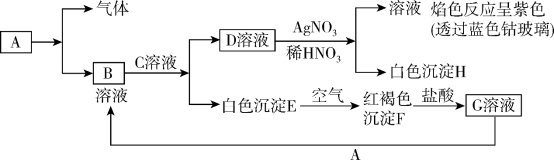
试回答:
(1)写出B的化学式_______ ,H的化学式_______
(2)写出由E→F反应的化学方程式:_______ 。
(3)把KSCN溶液加到G溶液中的现象是_______ ;向G溶液加入A的有关离子反应方程式:_______ 。

试回答:
(1)写出B的化学式
(2)写出由E→F反应的化学方程式:
(3)把KSCN溶液加到G溶液中的现象是
您最近半年使用:0次
9 . 下列说法正确的是
| A.KSCN溶液可用于检验实验室久置的FeSO4溶液是否含有Fe3+ |
| B.工业上将Cl2通入澄清石灰水制取漂白粉 |
| C.某无色澄清溶液中滴加AgNO3溶液,有白色沉淀生成,则溶液中有Cl- |
| D.铁与水蒸气反应生成氢氧化铁和氢气 |
您最近半年使用:0次
名校
解题方法
10 . 某研究小组同学欲探究某袋敞口放置一段时间的名为“硫酸亚铁家庭园艺精品肥料”的花肥的主要成分及性质。首先对该花肥的主要成分进行了如下假设:
a.只含有 b.含有
b.含有 和
和 c.只含有
c.只含有
将花肥固体粉末溶于水中得到溶液 ,然后进行如下实验:
,然后进行如下实验:
(1)提出假设 的依据是
的依据是___________ (用离子方程式表示)。
(2)实验Ⅰ的预期现象是先产生白色沉淀,然后变成灰绿色,最后变成红褐色沉淀,产生该预期现象的依据是___________ (用化学方程式和离子方程式表示)。
(3)实验Ⅱ中所加试剂的名称是___________ ,由此得出的结论是___________ 。
(4)为进一步验证假设,该小组同学进行了如下实验:
实验Ⅳ中新制氯水参加反应的离子方程式是___________ 。
(5)通过以上实验,可得到的结论是___________ 。还可以通过实验___________ 证明 的存在(填具体的操作及现象)。
的存在(填具体的操作及现象)。
a.只含有
 b.含有
b.含有 和
和 c.只含有
c.只含有
将花肥固体粉末溶于水中得到溶液
 ,然后进行如下实验:
,然后进行如下实验:| 实验序号 | 操作 | 现象 |
| Ⅰ | 取 溶液 溶液 ,加入 ,加入 的 的 溶液 溶液 | 产生红褐色沉淀 |
| Ⅱ | 取 溶液 溶液 ,加入1滴___________溶液 ,加入1滴___________溶液 | 溶液显红色 |
 的依据是
的依据是(2)实验Ⅰ的预期现象是先产生白色沉淀,然后变成灰绿色,最后变成红褐色沉淀,产生该预期现象的依据是
(3)实验Ⅱ中所加试剂的名称是
(4)为进一步验证假设,该小组同学进行了如下实验:
| 实验序号 | 操作 | 现象 |
| Ⅲ | 取 溶液 溶液 ,加入1滴 ,加入1滴 溶液,再加入 溶液,再加入 水 水 | 溶液显红色 |
| Ⅳ | 取 溶液 溶液 ,加入1滴 ,加入1滴 溶液,再加入 溶液,再加入 新制氯水 新制氯水 | 溶液显红色,且颜色比实验而的深 |
(5)通过以上实验,可得到的结论是
 的存在(填具体的操作及现象)。
的存在(填具体的操作及现象)。
您最近半年使用:0次



