解题方法
1 . 汽车已成为现代社会的重要交通工具之一。它所使用燃料经历了从煤到汽油的变迁。时至今日,人们依然在探索、优化车用燃料。
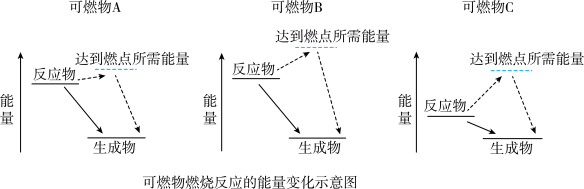
(1)某同学根据所查阅资料,绘制了三种可燃物在空气中发生燃烧反应的能量变化示意图(如图)。根据示意图,你认为哪种物质更适合用作车用燃料______ (填写字母);并说出你的选择依据______ 。
(2)庚烷(C7H16)是汽油的主要成分之一。完全燃烧1g庚烷生成二氧化碳气体和液态水时产生的热量为48kJ。请写出表示庚烷燃烧热的热化学方程式______ ;
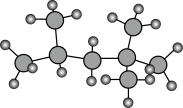
(3)目前汽车主要使用燃料为汽油。“辛烷值”用来表示汽油的质量。异辛烷用作抗爆性优良的标准,辛烷值为100。正庚烷用作抗爆性低劣的标准,辛烷值为0。如图是异辛烷的球棍模型:
①1mol异辛烷和1mol正庚烷分别完全燃烧生成水和二氧化碳,消耗氧气的质量之差是______ g。
②异辛烷的同分异构体有很多,其中一种同分异构体X,其一氯代物只有一种结构,则X的结构简式为______ 。
(4)车用燃料在使用过程中会产生汽车尾气(主要含有一氧化碳,一氧化氮),是造成空气污染的主要因素之一。可在汽车尾气系统中安装催化转化器,使CO和NO在催化剂的作用下反应生成两种无污染的气体。其中,氮气和氧气反应生成一氧化氮的能量变化如图所示,则由该反应生成2mol NO(g),对应热化学方程式的△H=______

(1)某同学根据所查阅资料,绘制了三种可燃物在空气中发生燃烧反应的能量变化示意图(如图)。根据示意图,你认为哪种物质更适合用作车用燃料

(2)庚烷(C7H16)是汽油的主要成分之一。完全燃烧1g庚烷生成二氧化碳气体和液态水时产生的热量为48kJ。请写出表示庚烷燃烧热的热化学方程式
(3)目前汽车主要使用燃料为汽油。“辛烷值”用来表示汽油的质量。异辛烷用作抗爆性优良的标准,辛烷值为100。正庚烷用作抗爆性低劣的标准,辛烷值为0。如图是异辛烷的球棍模型:

①1mol异辛烷和1mol正庚烷分别完全燃烧生成水和二氧化碳,消耗氧气的质量之差是
②异辛烷的同分异构体有很多,其中一种同分异构体X,其一氯代物只有一种结构,则X的结构简式为
(4)车用燃料在使用过程中会产生汽车尾气(主要含有一氧化碳,一氧化氮),是造成空气污染的主要因素之一。可在汽车尾气系统中安装催化转化器,使CO和NO在催化剂的作用下反应生成两种无污染的气体。其中,氮气和氧气反应生成一氧化氮的能量变化如图所示,则由该反应生成2mol NO(g),对应热化学方程式的△H=

您最近一年使用:0次
名校
2 . Ⅰ.纯过氧化氢是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体。实验室常用过氧化氢制取氧气,工业上过氧化氢是重要的氧化剂和还原剂,常用于消毒、杀菌、漂白等。某化学兴趣小组的同学围绕过氧化氢开展了调查研究与实验,请你参与其中一起完成下列学习任务:
(1)写出过氧化氢的电子式:____________ 。
(2)实验室中用过氧化氢制取氧气的化学方程式为_______________ ,当生成标准状况下2.24L O2时,转移电子为______ mol。
(3)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在其水溶液中的电离方程式:______ 。(只写第一步)
(4)同学们发现向滴加了酚酞的NaOH溶液中加入H2O2后,溶液中红色消失。关于褪色原因:甲同学认为H2O2是二元弱酸,消耗了OH-使红色消失;乙同学认为H2O2具有漂白性使溶液褪色。请设计一个简单的实验方案来判断甲、乙两位同学的说法是否正确:___________
Ⅱ.工业尾气中含有大量的氮氧化物,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
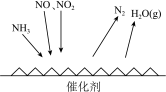
(1)由上图可知SCR技术中的氧化剂为________ 。
(2)用Fe作催化剂加热时,在氨气足量的情况下,当NO2与NO的物质的量之比为1∶1时,写出该反应的化学方程式:________________________________
Ⅲ.研究减少CO2排放是一项重要课题。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应①:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1= -49.6 kJ/mol
CH3OH(g)+H2O(g) △H1= -49.6 kJ/mol
反应②:CH3OCH3(g)+H2O(g) 2CH3OH(g) △H2= +23.4 kJ/mol
2CH3OH(g) △H2= +23.4 kJ/mol
反应③:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H3=
CH3OCH3(g)+3H2O(g) △H3=___________ kJ/mol。
(1)写出过氧化氢的电子式:
(2)实验室中用过氧化氢制取氧气的化学方程式为
(3)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在其水溶液中的电离方程式:
(4)同学们发现向滴加了酚酞的NaOH溶液中加入H2O2后,溶液中红色消失。关于褪色原因:甲同学认为H2O2是二元弱酸,消耗了OH-使红色消失;乙同学认为H2O2具有漂白性使溶液褪色。请设计一个简单的实验方案来判断甲、乙两位同学的说法是否正确:
Ⅱ.工业尾气中含有大量的氮氧化物,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:

(1)由上图可知SCR技术中的氧化剂为
(2)用Fe作催化剂加热时,在氨气足量的情况下,当NO2与NO的物质的量之比为1∶1时,写出该反应的化学方程式:
Ⅲ.研究减少CO2排放是一项重要课题。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应①:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1= -49.6 kJ/mol
CH3OH(g)+H2O(g) △H1= -49.6 kJ/mol反应②:CH3OCH3(g)+H2O(g)
 2CH3OH(g) △H2= +23.4 kJ/mol
2CH3OH(g) △H2= +23.4 kJ/mol反应③:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) △H3=
CH3OCH3(g)+3H2O(g) △H3=
您最近一年使用:0次
3 . 研究煤的合理利用及CO2的综合应用有着重要的意义。请回答以下问题:
I.煤的气化
已知煤的气化过程涉及的基本化学反应有:
C(s)+H2O(g) CO(g)+H2(g)△H=+131kJ/mol
CO(g)+H2(g)△H=+131kJ/mol
②CO(g)+3H2(g) CH4(g)+H2O(g)△H=akJ/mol
CH4(g)+H2O(g)△H=akJ/mol
查阅资料反应②中相关化学键键能数据如下表:
(1)煤直接甲烷化反应C(s)+2H2(g) CH4(g)的△H为
CH4(g)的△H为_______ kJ/mol,该反应在______ (填“高温”或“低温”)下自发进行。
Ⅱ.合成低碳烯烃
在体积为1 L的密闭容器中,充入1molCO2和2.5molH2,发生反应:
2CO2(g)+6H2(g) C2H4(g)+4H2O(g)△H=-128kJ/mol,测得温度对催化剂催化效率和C02平衡转化率的影响如图所示:
C2H4(g)+4H2O(g)△H=-128kJ/mol,测得温度对催化剂催化效率和C02平衡转化率的影响如图所示:

(2)图中低温时,随着温度升高催化剂的催化效率提高,但C02的平衡转化率却反而降低,其原因是__________ 。
(3)250℃时,该反应的平衡常数K值为__________ 。
Ⅲ.合成甲醇
在恒温2 L容积不变的密闭容器中,充入lmolCO2和3molH2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得不同时刻反应前后容器内压强变化(p后/p前)如下表:
CH3OH(g)+H2O(g),测得不同时刻反应前后容器内压强变化(p后/p前)如下表:
(4)反应前1小时内的平均反应速率V(H2)为_________ mol/(L·h),该温度下CO2的平衡转化率为_________ 。
IV.电解逆转化制乙醇
(5)科研人员通过反复实验发现:CO2可以在酸性水溶液中电解生成乙醇,则生成乙醇的反应发生在_________ 极(“阴”或“阳”),该电极的反应式为_________ 。
I.煤的气化
已知煤的气化过程涉及的基本化学反应有:
C(s)+H2O(g)
 CO(g)+H2(g)△H=+131kJ/mol
CO(g)+H2(g)△H=+131kJ/mol②CO(g)+3H2(g)
 CH4(g)+H2O(g)△H=akJ/mol
CH4(g)+H2O(g)△H=akJ/mol查阅资料反应②中相关化学键键能数据如下表:
| 化学键 |  | H-H | H—C | H-O |
| E/(kJ/mol) | 1072 | 436 | 414 | 465 |
 CH4(g)的△H为
CH4(g)的△H为Ⅱ.合成低碳烯烃
在体积为1 L的密闭容器中,充入1molCO2和2.5molH2,发生反应:
2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g)△H=-128kJ/mol,测得温度对催化剂催化效率和C02平衡转化率的影响如图所示:
C2H4(g)+4H2O(g)△H=-128kJ/mol,测得温度对催化剂催化效率和C02平衡转化率的影响如图所示:
(2)图中低温时,随着温度升高催化剂的催化效率提高,但C02的平衡转化率却反而降低,其原因是
(3)250℃时,该反应的平衡常数K值为
Ⅲ.合成甲醇
在恒温2 L容积不变的密闭容器中,充入lmolCO2和3molH2,发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得不同时刻反应前后容器内压强变化(p后/p前)如下表:
CH3OH(g)+H2O(g),测得不同时刻反应前后容器内压强变化(p后/p前)如下表:| 时间/h | 1 | 2 | 3 | 4 | 5 | 6 |
| p后/p前 | 0.90 | 0.85 | 0.82 | 0.81 | 0.80 | 0.80 |
IV.电解逆转化制乙醇
(5)科研人员通过反复实验发现:CO2可以在酸性水溶液中电解生成乙醇,则生成乙醇的反应发生在
您最近一年使用:0次
2019高三·全国·专题练习
4 . (1)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,从而减少SO2的排放,但产生的CO又会与CaSO4发生化学反应,从而降低脱硫效率。相关的热化学方程式如下:
①CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g)ΔH1=+210.5 kJ·mol-1
CaO(s)+SO2(g)+CO2(g)ΔH1=+210.5 kJ·mol-1
② CaSO4(s)+CO(g)
CaSO4(s)+CO(g) 
 CaS(s)+CO2(g) ΔH2=-47.3 kJ·mol-1
CaS(s)+CO2(g) ΔH2=-47.3 kJ·mol-1
请回答下列问题:
反应CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g) ΔH3=
CaS(s)+3CO2(g) ΔH3=________ kJ•mol-1;平衡时增大压强,此反应________ (填“正向”“逆向”或“不”)移动。
(2)有机物加氢反应中镍是常用的催化剂,但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为弄清该方法对催化剂的影响,查得资料如下:
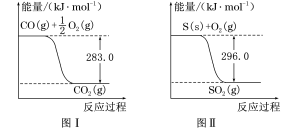
则:①不用通入O2氧化的方法除去CO的原因是_______________________ 。
②SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=____________ 。
(3)汽车发动机工作时会引发N2(g)+O2(g)===2NO(g) ΔH=+180 kJ·mol-1,其能量变化示意图如下:
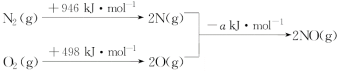
则NO中氮氧键的键能为____________ kJ·mol-1。
①CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g)ΔH1=+210.5 kJ·mol-1
CaO(s)+SO2(g)+CO2(g)ΔH1=+210.5 kJ·mol-1 ②
 CaSO4(s)+CO(g)
CaSO4(s)+CO(g) 
 CaS(s)+CO2(g) ΔH2=-47.3 kJ·mol-1
CaS(s)+CO2(g) ΔH2=-47.3 kJ·mol-1请回答下列问题:
反应CaO(s)+3CO(g)+SO2(g)
 CaS(s)+3CO2(g) ΔH3=
CaS(s)+3CO2(g) ΔH3=(2)有机物加氢反应中镍是常用的催化剂,但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为弄清该方法对催化剂的影响,查得资料如下:

则:①不用通入O2氧化的方法除去CO的原因是
②SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=
(3)汽车发动机工作时会引发N2(g)+O2(g)===2NO(g) ΔH=+180 kJ·mol-1,其能量变化示意图如下:

则NO中氮氧键的键能为
您最近一年使用:0次
5 . 研究煤的合理利用及CO2的综合应用有着重要的意义。请回答以下问题:
Ⅰ.煤的气化
已知煤的气化过程涉及的基本化学反应有:
①C(s)+H2O(g) CO(g)+H2(g) ΔH=+131 kJ/mol
CO(g)+H2(g) ΔH=+131 kJ/mol
②CO(g)+3H2(g) CH4(g)+H2O(g) ΔH=a kJ/mol
CH4(g)+H2O(g) ΔH=a kJ/mol
查阅资料反应②中相关化学键键能数据如下表:
(1)则反应②中a=______ 。
(2)煤直接甲烷化反应C(s)+2H2 (g) CH4(g)的ΔH为
CH4(g)的ΔH为______ kJ/mol,该反应在______ (填“高温”或“低温”)下自发进行。
Ⅱ.合成低碳烯烃
在体积为1 L的密闭容器中,充入1 mol CO2和2.5 mol H2,发生反应: 2CO2(g)+6H2(g) C2H4(g)+4H2O(g) ΔH=-128 kJ/mol,测得温度对催化剂催化效率和CO2平衡转化率的影响如右图所示:
C2H4(g)+4H2O(g) ΔH=-128 kJ/mol,测得温度对催化剂催化效率和CO2平衡转化率的影响如右图所示:

(3)图中低温时,随着温度升高催化剂的催化效率提高,但CO2的平衡转化率却反而降低,其原因是______ 。
(4)250℃时,该反应的平衡常数K值为______ 。
Ⅲ.合成甲醇
在恒温2 L容积不变的密闭容器中,充入1 molCO2和3 molH2,发生反应:CO2(g)+3H2(g) CH3OH(g) +H2O(g) ,测得不同时刻反应前后容器内压强变化(p后/p前)如下表:
CH3OH(g) +H2O(g) ,测得不同时刻反应前后容器内压强变化(p后/p前)如下表:
(5)反应前1小时内的平均反应速率v(H2)为______ mol/(L·h),该温度下CO2的平衡转化率为______ 。
Ⅳ.电解逆转化制乙醇
(6)科研人员通过反复实验发现:CO2可以在酸性水溶液中电解生成乙醇,则生成乙醇的反应发生在______ 极(填“阴”或“阳”),该电极的反应式为______ 。
Ⅰ.煤的气化
已知煤的气化过程涉及的基本化学反应有:
①C(s)+H2O(g)
 CO(g)+H2(g) ΔH=+131 kJ/mol
CO(g)+H2(g) ΔH=+131 kJ/mol②CO(g)+3H2(g)
 CH4(g)+H2O(g) ΔH=a kJ/mol
CH4(g)+H2O(g) ΔH=a kJ/mol查阅资料反应②中相关化学键键能数据如下表:
| 化学键 | C≡O | H-H | H-C | H-O |
| E/(kJ/mol) | 1072 | 436 | 414 | 465 |
(1)则反应②中a=
(2)煤直接甲烷化反应C(s)+2H2 (g)
 CH4(g)的ΔH为
CH4(g)的ΔH为Ⅱ.合成低碳烯烃
在体积为1 L的密闭容器中,充入1 mol CO2和2.5 mol H2,发生反应: 2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g) ΔH=-128 kJ/mol,测得温度对催化剂催化效率和CO2平衡转化率的影响如右图所示:
C2H4(g)+4H2O(g) ΔH=-128 kJ/mol,测得温度对催化剂催化效率和CO2平衡转化率的影响如右图所示: 
(3)图中低温时,随着温度升高催化剂的催化效率提高,但CO2的平衡转化率却反而降低,其原因是
(4)250℃时,该反应的平衡常数K值为
Ⅲ.合成甲醇
在恒温2 L容积不变的密闭容器中,充入1 molCO2和3 molH2,发生反应:CO2(g)+3H2(g)
 CH3OH(g) +H2O(g) ,测得不同时刻反应前后容器内压强变化(p后/p前)如下表:
CH3OH(g) +H2O(g) ,测得不同时刻反应前后容器内压强变化(p后/p前)如下表:| 时间/h | 1 | 2 | 3 | 4 | 5 | 6 |
| p后/p前 | 0.90 | 0.85 | 0.82 | 0.81 | 0.80 | 0.80 |
Ⅳ.电解逆转化制乙醇
(6)科研人员通过反复实验发现:CO2可以在酸性水溶液中电解生成乙醇,则生成乙醇的反应发生在
您最近一年使用:0次
名校
6 . 肼(N2H4)是一种无色易溶于水的油状液体,具有碱性和极强的还原性,在工业生产中应用非常广泛。

(1)已知肼的球棍模型如图所示,写出肼的电子式:____________ 。
(2)已知1g肼(N2H4)气体燃烧生成氮气和水蒸气,放出16.7kJ的热量。写出该反应的热化学方程式:______________ 。
(3)目前正在研发的一-种肼燃料电池的结构如下图所示。
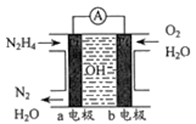
①该电池的负极是______ (填“a”或“b”)电极。
②写出正极的电极反应式:_____________ 。
(4)在1L固定体积的容器中加入0.1molN2H4,在303K、Pt催化下发生反应:N2H4(l) N2(g)+2H2(g)。测得容器中
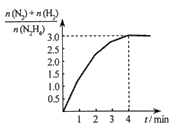
N2(g)+2H2(g)。测得容器中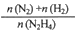 与时间关系如下图所示,则0~4min内氮气的平均反应速率v(N2)=
与时间关系如下图所示,则0~4min内氮气的平均反应速率v(N2)=______ 。

(1)已知肼的球棍模型如图所示,写出肼的电子式:
(2)已知1g肼(N2H4)气体燃烧生成氮气和水蒸气,放出16.7kJ的热量。写出该反应的热化学方程式:
(3)目前正在研发的一-种肼燃料电池的结构如下图所示。

①该电池的负极是
②写出正极的电极反应式:
(4)在1L固定体积的容器中加入0.1molN2H4,在303K、Pt催化下发生反应:N2H4(l)
 N2(g)+2H2(g)。测得容器中
N2(g)+2H2(g)。测得容器中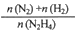 与时间关系如下图所示,则0~4min内氮气的平均反应速率v(N2)=
与时间关系如下图所示,则0~4min内氮气的平均反应速率v(N2)=
您最近一年使用:0次
2018-07-04更新
|
367次组卷
|
3卷引用:【全国百强校】江苏省常熟中学2017-2018学年高一下学期期末调研测试化学试题
名校
解题方法
7 . I.锰是在地壳中广泛分布的元素之一,其单质和化合物在工农业生产中有着重要的作用。已知Al的燃烧热为ΔH=—ckJ·mol—1,金属锰可用铝热法制得。其余相关热化学方程式为:3Mn3O4(s)+8Al(s)=9Mn(s)+4Al2O3(s) ΔH1 = akJ·mol—1
3MnO2(s)=Mn3O4(s)+O2(g) ΔH2 = b kJ·mol—1
则3MnO2(s)+4Al(s)=3Mn(s)+2Al2O3(s) ΔH3 =__________ kJ·mol—1(用含a、b、c的式子表示)
II.无机和有机氰化物在工农业生产中应用广泛,尤其是冶金工业常用氰化物,含氰废水的处理显得尤为重要。含氰废水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。
(1)电解处理法:用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为__________ (填“阴极”或“阳极”),阳极产生ClO-的电极反应为__________ ,阳极产生的ClO-将CN-氧化为无害物质而除去的离子方程式为__________ 。

(2)UV(紫外光线的简称)—H2O2氧化法。
实验过程:取一定量含氰废水,调节pH,加入一定物质的量的H2O2,置于UV工艺装置中,光照一定时间后取样分析。
【查阅资料】
①在强碱性溶液中4[Fe(CN)6]3-+4OH—=4[Fe(CN)6]4-+O2↑+2H2O,[Fe(CN)6]4-更稳定;
②[Fe(CN)6]3-转化为CN-容易被H2O2除去;
③HCN是有毒的弱酸,易挥发。
①废水中的CN一经以下反应实现转化:CN—+H2O2+H2O=A+NH3↑,则A是__________ (用符号表示)。
②含氰废水在不同pH下的除氰效果如图所示,pH选择的最佳范围应为__________ (a.7-10;b.10-11;c.11-13),解释该pH不宜太大的原因__________ 。
3MnO2(s)=Mn3O4(s)+O2(g) ΔH2 = b kJ·mol—1
则3MnO2(s)+4Al(s)=3Mn(s)+2Al2O3(s) ΔH3 =
II.无机和有机氰化物在工农业生产中应用广泛,尤其是冶金工业常用氰化物,含氰废水的处理显得尤为重要。含氰废水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。
(1)电解处理法:用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为

(2)UV(紫外光线的简称)—H2O2氧化法。
实验过程:取一定量含氰废水,调节pH,加入一定物质的量的H2O2,置于UV工艺装置中,光照一定时间后取样分析。
【查阅资料】
①在强碱性溶液中4[Fe(CN)6]3-+4OH—=4[Fe(CN)6]4-+O2↑+2H2O,[Fe(CN)6]4-更稳定;
②[Fe(CN)6]3-转化为CN-容易被H2O2除去;
③HCN是有毒的弱酸,易挥发。
①废水中的CN一经以下反应实现转化:CN—+H2O2+H2O=A+NH3↑,则A是
②含氰废水在不同pH下的除氰效果如图所示,pH选择的最佳范围应为

您最近一年使用:0次
8 . 2018年6月27日,国务院发布《打赢蓝天保卫战三年行动计划》,该计划是中国政府部署的一项污染防治行动计划,旨在持续改善空气质量,为群众留住更多蓝天。对废气的进行必要的处理,让空气更加清洁是环境科学的重要课题。
(1)已知:N2(g)+O2(g)=2NO(g)△H1=+180.5kJ/mol
C(s)+O2(g)=CO2(g)△H2=-393.5kJ/mol
2C(s)+O2(g)=2CO(g)△H3=-221.0kJ/mol
若某反应的平衡常数表达式为 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式_____________ 。
(2)用如图所示的电解装置可将雾霾中的NO、SO2分别转化为 和
和

①NO在电极上发生的反应为_________________ 。
②SO2在电极上发生的反应为__________________ 。
③写出物质A的化学式____________ 。
(3)利用氨气可以设计高能环保燃料电池(反应原理:4NH3+3O2=2N2+6H2O),用该电池电解含有 的碱性工业废水,在阴极产生N2。阴极的电极反应式为
的碱性工业废水,在阴极产生N2。阴极的电极反应式为__________ ;在标准状况下,当阴极收集到13.44LN2时,理论上消耗NH3的体积为________ L。
(1)已知:N2(g)+O2(g)=2NO(g)△H1=+180.5kJ/mol
C(s)+O2(g)=CO2(g)△H2=-393.5kJ/mol
2C(s)+O2(g)=2CO(g)△H3=-221.0kJ/mol
若某反应的平衡常数表达式为
 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式(2)用如图所示的电解装置可将雾霾中的NO、SO2分别转化为
 和
和

①NO在电极上发生的反应为
②SO2在电极上发生的反应为
③写出物质A的化学式
(3)利用氨气可以设计高能环保燃料电池(反应原理:4NH3+3O2=2N2+6H2O),用该电池电解含有
 的碱性工业废水,在阴极产生N2。阴极的电极反应式为
的碱性工业废水,在阴极产生N2。阴极的电极反应式为
您最近一年使用:0次
解题方法
9 . 氮是地球上含量丰富的一种元素,氮及其化合物在生产、生活中有着重要作用。
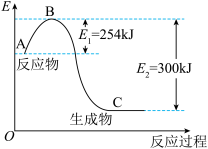
(1)如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:____________________________________ 。
(2)已知化学键键能是形成或断裂1mol化学键放出或吸收的能量,单位为kJ·mol-1。
试根据表中及(1)的图中数据计算N—H键的键能为________ kJ·mol-1。
(3)用NH3催化还原NOx还可以消除氮氧化物的污染。例如:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)ΔH1=-akJ·mol-1①
N2(g)+O2(g)=2NO(g)ΔH2=-bkJ·mol-1②
若1molNH3还原NO至N2,则该反应过程中的反应热ΔH3=________ kJ·mol-1(用含a、b的式子表示)。
(4)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极在碱性条件下发生反应的电极反应式为____________ 。
(1)如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:

(2)已知化学键键能是形成或断裂1mol化学键放出或吸收的能量,单位为kJ·mol-1。
| 化学键 | H—H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
(3)用NH3催化还原NOx还可以消除氮氧化物的污染。例如:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)ΔH1=-akJ·mol-1①
N2(g)+O2(g)=2NO(g)ΔH2=-bkJ·mol-1②
若1molNH3还原NO至N2,则该反应过程中的反应热ΔH3=
(4)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极在碱性条件下发生反应的电极反应式为
您最近一年使用:0次
解题方法
10 . 氮的重要化合物如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等,在生产、生活中具有重要作用.
(1)利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g)△H1=44.0kJ•mol-1
N2(g)+O2(g)=2NO(g)△H2=229.3kJ•mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3=-906.5kJ•mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H4
则△H4=_____________ kJ•mol-1.
(2)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
①写出该反应的离子方程式:_____________ ;
②在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝.若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为:_____________ ;为抑制肼的分解,可采取的合理措施有_____________ (任写一种)。
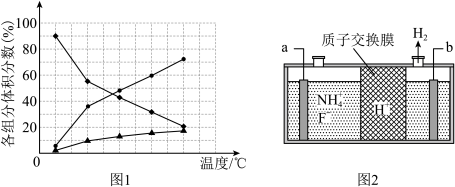
(3)在微电子工业中NF3常用作半导体、液晶和薄膜太阳能电池等生产过程的蚀刻剂,在对硅、氮化硅等材料进行蚀刻时具有非常优异的蚀刻速率和选择性,在被蚀刻物表明不留任何残留物,对表面物污染。工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示。
①a电极为电解池的_____________ (填“阴”或“阳”)极,写出该电极的电极反应式:_____________ ;
②以NF3对氮化硅(Si3N4)材料的蚀刻为例,用反应方程式来解释为什么在被蚀刻物表面不留任何残留物_____________ 。
③气体NF3不可燃但可助燃,故气体NF3应远离火种且与还原剂、易燃或可燃物等分开存放,结构决定性质,试从结构角度加以分析_____________ 。
④能与水发生反应,生成两种酸及一种气态氧化物,试写出相应的化学方程式_____________ 。
(1)利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g)△H1=44.0kJ•mol-1
N2(g)+O2(g)=2NO(g)△H2=229.3kJ•mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3=-906.5kJ•mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H4
则△H4=
(2)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
①写出该反应的离子方程式:
②在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝.若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为:

(3)在微电子工业中NF3常用作半导体、液晶和薄膜太阳能电池等生产过程的蚀刻剂,在对硅、氮化硅等材料进行蚀刻时具有非常优异的蚀刻速率和选择性,在被蚀刻物表明不留任何残留物,对表面物污染。工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示。
①a电极为电解池的
②以NF3对氮化硅(Si3N4)材料的蚀刻为例,用反应方程式来解释为什么在被蚀刻物表面不留任何残留物
③气体NF3不可燃但可助燃,故气体NF3应远离火种且与还原剂、易燃或可燃物等分开存放,结构决定性质,试从结构角度加以分析
④能与水发生反应,生成两种酸及一种气态氧化物,试写出相应的化学方程式
您最近一年使用:0次



