解题方法
1 . 石油是宝贵的能源,属于战略资源。 、
、 均是石油裂解的产物。请回答下列问题:
均是石油裂解的产物。请回答下列问题:
(1)石油裂化、裂解为_______ (填“物理”或“化学")变化。
(2)已知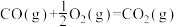
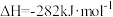
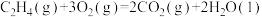
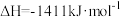
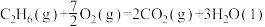
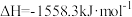
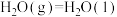
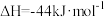
则反应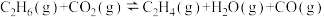

_______  。
。
(3)一定温度下,在某2L恒容密闭容器中充入1mol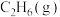 和1mol
和1mol 发生反应
发生反应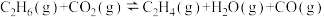 ,10min后达到平衡,容器内压强为起始压强的1.25倍。
,10min后达到平衡,容器内压强为起始压强的1.25倍。
①下列说法可以判定反应到达平衡状态的是_______ 。(填字母序号)
A.
B.相同时间内,断裂2mol 的同时断裂1mol
的同时断裂1mol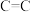
C.容器内气体的密度不再发生变化
D.容器内气体的平均相对分子质量不再发生变化
②0~10min,v(CO)=_______  ,
, 的转化率为
的转化率为_______ %, 的体积分数为
的体积分数为_______ %。
 、
、 均是石油裂解的产物。请回答下列问题:
均是石油裂解的产物。请回答下列问题:(1)石油裂化、裂解为
(2)已知
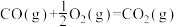
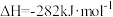
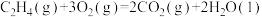
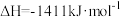
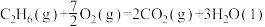
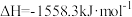
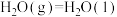
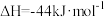
则反应
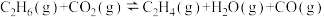

 。
。(3)一定温度下,在某2L恒容密闭容器中充入1mol
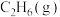 和1mol
和1mol 发生反应
发生反应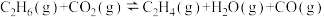 ,10min后达到平衡,容器内压强为起始压强的1.25倍。
,10min后达到平衡,容器内压强为起始压强的1.25倍。①下列说法可以判定反应到达平衡状态的是
A.

B.相同时间内,断裂2mol
 的同时断裂1mol
的同时断裂1mol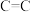
C.容器内气体的密度不再发生变化
D.容器内气体的平均相对分子质量不再发生变化
②0~10min,v(CO)=
 ,
, 的转化率为
的转化率为 的体积分数为
的体积分数为
您最近一年使用:0次
解题方法
2 . (1)研究 、
、 等大气污染气体的处理方法具有重要的意义。
等大气污染气体的处理方法具有重要的意义。
已知:①
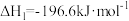
②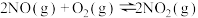
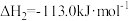
则反应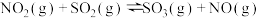 的
的
_______  。
。
(2)t℃时,将2mol 和1mol
和1mol 通入体积为2L的恒温、恒容密闭容器中,发生如下反应:
通入体积为2L的恒温、恒容密闭容器中,发生如下反应: ,2min时反应达到化学平衡,此时测得容器内的压强为起始压强的0.8倍,请回答:
,2min时反应达到化学平衡,此时测得容器内的压强为起始压强的0.8倍,请回答:
①下列叙述能证明该反应已达到化学平衡状态的是_______ (选填字母)。
A.容器内压强不再发生变化
B. 的体积分数不再发生变化
的体积分数不再发生变化
C.容器内气体原子总数不再发生变化
D.相同时间内消耗2nmol 的同时消耗nmol
的同时消耗nmol
E.相同时间内消耗2nmol 的同时生成nmol
的同时生成nmol
F.混合气体密度不再变化
②从反应开始到达化学平衡,生成 的平均反应速率为
的平均反应速率为___ ;平衡时, 的转化率为
的转化率为___ 。
(3)已知 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是
电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是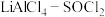 。电池的总反应可表示为
。电池的总反应可表示为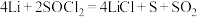 。请回答下列问题:
。请回答下列问题:
①电池的负极材料为_______ ,发生的电极反应为_______ 。
②电池正极发生的电极反应为_______ 。
 、
、 等大气污染气体的处理方法具有重要的意义。
等大气污染气体的处理方法具有重要的意义。已知:①

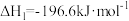
②
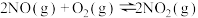
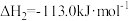
则反应
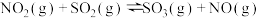 的
的
 。
。(2)t℃时,将2mol
 和1mol
和1mol 通入体积为2L的恒温、恒容密闭容器中,发生如下反应:
通入体积为2L的恒温、恒容密闭容器中,发生如下反应: ,2min时反应达到化学平衡,此时测得容器内的压强为起始压强的0.8倍,请回答:
,2min时反应达到化学平衡,此时测得容器内的压强为起始压强的0.8倍,请回答:①下列叙述能证明该反应已达到化学平衡状态的是
A.容器内压强不再发生变化
B.
 的体积分数不再发生变化
的体积分数不再发生变化C.容器内气体原子总数不再发生变化
D.相同时间内消耗2nmol
 的同时消耗nmol
的同时消耗nmol
E.相同时间内消耗2nmol
 的同时生成nmol
的同时生成nmol
F.混合气体密度不再变化
②从反应开始到达化学平衡,生成
 的平均反应速率为
的平均反应速率为 的转化率为
的转化率为(3)已知
 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是
电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是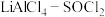 。电池的总反应可表示为
。电池的总反应可表示为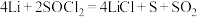 。请回答下列问题:
。请回答下列问题:①电池的负极材料为
②电池正极发生的电极反应为
您最近一年使用:0次
3 . 某温度时,VIA元素单质与H2反应生成气态H2X的热化学方程式如下:
①H2(g)+ O2(g)=H2O(g) ΔH=-242kJ•mol-1
O2(g)=H2O(g) ΔH=-242kJ•mol-1
②H2(g)+S(g)=H2S(g) ΔH=-20kJ•mol-1
③H2(g)+Se(g)⇌H2Se(g) ΔH=+81kJ•mol-1
④H2O(g)=H2O(l) ∆H=-44kJ/mol
请回答:
(1)上述反应中属于放热反应的是_______ (填序号,下同),属于吸热反应的是_______ 。
(2)2gH2完全燃烧生成气态水,放出的热量为_______ 。
(3)请写出O2与H2S反应生成S的热化学方程式_______ 。
(4)根据下图写出热化学方程式_______ 。
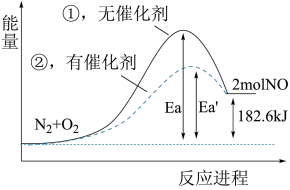
(5)加入催化剂该反应的反应热∆H是否发生了改变_______ (填“是”或“否”)。
(6)请写出H2燃烧热的热化学方程式_______ 。
①H2(g)+
 O2(g)=H2O(g) ΔH=-242kJ•mol-1
O2(g)=H2O(g) ΔH=-242kJ•mol-1②H2(g)+S(g)=H2S(g) ΔH=-20kJ•mol-1
③H2(g)+Se(g)⇌H2Se(g) ΔH=+81kJ•mol-1
④H2O(g)=H2O(l) ∆H=-44kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)2gH2完全燃烧生成气态水,放出的热量为
(3)请写出O2与H2S反应生成S的热化学方程式
(4)根据下图写出热化学方程式

(5)加入催化剂该反应的反应热∆H是否发生了改变
(6)请写出H2燃烧热的热化学方程式
您最近一年使用:0次
4 . 氢气因燃值高、燃烧产物无污染,被公认为清洁能源。
(1)电解饱和食盐水可制取氢气,该反应的化学方程式为___________ 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①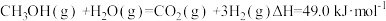
②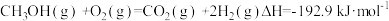
又知:③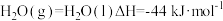
则表示甲醇摩尔燃烧焓的热化学方程式为___________
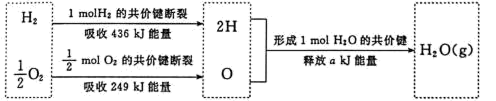
(3)已知1molH2 完全燃烧生成H2O(g) ,放出 245kJ 能量。根据下列信息,计算a____ 。
(4)氢氧燃料电池是符合绿色化学理念的新型发电装置,下图为氢氧燃料电池的示意图。
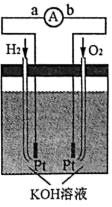
①在导线中电子流动方向为___________ (用 a、b 表示)。
②电极表面镀一层细小的铂粉,其目的是___________ 。
③该电池的负极反应式为H2 2e 2OH 2H2O,请写出正极反应式___________ 。
④假设该电池每发 1 度电(1 度 3.6 106 J )能生成 450g 水蒸气,则该电池的能量转化率为___________ (保留小数点后一位)。
(1)电解饱和食盐水可制取氢气,该反应的化学方程式为
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①
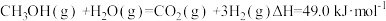
②
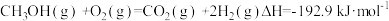
又知:③
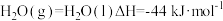
则表示甲醇摩尔燃烧焓的热化学方程式为
(3)已知1molH2 完全燃烧生成H2O(g) ,放出 245kJ 能量。根据下列信息,计算a

(4)氢氧燃料电池是符合绿色化学理念的新型发电装置,下图为氢氧燃料电池的示意图。

①在导线中电子流动方向为
②电极表面镀一层细小的铂粉,其目的是
③该电池的负极反应式为H2 2e 2OH 2H2O,请写出正极反应式
④假设该电池每发 1 度电(1 度 3.6 106 J )能生成 450g 水蒸气,则该电池的能量转化率为
您最近一年使用:0次
名校
5 . 按要求书写下列方程式:
(1)制备粗硅的化学方程式___________ 。
(2)碱性锌锰干电池的正极反应式___________ 。
(3)用氢氧化钠溶液处理NO2尾气的化学方程式___________ 。
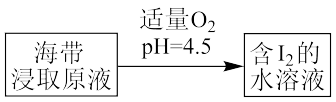
(4)海带提取碘下图所示步骤中反应的离子方程式___________ 。
(5)甲硅烷(SiH4)常温下是无色气体遇空气能自燃,生成二氧化硅和水。已知101kPa 25℃时,测得1g SiH4自燃放出热量44.6kJ/mol。写出其热化学方程式___________ 。
(1)制备粗硅的化学方程式
(2)碱性锌锰干电池的正极反应式
(3)用氢氧化钠溶液处理NO2尾气的化学方程式
(4)海带提取碘下图所示步骤中反应的离子方程式

(5)甲硅烷(SiH4)常温下是无色气体遇空气能自燃,生成二氧化硅和水。已知101kPa 25℃时,测得1g SiH4自燃放出热量44.6kJ/mol。写出其热化学方程式
您最近一年使用:0次
名校
6 . 下列说法正确的是
| A.已知H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ/mol,则1molH2SO4与1molBa(OH)2的反应热ΔH=2×(-57.3)kJ/mol |
| B.已知4P(红磷,s)=P4(白磷,s)ΔH=+17kJ/mol,则白磷比红磷更稳定 |
| C.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
D.一定条件下,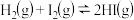 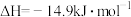 ,则该条件下分解1mol HI吸收的热量为7.45kJ ,则该条件下分解1mol HI吸收的热量为7.45kJ |
您最近一年使用:0次
2021-07-15更新
|
238次组卷
|
2卷引用:黑龙江省鹤岗市第一中学2020-2021学年高一下学期期末考试化学试题
名校
解题方法
7 . 氧化亚铜常用于制船底防污漆。用CuO与Cu高温烧结可制取Cu2O。已知反应:
2Cu(s)+O2(g)=2CuO(s) ΔH=−314kJ·mol−1
2Cu2O(s)+O2(g)=4CuO(s) ΔH=−292kJ·mol−1
则CuO(s)+Cu(s)=Cu2O(s)的ΔH等于
2Cu(s)+O2(g)=2CuO(s) ΔH=−314kJ·mol−1
2Cu2O(s)+O2(g)=4CuO(s) ΔH=−292kJ·mol−1
则CuO(s)+Cu(s)=Cu2O(s)的ΔH等于
| A.−11kJ·mol−1 | B.+11kJ·mol−1 | C.+22kJ·mol−1 | D.−22kJ·mol−1 |
您最近一年使用:0次
2021-07-15更新
|
1380次组卷
|
22卷引用:海南省北京师范大学万宁附中2020-2021学年高一下学期期中考试化学试题
海南省北京师范大学万宁附中2020-2021学年高一下学期期中考试化学试题湖南省长沙市周南中学2020-2021学年高一年级下学期期末考试化学试题安徽省阜阳市第三中学2018-2019学年高一下学期期末考试化学试题安徽省合肥新城高升学校2021-2022学年高二上学期第一次月考化学试题海南省屯昌县屯昌中学2021-2022学年高二上学期10月月考化学试题云南省昭通市镇雄县第四中学2021-2022学年高二上学期第一次月考化学试题山东省济宁市微山县第二中学2021-2022学年高二上学期第一学段考试化学试题北京市第一五九中学2021-2022学年高二上学期期中考试化学试题【区级联考】北京市东城区2018-2019学年高二上学期期末检测化学试题内蒙古通辽市科左后旗甘旗卡第二高级中学2020届高三12月月考化学试题安徽省亳州市第二中学2020届高三上学期第五次月考化学试题海南省海口市灵山中学2020-2021学年高二上学期期中考试化学试题广西钦州市2021-2022学年高二上学期期末考试化学试题浙江省宁波市奉化区2021-2022学年高二上学期期末联考化学试题新疆叶城县第八中学2021-2022学年高二上学期期末考试化学(理)试题 吉林省长春市北师大附属学校2021-2022学年高二上学期期末考试化学试题天津市和平区2022-2023学年高二上学期期末质量调查化学试卷天津市和平区2022-2023学年高二上学期期末质量检测化学试题 吉林省长春市实验中学2022-2023学年高二上学期期末考试化学试题北京汇文中学2022-2023学年高二下学期期中考试化学试题河南省信阳高级中学2023-2024学年高二上学期开学考试化学试题北京市第六十六中学2023-2024学年高二上学期期中质量检测化学试题
名校
解题方法
8 . Ⅰ.我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。
甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式 A:CH3OH* →CH3O* +H* Ea= +103.1kJ·mol-1
方式 B:CH3OH* →CH3* +OH* Eb= +249.3kJ·mol-1
由活化能E值推测,甲醇裂解过程主要历经的方式应为___________ (填A、B)。
下图为计算机模拟的各步反应的能量变化示意图。

该历程中,放热最多的步骤的化学方程式为___________ 。
Ⅱ.TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:

氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行。
已知:TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) ΔH1=+175.4 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-220.9 kJ·mol-1
(1)沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式_____ 。
(2)工业上处理尾气中NO的方法为:将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,其物质转化如图所示。写出图示转化的总反应的化学方程式_____ 。

Ⅲ.甲醇可作为燃料电池的原料。CO2和CO可作为工业合成甲醇(CH3OH)的直接碳源,
(1)已知在常温常压下:①CH3OH(l)+ O2(g)=CO(g) + 2H2O(g); ΔH=﹣355.0 kJ∕mol
②2CO(g)+ O2(g)= 2CO2(g) ΔH=-566.0 kJ/mol ③H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
写出表示甲醇燃烧热的热化学方程式:___________
(2)利用CO和H2在一定条件下可合成甲醇,发生如下反应:CO(g)+2H2(g)=CH3OH(g),其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是___________ 。
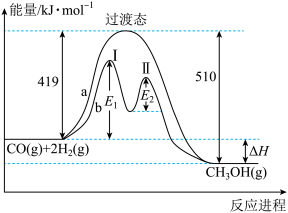
A.上述反应的ΔH=-91kJ·mol-1
B.a反应正反应的活化能为510kJ·mol-1
C.b过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D.b过程使用催化剂后降低了反应的活化能和ΔH
E.b过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式 A:CH3OH* →CH3O* +H* Ea= +103.1kJ·mol-1
方式 B:CH3OH* →CH3* +OH* Eb= +249.3kJ·mol-1
由活化能E值推测,甲醇裂解过程主要历经的方式应为
下图为计算机模拟的各步反应的能量变化示意图。

该历程中,放热最多的步骤的化学方程式为
Ⅱ.TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:

氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行。
已知:TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) ΔH1=+175.4 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-220.9 kJ·mol-1
(1)沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式
(2)工业上处理尾气中NO的方法为:将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,其物质转化如图所示。写出图示转化的总反应的化学方程式

Ⅲ.甲醇可作为燃料电池的原料。CO2和CO可作为工业合成甲醇(CH3OH)的直接碳源,
(1)已知在常温常压下:①CH3OH(l)+ O2(g)=CO(g) + 2H2O(g); ΔH=﹣355.0 kJ∕mol
②2CO(g)+ O2(g)= 2CO2(g) ΔH=-566.0 kJ/mol ③H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
写出表示甲醇燃烧热的热化学方程式:
(2)利用CO和H2在一定条件下可合成甲醇,发生如下反应:CO(g)+2H2(g)=CH3OH(g),其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是

A.上述反应的ΔH=-91kJ·mol-1
B.a反应正反应的活化能为510kJ·mol-1
C.b过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D.b过程使用催化剂后降低了反应的活化能和ΔH
E.b过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
您最近一年使用:0次
2021-07-14更新
|
648次组卷
|
3卷引用:江西省景德镇一中2020-2021学年高一下学期期末考试化学试题
江西省景德镇一中2020-2021学年高一下学期期末考试化学试题湖北省襄阳市第一中学2022-2023学年高一下学期4月月考化学试题(已下线)易错点20 化学反应机理-备战2023年高考化学考试易错题
名校
解题方法
9 . 已知:C(s,石墨)=C(s,金刚石) ΔH=+1.9kJ·mol-1.下列有关说法正确的是
| A.相同条件下,1mol石墨比1mol金刚石能量高 |
| B.断裂1mol石墨中的化学键吸收的能量比断裂1mol金刚石中的化学键吸收的能量少 |
| C.若:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1 则有:C(s,金刚石)+O2(g)=CO2(g) ΔH2=-395.4kJ·mol-1 |
| D.相同条件下,金刚石比石墨稳定 |
您最近一年使用:0次
名校
10 . 2021年6月17日,搭载神舟十二号载人飞船的长征二号F摇十二运载火箭,在酒泉卫星发射中心发射。该运载火箭推进物分为偏二甲基肼(C2H8N2)、四氧化二氮和液氢、液氧两种。
(1)氨热分解法制氢气,相关化学键的键能数据如下表所示:
由以上数据可求得2NH3(g)⇌N2(g)+3H2(g)∆H=_______ 。
(2)在298.15K、100kPa条件下,N2(g)、H2(g)和NH3(g)的摩尔热容分别为29.1、28.9和35.6J·K-1·mol-1(已知:摩尔热容是指单位物质的量的某种物质升高单位温度所需的热量)。N2(g)、H2(g)合成NH3(g)的能量随温度T的变化示意图合理的是_______ 。
A.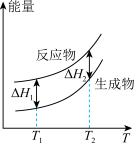 B.
B. 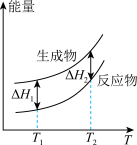 C.
C. 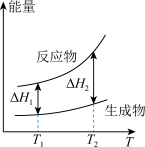 D.
D.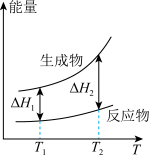
(3)甲烷水蒸气催化重整是制高纯氢的方法之一、反应器中存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH1
ii.CO(g)+H2O(g)=CO2(g)+H2(g)ΔH2
iii.C(s)+2H2O(g)=CO2(g)+2H2(g)ΔH3
iv.CH4(g)=C(s)+2H2(g)ΔH4
ⅳ为积炭反应,利用ΔH1、ΔH2和ΔH3,可计算ΔH4=_______ 。
(4)3.0g液态偏二甲基肼与足量液态四氧化二氮完全反应生成N2(g)、H2O(g)和CO2(g),放出112.5kJ的热量,写出上述反应的热化学方程式_______ 。
(5)对C2H8N2和N2O4反应的说法正确的是_______ 。
A.偏二甲肼是比液氢更环保的燃料
B.N2即是氧化产物,又是还原产物
C.偏二甲基肼的燃烧热为2250kJ/mol
D.偏二甲肼在四氧化二氮中的燃烧是放热反应
(1)氨热分解法制氢气,相关化学键的键能数据如下表所示:
| 化学键 | N≡N | H—H | N—H |
| 键能E(kJ/mol) | 946.0 | 436.0 | 390.8 |
(2)在298.15K、100kPa条件下,N2(g)、H2(g)和NH3(g)的摩尔热容分别为29.1、28.9和35.6J·K-1·mol-1(已知:摩尔热容是指单位物质的量的某种物质升高单位温度所需的热量)。N2(g)、H2(g)合成NH3(g)的能量随温度T的变化示意图合理的是
A.
 B.
B.  C.
C.  D.
D.
(3)甲烷水蒸气催化重整是制高纯氢的方法之一、反应器中存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH1
ii.CO(g)+H2O(g)=CO2(g)+H2(g)ΔH2
iii.C(s)+2H2O(g)=CO2(g)+2H2(g)ΔH3
iv.CH4(g)=C(s)+2H2(g)ΔH4
ⅳ为积炭反应,利用ΔH1、ΔH2和ΔH3,可计算ΔH4=
(4)3.0g液态偏二甲基肼与足量液态四氧化二氮完全反应生成N2(g)、H2O(g)和CO2(g),放出112.5kJ的热量,写出上述反应的热化学方程式
(5)对C2H8N2和N2O4反应的说法正确的是
A.偏二甲肼是比液氢更环保的燃料
B.N2即是氧化产物,又是还原产物
C.偏二甲基肼的燃烧热为2250kJ/mol
D.偏二甲肼在四氧化二氮中的燃烧是放热反应
您最近一年使用:0次



