1 . 下列与化学反应能量变化相关的叙述中,正确的是
| A.热化学方程式的ΔH大小与化学计量数无关 |
| B.利用盖斯定律,可计算某些难以直接测量的反应焓变 |
| C.H2(g)的燃烧热ΔH=-285.8kJ·mol-1,则反应2H2O(g)=2H2(g)+O2(g)的反应热ΔH=+571.6kJ·mol-1 |
| D.测定中和反应反应热的时候,测量盐酸和NaOH混合溶液刚开始的温度,记为反应前体系的温度 |
您最近一年使用:0次
名校
解题方法
2 . (1)①已知:
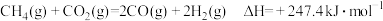
则 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为_______ 。
(2)一定条件下,在水溶液中所含离子 、
、 、
、 、
、 、
、 各
各 ,其相对能量的大小如下图所示(各离子在图中用氯元素的相应化合价表示),则反应
,其相对能量的大小如下图所示(各离子在图中用氯元素的相应化合价表示),则反应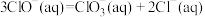 的
的
_______  。
。
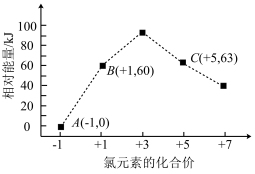
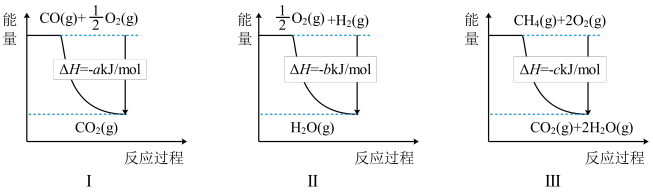
(3)工业上可通过天然气跟水蒸气反应制取 :
: ,有关反应的能量变化如下图所示,则该反应的
,有关反应的能量变化如下图所示,则该反应的
_______  (用含
(用含 、
、 、c的式子表示)。
、c的式子表示)。

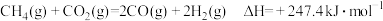
则
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(2)一定条件下,在水溶液中所含离子
 、
、 、
、 、
、 、
、 各
各 ,其相对能量的大小如下图所示(各离子在图中用氯元素的相应化合价表示),则反应
,其相对能量的大小如下图所示(各离子在图中用氯元素的相应化合价表示),则反应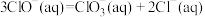 的
的
 。
。
(3)工业上可通过天然气跟水蒸气反应制取
 :
: ,有关反应的能量变化如下图所示,则该反应的
,有关反应的能量变化如下图所示,则该反应的
 (用含
(用含 、
、 、c的式子表示)。
、c的式子表示)。
您最近一年使用:0次
解题方法
3 .  、
、 、
、 等是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。
等是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。
(1)二甲醚( )被誉为“21世纪的清洁燃料”,由
)被誉为“21世纪的清洁燃料”,由 和
和 制备二甲醚的反应原理如下:
制备二甲醚的反应原理如下:


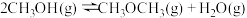
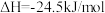
已知: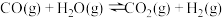
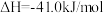
则 的
的
_______ 。
(2)200℃,在2L的密闭容器中充入
 和
和
 ,发生反应
,发生反应 (I);
(I); (II),
(II), 达到平衡,平衡时
达到平衡,平衡时 的转化率为80%,且
的转化率为80%,且 ,则:
,则:
① 内,反应(Ⅰ)平均反应速率
内,反应(Ⅰ)平均反应速率
_______ 。
②反应(Ⅱ)中 的转化率
的转化率
_______ 。
(3)利用电化学原理将 、
、 转化为重要化工原料,装置如图所示:
转化为重要化工原料,装置如图所示:

①若A为 ,B为
,B为 ,C为
,C为 ,则通入
,则通入 一极的电极反应式为
一极的电极反应式为_______ 。
②若A为 ,B为
,B为 ,C为
,C为 ,则负极的电极反应式为
,则负极的电极反应式为_______ 。
 、
、 、
、 等是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。
等是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。(1)二甲醚(
 )被誉为“21世纪的清洁燃料”,由
)被誉为“21世纪的清洁燃料”,由 和
和 制备二甲醚的反应原理如下:
制备二甲醚的反应原理如下:

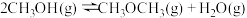
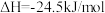
已知:
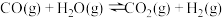
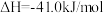
则
 的
的
(2)200℃,在2L的密闭容器中充入

 和
和
 ,发生反应
,发生反应 (I);
(I); (II),
(II), 达到平衡,平衡时
达到平衡,平衡时 的转化率为80%,且
的转化率为80%,且 ,则:
,则:①
 内,反应(Ⅰ)平均反应速率
内,反应(Ⅰ)平均反应速率
②反应(Ⅱ)中
 的转化率
的转化率
(3)利用电化学原理将
 、
、 转化为重要化工原料,装置如图所示:
转化为重要化工原料,装置如图所示:
①若A为
 ,B为
,B为 ,C为
,C为 ,则通入
,则通入 一极的电极反应式为
一极的电极反应式为②若A为
 ,B为
,B为 ,C为
,C为 ,则负极的电极反应式为
,则负极的电极反应式为
您最近一年使用:0次
解题方法
4 . 消除氮氧化物污染对优化环境至关重要。
(1)用 催化还原
催化还原 消除氮氧化物污染的变化如下:
消除氮氧化物污染的变化如下:
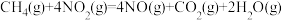
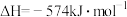

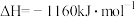
若用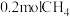 还原
还原 至
至 ,整个过程中放出的热量为
,整个过程中放出的热量为___________ kJ。(假设水全部以气态形成存在)
(2)活性炭(C)可处理大气污染物NO。在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F,当温度分别在 和
和 时,测得各物质平衡时物质的量如下表:
时,测得各物质平衡时物质的量如下表:
①根据上表数据,可推测NO与活性炭反应的化学方程式为___________ 。
②如果已知 ,则该反应正反应的
,则该反应正反应的
___________ 0(填“>”、“<”或“=”)。
③在 温度下反应达到平衡后,下列措施能增大NO的转化率的是
温度下反应达到平衡后,下列措施能增大NO的转化率的是___________ 。
a.降低温度 b.增大压强 c.增大 d.移去部分F
d.移去部分F
(3)汽车尾气处理中的反应有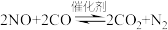 。某温度时,在1L密闭容器中充入0.1mol CO和0.1mol NO,5s时反应达到平衡,测得NO的浓度为0.02mol/L,则反应开始至平衡时,NO的平均反应速率
。某温度时,在1L密闭容器中充入0.1mol CO和0.1mol NO,5s时反应达到平衡,测得NO的浓度为0.02mol/L,则反应开始至平衡时,NO的平均反应速率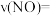
___________ 。此平衡体系中,CO、NO、 、
、 的物质的量比为
的物质的量比为___________ 。
(1)用
 催化还原
催化还原 消除氮氧化物污染的变化如下:
消除氮氧化物污染的变化如下: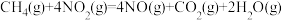
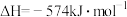

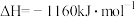
若用
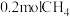 还原
还原 至
至 ,整个过程中放出的热量为
,整个过程中放出的热量为(2)活性炭(C)可处理大气污染物NO。在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F,当温度分别在
 和
和 时,测得各物质平衡时物质的量如下表:
时,测得各物质平衡时物质的量如下表:| 物质 n/mol T/℃ | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.100 | 0 | 0 |
 | 2.000 | 0.040 | 0.030 | 0.030 |
 | 2.005 | 0.050 | 0.025 | 0.025 |
②如果已知
 ,则该反应正反应的
,则该反应正反应的
③在
 温度下反应达到平衡后,下列措施能增大NO的转化率的是
温度下反应达到平衡后,下列措施能增大NO的转化率的是a.降低温度 b.增大压强 c.增大
 d.移去部分F
d.移去部分F(3)汽车尾气处理中的反应有
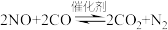 。某温度时,在1L密闭容器中充入0.1mol CO和0.1mol NO,5s时反应达到平衡,测得NO的浓度为0.02mol/L,则反应开始至平衡时,NO的平均反应速率
。某温度时,在1L密闭容器中充入0.1mol CO和0.1mol NO,5s时反应达到平衡,测得NO的浓度为0.02mol/L,则反应开始至平衡时,NO的平均反应速率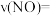
 、
、 的物质的量比为
的物质的量比为
您最近一年使用:0次
5 . I.(1)如图是化学反应中物质变化和能量变化的示意图。
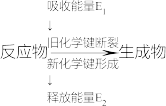
在锌与稀盐酸的反应中,E1______ E2(填“>”或“<”或“=”)
(2)工业上利用 和
和 比在催化剂作用下合成甲醇:
比在催化剂作用下合成甲醇: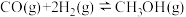 ,已知反应中有关物质的化学键键能数据如下表所示:
,已知反应中有关物质的化学键键能数据如下表所示:
则 生成
生成
 放出
放出______  热量。
热量。
(3)化学兴趣小组进行测定中和热的实验,装置如图,步骤如下。
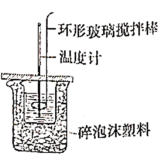
a.用量筒量取
 盐酸倒入如图装置的小烧杯中,测出盐酸温度。
盐酸倒入如图装置的小烧杯中,测出盐酸温度。
b.用另一量筒量取

 溶液,并用另一温度计测出其温度。
溶液,并用另一温度计测出其温度。
c.将 溶液倒入小烧杯中,使之混合均匀,测得混合液最高温度。
溶液倒入小烧杯中,使之混合均匀,测得混合液最高温度。
①实验中,倒入 溶液的正确操作是
溶液的正确操作是_______ 。
A.一次性快速倒入 B.分3次倒入 C.边搅拌边慢慢倒入
②若将各含 溶质的
溶质的 稀溶液、
稀溶液、 稀溶液、稀氨水,分别与足量的稀盐酸反应,放出的热量分别为Q1、Q2、Q3,则Q1、Q2、Q3的关系为
稀溶液、稀氨水,分别与足量的稀盐酸反应,放出的热量分别为Q1、Q2、Q3,则Q1、Q2、Q3的关系为______ 。
II.甲烷燃料电池。已知电池的总反应为 ,
,
①负极的电极反应式为_______ 。
②当消耗甲烷11.2L(标准状况下时),则导线中转移的电子的物质的量为______ mol。

在锌与稀盐酸的反应中,E1
(2)工业上利用
 和
和 比在催化剂作用下合成甲醇:
比在催化剂作用下合成甲醇: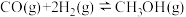 ,已知反应中有关物质的化学键键能数据如下表所示:
,已知反应中有关物质的化学键键能数据如下表所示:| 化学键 |  |  |  |  |  |
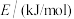 | 436 | 343 | 1076 | 465 | 413 |
则
 生成
生成
 放出
放出 热量。
热量。(3)化学兴趣小组进行测定中和热的实验,装置如图,步骤如下。

a.用量筒量取

 盐酸倒入如图装置的小烧杯中,测出盐酸温度。
盐酸倒入如图装置的小烧杯中,测出盐酸温度。b.用另一量筒量取


 溶液,并用另一温度计测出其温度。
溶液,并用另一温度计测出其温度。c.将
 溶液倒入小烧杯中,使之混合均匀,测得混合液最高温度。
溶液倒入小烧杯中,使之混合均匀,测得混合液最高温度。①实验中,倒入
 溶液的正确操作是
溶液的正确操作是A.一次性快速倒入 B.分3次倒入 C.边搅拌边慢慢倒入
②若将各含
 溶质的
溶质的 稀溶液、
稀溶液、 稀溶液、稀氨水,分别与足量的稀盐酸反应,放出的热量分别为Q1、Q2、Q3,则Q1、Q2、Q3的关系为
稀溶液、稀氨水,分别与足量的稀盐酸反应,放出的热量分别为Q1、Q2、Q3,则Q1、Q2、Q3的关系为II.甲烷燃料电池。已知电池的总反应为
 ,
,①负极的电极反应式为
②当消耗甲烷11.2L(标准状况下时),则导线中转移的电子的物质的量为
您最近一年使用:0次
解题方法
6 . (1)已知0.5mol的液态甲醇(CH3OH)在空气中完全燃烧生成CO2气体和液态水时放出350kJ的热量,则表示甲醇燃烧热的热化学方程式为___________ 。
(2)已知:①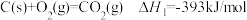
②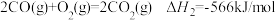
③
则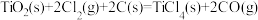 的
的
___________ 。
(3)燃料电池是一种具有应用前景的绿色电源。下图为燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:
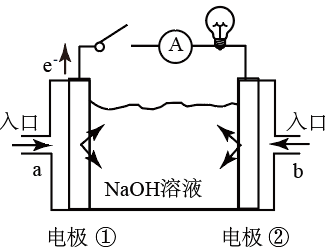
若该燃料电池为氢氧燃料电池。
①a极通入的物质为___________ (填物质名称),电解质溶液中的 移向
移向___________ 极(填“负”或“正”)。
②写出此氢氧燃料电池工作时,负极的电极反应式:___________ 。
若该燃料电池为甲烷燃料电池。已知电池的总反应为:
③下列有关说法正确的是___________ (填字母代号)。
A.燃料电池将电能转变为化学能
B.负极的电极反应式为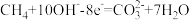
C.正极的电极反应式为
D.通入甲烷的电极发生还原反应
(2)已知:①
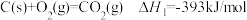
②
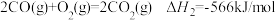
③

则
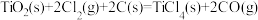 的
的
(3)燃料电池是一种具有应用前景的绿色电源。下图为燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:

若该燃料电池为氢氧燃料电池。
①a极通入的物质为
 移向
移向②写出此氢氧燃料电池工作时,负极的电极反应式:
若该燃料电池为甲烷燃料电池。已知电池的总反应为:

③下列有关说法正确的是
A.燃料电池将电能转变为化学能
B.负极的电极反应式为
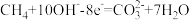
C.正极的电极反应式为

D.通入甲烷的电极发生还原反应
您最近一年使用:0次
7 . 氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示:
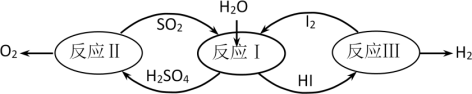
(1)反应Ⅰ的化学方程式是___ 。
(2)反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550kJ•mol-1。该反应自发进行的条件是__ (填“高温”、“低温”或“任意温度”),理由是__ 。
反应Ⅱ由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g) △H=+177kJ•mol-1
ii.SO3(g)分解。则SO3(g)分解的热化学方程式为___ 。
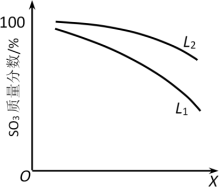
(3)L(L1、L2)、X可分别代表压强或温度。如图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。
①X代表的物理量是___ 。
②判断L1、L2的大小关系,L1___ L2,并简述理由:___ 。
(4)煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H1=218.4kJ•mol-1(反应Ⅰ)
CaO(s)+SO2(g)+CO2(g) △H1=218.4kJ•mol-1(反应Ⅰ)
CaSO4(s)+4CO(g) CaS(s)+4CO2(g) △H2=-175.6kJ•mol-1(反应Ⅱ)
CaS(s)+4CO2(g) △H2=-175.6kJ•mol-1(反应Ⅱ)
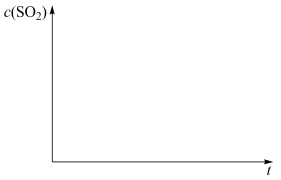
恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且v1>v2,请画出反应体系中c(SO2)随时间 变化的总趋势图
变化的总趋势图___ 。
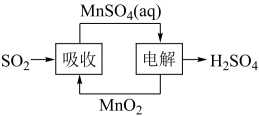
(5)工业生产中产生的SO2废气也可用如图方法获得H2SO4。写出电解的阳极反应式___ 。

(1)反应Ⅰ的化学方程式是
(2)反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550kJ•mol-1。该反应自发进行的条件是
反应Ⅱ由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g) △H=+177kJ•mol-1
ii.SO3(g)分解。则SO3(g)分解的热化学方程式为
(3)L(L1、L2)、X可分别代表压强或温度。如图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。
①X代表的物理量是
②判断L1、L2的大小关系,L1

(4)煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g) △H1=218.4kJ•mol-1(反应Ⅰ)
CaO(s)+SO2(g)+CO2(g) △H1=218.4kJ•mol-1(反应Ⅰ)CaSO4(s)+4CO(g)
 CaS(s)+4CO2(g) △H2=-175.6kJ•mol-1(反应Ⅱ)
CaS(s)+4CO2(g) △H2=-175.6kJ•mol-1(反应Ⅱ)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且v1>v2,请画出反应体系中c(SO2)随时间
 变化的总趋势图
变化的总趋势图
(5)工业生产中产生的SO2废气也可用如图方法获得H2SO4。写出电解的阳极反应式

您最近一年使用:0次
名校
8 . 已知:①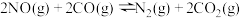

②

③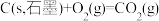

④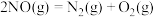

下列关系正确的是
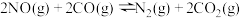

②


③
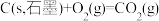

④
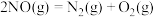

下列关系正确的是
A. |
B. |
C.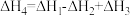 |
D.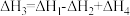 |
您最近一年使用:0次
2021-06-25更新
|
628次组卷
|
4卷引用:四川省成都市蓉城名校联盟2020-2021学年高一下学期期末联考化学试题
四川省成都市蓉城名校联盟2020-2021学年高一下学期期末联考化学试题西藏自治区拉萨中学2020-2021学年高一下学期期末考试化学试题(已下线)第一章 第三节 化学反应热的计算(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)第03讲 盖斯定律(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
9 . 在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
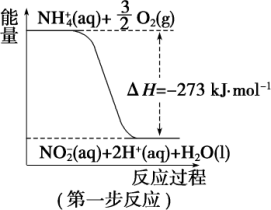
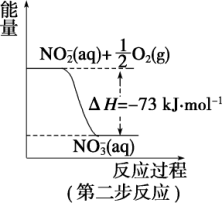
(1)第一步反应是_______ (填“放热”或“吸热”)反应,判断依据是_______ 。
(2)1 molNH (aq) 全部氧化成NO
(aq) 全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
(3) HCl与氧气在催化剂加热条件下可生成氯气:4HCl+O2 2Cl2+2H2O,已知某些化学键的键能数据如表:
2Cl2+2H2O,已知某些化学键的键能数据如表:
该反应的热化学方程式是_______ 。
(4)FeCl3溶液常用于腐蚀印刷电路铜板,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则正极所用的电极材料为_______ ;电解质溶液为_______ ,当电路中转移0.2 mol 电子时,被腐蚀的负极反应物的质量为_______ g。
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:

(1)第一步反应是
(2)1 molNH
 (aq) 全部氧化成NO
(aq) 全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(3) HCl与氧气在催化剂加热条件下可生成氯气:4HCl+O2
 2Cl2+2H2O,已知某些化学键的键能数据如表:
2Cl2+2H2O,已知某些化学键的键能数据如表:| 化学键 | H-Cl | O=O | Cl-Cl | H-O |
| 键能/kJ/mol | 431 | 498 | 243 | 463 |
该反应的热化学方程式是
(4)FeCl3溶液常用于腐蚀印刷电路铜板,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则正极所用的电极材料为
您最近一年使用:0次
名校
解题方法
10 . 研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
①CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是____________ 。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
①CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
②2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO还原NO2至N2(CO完全反应),整个过程中转移电子的物质的量为___ mol,放出的热量为_______ kJ(用含有a和b的代数式表示)。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1①
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若1 mol CH4还原NO2至N2,整个过程中放出的热量为867kJ,则ΔH2=__________ 。
(4)已知:N2、O2分子中化学键的键能分别是946kJ·mol−1、497kJ·mol−1。N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol−1。NO分子中化学键的键能为______ 。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
①CO(g)+
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
①CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
②2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO还原NO2至N2(CO完全反应),整个过程中转移电子的物质的量为
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1①
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若1 mol CH4还原NO2至N2,整个过程中放出的热量为867kJ,则ΔH2=
(4)已知:N2、O2分子中化学键的键能分别是946kJ·mol−1、497kJ·mol−1。N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol−1。NO分子中化学键的键能为
您最近一年使用:0次
2021-06-24更新
|
357次组卷
|
2卷引用:甘肃省静宁县第一中学2020-2021学年高一下学期第三次月考化学(普通班)试题



