解题方法
1 . 关于2A(g)+B(g) 3C(g)的化学反应,下列表示的反应速率最快的是
3C(g)的化学反应,下列表示的反应速率最快的是
 3C(g)的化学反应,下列表示的反应速率最快的是
3C(g)的化学反应,下列表示的反应速率最快的是| A.v(A)=0.5 mol/(L·min) | B.v(B)=0.4 mol/(L·min) |
| C.v(C)=0.01 mol/(L·s) | D.v(C)=1.1mol/(L·min) |
您最近一年使用:0次
解题方法
2 . 室温下,某溶液初始时仅 A,同时发生两个反应:①A B+C;②A
B+C;②A B+D,反应①的速率可表示为v1=k1c(A),反应②的速率可表示为v2=k2c(A), (k1、k2为速率常数),图1为T2时,该体系中A、B、C、D的浓度随时间变化的曲线,图2为反应①和②的lnk—
B+D,反应①的速率可表示为v1=k1c(A),反应②的速率可表示为v2=k2c(A), (k1、k2为速率常数),图1为T2时,该体系中A、B、C、D的浓度随时间变化的曲线,图2为反应①和②的lnk— 曲线,下列说法正确的是
曲线,下列说法正确的是
 B+C;②A
B+C;②A B+D,反应①的速率可表示为v1=k1c(A),反应②的速率可表示为v2=k2c(A), (k1、k2为速率常数),图1为T2时,该体系中A、B、C、D的浓度随时间变化的曲线,图2为反应①和②的lnk—
B+D,反应①的速率可表示为v1=k1c(A),反应②的速率可表示为v2=k2c(A), (k1、k2为速率常数),图1为T2时,该体系中A、B、C、D的浓度随时间变化的曲线,图2为反应①和②的lnk— 曲线,下列说法正确的是
曲线,下列说法正确的是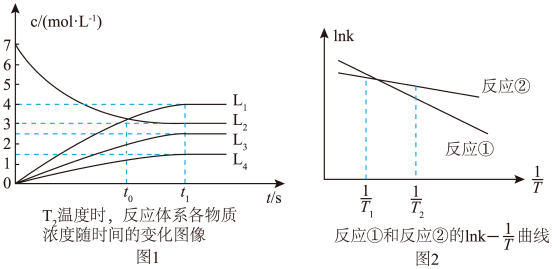
| A.L4表示B浓度随时间变化曲线 |
| B.t1≈2s时曲线L1表示的物质的化学反应速率为2 mol/(L·s) |
| C.T2温度时,反应①的活化能比反应②的活化能大 |
D.若图Ⅰ的温度降低,t0时刻体系中 值变小 值变小 |
您最近一年使用:0次
解题方法
3 . 将 和
和 充入
充入 恒容密闭容器中发生反应:
恒容密闭容器中发生反应:
Ⅰ.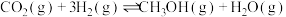
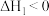 (慢反应)
(慢反应)
Ⅱ.
 (快反应)
(快反应)
测得相同时间内 、
、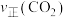 与温度的关系如图所示,下列说法错误的是
与温度的关系如图所示,下列说法错误的是
 和
和 充入
充入 恒容密闭容器中发生反应:
恒容密闭容器中发生反应:Ⅰ.
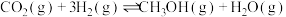
 (慢反应)
(慢反应)Ⅱ.

 (快反应)
(快反应)测得相同时间内
 、
、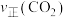 与温度的关系如图所示,下列说法错误的是
与温度的关系如图所示,下列说法错误的是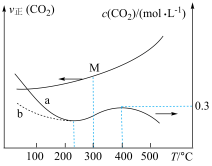
A.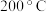 前,加入催化剂可使a线转化为b线 前,加入催化剂可使a线转化为b线 |
B. 时,M点对应的反应体系中, 时,M点对应的反应体系中, |
C. 时,若 时,若 时达到平衡,则 时达到平衡,则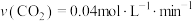 |
D. 后,温度对正反应速率的影响比浓度大 后,温度对正反应速率的影响比浓度大 |
您最近一年使用:0次
4 . 能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。请回答下列问题。
Ⅰ.工业合成氨反应N2(g)+3H2(g) 2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。
2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。
(1)已知1molN2(g)完全反应生成NH3(g)可放出92kJ热量。如果将10molN2(g)和足量H2(g)混合,使其充分反应,放出的热量___________ (填“大于”小于或“等于”)920kJ。
(2)工业合成氨选择高温(400-500℃)、高压(10MPa~30MPa)和催化剂的原因是___________ 。
Ⅱ.实验室模拟工业合成氨时,在容积为2L的密闭容器内,开始时加入3molN2(g)和6molH2(g),在10min末,测得NH3(g)的物质的量是2mol。
(3)用N2表示的化学反应速率为___________ mol/(L·min)。
(4)在10min末,H2(g)的转化率为___________ 。
(5)保持容器体积不变,充入惰性气体Ar,化学反应速率___________ (填“增大“减小”或“不变”)。
(6)一定条件下,能说明该反应进行到最大限度的是_______ (填字母)。
a.正、逆反应速率都为零
b.单位时间内消耗3amnolH2(g),同时生成2amolNH3(g)
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
Ⅰ.工业合成氨反应N2(g)+3H2(g)
 2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。
2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。(1)已知1molN2(g)完全反应生成NH3(g)可放出92kJ热量。如果将10molN2(g)和足量H2(g)混合,使其充分反应,放出的热量
(2)工业合成氨选择高温(400-500℃)、高压(10MPa~30MPa)和催化剂的原因是
Ⅱ.实验室模拟工业合成氨时,在容积为2L的密闭容器内,开始时加入3molN2(g)和6molH2(g),在10min末,测得NH3(g)的物质的量是2mol。
(3)用N2表示的化学反应速率为
(4)在10min末,H2(g)的转化率为
(5)保持容器体积不变,充入惰性气体Ar,化学反应速率
(6)一定条件下,能说明该反应进行到最大限度的是
a.正、逆反应速率都为零
b.单位时间内消耗3amnolH2(g),同时生成2amolNH3(g)
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
您最近一年使用:0次
名校
解题方法
5 . 甲烷是重要的燃料和化工原料,一种利用CO2制备CH4的反应为CO2(g)+4H2(g) CH4(g)+2H2O(g)。T℃下,在2L的恒容密闭容器中通入2molCO2和2molH2,发生上述反应,容器内两种气体的物质的量随时间变化的关系如图所示。回答下列问题:
CH4(g)+2H2O(g)。T℃下,在2L的恒容密闭容器中通入2molCO2和2molH2,发生上述反应,容器内两种气体的物质的量随时间变化的关系如图所示。回答下列问题:___________ ;5~10min内,用H2O(g)表示的平均反应速率v(H2O)=___________ mol/(L·min);下列措施能加快上述反应的正反应速率的是___________ (填标号)。
A.升高温度 B.通入He C.通入CO2 D.分离出CH4
(2)下列情况能说明上述反应已达到平衡状态的是___________ (填标号);反应达到平衡时,H2的转化率为___________ ,平衡时的压强与初始压强的比值为___________ (填最简整数比)。
a.混合气体的密度不再改变
b.n(CO2)∶n(H2)的值不再改变
c.CO2、H2、CH4、H2O同时存在
d.c(CH4):c(H2O)的值不再改变
e.消耗22gCO2的同时生成18gH2O
f.断裂1个H-H键的同时断裂1个C-H键
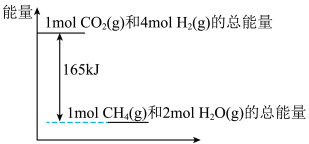
(3)T℃时,上述反应中相关物质的能量如图所示,若该条件下,反应放出33kJ能量,则共消耗___________ L(换算成标准状况下)H2,生成___________ gCH4。
 CH4(g)+2H2O(g)。T℃下,在2L的恒容密闭容器中通入2molCO2和2molH2,发生上述反应,容器内两种气体的物质的量随时间变化的关系如图所示。回答下列问题:
CH4(g)+2H2O(g)。T℃下,在2L的恒容密闭容器中通入2molCO2和2molH2,发生上述反应,容器内两种气体的物质的量随时间变化的关系如图所示。回答下列问题: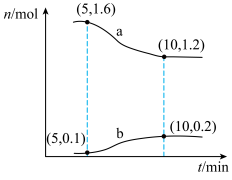
A.升高温度 B.通入He C.通入CO2 D.分离出CH4
(2)下列情况能说明上述反应已达到平衡状态的是
a.混合气体的密度不再改变
b.n(CO2)∶n(H2)的值不再改变
c.CO2、H2、CH4、H2O同时存在
d.c(CH4):c(H2O)的值不再改变
e.消耗22gCO2的同时生成18gH2O
f.断裂1个H-H键的同时断裂1个C-H键
(3)T℃时,上述反应中相关物质的能量如图所示,若该条件下,反应放出33kJ能量,则共消耗
您最近一年使用:0次
名校
6 . T℃时,某化学兴趣小组将1.0mL0.015mol/LKMnO4和1.5mol/LH2SO4的混合溶液与1.0mL0.15mol/L乙醛(CH3CHO)溶液混合后,得到c( )随时间变化的关系如图,已知反应原理为
)随时间变化的关系如图,已知反应原理为 +CH3CHO+H+→Mn2++CH3COOH+H2O(未配平)。下列说法正确的是
+CH3CHO+H+→Mn2++CH3COOH+H2O(未配平)。下列说法正确的是
 )随时间变化的关系如图,已知反应原理为
)随时间变化的关系如图,已知反应原理为 +CH3CHO+H+→Mn2++CH3COOH+H2O(未配平)。下列说法正确的是
+CH3CHO+H+→Mn2++CH3COOH+H2O(未配平)。下列说法正确的是
| A.可用浓盐酸和KMnO4配制成酸性KMnO4溶液 |
B.30.0~50.0s内, 的平均速率为0.54mol/(L·h) 的平均速率为0.54mol/(L·h) |
| C.0~30s的平均反应速率大于30~50s的原因是0~30s内生成物的浓度更小 |
D.该实验中反应的离子方程式为2 +5CH3CHO+6H+=2Mn2++5CH3COOH+3H2O +5CH3CHO+6H+=2Mn2++5CH3COOH+3H2O |
您最近一年使用:0次
7 . 常温下,往烧杯中加入10mL1mol/LFeCl3溶液和10mL2mol/LKI溶液,c(I-)随时间变化如图所示,不考虑溶液混合时体积的改变。下列说法正确的是
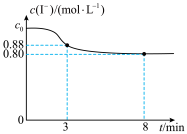
| A.c0=2 |
| B.3~8min内,Fe3+的平均反应速率为0.08mol/(L·min) |
| C.8min时,往烧杯中滴加KSCN溶液,溶液不变红 |
D.烧杯中发生反应的离子方程式为2Fe3++2I- 2Fe2++I2 2Fe2++I2 |
您最近一年使用:0次
解题方法
8 . 已知反应4CO(g)+2NO2(g)  N2(g)+4CO2(g)在不同条件下的化学反应速率如下,表示反应最快的是
N2(g)+4CO2(g)在不同条件下的化学反应速率如下,表示反应最快的是
 N2(g)+4CO2(g)在不同条件下的化学反应速率如下,表示反应最快的是
N2(g)+4CO2(g)在不同条件下的化学反应速率如下,表示反应最快的是| A.v(CO)=1.5mol/(L·min) | B.v(NO2)=0.01mol/(L·s) |
| C.v(CO2)=1.1mol/(L·min) | D.v(N2)=0.4mol/(L·min) |
您最近一年使用:0次
9 . 一定温度下,在容积为VL的密闭容器中进行反应,M、N两种气体的物质的量随时间的变化曲线如图所示:___________ ;
(2)t 1到t 2时刻,以M的浓度变化表示的平均反应速率为:___________ ;(用符号表示)
(3)若达到平衡状态的时间是4 min,N物质在该4 min内的平均反应速率为1.5mol⋅L−1⋅min−1,则此容器的容积为V=___________ L。

(2)t 1到t 2时刻,以M的浓度变化表示的平均反应速率为:
(3)若达到平衡状态的时间是4 min,N物质在该4 min内的平均反应速率为1.5mol⋅L−1⋅min−1,则此容器的容积为V=
您最近一年使用:0次
解题方法
10 . 回答下列问题:
(1)一定温度下,向1 L恒容密闭容器中加入1 mol HI(g),发生反应2HI(g) H2(g)+I2(g),H2的物质的量随时间的变化如图所示。
H2(g)+I2(g),H2的物质的量随时间的变化如图所示。___________ 。
②该温度下,H2(g)+I2(g) ⇌2HI(g)的平衡常数K=___________ 。
(2)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡___________ 移动(填“向左”、“向右”或“不”);若加入少量下列试剂中的___________ (填字母序号),产生H2的速率将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(3)以H2为燃料,KOH溶液为电解质溶液可制得氢氧燃料电池。该电池负极反应式为___________ 。已知2H2(g)+O2(g)=2H2O(l) ΔH=-572 kJ·mol-1.若该氢氧燃料电池释放228.8 kJ电能时,生成1 mol液态水,则该电池的能量转化率为___________ 。
(1)一定温度下,向1 L恒容密闭容器中加入1 mol HI(g),发生反应2HI(g)
 H2(g)+I2(g),H2的物质的量随时间的变化如图所示。
H2(g)+I2(g),H2的物质的量随时间的变化如图所示。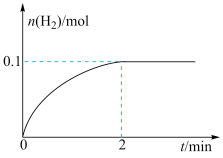
②该温度下,H2(g)+I2(g) ⇌2HI(g)的平衡常数K=
(2)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(3)以H2为燃料,KOH溶液为电解质溶液可制得氢氧燃料电池。该电池负极反应式为
您最近一年使用:0次



