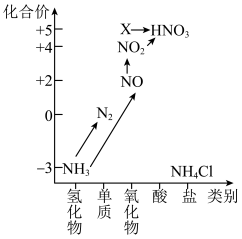
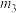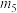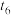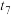1 . 依据图中氮元素及其化合物的转化关系,回答下列问题:______ 。
(2)回答下列关于 的问题:
的问题:
①利用下列方法制氨气,其中合理的是______ (填字母)。
A.将浓氨水滴入氢氧化钠固体中
B.将氯化铵稀溶液滴入氧化钙固体中
C.将氯化铵固体加热分解
D.加热浓氨水
E.将浓氨水滴入碱石灰固体中
②氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:______ 。
③ 、
、 合成
合成 的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是
的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是______ 。
A. B.
B.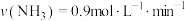
C.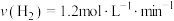 D.
D.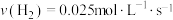
(3)下列关于NO、 的问题:
的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体C0和NO反应可转化为无害气体排放,写出相关反应的化学方程式:______ 。
②NO和 按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:______ 。
(2)回答下列关于
 的问题:
的问题:①利用下列方法制氨气,其中合理的是
A.将浓氨水滴入氢氧化钠固体中
B.将氯化铵稀溶液滴入氧化钙固体中
C.将氯化铵固体加热分解
D.加热浓氨水
E.将浓氨水滴入碱石灰固体中
②氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:
③
 、
、 合成
合成 的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是
的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是A.
 B.
B.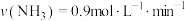
C.
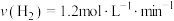 D.
D.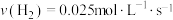
(3)下列关于NO、
 的问题:
的问题:①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体C0和NO反应可转化为无害气体排放,写出相关反应的化学方程式:
②NO和
 按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
您最近一年使用:0次
解题方法
2 . Ⅰ.控制变量法是化学实验的一种常用方法。下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
(1)化学反应速率本质上是由反应物本身的性质决定的,但外界条件也会影响反应速率的大小。本实验中实验2和实验3表明______ 对反应速率有影响。
(2)我们最好选取实验______ (填3个实验序号)研究锌的形状对反应速率的影响。我们发现在其它条件相同时,反应物间的______ 反应速率越快。
(3)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快。原因是______ 。
Ⅱ.某温度时,在5L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:______ 。
(5)分析有关数据,写出X、Y、Z的反应方程式______ 。
序号 | 硫酸的体积/mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
1 | 50.0 | 2.0 | 薄片 | 25 | 100 |
|
2 | 50.0 | 2.0 | 颗粒 | 25 | 70 |
|
3 | 50.0 | 2.0 | 颗粒 | 35 | 35 |
|
4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
5 | 50.0 | 6.0 | 粉末 | 35 | 30 |
|
6 | 50.0 | 8.0 | 粉末 | 25 |
| 16.1 |
7 | 50.0 | 10.0 | 粉末 | 25 |
| 16.1 |
(1)化学反应速率本质上是由反应物本身的性质决定的,但外界条件也会影响反应速率的大小。本实验中实验2和实验3表明
(2)我们最好选取实验
(3)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快。原因是
Ⅱ.某温度时,在5L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:
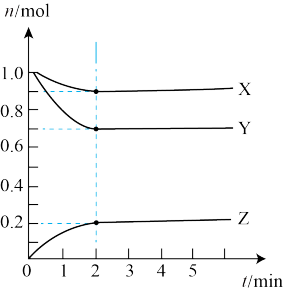
(5)分析有关数据,写出X、Y、Z的反应方程式
您最近一年使用:0次
3 . 在2L密闭容器中进行的反应 ,在10秒内反应物
,在10秒内反应物 的物质的量由1mol降到0.6mol,则反应速率
的物质的量由1mol降到0.6mol,则反应速率 )为
)为
 ,在10秒内反应物
,在10秒内反应物 的物质的量由1mol降到0.6mol,则反应速率
的物质的量由1mol降到0.6mol,则反应速率 )为
)为A.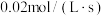 | B. | C.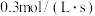 | D. |
您最近一年使用:0次
解题方法
4 . 回答下列问题:
(1)一定温度下,反应 在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”“减小”或“不变”)
在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”“减小”或“不变”)
①缩小体积使压强增大:________ ;②恒容充入 :
:________ ;③恒压充入He:________ 。
(2)在恒温恒容条件下,可逆反应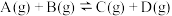 。判断该反应是否达到平衡的依据为
。判断该反应是否达到平衡的依据为________ (填正确选项前的字母)。
a.压强不随时间改变 b.气体的密度不随时间改变
c.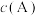 不随时间改变 d.单位时间里生成C和D的物质的量相等
不随时间改变 d.单位时间里生成C和D的物质的量相等
(3)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
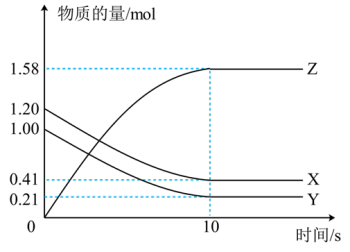
①从反应开始到10s时,用Z表示的反应速率为________ ,X的物质的量浓度减少了________ ,Y的转化率为________ 。
②该反应的化学方程式为________ 。
(1)一定温度下,反应
 在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”“减小”或“不变”)
在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”“减小”或“不变”)①缩小体积使压强增大:
 :
:(2)在恒温恒容条件下,可逆反应
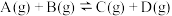 。判断该反应是否达到平衡的依据为
。判断该反应是否达到平衡的依据为a.压强不随时间改变 b.气体的密度不随时间改变
c.
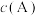 不随时间改变 d.单位时间里生成C和D的物质的量相等
不随时间改变 d.单位时间里生成C和D的物质的量相等(3)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:

①从反应开始到10s时,用Z表示的反应速率为
②该反应的化学方程式为
您最近一年使用:0次
解题方法
5 . 无论是在环境保护领域还是在工农业生产领域,氮及其化合物一直是我国科研重点。回答下列问题:
(1)下列过程属于氮的固定过程的是_______(填选项字母)。
(2)消除汽车尾气中的氮氧化合物的原理之一为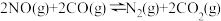 。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
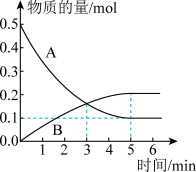
①其中B表示_______ (填“ ”或“
”或“ ”)物质的量的变化曲线。
”)物质的量的变化曲线。
②该温度下,反应开始至5min时该反应的平均反应速率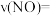
_______ 。
③3min时,反应_______ (填“达到”或“未达到”)化学平衡,6min时,正反应速率_______ (填“>”“<”或“=”)逆反应速率。
④下列情况能说明该反应达到平衡状态的是_______ (填选项字母)。
A.化学反应速率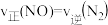
B.CO与 的物质的量之和不再发生变化
的物质的量之和不再发生变化
C.容器内气体压强不再发生变化
D.容器内混合气体密度不再发生变化
(3)实验室用NaOH溶液对氮氧化合物进行尾气吸收,例如NaOH溶液可将 转化为
转化为 和
和 。该吸收过程中发生反应的离子方程式为
。该吸收过程中发生反应的离子方程式为_______ 。
(4)某固体氧化物为电解质的新型燃料电池是以液态肼(N2H4)为燃料,氧气为氧化剂构成,其原理示意图如图所示。
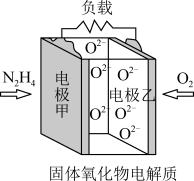
该电池的正极为_______ (填“电极甲”或“电极乙”,下同);电池工作时, 向
向_______ 移动。
(1)下列过程属于氮的固定过程的是_______(填选项字母)。
| A.工业合成氨 |
| B.工业利用氨气合成硝酸 |
| C.雷雨天中氮气与氧气生成氮氧化合物 |
| D.通过碱性试剂将气态的氮氧化合物转化为固态含氮化合物 |
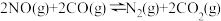 。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
①其中B表示
 ”或“
”或“ ”)物质的量的变化曲线。
”)物质的量的变化曲线。②该温度下,反应开始至5min时该反应的平均反应速率
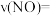
③3min时,反应
④下列情况能说明该反应达到平衡状态的是
A.化学反应速率
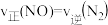
B.CO与
 的物质的量之和不再发生变化
的物质的量之和不再发生变化C.容器内气体压强不再发生变化
D.容器内混合气体密度不再发生变化
(3)实验室用NaOH溶液对氮氧化合物进行尾气吸收,例如NaOH溶液可将
 转化为
转化为 和
和 。该吸收过程中发生反应的离子方程式为
。该吸收过程中发生反应的离子方程式为(4)某固体氧化物为电解质的新型燃料电池是以液态肼(N2H4)为燃料,氧气为氧化剂构成,其原理示意图如图所示。

该电池的正极为
 向
向
您最近一年使用:0次
解题方法
6 . 下列做法不属于调控化学反应速率的是
| A.将食物储存在冰箱中 | B.在钢铁护栏表面刷油漆 |
C.向过氧化氢溶液中加入 | D.用浓硝酸与Cu反应制 |
您最近一年使用:0次
7 . 在相同条件下研究催化剂I、Ⅱ对反应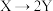 的影响,各物质浓度c随反应时间t的部分变化曲线如图,则
的影响,各物质浓度c随反应时间t的部分变化曲线如图,则
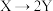 的影响,各物质浓度c随反应时间t的部分变化曲线如图,则
的影响,各物质浓度c随反应时间t的部分变化曲线如图,则
| A.无催化剂时,反应不能进行 |
| B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低 |
| C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化 |
D.使用催化剂Ⅰ时, 内, 内,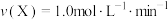 |
您最近一年使用:0次
2022-06-10更新
|
14245次组卷
|
61卷引用:广东省乐昌市第二中学2023-2024学年高三下学期保温测试(5月模拟)化学试题
广东省乐昌市第二中学2023-2024学年高三下学期保温测试(5月模拟)化学试题2022年新高考广东化学高考真题(已下线)2022年广东卷高考真题变式题(11-16)(已下线)专题09 化学反应速率、化学平衡-2022年高考真题模拟题分项汇编(已下线)专题09 化学反应速率、化学平衡-三年(2020-2022)高考真题分项汇编(已下线)第11练 以化学平衡图像突破化学平衡移动原理-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)考点21 化学反应速率-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第26练 化学反应速率-2023年高考化学一轮复习小题多维练(全国通用)(已下线)专题13 化学反应速率与化学平衡-备战2023年高考化学母题题源解密(广东卷)(已下线)第20讲 化学反应速率(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第18讲 化学反应速率(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第二章 化学反应速率与化学平衡(A卷·知识通关练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)上海市复旦大学附属中学2022-2023学年高二上学期9月月考化学试题湖南省长沙市雅礼中学2022-2023学年高二上学期第一次月考化学试题江苏省扬州中学2022-2023学年高二上学期10月月考化学试题山东省莱州一中2022-2023学年高二上学期第一次月考化学试题福建省厦门集美中学2022-2023学年高三上学期10月月考化学试题(已下线)易错点21 化学反应速率-备战2023年高考化学考试易错题湖北省沙市中学2022-2023学年高二上学期第二次月考化学试题河南省洛阳市新安县第一高级中学2022-2023学年高三上学期9月阶段性考试化学试题宁夏银川市第二中学2022-2023学年高三上学期统练三化学试题吉林省延边第二中学2022-2023学年高三上学期第三次阶段测试化学试题广东省高州市第七中学等三校2022-2023学年高二上学期11月月考化学试题福建省厦门外国语学校石狮分校2022-2023学年高二上学期期中考试化学试题(已下线)【2022】【高二上】【期中考】【高中化学】59(已下线)专题09 化学反应速率与化学平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题17 化学平衡图表分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型114 影响化学反应速率的因素(已下线)【2022】【高二化学】【期中考】-178(已下线)回归教材重难点08 聚焦热、速率、平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)专题15 化学反应速率和化学平衡(已下线)专题15 化学反应速率和化学平衡(已下线)第13练 化学反应速率与化学平衡的综合考查 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)天津市红桥区2022-2023学年高三上学期期末考试化学试题广东省信宜市第二中学2022-2023学年高二上学期期中考试化学试题章末检测卷(二) 化学反应速率与化学平衡四川省成都市树德中学2022-2023学年高一下学期期末考试化学试题(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)安徽省滁州市实验中学等2校2022-2023学年高二上学期1月期末考试化学试题第二章 化学反应速率与化学平衡 第一节 化学反应速率 第2课时 影响化学反应速率的因素 活化能河南省开封市祥符高级中学2023-2024学年高二上学期第一次月考化学试题(已下线)实验02 定性与定量研究影响化学反应速率的因素-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)(已下线)考点1 化学反应速率(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省肇庆市封开县广信中学、四会中学2023-2024学年高二上学期第一次联考化学试题广东省珠海市2023-2024年高二上学期期中联考化学试题安徽省马鞍山市第二中学2022-2023学年高二上学期11月期中考试化学试题河南省实验中学2023-2024学年高二上学期期中考试化学试题江苏省苏州实验中学科技城校2023-2024学年高二上学期10月月考化学试题广东省佛山市顺德区郑裕彤中学2023-2024学年上学期高一10月月考化学试题安徽省当涂第一中学2023-2024学年高二上学期10月月考化学试题福建省泉州市晋江市南侨中学2023-2024学年高二上学期11月期中考试化学试题北京市第二十二中学2022-2023学年高二上学期期中考试化学试题广东省广州市第四十一中学2023-2024学年高二上学期期中考试化学试题(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)天津市和平区2023-2024学年高二上学期期末考试化学试卷广东省台山市某校2023-2024学年高二上学期期中考试化学试题山西省运城市河津中学2023-2024学年高二下学期开学考试化学试题北京市第五十五中学2022-2023学年高三上学期期中考试化学试题
名校
解题方法
8 . 下列装置或操作能达到实验目的是
| A | B | C | D |
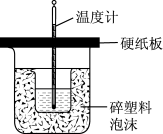 | 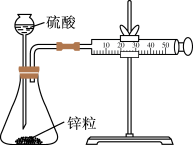 | 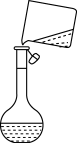 | 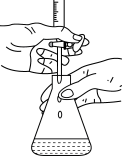 |
| 中和热测定 | 测定 生成速率 生成速率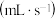 | 定容 | 高锰酸钾滴定草酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-09更新
|
183次组卷
|
2卷引用:广东省韶关市武江区广东北江实验中学2021-2022学年高三下学期适应性考试(四)化学试题
名校
解题方法
9 . 汽车尾气是否为导致空气质量问题的主要原因,由此引发的“汽车限行”争议,是当前备受关注的社会性科学议题。
(1)反应
 可有效降低汽车尾气污染物的排放。一定条件下该反应经历三个基元反应阶段,反应历程如下图所示(TS表示过渡态、IM表示中间产物)。三个基元反应中,属于放热反应的是
可有效降低汽车尾气污染物的排放。一定条件下该反应经历三个基元反应阶段,反应历程如下图所示(TS表示过渡态、IM表示中间产物)。三个基元反应中,属于放热反应的是___________ (填标号①、②或③)图中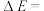
___________  。
。

(2)探究温度、压强(2MPa、5MPa)对反应 的影响,如下图所示,表示2MPa的是反应
的影响,如下图所示,表示2MPa的是反应___________ (填标号a、b、c、或d)。

(3)在一定温度下向容积为2L的密闭容器中加入0.5molNO、0.5molCO,此时容器总压为1×105Pa,发生上述反应,4min时达平衡,此时测得氮气的物质的量为0.2mol,则0~4min内用CO2表示的的平均速率为___________  该反应的
该反应的 为
为___________
[标准平衡常数 ,其中
,其中 为标准压强
为标准压强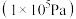 ,
,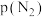 、p(CO2)、p(CO)和p(NO)为各组分的平衡分压[已知
、p(CO2)、p(CO)和p(NO)为各组分的平衡分压[已知 ,其中p为平衡总压,
,其中p为平衡总压, 为平衡系统中NO的物质的量分数]
为平衡系统中NO的物质的量分数]
(4)用NH3可催化消除NO污染:
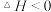
①某条件下该反应速率 ,
, ,该反应的平衡常数
,该反应的平衡常数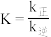 ,则a=
,则a=___________ ,b=___________ 。
②一定温度下,在体积为1L的恒容密闭容器中加入4molNH3和6molNO发生上述反应,若在相同时间内测得NH3的转化率随温度的变化曲线如图,400℃~900℃之间NH3的转化率下降由缓到急的原因是___________

(1)反应

 可有效降低汽车尾气污染物的排放。一定条件下该反应经历三个基元反应阶段,反应历程如下图所示(TS表示过渡态、IM表示中间产物)。三个基元反应中,属于放热反应的是
可有效降低汽车尾气污染物的排放。一定条件下该反应经历三个基元反应阶段,反应历程如下图所示(TS表示过渡态、IM表示中间产物)。三个基元反应中,属于放热反应的是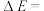
 。
。
(2)探究温度、压强(2MPa、5MPa)对反应
 的影响,如下图所示,表示2MPa的是反应
的影响,如下图所示,表示2MPa的是反应
(3)在一定温度下向容积为2L的密闭容器中加入0.5molNO、0.5molCO,此时容器总压为1×105Pa,发生上述反应,4min时达平衡,此时测得氮气的物质的量为0.2mol,则0~4min内用CO2表示的的平均速率为
 该反应的
该反应的 为
为[标准平衡常数
 ,其中
,其中 为标准压强
为标准压强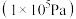 ,
,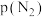 、p(CO2)、p(CO)和p(NO)为各组分的平衡分压[已知
、p(CO2)、p(CO)和p(NO)为各组分的平衡分压[已知 ,其中p为平衡总压,
,其中p为平衡总压, 为平衡系统中NO的物质的量分数]
为平衡系统中NO的物质的量分数](4)用NH3可催化消除NO污染:

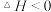
①某条件下该反应速率
 ,
, ,该反应的平衡常数
,该反应的平衡常数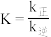 ,则a=
,则a=②一定温度下,在体积为1L的恒容密闭容器中加入4molNH3和6molNO发生上述反应,若在相同时间内测得NH3的转化率随温度的变化曲线如图,400℃~900℃之间NH3的转化率下降由缓到急的原因是

您最近一年使用:0次
2021-12-14更新
|
828次组卷
|
4卷引用:广东省韶关市北江中等职业学校等九校 2021-2022学年高三上学期11月联考化学试题
广东省韶关市北江中等职业学校等九校 2021-2022学年高三上学期11月联考化学试题福建省厦门第一中学2021-2022学年高三上学期12月考试化学试题(已下线)第18周 晚练题-备战2022年高考化学周测与晚练(新高考专用)内蒙古自治区赤峰市松山区2022届高三下学期三月份模拟考试理综化学试题
名校
解题方法
10 . 在一定温度条件下,将1molA和2molB放入容积为5L的密闭容器中发生如下反应:A(s)+2B(g) C(g)+2D(g),反应经5min后达到平衡状态,测得容器内B物质的浓度减少了0.2mol·L-1。下列叙述不正确的是
C(g)+2D(g),反应经5min后达到平衡状态,测得容器内B物质的浓度减少了0.2mol·L-1。下列叙述不正确的是
 C(g)+2D(g),反应经5min后达到平衡状态,测得容器内B物质的浓度减少了0.2mol·L-1。下列叙述不正确的是
C(g)+2D(g),反应经5min后达到平衡状态,测得容器内B物质的浓度减少了0.2mol·L-1。下列叙述不正确的是| A.在5min内该反应用C的浓度变化表示的反应速率0.02mol•L-1•min-1 |
| B.平衡时A、B的转化率均为50% |
| C.初始压强和平衡时压强比为4:5 |
| D.平衡时混合气体中B的体积分数为33.3% |
您最近一年使用:0次
2021-04-29更新
|
455次组卷
|
19卷引用:广东省韶关市北江实验学校2021-2022学年高一下学期期中考试化学试题
广东省韶关市北江实验学校2021-2022学年高一下学期期中考试化学试题湖北省重点高中联考协作体2017-2018学年高一下学期期中考试化学试题山西省阳泉二中2018-2019学年高二上学期期中考试化学试题四川省三台中学实验学校2019-2020学年高二上学期开学考试理综化学试题高一必修第二册(人教2019版)第六章 第二节 化学反应的速率与限度 课时2 化学反应的限度四川省新津中学2020-2021学年高二10月月考化学试题人教版2019必修第二册 六章 第二节 第2课时 化学反应的限度湖北省鄂西北六校联考2020-2021学年高一下学期期中考试化学试题四川省凉山宁南中学2021-2022学年高二上学期开学考试化学试题河南省焦作市武陟县第一中学东校区2021-2022学年高一下学期4月月考化学试题 山西省山西大学附属中学校2021-2022学年高一下学期4月考化学试题(已下线)6.2.2 化学反应的限度-2021-2022学年高一化学课后培优练(人教版2019必修第二册)(已下线)第08练 化学反应的限度-2022年【暑假分层作业】高一化学(人教版2019必修第二册)辽宁省铁岭市六校协作体2021-2022学年高一下学期期末联考化学试题新疆生产建设兵团第一师高级中学2022-2023学年高一下学期4月月考化学试题四川省资阳市乐至中学2022-2023学年高一下学期期中考试化学试题吉林省长春外国语学校2022-2023学年高一下学期5月期中考试化学试题河南省栾川县第一高级中学2022-2023学年高一下学期6月阶段测试化学试题辽宁省东港市第二中学2023-2024学年高二上学期开学考试化学试题