名校
解题方法
1 . 美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图所示:
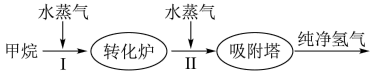
(1)此流程的第Ⅱ步反应为:CO(g)+H2O(g) H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
H2(g)+CO2(g),该反应的化学平衡常数表达式为K=____________ ;反应的平衡常数随温度的变化如下表所示。
从上表可以推断:此反应是__________ (填“吸”或“放”)热反应。
在830 ℃下,若开始时向恒容密闭容器中充入CO与H2O均为1 mol,则达到平衡后CO的转化率为________ 。
(2)此流程的第Ⅱ步反应CO(g)+H2O(g) H2(g)+CO2(g),在830 ℃时,以下表的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有
H2(g)+CO2(g),在830 ℃时,以下表的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有________ (填实验编号)。
(3)在一个不传热的固定容积的容器中,判断此流程的第Ⅱ步反应达到平衡的标志是________ (填序号)。
①体系的压强不再发生变化 ②混合气体的密度不变 ③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变 ⑤体系的温度不再发生变化 ⑥v(CO2正)=v(H2O逆)
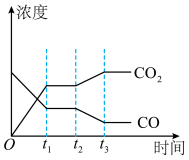
(4)下图表示此流程的第Ⅱ步反应在t1时刻达到平衡,在t2时刻分别因改变某个条件而发生变化的情况:图中t2时刻发生改变的条件可能是________________________ (写出两种)。

(1)此流程的第Ⅱ步反应为:CO(g)+H2O(g)
 H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
H2(g)+CO2(g),该反应的化学平衡常数表达式为K=| 温度/℃ | 400 | 500 | 830 | 1 000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
从上表可以推断:此反应是
在830 ℃下,若开始时向恒容密闭容器中充入CO与H2O均为1 mol,则达到平衡后CO的转化率为
(2)此流程的第Ⅱ步反应CO(g)+H2O(g)
 H2(g)+CO2(g),在830 ℃时,以下表的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有
H2(g)+CO2(g),在830 ℃时,以下表的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有| 实验编号 | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
(3)在一个不传热的固定容积的容器中,判断此流程的第Ⅱ步反应达到平衡的标志是
①体系的压强不再发生变化 ②混合气体的密度不变 ③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变 ⑤体系的温度不再发生变化 ⑥v(CO2正)=v(H2O逆)
(4)下图表示此流程的第Ⅱ步反应在t1时刻达到平衡,在t2时刻分别因改变某个条件而发生变化的情况:图中t2时刻发生改变的条件可能是

您最近一年使用:0次
2019-02-26更新
|
348次组卷
|
4卷引用:广东省广州市北师大附中为明学校2021-2022学年高二10月月考化学试题
9-10高二下·江苏宿迁·期中
名校
解题方法
2 . 一定温度下的反应A(g)+3B(g)≒2C(g),下列叙述不能表明它达到化学平衡的是
| A.A、B、C的浓度不再变化 |
| B.混合气体的总物质的量不再变化 |
| C.单位时间内amol A生成,同时生成3amol B |
| D.C的生成速率与C的分解速率相等 |
您最近一年使用:0次
13-14高二上·河南平顶山·期末
3 . 已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的平衡常数表达式K=____________ ,△H____ 0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。则6s时c(A)=_____ mol·L-1, C的物质的量为______ mol;若反应经一段时间后,达到平衡时A的转化率为_____ ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为_________ ;
(3)判断该反应是否达到平衡的依据为______ (填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
(4)1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为
A(g)+B(g)的平衡常数的值为_____________ 。
 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:| |温度/ ℃ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K=
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。则6s时c(A)=
(3)判断该反应是否达到平衡的依据为
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
(4)1200℃时反应C(g)+D(g)
 A(g)+B(g)的平衡常数的值为
A(g)+B(g)的平衡常数的值为
您最近一年使用:0次
2019-01-30更新
|
2302次组卷
|
28卷引用:广东省揭阳市惠来慈云实验中学2021-2022学年高二上学期第一次月考化学试题
广东省揭阳市惠来慈云实验中学2021-2022学年高二上学期第一次月考化学试题湖北省襄阳市南漳县第二中学2021-2022学年高二上学期10月考化学试题甘肃省秦安县第一中学2021-2022学年高二上学期期中考试化学试题江西省余干县黄金埠中学2021-2022年高二上学期期中考试化学试题海南省临高县新盈中学2021-2022学年高二上学期(1-4班)期中考试化学试题(已下线)2012-2013学年河南省平顶山市高二上学期期末考试化学试卷(已下线)2013-2014学年天津市南开区高二上学期期末考试化学试卷(已下线)2013-2014学年内蒙古赤峰市元宝山区高二上学期期末化学试卷2012年普通高等学校招生全国统一考试化学(海南卷)2015-2016学年海南省嘉积中学高二上12月段考化学试卷2015-2016学年陕西省宝鸡市岐山县高二上学期期末理化学试卷2016-2017学年四川省乐山市高二上学期期末化学试卷吉林省长春市九台区师范高级中学2018-2019学年高二上学期期中考试化学试题山西省运城市河津中学2019-2020学年高二9月月考化学试题安徽省天长市炳辉中学2019-2020学年高二上学期第二次月考化学试题步步为赢 高二化学寒假作业:作业三 化学反应的方向与平衡常数的应用广西壮族自治区百色市田阳高中2019-2020学年高二上学期12月月考理科综合化学试题海南省海口市灵山中学2020-2021学年高二上学期期中考试化学试题广东省揭阳市第三中学2020-2021学年高二上学期期中考化学试题四川省成都新津为明学校2020-2021学年高二上学期期中测试化学试题陕西省咸阳市实验中学2020-2021学年高二上学期第二次月考化学试题四川广元川师大万达中学2020-2021学年高二上学期期中考试化学试题海南省海南鑫源高级中学2019-2020学年高二上学期期中考试化学试题云南省开远市第一中学校2021-2022学年高三下学期开学考试理综化学试题四川省南充市嘉陵第一中学2022-2023学年高二下学期6月月考化学试题福建省厦门市湖滨中学2023-2024学年高二上学期期中考试化学试题四川省内江市2023-2024学年第一中学高二上学期化学试卷海南省首都师范大学附属昌江矿区中学2023-2024学年高二上学期12月月考化学试题
12-13高二上·陕西西安·期末
解题方法
4 . 一定温度下,可逆反应A2(g)+3B2(g)  2AB3(g)达到平衡的标志是( )
2AB3(g)达到平衡的标志是( )
 2AB3(g)达到平衡的标志是( )
2AB3(g)达到平衡的标志是( )| A.容器内每减少1mol A2,同时生成2mol AB3 |
| B.容器内每减少1mol A2,同时生成3mol B2 |
| C.容器内A2、B2、AB3的物质的量之比为1:3:2 |
| D.容器内A2、B2、AB3的物质的量浓度之比为1:1:1 |
您最近一年使用:0次
2019-01-30更新
|
614次组卷
|
6卷引用:广东省揭阳普宁市普师高级中学2021-2022学年高二上学期期中考试化学试题
广东省揭阳普宁市普师高级中学2021-2022学年高二上学期期中考试化学试题黑龙江省牡丹江市海林市朝鲜族中学2021-2022学年高二上学期第三次月考化学试题(已下线)2011-2012学年陕西省西安市第一中学高二上学期期末考试化学(理)试卷(已下线)2012-2013学年广东省实验中学高二上学期期中化学试卷广东省潮州市潮安区颜锡祺中学2019-2020学年高二上学期期中考试化学试题天津市第八中学2020-2021学年高二上学期第三次统练化学试题
9-10高一下·河北衡水·期末
名校
5 . 一定温度下,可逆反应2NO2 2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:
2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成nmol O2的同时生成2nmol NO2;
②单位时间内生成nmol O2 的同时生成2nmol NO;
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态;
④混合气体的颜色不再改变的状态;
⑤密闭容器中压强不再改变的状态;
⑥混合气体的平均相对分子质量不再改变的状态。
 2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:
2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:①单位时间内生成nmol O2的同时生成2nmol NO2;
②单位时间内生成nmol O2 的同时生成2nmol NO;
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态;
④混合气体的颜色不再改变的状态;
⑤密闭容器中压强不再改变的状态;
⑥混合气体的平均相对分子质量不再改变的状态。
| A.①④⑤⑥ | B.②③⑤⑥ | C.①③④⑥ | D.全部 |
您最近一年使用:0次
2019-01-30更新
|
631次组卷
|
12卷引用:河北省石家庄私立第一中学2020-2021学年高一下学期第二次调研考试化学试题
河北省石家庄私立第一中学2020-2021学年高一下学期第二次调研考试化学试题河南省新乡市铁路高级中学2020-2021学年高一下学期6月月考化学试题(已下线)09-10学年河北省衡水中学高一年级下学期期末考试化学试卷(已下线)2010-2011学年内蒙古赤峰二中高一下学期期中考试化学试卷2015-2016学年江苏省扬州中学高一下期中化学试卷2015-2016学年湖北省枣阳市一中高一5月月考化学试卷黑龙江省虎林市高级中学2016-2017学年高一5月月考化学试题河北省张家口第一中学2019-2020学年高二9月月考(衔接班)化学试题河北省唐山市第一中学2019-2020学年高一下学期期中考试化学试题江西省新余市第一中学2019-2020学年高一下学期5月段考化学试题福建省南安市柳城中学2020-2021学年高二上学期期中考试化学试题四川省德阳市广汉中学2022-2023学年高二上学期开学考试化学试题
11-12高二下·广东中山·阶段练习
名校
解题方法
6 . 在一定温度下的定容密闭容器中,当下列条件不再改变时,表明反应:A(s)+2B(g)  C(g)+D(g)已达到平衡状态的是
C(g)+D(g)已达到平衡状态的是
 C(g)+D(g)已达到平衡状态的是
C(g)+D(g)已达到平衡状态的是| A.混合气体的压强 | B.气体的总物质的量 |
| C.混合气体的密度 | D.单位时间内生成n molC的同时消耗2n molB |
您最近一年使用:0次
2019-01-15更新
|
281次组卷
|
10卷引用:四川省成都市新津中学2020—2021学年高二下学期开学考化学试题
四川省成都市新津中学2020—2021学年高二下学期开学考化学试题(已下线)2011-2012学年广东省中山一中高二下学期第一次段考化学试卷(已下线)2012-2013学年广东省陆丰市碣石中学高二上学期期末考试化学试卷(已下线)2013-2014陕西省延安市一中第一学期期末考试高二化学试卷2014-2015浙江省杭州市西湖中学高二12月月考化学试卷【校级联考】江西省上饶市“山江湖”协作体2018-2019学年高二上学期第三次月考化学试题【校级联考】湖北省重点高中联考协作体2018-2019学年高二上学期期中考试化学试题湖南省双峰县第一中学2018-2019学年高一6月月考化学试题贵州省贵阳市清镇北大培文学校2018-2019学年高一下学期期中考试化学试题湖南省湘潭电机子弟中学2019-2020学年高二下学期期中考试化学(理)试题
名校
解题方法
7 . 中共十九大报告指出,加快水污染防治、实施流域环境和近岸海域综合治理、环境污染的治理是化学工作者研究的重要课题,也是践行“绿水青山就是金山银山”的重要举措。在适当的条件下,将CO2转化为甲醇、甲醚等有机物,既可降低CO2造成的温室效应对环境的影响,还可得到重要的有机产物。
(1)已知T K时,某恒容密闭容器中存在如下反应:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) ΔH<0,测得容器中不同时刻时各物质的浓度(mol/L)如下表所示:
CH3OCH3(g)+3H2O(g) ΔH<0,测得容器中不同时刻时各物质的浓度(mol/L)如下表所示:
①若T K时,化学平衡常数K=15,则10 s 时v(正)_______ v(逆)(填“>”“<”或“=”),此时CO2的转化率为________ 。
②既能提高反应速率,又能提高H2转化率的方法是___________ (填序号)。
A.加入过量CO2气体 B.升高温度 C.适当压缩容器体积 D. 将CH3OCH3(g) 分离出去
(2)一定条件下,向某恒容密闭容器中充入x mol CO2和y mol H2,发生的反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=−50 kJ·mol−1。
CH3OH(g)+H2O(g) ΔH=−50 kJ·mol−1。
①下图1中能表示该反应的平衡常数K与温度T之间的变化关系曲线为______ (填“a”或“b”),其判断依据是__________________________________ 。
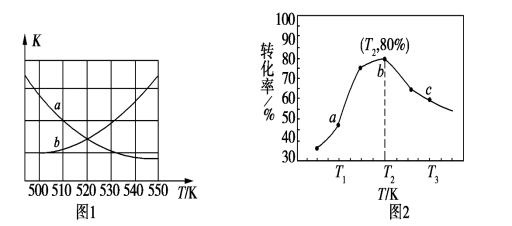
②若x=2、y=3,测得在相同时间内不同温度下H2的转化率如图2所示,则在该时间段内,恰好达到化学平衡时,容器内的压强与反应开始时的压强之比为____________ 。
(1)已知T K时,某恒容密闭容器中存在如下反应:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) ΔH<0,测得容器中不同时刻时各物质的浓度(mol/L)如下表所示:
CH3OCH3(g)+3H2O(g) ΔH<0,测得容器中不同时刻时各物质的浓度(mol/L)如下表所示:| c(CO2) | c(H2) | c(CH3OCH3) | c(H2O) | |
| 开始时 | a | b | 0 | 0 |
| 10 s时 | 3 | 0.5 | c | 1.5 |
①若T K时,化学平衡常数K=15,则10 s 时v(正)
②既能提高反应速率,又能提高H2转化率的方法是
A.加入过量CO2气体 B.升高温度 C.适当压缩容器体积 D. 将CH3OCH3(g) 分离出去
(2)一定条件下,向某恒容密闭容器中充入x mol CO2和y mol H2,发生的反应为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=−50 kJ·mol−1。
CH3OH(g)+H2O(g) ΔH=−50 kJ·mol−1。①下图1中能表示该反应的平衡常数K与温度T之间的变化关系曲线为

②若x=2、y=3,测得在相同时间内不同温度下H2的转化率如图2所示,则在该时间段内,恰好达到化学平衡时,容器内的压强与反应开始时的压强之比为
您最近一年使用:0次
2018-11-17更新
|
295次组卷
|
3卷引用:山东省潍坊市临朐县实验中学2021-2022学年高二上学期9月月考化学试题
名校
8 . 已知化学反应①:Fe(s)+CO2(g)  FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)  FeO(s)+H2(g),其平衡常数为K2。在温度973K和1173K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数为K2。在温度973K和1173K情况下,K1、K2的值分别如下:
(1)通过表格中的数值可以推断:反应①是__________ (填“吸热”或“放热”)反应。
(2)现有反应③CO2(g)+H2(g) CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=
CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=_______________________________________________ 。
(3)能判断反应③已达平衡状态的是_______________________________
A.容器中压强不变 B.混合气体中c(CO)不变
C.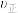 (H2)=
(H2)= (H2O) D.c(CO2)=c(CO)
(H2O) D.c(CO2)=c(CO)
(4)根据反应①与②可推导出K1、K2与K3之间的关系式_______________________ 。据此关系式及上表数据,也能推断出反应③是______ (填“吸热”或“放热”)反应。要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施是______ (填写序号)。
A.缩小反应容器容积 B.扩大反应容器容积 C.降低温度
D.升高温度 E.使用合适的催化剂 F.设法减少CO的量
(5)氢气用于工业合成氨 N2(g) + 3H2(g) 2NH3(g);ΔH = -92.2 kJ·mol-1。一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 、t5 、t7时刻所对应的实验条件改变分别是
2NH3(g);ΔH = -92.2 kJ·mol-1。一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 、t5 、t7时刻所对应的实验条件改变分别是
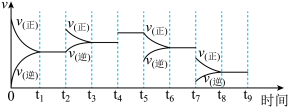
t4___________________ 、t5 ___________________ 、t7___________________ 。
 FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)  FeO(s)+H2(g),其平衡常数为K2。在温度973K和1173K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数为K2。在温度973K和1173K情况下,K1、K2的值分别如下:| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是
(2)现有反应③CO2(g)+H2(g)
 CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=
CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=(3)能判断反应③已达平衡状态的是
A.容器中压强不变 B.混合气体中c(CO)不变
C.
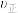 (H2)=
(H2)= (H2O) D.c(CO2)=c(CO)
(H2O) D.c(CO2)=c(CO) (4)根据反应①与②可推导出K1、K2与K3之间的关系式
A.缩小反应容器容积 B.扩大反应容器容积 C.降低温度
D.升高温度 E.使用合适的催化剂 F.设法减少CO的量
(5)氢气用于工业合成氨 N2(g) + 3H2(g)
 2NH3(g);ΔH = -92.2 kJ·mol-1。一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 、t5 、t7时刻所对应的实验条件改变分别是
2NH3(g);ΔH = -92.2 kJ·mol-1。一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 、t5 、t7时刻所对应的实验条件改变分别是
t4
您最近一年使用:0次
2018-11-16更新
|
528次组卷
|
5卷引用:吉林省长春市第二十九中学2021-2022学年高二上学期第一学程考试化学试题
9 . 在一定温度下的恒容密闭容器中,反应3X(g)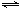 2Y(g)+Z(g)+W(s),ΔH=-QkJ·mol-1,反应已达到平衡的标志是
2Y(g)+Z(g)+W(s),ΔH=-QkJ·mol-1,反应已达到平衡的标志是
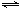 2Y(g)+Z(g)+W(s),ΔH=-QkJ·mol-1,反应已达到平衡的标志是
2Y(g)+Z(g)+W(s),ΔH=-QkJ·mol-1,反应已达到平衡的标志是| A.混合气体的压强不再变化 | B.混合气体的密度不再改变 |
| C.反应混合物中各组分的浓度相等 | D.两种物质X、Y的反应速率之比为3∶2 |
您最近一年使用:0次
2018-11-12更新
|
226次组卷
|
4卷引用:浙江省绍兴鲁迅中学2021-2022学年高二上学期第一次限时训练化学试题
10 . 已知X(g)+3Y(g)⇌2W(g) +M (g) △H=-a kJ·mol-1(a>0)。一定温度下,在体积恒定的密闭容器中,加入1 mol X(g) 与1mol Y (g),下列说法正确的是
| A.充分反应后,放出热量为a kJ |
| B.当反应达到平衡状态时,X与W的物质的量浓度之比一定为1:2 |
| C.当X的物质的量分数不再改变,表明该反应已达平衡 |
| D.若增大Y的浓度,正反应速率增大,逆反应速率减小 |
您最近一年使用:0次
2018-11-07更新
|
5243次组卷
|
13卷引用:四川省蓬安中学校2019-2020学年高二上学期开学考试化学试题
四川省蓬安中学校2019-2020学年高二上学期开学考试化学试题(已下线)课时35 化学反应速率及影响因素-2022年高考化学一轮复习小题多维练(全国通用)甘肃省古浪县第五中学2021-2022学年高二上学期开学考试测试化学试题(已下线)专题12.化学反应速率与化学平衡-十年(2012-2021)高考化学真题分项汇编(浙江专用)2018年11月浙江省普通高校招生选考科目考试化学试题云南省曲靖市会泽县第一中学2019-2020高二上学期开学考试化学试题浙江省2019届高三11月选考科目考试化学试卷北京二中2020-2021学年高二上学期10月月考化学试题(已下线)小题必刷28 化学平衡及平衡移动——2021年高考化学一轮复习小题必刷(通用版本)湖南省宁乡市四校联考2022-2023学年高二上学期10月月考化学试题(已下线)专题15 化学反应速率和化学平衡辽宁省大连市第四十四中学2022-2023学年高三上学期10月考试化学试题重庆十八中两江实验中学校2022-2023学年高二上学期第一次月考化学试题



