解题方法
1 . 利用反应2NO(g)+2CO(g) 2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比
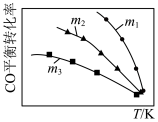
2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比
2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
| A.若m=2,反应达平衡时,NO的转化率为40%,则N2的体积分数为15.4% |
B.该反应的 |
C.投料比: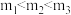 |
| D.汽车排气管中的催化剂可提高NO的平衡转化率 |
您最近半年使用:0次
2 . 重铬酸铵[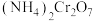 ]可用作媒染剂和有机合成催化剂,具有强氧化性。实验室中将
]可用作媒染剂和有机合成催化剂,具有强氧化性。实验室中将 通入重铬酸(
通入重铬酸(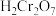 )溶液制备
)溶液制备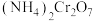 的装置如图所示(夹持装置略)。已知:
的装置如图所示(夹持装置略)。已知: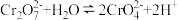 。下列说法错误的是
。下列说法错误的是
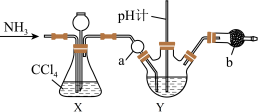
A.装置X可控制通入 的速度且能观察装置Y中是否堵塞 的速度且能观察装置Y中是否堵塞 |
| B.仪器a的作用是防止倒吸 |
C.装置Y中溶液的pH不宜过大,否则会有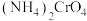 生成 生成 |
D.仪器b中装入的试剂为碱石灰,目的是吸收过量的 |
您最近半年使用:0次
3 . 工业上通过将 与氢气反应,实现碳中和。
与氢气反应,实现碳中和。
(1)已知反应 。根据理论计算,在恒压、起始物质的量之比
。根据理论计算,在恒压、起始物质的量之比 条件下,该反应达平衡时各组分的物质的量分数随温度变化的曲线如图所示。
条件下,该反应达平衡时各组分的物质的量分数随温度变化的曲线如图所示。
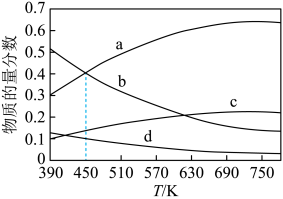
①该反应的平衡常数表达式为___________ ,该反应的
___________ 0(填“>”或“<”)。
②图中曲线b、c分别表示的是平衡时___________ 和___________ 的物质的量分数变化。
(2)用 和
和 合成
合成 的反应为
的反应为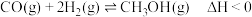 ,按照相同的物质的量投料,测得
,按照相同的物质的量投料,测得 在不同温度下的平衡转化率与压强的关系如图所示。
在不同温度下的平衡转化率与压强的关系如图所示。

①图中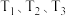 的大小关系为
的大小关系为___________ 。
②图中b、c、d点上正反应速率的关系为___________ 。
②图中a、b、d点上平衡常数的大小关系为___________ 。
(3)合成二甲醚:
反应Ⅰ:
反应Ⅱ: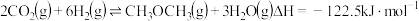
在恒压、 和
和 的起始量一定的条件下,
的起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。其中:
的选择性随温度的变化如图所示。其中: 的选择性
的选择性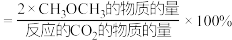 。
。

①温度高于 ,
, 平衡转化率随温度升高而上升的原因是
平衡转化率随温度升高而上升的原因是___________ 。
② 时,起始投入
时,起始投入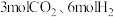 ,在催化剂作用下
,在催化剂作用下 与H2反应一段时间后,测得
与H2反应一段时间后,测得 平衡转化率为40%,
平衡转化率为40%, 的选择性为50%(图中A点),达到平衡时反应Ⅱ理论上消耗
的选择性为50%(图中A点),达到平衡时反应Ⅱ理论上消耗 的物质的量为
的物质的量为___________  。不改变反应时间和温度,一定能提高
。不改变反应时间和温度,一定能提高 选择性的措施有
选择性的措施有___________ 。
③合成二甲醚时较适宜的温度为 ,其原因是
,其原因是___________ 。
 与氢气反应,实现碳中和。
与氢气反应,实现碳中和。(1)已知反应
 。根据理论计算,在恒压、起始物质的量之比
。根据理论计算,在恒压、起始物质的量之比 条件下,该反应达平衡时各组分的物质的量分数随温度变化的曲线如图所示。
条件下,该反应达平衡时各组分的物质的量分数随温度变化的曲线如图所示。
①该反应的平衡常数表达式为

②图中曲线b、c分别表示的是平衡时
(2)用
 和
和 合成
合成 的反应为
的反应为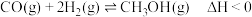 ,按照相同的物质的量投料,测得
,按照相同的物质的量投料,测得 在不同温度下的平衡转化率与压强的关系如图所示。
在不同温度下的平衡转化率与压强的关系如图所示。
①图中
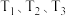 的大小关系为
的大小关系为②图中b、c、d点上正反应速率的关系为
②图中a、b、d点上平衡常数的大小关系为
(3)合成二甲醚:
反应Ⅰ:

反应Ⅱ:
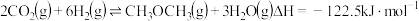
在恒压、
 和
和 的起始量一定的条件下,
的起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。其中:
的选择性随温度的变化如图所示。其中: 的选择性
的选择性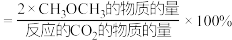 。
。
①温度高于
 ,
, 平衡转化率随温度升高而上升的原因是
平衡转化率随温度升高而上升的原因是②
 时,起始投入
时,起始投入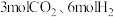 ,在催化剂作用下
,在催化剂作用下 与H2反应一段时间后,测得
与H2反应一段时间后,测得 平衡转化率为40%,
平衡转化率为40%, 的选择性为50%(图中A点),达到平衡时反应Ⅱ理论上消耗
的选择性为50%(图中A点),达到平衡时反应Ⅱ理论上消耗 的物质的量为
的物质的量为 。不改变反应时间和温度,一定能提高
。不改变反应时间和温度,一定能提高 选择性的措施有
选择性的措施有③合成二甲醚时较适宜的温度为
 ,其原因是
,其原因是
您最近半年使用:0次
4 . 某学习小组研究可逆反应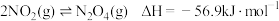 ,请回答下列问题。
,请回答下列问题。
(1)将一定量的 和
和 混合气体充入恒容密闭容器中,反应一段时间,能说明该反应达到化学平衡状态的是___________(填字母)。
混合气体充入恒容密闭容器中,反应一段时间,能说明该反应达到化学平衡状态的是___________(填字母)。
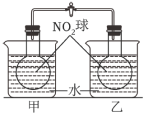
(2)将玻璃球分别浸泡在甲、乙两个烧杯中,向甲中加入 晶体,此烧杯中
晶体,此烧杯中 球的红棕色变浅,说明平衡
球的红棕色变浅,说明平衡 向
向___________ (填“正反应”或“逆反应”)方向移动,所以 晶体溶于水是
晶体溶于水是___________ (填“放热”或“吸热”)过程。
(3)将一定量的 充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。
充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。
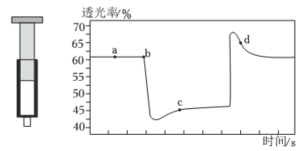
①b点的操作是___________ 注射器(填“压缩”或“拉伸”)。
②c点与a点相比,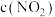
___________ ,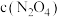
___________ (填“增大”或“减小”)。
③若不忽略体系温度变化,且没有能量损失,则温度
___________ 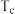 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
④d点的V(正)___________ V(逆)(填“>”、“<”或“=”)。
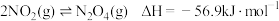 ,请回答下列问题。
,请回答下列问题。(1)将一定量的
 和
和 混合气体充入恒容密闭容器中,反应一段时间,能说明该反应达到化学平衡状态的是___________(填字母)。
混合气体充入恒容密闭容器中,反应一段时间,能说明该反应达到化学平衡状态的是___________(填字母)。| A.容器内气体颜色保持不变 |
B.单位时间内消耗 ,同时生成 ,同时生成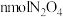 |
| C.容器内气体的压强不随时间变化 |
| D.容器内气体质量不随时间变化 |
 晶体,此烧杯中
晶体,此烧杯中 球的红棕色变浅,说明平衡
球的红棕色变浅,说明平衡 向
向 晶体溶于水是
晶体溶于水是
(3)将一定量的
 充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。
充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。
①b点的操作是
②c点与a点相比,
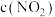
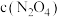
③若不忽略体系温度变化,且没有能量损失,则温度

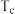 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。④d点的V(正)
您最近半年使用:0次
5 . 下列平衡移动方向和现象判断正确的是
A. ,加水,平衡逆向移动,溶液黄色变浅 ,加水,平衡逆向移动,溶液黄色变浅 |
B. ,加入 ,加入 粉,平衡正向移动,气体颜色变浅 粉,平衡正向移动,气体颜色变浅 |
C.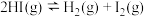 ,压缩容器体积,平衡不移动,气体颜色无变化 ,压缩容器体积,平衡不移动,气体颜色无变化 |
D. ,升高温度,溶液由蓝绿色变为黄绿色 ,升高温度,溶液由蓝绿色变为黄绿色 |
您最近半年使用:0次
6 . 已知:[Co( H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2- 为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:
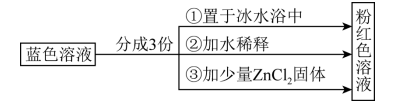
以下结论和解释正确的是
 ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:
以下结论和解释正确的是
| A.由实验①可推知正反应为放热反应 |
| B.等物质的量的 [Co( H2O)6]2+和 [CoCl4]2-中σ键数之比为 9:2 |
| C.实验②是由于c(H2O)增大,导致平衡逆向移动 |
| D.由实验③可知配离子的稳定性:[ZnCl4]2->[CoCl4]2- |
您最近半年使用:0次
7 . CO与H2S按体积比1∶2在容积不变的密闭容器中发生如下反应并达到平衡: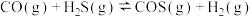 。下列说法正确的是
。下列说法正确的是
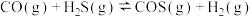 。下列说法正确的是
。下列说法正确的是| A.通入H2S后,正反应速率逐渐增大 |
| B.升高温度后,CO的浓度增大,表明该反应吸热 |
| C.CO和H2S体积比不变时说明反应达到平衡状态 |
| D.选用合适的催化剂,可提高CO的平衡转化率 |
您最近半年使用:0次
解题方法
8 . 芙蓉洞位于武隆乌江最大支流芙蓉江畔的半山腰上,形成于100万年前,在2007年被列人世界遗产名录,属于武隆喀斯特地质的一部分。某小组研究发现,芙蓉洞内石样质量与温度、日游客流量关系如图所示。

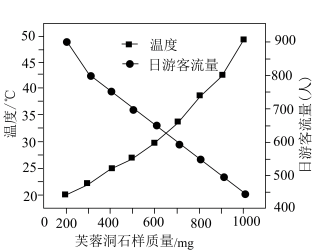
下列叙述错误的是


下列叙述错误的是
| A.芙蓉洞的形成与气候、地理环境有密切关系 |
| B.芙蓉洞形成与风化过程中只发生了物理变化 |
C.日游客流量增大, 浓度增大导致芙蓉洞石样质量减小 浓度增大导致芙蓉洞石样质量减小 |
| D.芙蓉洞石样质量减小过程中发生了化合反应 |
您最近半年使用:0次
9 . 利用含钴废料(主要成分为 ,还含有少量的铝箔、
,还含有少量的铝箔、 等杂质)制备碳酸钴的工艺流程如图:
等杂质)制备碳酸钴的工艺流程如图:
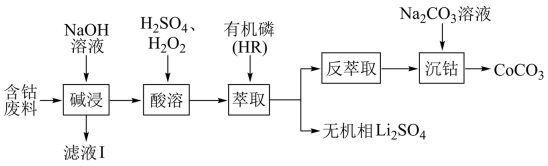
已知:萃取 的反应原理:
的反应原理: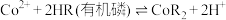 。下列说法错误的是
。下列说法错误的是
A.“滤液Ⅰ”中溶质的主要成分是 |
B.“酸溶”反应中 做氧化剂 做氧化剂 |
C.“反萃取”中可加入 分离出 分离出 |
D.“沉钴”时 溶液滴加速率不宜过快,目的是防止生成 溶液滴加速率不宜过快,目的是防止生成 |
您最近半年使用:0次
10 . 某兴趣小组将过量Cu与 溶液充分反应,静置后取上层清液于试管中,将KSCN溶液滴加到清液中,瞬间产生白色沉淀,附近溶液出现红色;振荡试管,红色又迅速褪去。已知:
溶液充分反应,静置后取上层清液于试管中,将KSCN溶液滴加到清液中,瞬间产生白色沉淀,附近溶液出现红色;振荡试管,红色又迅速褪去。已知:
①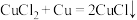 (白色)慢反应
(白色)慢反应
② 快反应
快反应
③ 是拟卤素,化学性质和氯气相似
是拟卤素,化学性质和氯气相似
下列说法正确的是
 溶液充分反应,静置后取上层清液于试管中,将KSCN溶液滴加到清液中,瞬间产生白色沉淀,附近溶液出现红色;振荡试管,红色又迅速褪去。已知:
溶液充分反应,静置后取上层清液于试管中,将KSCN溶液滴加到清液中,瞬间产生白色沉淀,附近溶液出现红色;振荡试管,红色又迅速褪去。已知:①
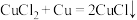 (白色)慢反应
(白色)慢反应②
 快反应
快反应③
 是拟卤素,化学性质和氯气相似
是拟卤素,化学性质和氯气相似下列说法正确的是
A.用KSCN溶液检验 时, 时, 的存在不会对检验产生干扰 的存在不会对检验产生干扰 |
B.局部出现红色主要是因为溶液中的 被空气中的 被空气中的 氧化成 氧化成 , , 与KSCN反应生成 与KSCN反应生成 |
C.白色沉淀是 ,是溶液中 ,是溶液中 与Cu反应生成的 与Cu反应生成的 |
D.红色迅速褪去的原因是振荡试管时 与 与 发生反应,从而使 发生反应,从而使 平衡逆向移动 平衡逆向移动 |
您最近半年使用:0次



