名校
解题方法
1 . 我国已探明或开发的天然气中含有一定含量的 ,而且随着原油中硫含量的上升,炼油厂中干气及液化气等含硫气体的排放量逐年增加。与此同时,我国汽油、柴油标准不断升级、环保排放要求不断升高,新增的加氢装置也越来越多,气体中
,而且随着原油中硫含量的上升,炼油厂中干气及液化气等含硫气体的排放量逐年增加。与此同时,我国汽油、柴油标准不断升级、环保排放要求不断升高,新增的加氢装置也越来越多,气体中 含量也不断增加。
含量也不断增加。 会引起设备腐蚀,还会威胁生命安全。因此,炼油厂中的干气、液化气、加氨后气体以及气田中的天然气都必须首先进行脱硫净化处理。
会引起设备腐蚀,还会威胁生命安全。因此,炼油厂中的干气、液化气、加氨后气体以及气田中的天然气都必须首先进行脱硫净化处理。
I.胺液脱硫
胺液脱硫系统已成为石油、天然气加工的重要组成部分。含氨基的有机化合物称为胺,现用 表示(R代烃基)。
表示(R代烃基)。
(1)用化学方程式解释胺的水溶液呈碱性原因:_____ 。
(2)用胺液吸收足量 的离子方程式是
的离子方程式是_____ 。
(3)某胺(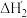 )的
)的 ,
, 的两级电离平衡常数分别为
的两级电离平衡常数分别为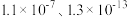 ,则(
,则(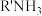 )HS的水溶液呈
)HS的水溶液呈_____ (填标号)。
A.碱性 B.中性 C.酸性
Ⅱ.热分解法脱硫
在密闭容器中模拟工业热分解法脱硫,发生反应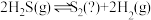 。其他条件不变时,
。其他条件不变时, 的平衡转化率随温度和压强的变化如图。
的平衡转化率随温度和压强的变化如图。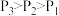 ,反应中
,反应中
_____ (填“是”或“不是")气态,理由是_____ 。
(5)实际反应在高温下进行的原因可能是_____ (答出2条即可)。
 ,而且随着原油中硫含量的上升,炼油厂中干气及液化气等含硫气体的排放量逐年增加。与此同时,我国汽油、柴油标准不断升级、环保排放要求不断升高,新增的加氢装置也越来越多,气体中
,而且随着原油中硫含量的上升,炼油厂中干气及液化气等含硫气体的排放量逐年增加。与此同时,我国汽油、柴油标准不断升级、环保排放要求不断升高,新增的加氢装置也越来越多,气体中 含量也不断增加。
含量也不断增加。 会引起设备腐蚀,还会威胁生命安全。因此,炼油厂中的干气、液化气、加氨后气体以及气田中的天然气都必须首先进行脱硫净化处理。
会引起设备腐蚀,还会威胁生命安全。因此,炼油厂中的干气、液化气、加氨后气体以及气田中的天然气都必须首先进行脱硫净化处理。I.胺液脱硫
胺液脱硫系统已成为石油、天然气加工的重要组成部分。含氨基的有机化合物称为胺,现用
 表示(R代烃基)。
表示(R代烃基)。(1)用化学方程式解释胺的水溶液呈碱性原因:
(2)用胺液吸收足量
 的离子方程式是
的离子方程式是(3)某胺(
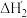 )的
)的 ,
, 的两级电离平衡常数分别为
的两级电离平衡常数分别为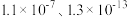 ,则(
,则(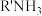 )HS的水溶液呈
)HS的水溶液呈A.碱性 B.中性 C.酸性
Ⅱ.热分解法脱硫
在密闭容器中模拟工业热分解法脱硫,发生反应
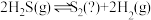 。其他条件不变时,
。其他条件不变时, 的平衡转化率随温度和压强的变化如图。
的平衡转化率随温度和压强的变化如图。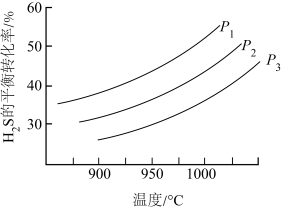
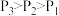 ,反应中
,反应中
(5)实际反应在高温下进行的原因可能是
您最近一年使用:0次
名校
2 . 恒温恒容,可逆反应N2O4(g) 2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是
2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是
 2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是
2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是| A.NO2的体积分数增大 | B.达新平衡后平衡体系压强比原平衡大 |
| C.平衡正向移动 | D.达新平衡后N2O4转化率降低 |
您最近一年使用:0次
名校
3 . 下列有关对应图像的说法正确的是

A.据①知,某温度下,平衡状态由A变到B时,平衡常数 |
B.据平衡常数的负对数(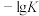 )—温度(T)图像②知,30℃时,B点对应状态的 )—温度(T)图像②知,30℃时,B点对应状态的 |
C.由 的稳定性与溶液pH的关系可知图③中 的稳定性与溶液pH的关系可知图③中 |
D.图④所示体系中气体平均摩尔质量: , , |
您最近一年使用:0次
名校
4 . 在 温度下,向1L恒容容器中加入1molCO和
温度下,向1L恒容容器中加入1molCO和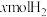 ,发生反应
,发生反应
 ,得到
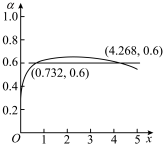
,得到 的平衡转化率α随着x的变化情况如下图所示。下列说法正确的是(已知
的平衡转化率α随着x的变化情况如下图所示。下列说法正确的是(已知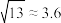 )
)
 温度下,向1L恒容容器中加入1molCO和
温度下,向1L恒容容器中加入1molCO和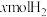 ,发生反应
,发生反应
 ,得到
,得到 的平衡转化率α随着x的变化情况如下图所示。下列说法正确的是(已知
的平衡转化率α随着x的变化情况如下图所示。下列说法正确的是(已知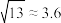 )
)
A.起始时向容器中加入 ,平衡后再加入 ,平衡后再加入 ,再次平衡时 ,再次平衡时 的转化率会减小 的转化率会减小 |
B.其他条件相同,只改变温度和 初始投料,使 初始投料,使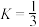 ,x=3,此时 ,x=3,此时 的平衡转化率约为56.7% 的平衡转化率约为56.7% |
C.与x=0.732相比,当x=4.268时,平衡体系中 的体积分数更小 的体积分数更小 |
D.一定温度下,向1L恒容容器中加入HI(g),使其分解达到平衡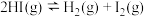 ,当HI投料量增大时,HI的平衡转化率先增大后减小 ,当HI投料量增大时,HI的平衡转化率先增大后减小 |
您最近一年使用:0次
5 . 一定温度下,向三个容积不等的恒容密闭容器中分别投入2molNOCl,发生反应: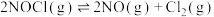 。反应tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
。反应tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
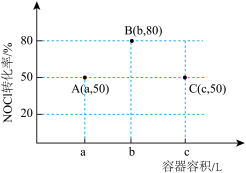
| A.A点加入适当催化剂,可以提高NOCl的转化率 |
| B.容积为aL的容器达到平衡后再投入1molNOCl、1molNO,平衡向左移动 |
| C.A、B两点的压强之比为25:28 |
| D.容积为cL的容器NOCl的平衡转化率大于80% |
您最近一年使用:0次
名校
6 . 以下说法中操作正确、能达到目的且判断正确的是
选项 | 操作 | 目的 | 判断 |
A | 向 | 使 | 错误,根据反应 |
B | 合成氨时在经济性良好的范围内选择尽可能高的压强 | 增加 转化率 转化率 | 正确,压强增大使得反应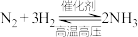 向右进行 向右进行 |
C | 向两支盛有2ml0.2mol/L的乙二酸试管中滴加1ml浓度分别为0.1mol/L和0.2mol/L的 溶液 溶液 | 探究反应物浓度对反应速率的影响 | 正确,浓度越大反应速率越快, 褪色越快 褪色越快 |
D | 向滴有KSCN溶液的 溶液中加入 溶液中加入 固体 固体 | 探究浓度对平衡的影响 | 正确,增加 浓度,使 浓度,使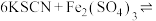 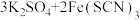 平衡移动 平衡移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 近年来,碳中和、碳达峰成为热点。以CO2、H2为原料生产甲醇是一种有效利用二氧化碳的途径。
途径一:涉及的反应有
I.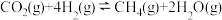
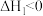
Ⅱ.

III.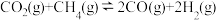
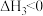
(1)关于反应I,下列描述正确的是___________(填字母序号)。
(2)根据反应I~Ⅲ,计算 ΔH=
ΔH=___________ 。
(3)工业中,对于反应I,通常同时存在副反应IV: ΔH4。在一定条件下,在合成塔中充入一定量CO2和H2。不同压强时,CO2的平衡转化率如图a所示。当气体总压强恒定为1MPa时,平衡时各物质的物质的量分数如图b所示。
ΔH4。在一定条件下,在合成塔中充入一定量CO2和H2。不同压强时,CO2的平衡转化率如图a所示。当气体总压强恒定为1MPa时,平衡时各物质的物质的量分数如图b所示。

①图a中,相同温度下,压强越大,CO2的平衡转化率越大,其原因是___________ 。
②由图b可知,ΔH4___________ 0(填“>”、“<”或“=”);H2的物质的量分数随温度升高而增大,原因是___________ 。
(4)在一定条件下(温度为T1℃),往恒容密闭容器中充入1.0molCO2和4.0molH2,发生反应I,初始压强为p0,5min达到平衡,压强为0.8p0,则CO2的平衡转化率为___________ 。
途径二:涉及的反应有
I.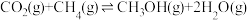
Ⅱ.
III.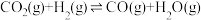
(5)一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平行时,容器中CH3OH(g)为amol,CO为bmol,反应Ⅲ的平衡常数为___________ (用含a、b、V的代数式表示)。
途径一:涉及的反应有
I.
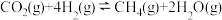
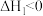
Ⅱ.


III.
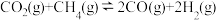
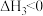
(1)关于反应I,下列描述正确的是___________(填字母序号)。
| A.恒容下达平衡状态时,再充入少量氦气,正逆反应速率不变 |
| B.当混合气体的平均摩尔质量不再发生变化时,反应达平衡状态 |
| C.当反应达平衡状态时,2V正(H2)=V逆(H2O) |
| D.恒温下缩小容器体积,反应物的活化分子百分数增大 |
 ΔH=
ΔH=(3)工业中,对于反应I,通常同时存在副反应IV:
 ΔH4。在一定条件下,在合成塔中充入一定量CO2和H2。不同压强时,CO2的平衡转化率如图a所示。当气体总压强恒定为1MPa时,平衡时各物质的物质的量分数如图b所示。
ΔH4。在一定条件下,在合成塔中充入一定量CO2和H2。不同压强时,CO2的平衡转化率如图a所示。当气体总压强恒定为1MPa时,平衡时各物质的物质的量分数如图b所示。
①图a中,相同温度下,压强越大,CO2的平衡转化率越大,其原因是
②由图b可知,ΔH4
(4)在一定条件下(温度为T1℃),往恒容密闭容器中充入1.0molCO2和4.0molH2,发生反应I,初始压强为p0,5min达到平衡,压强为0.8p0,则CO2的平衡转化率为
途径二:涉及的反应有
I.
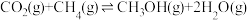
Ⅱ.

III.
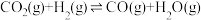
(5)一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平行时,容器中CH3OH(g)为amol,CO为bmol,反应Ⅲ的平衡常数为
您最近一年使用:0次
名校
解题方法
8 . 向体积均为1L的两恒容容器中分别充入2molX和1molY发生反应: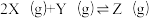
 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
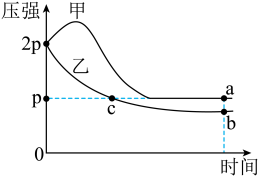
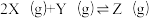
 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
| A.△H>0 | B.气体的总物质的量:na>nc |
| C.a点平衡常数:K<12 | D.反应速率:Va正>Vb正 |
您最近一年使用:0次
名校
9 . 一定温度下,将1molA(g)和1molB(g)充入2L密闭容器中发生反应:A(g)+B(g) xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是

 xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
| A.x=1 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是增大反应物的浓度或降温 |
| D.t1~t2、t2~t3平衡常数相等,且K=4 |
您最近一年使用:0次
名校
解题方法
10 . 研究氮氧化物反应的特征及机理,对处理该类化合物的污染问题具有重要意义。回答下列问题:
(1)氮的氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
Ⅰ.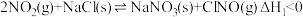
Ⅱ.
①反应: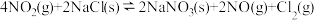 只有在低温时自发进行,则该反应的活化能:
只有在低温时自发进行,则该反应的活化能: (正)
(正)___________  (逆)(填“>”或“<”),。
(逆)(填“>”或“<”),。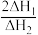 的数值范围是
的数值范围是___________ (填序号)。
A.<-1 B.-1~0 C.0~1 D.>1
②为研究上述反应体系的平衡关系,恒温条件下,向盛有足量NaCl(s)的恒容密闭容器中加入0.2mol 、0.2molNO和0.1mol
、0.2molNO和0.1mol ,初始压强为
,初始压强为 ,只发生反应Ⅰ、Ⅱ,达到平衡时测得体系的压强减少20%,
,只发生反应Ⅰ、Ⅱ,达到平衡时测得体系的压强减少20%, 的平衡转化率为20%,则平衡反应时
的平衡转化率为20%,则平衡反应时
___________ mol,Ⅱ的压强平衡常数
___________ ( 为以分压表示的平衡常数,气体分压=气体总压×体积分数)。
为以分压表示的平衡常数,气体分压=气体总压×体积分数)。
(2)CO还原氮氧化物的反应如下: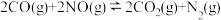
 。
。
①该反应分别在不同温度、不同催化剂下,保持其他初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图甲所示。
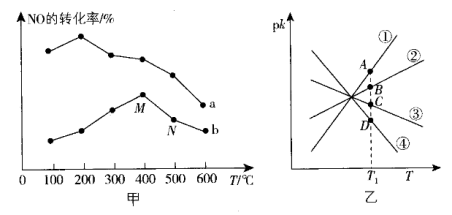
在催化剂作用下,图中M点___________ (填“达到了”或“未达到”)平衡状态。温度高于400℃,NO转化率降低的原因可能是___________ 。
②实验测得 (
( 是速率常数,只与温度有关)。如图乙所示①②③④四条斜线中,能表示
是速率常数,只与温度有关)。如图乙所示①②③④四条斜线中,能表示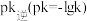 随温度变化的是
随温度变化的是___________ (填序号)升高温度,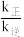
___________ (填“增大”“减小”或“不变”)图中 点的纵坐标分别为
点的纵坐标分别为 ,则温度T1时化学平衡常数
,则温度T1时化学平衡常数
___________ L/mol。
③同温同压下,再向该容器中注入稀有气体氦气,该反应的化学平衡将___________ (填“正向移动”“逆向移动”或“不移动”)。
(1)氮的氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
Ⅰ.
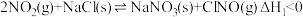
Ⅱ.

①反应:
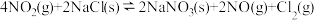 只有在低温时自发进行,则该反应的活化能:
只有在低温时自发进行,则该反应的活化能: (正)
(正) (逆)(填“>”或“<”),。
(逆)(填“>”或“<”),。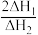 的数值范围是
的数值范围是A.<-1 B.-1~0 C.0~1 D.>1
②为研究上述反应体系的平衡关系,恒温条件下,向盛有足量NaCl(s)的恒容密闭容器中加入0.2mol
 、0.2molNO和0.1mol
、0.2molNO和0.1mol ,初始压强为
,初始压强为 ,只发生反应Ⅰ、Ⅱ,达到平衡时测得体系的压强减少20%,
,只发生反应Ⅰ、Ⅱ,达到平衡时测得体系的压强减少20%, 的平衡转化率为20%,则平衡反应时
的平衡转化率为20%,则平衡反应时

 为以分压表示的平衡常数,气体分压=气体总压×体积分数)。
为以分压表示的平衡常数,气体分压=气体总压×体积分数)。(2)CO还原氮氧化物的反应如下:
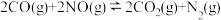
 。
。①该反应分别在不同温度、不同催化剂下,保持其他初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图甲所示。

在催化剂作用下,图中M点
②实验测得
 (
( 是速率常数,只与温度有关)。如图乙所示①②③④四条斜线中,能表示
是速率常数,只与温度有关)。如图乙所示①②③④四条斜线中,能表示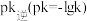 随温度变化的是
随温度变化的是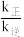
 点的纵坐标分别为
点的纵坐标分别为 ,则温度T1时化学平衡常数
,则温度T1时化学平衡常数
③同温同压下,再向该容器中注入稀有气体氦气,该反应的化学平衡将
您最近一年使用:0次

 和生石灰混合体系加压
和生石灰混合体系加压 的K的表达式可知,压强增大不能使
的K的表达式可知,压强增大不能使

