1 . 在容积2L的刚性容器中充入1molX和2molY,发生反应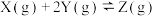 ,正反应为放热反应,反应过程中测得容器内压强的变化如表所示。下列说法正确的是
,正反应为放热反应,反应过程中测得容器内压强的变化如表所示。下列说法正确的是
(用压强计算平衡常数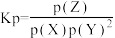 ;分压=总压×物质的量分数)
;分压=总压×物质的量分数)
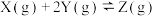 ,正反应为放热反应,反应过程中测得容器内压强的变化如表所示。下列说法正确的是
,正反应为放热反应,反应过程中测得容器内压强的变化如表所示。下列说法正确的是| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/Mpa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
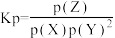 ;分压=总压×物质的量分数)
;分压=总压×物质的量分数)| A.20min后,增大压强,反应速率增大且v(逆)>v(正) |
| B.20min内Y转化率为50% |
| C.25min时,再向容器中通入X、Z各1mol,平衡不移动 |
D.该温度下平衡常数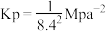 |
您最近一年使用:0次
名校
2 . 溴代烷的制备,常规工艺分“氧化”和“溴化”两个过程,通常以 在合适温度下催化氧化
在合适温度下催化氧化 制备
制备 (溴易液化,注意控制温度和压强)。再利用
(溴易液化,注意控制温度和压强)。再利用 完成溴代过程来制备:新工艺是将烷烃、
完成溴代过程来制备:新工艺是将烷烃、 和
和 混合,直按催化“氧化溴化”得到溴代烷。回答下列问题:
混合,直按催化“氧化溴化”得到溴代烷。回答下列问题:
(1)已知:TK时,部分物质的相对能量如下表:
此温度下,在恒容密闭容器中充入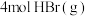 和
和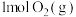 发生“氧化”,测得反应物的平衡转化率为60%。若保持其他条件不变,改为绝热状态,平衡时测得放出热量为
发生“氧化”,测得反应物的平衡转化率为60%。若保持其他条件不变,改为绝热状态,平衡时测得放出热量为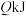 ,则下列关系正确的是___________(填标号)。
,则下列关系正确的是___________(填标号)。
(2)“溴化”时容器体积可变,在温度为TK时,向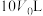 容器中投入初始浓度均为
容器中投入初始浓度均为 的
的 和
和 ,发生反应:
,发生反应: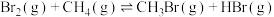 。保持温度不变,压缩容器体积,测得不同容积下
。保持温度不变,压缩容器体积,测得不同容积下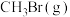 的平衡浓度如下表:
的平衡浓度如下表:
当容器体积从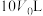 缩小到
缩小到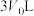 时,测得此时容器内仅有四种气态组分,平衡
时,测得此时容器内仅有四种气态组分,平衡___________ 移动(填“正向”“逆向”或“不”),m=___________ ;容器体积缩小到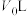 时,平衡
时,平衡___________ 移动(填“正向”“逆向”或“不”)。
(3)新工艺中,“氧化溴化“反应: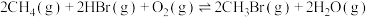
 ,反应起始物料
,反应起始物料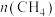 、
、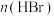 、
、 分别为
分别为 、
、 、
、 时,在不同条件下达到平衡,设体系中
时,在不同条件下达到平衡,设体系中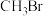 的物质的量分数为
的物质的量分数为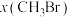 ,在T为
,在T为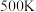 下的
下的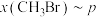 、在p为
、在p为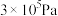 下的
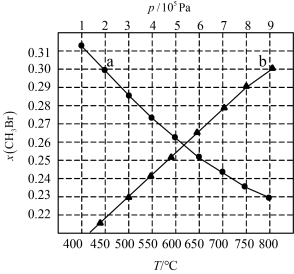
下的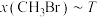 如图所示。a点对应的压强为
如图所示。a点对应的压强为___________ ;b点对应的反应条件为___________ ,此时
___________ (保留三位有效数字)。
 在合适温度下催化氧化
在合适温度下催化氧化 制备
制备 (溴易液化,注意控制温度和压强)。再利用
(溴易液化,注意控制温度和压强)。再利用 完成溴代过程来制备:新工艺是将烷烃、
完成溴代过程来制备:新工艺是将烷烃、 和
和 混合,直按催化“氧化溴化”得到溴代烷。回答下列问题:
混合,直按催化“氧化溴化”得到溴代烷。回答下列问题:(1)已知:TK时,部分物质的相对能量如下表:
| 物质 | 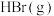 |  |  |  |
相对能量 | x | y | z | w |
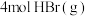 和
和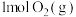 发生“氧化”,测得反应物的平衡转化率为60%。若保持其他条件不变,改为绝热状态,平衡时测得放出热量为
发生“氧化”,测得反应物的平衡转化率为60%。若保持其他条件不变,改为绝热状态,平衡时测得放出热量为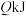 ,则下列关系正确的是___________(填标号)。
,则下列关系正确的是___________(填标号)。A.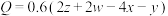 | B. |
C.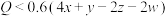 | D. |
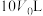 容器中投入初始浓度均为
容器中投入初始浓度均为 的
的 和
和 ,发生反应:
,发生反应: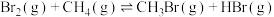 。保持温度不变,压缩容器体积,测得不同容积下
。保持温度不变,压缩容器体积,测得不同容积下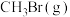 的平衡浓度如下表:
的平衡浓度如下表:容器体积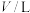 |  |  |  |
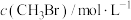 | m | 0.09 | 0.25 |
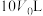 缩小到
缩小到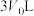 时,测得此时容器内仅有四种气态组分,平衡
时,测得此时容器内仅有四种气态组分,平衡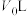 时,平衡
时,平衡(3)新工艺中,“氧化溴化“反应:
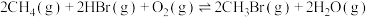
 ,反应起始物料
,反应起始物料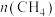 、
、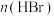 、
、 分别为
分别为 、
、 、
、 时,在不同条件下达到平衡,设体系中
时,在不同条件下达到平衡,设体系中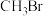 的物质的量分数为
的物质的量分数为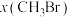 ,在T为
,在T为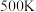 下的
下的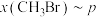 、在p为
、在p为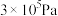 下的
下的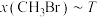 如图所示。a点对应的压强为
如图所示。a点对应的压强为

您最近一年使用:0次
3 . 工业上,用氢气还原乙酸甲酯制备乙醇:
主反应:
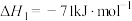
副反应:
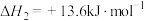
其他条件相同,将 和
和 按一定流速通过催化剂表面,乙酸甲酯的转化率与乙醇的选择性随氢酯比
按一定流速通过催化剂表面,乙酸甲酯的转化率与乙醇的选择性随氢酯比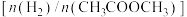 变化如图所示。下列叙述错误的是
变化如图所示。下列叙述错误的是

主反应:

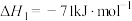
副反应:

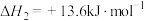
其他条件相同,将
 和
和 按一定流速通过催化剂表面,乙酸甲酯的转化率与乙醇的选择性随氢酯比
按一定流速通过催化剂表面,乙酸甲酯的转化率与乙醇的选择性随氢酯比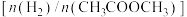 变化如图所示。下列叙述错误的是
变化如图所示。下列叙述错误的是
| A.在恒温恒容条件下进行上述反应,气体总压强不变时达到平衡状态 |
| B.本实验最佳氢酯比为10左右 |
| C.其他条件不变,氢酯比小于10时增大氢酯比,促进副反应,抑制主反应 |
| D.其他条件不变,达到平衡后升高温度,乙醇选择性减小 |
您最近一年使用:0次
名校
4 . 合成氨反应:N2+3H2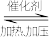 2NH3在密闭容器中进行。下列有关说法正确的是
2NH3在密闭容器中进行。下列有关说法正确的是
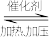 2NH3在密闭容器中进行。下列有关说法正确的是
2NH3在密闭容器中进行。下列有关说法正确的是| A.其他条件相同时在不同容器中发生反应,使用催化剂可能使相同时间内H2的转化率更高 |
| B.若在恒温恒容条件下达到平衡后增大氨气浓度,平衡将逆向移动,氨气产率下降 |
| C.其他条件不变,升高温度,平衡逆向移动,正反应速率下降 |
| D.其他条件不变,降低NH3的浓度,平衡正向移动,正反应速率增大 |
您最近一年使用:0次
名校
5 . 向体积为 的固定密闭容器中通入
的固定密闭容器中通入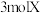 气体,在一定温度下发生如下反应:
气体,在一定温度下发生如下反应: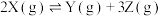
(1)经 后达平衡,此时容器内压强为起始时的1.2倍,则用Y表示的速率为
后达平衡,此时容器内压强为起始时的1.2倍,则用Y表示的速率为_____ 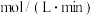 。
。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一时间内测得的反应速率分别为:甲: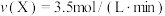 ;乙:
;乙: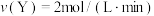 ;丙:
;丙: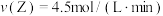 ;丁:
;丁: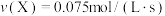 。若其他条件相同,温度不同,温度由高到低的顺序是(填序号)
。若其他条件相同,温度不同,温度由高到低的顺序是(填序号)_____ 。
(3)若向达到(1)的平衡体系中充入氩气,则平衡向_____ (填“左”“右”或“不”,下同)移动。
(4)若在相同条件下向达到(1)所述平衡体系中再充入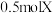 气体,则平衡后X的转化率与(1)的平衡中X的转化率相比_____。
气体,则平衡后X的转化率与(1)的平衡中X的转化率相比_____。
(5)若保持与(1)的温度和压强不变,起始时加入X、Y、Z物质的量分别为 、
、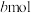 、
、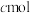 ,达平衡时各物质百分含量与(1)平衡时相等,则
,达平衡时各物质百分含量与(1)平衡时相等,则 应满足的关系为
应满足的关系为_____ 。
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为 、
、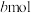 、
、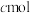 ,达平衡时各物质浓度与(1)平衡时相等,则起始时维持化学反应向逆反应方向进行,则
,达平衡时各物质浓度与(1)平衡时相等,则起始时维持化学反应向逆反应方向进行,则 的取值范围应为
的取值范围应为_____ 。
 的固定密闭容器中通入
的固定密闭容器中通入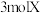 气体,在一定温度下发生如下反应:
气体,在一定温度下发生如下反应: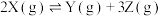
(1)经
 后达平衡,此时容器内压强为起始时的1.2倍,则用Y表示的速率为
后达平衡,此时容器内压强为起始时的1.2倍,则用Y表示的速率为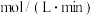 。
。(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一时间内测得的反应速率分别为:甲:
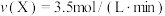 ;乙:
;乙: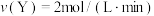 ;丙:
;丙: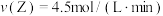 ;丁:
;丁: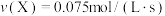 。若其他条件相同,温度不同,温度由高到低的顺序是(填序号)
。若其他条件相同,温度不同,温度由高到低的顺序是(填序号)(3)若向达到(1)的平衡体系中充入氩气,则平衡向
(4)若在相同条件下向达到(1)所述平衡体系中再充入
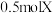 气体,则平衡后X的转化率与(1)的平衡中X的转化率相比_____。
气体,则平衡后X的转化率与(1)的平衡中X的转化率相比_____。| A.无法确定 | B.前者一定大于后者 |
| C.前者一定等于后者 | D.前者一定小于后者 |
 、
、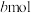 、
、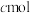 ,达平衡时各物质百分含量与(1)平衡时相等,则
,达平衡时各物质百分含量与(1)平衡时相等,则 应满足的关系为
应满足的关系为(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为
 、
、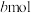 、
、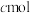 ,达平衡时各物质浓度与(1)平衡时相等,则起始时维持化学反应向逆反应方向进行,则
,达平衡时各物质浓度与(1)平衡时相等,则起始时维持化学反应向逆反应方向进行,则 的取值范围应为
的取值范围应为
您最近一年使用:0次
名校
解题方法
6 . 一定压强下,向 密闭容器中充入
密闭容器中充入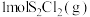 和
和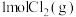 ,发生反应:
,发生反应: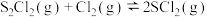 。
。 的消耗速率
的消耗速率 、
、 的消耗速率
的消耗速率 、温度
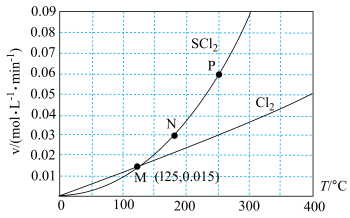
、温度 三者的关系如图所示。下列说法正确的是
三者的关系如图所示。下列说法正确的是
 密闭容器中充入
密闭容器中充入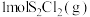 和
和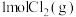 ,发生反应:
,发生反应: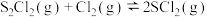 。
。 的消耗速率
的消耗速率 、
、 的消耗速率
的消耗速率 、温度
、温度 三者的关系如图所示。下列说法正确的是
三者的关系如图所示。下列说法正确的是
A.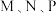 三点对应状态下,达到平衡状态的是 三点对应状态下,达到平衡状态的是 |
B.温度升高,平衡常数 增大 增大 |
C.保持其他条件不变,若投料改为通入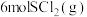 ,平衡时 ,平衡时 的体积分数增大 的体积分数增大 |
D.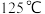 时,平衡时 时,平衡时 的消耗速率大于 的消耗速率大于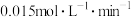 |
您最近一年使用:0次
名校
7 . 如图所示,甲容器容积固定不变,乙容器有可移动的活塞。甲中充入2mol SO2和1mol O2,乙中充入4mol SO3和1mol He,在恒定温度和相同的催化剂条件下,发生如下反应: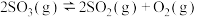 ,下列有关说法正确的是
,下列有关说法正确的是
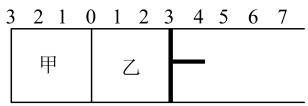
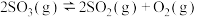 ,下列有关说法正确的是
,下列有关说法正确的是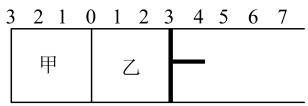
A.若活塞固定在6处不动,达平衡时甲乙两容器中的压强: |
B.若活塞固定在3处不动,达平衡时甲乙两容器中 的浓度: 的浓度: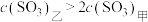 |
C.若活塞固定在3处不动,达平衡时甲乙两容器中 的体积分数: 的体积分数: |
D.若活塞固定在7处不动,达平衡时甲乙两容器中 的物质的量分数相等 的物质的量分数相等 |
您最近一年使用:0次
名校
解题方法
8 . 下列实验方案、现象和结论都正确的是
| 实验操作 | 现象 | 结论 | |
| A | 用玻璃棒蘸取新制氯水涂在pH试纸上 | pH试纸变红色 | 氯水显酸性 |
| B | 向酸性KMnO4和H2C2O4的混合溶液中 加入少量MnSO4(s) | 气泡迅速增多 溶液很快褪色 | MnSO4作催化剂 |
| C | 分别取5mL0.2mol/LNa2S2O3溶液和 10mL0.1mol/LNa2S2O3溶液于两支试管中 然后同时加入10mL0.1mol/LH2SO4溶液 | 产生等量浑浊 前者时间更短 | 增大Na2S2O3浓度 可以加快反应速率 |
| D | 对平衡体系2HI H2+I2(g)压缩容器 H2+I2(g)压缩容器 | 颜色加深 | 平衡正向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-17更新
|
260次组卷
|
3卷引用:浙江省海宁市高级中学2022-2023学年高二上学期10月月考化学试题
名校
9 . 工业上能利用甲烷重整制合成气 、
、 ,反应体系中主要反应如下:
,反应体系中主要反应如下:
主反应I.


副反应II.


已知在727℃时, 。
。
据此分析,下列判断错误的是
 、
、 ,反应体系中主要反应如下:
,反应体系中主要反应如下:主反应I.



副反应II.



已知在727℃时,
 。
。据此分析,下列判断错误的是
A.当体系中反应达到平衡时, |
B.727℃时,反应 的平衡常数 的平衡常数 |
| C.若反应体系为恒温体系,压缩容器容积,平衡时混合气体的平均摩尔质量增大 |
| D.若反应体系为恒温恒容体系,当气体的总压强不变时,反应达到平衡状态 |
您最近一年使用:0次
2023-09-01更新
|
278次组卷
|
2卷引用:安徽省合肥市第八中学2022-2023学年高三上学期12月月考化学试题
名校
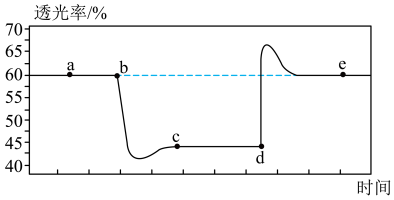
10 . 常温下某同学将一定量的 充入注射器中后封口,测得拉伸和压缩注射器的活塞过程中气体透光率随时间的变化如图所示(已知气体颜色越深,透光率越小;
充入注射器中后封口,测得拉伸和压缩注射器的活塞过程中气体透光率随时间的变化如图所示(已知气体颜色越深,透光率越小;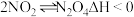 )。下列说法正确的是
)。下列说法正确的是
 充入注射器中后封口,测得拉伸和压缩注射器的活塞过程中气体透光率随时间的变化如图所示(已知气体颜色越深,透光率越小;
充入注射器中后封口,测得拉伸和压缩注射器的活塞过程中气体透光率随时间的变化如图所示(已知气体颜色越深,透光率越小;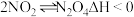 )。下列说法正确的是
)。下列说法正确的是
A. 点操作为压缩针管,因此 点操作为压缩针管,因此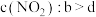 |
B. 点的操作为拉伸注射器到任意位置 点的操作为拉伸注射器到任意位置 |
C. 点平均相对分子质量与 点平均相对分子质量与 点相等 点相等 |
D.若注射器绝热,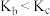 |
您最近一年使用:0次
2023-08-11更新
|
361次组卷
|
2卷引用:陕西西安市第八十三中学2023-2024学年高二上学期10月月考化学试题



