名校
解题方法
1 . 页岩气是从页岩层中开采的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和 ),
), 与
与 通入聚焦太阳能反应器,发生反应
通入聚焦太阳能反应器,发生反应
 。已知:
。已知:
①

②

③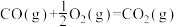

则
___________ (用含 、
、 、
、 的代数式表示)
的代数式表示)
(2)用合成气生成甲醇的反应为
 ,在10L恒容密闭容器中按物质的量之比1:2充入CO和
,在10L恒容密闭容器中按物质的量之比1:2充入CO和 ,测得CO的平衡转化率与温度和压强的关系如图所示:
,测得CO的平衡转化率与温度和压强的关系如图所示:
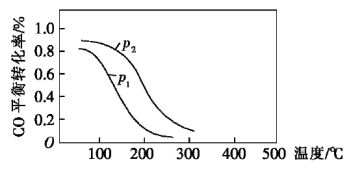
200℃时 随时间的变化如下表所示:
随时间的变化如下表所示:
①该反应的平衡常数表达式为
___________ ;
___________ (填“>”“<”或“=”)0。
②写出一条可同时提高反应速率和CO转化率的措施:___________ 。
③下列说法正确的是___________ (填字母)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强: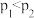
④0~1min内用 表示的反应速率
表示的反应速率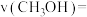
___________  。
。
⑤向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、4 mol 、2 mol
、2 mol  ,保持温度不变,则化学平衡
,保持温度不变,则化学平衡___________ (填“正向”“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。充入22.4L(折算为标准状况下)甲烷,测得电路中转移5.6mol电子,则甲烷的利用率为___________ 。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和
 ),
), 与
与 通入聚焦太阳能反应器,发生反应
通入聚焦太阳能反应器,发生反应
 。已知:
。已知:①


②


③
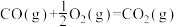

则

 、
、 、
、 的代数式表示)
的代数式表示)(2)用合成气生成甲醇的反应为

 ,在10L恒容密闭容器中按物质的量之比1:2充入CO和
,在10L恒容密闭容器中按物质的量之比1:2充入CO和 ,测得CO的平衡转化率与温度和压强的关系如图所示:
,测得CO的平衡转化率与温度和压强的关系如图所示:
200℃时
 随时间的变化如下表所示:
随时间的变化如下表所示:| t/min | 0 | 1 | 3 | 5 |
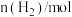 | 8.0 | 5.4 | 4.0 | 4.0 |
①该反应的平衡常数表达式为


②写出一条可同时提高反应速率和CO转化率的措施:
③下列说法正确的是
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强:
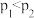
④0~1min内用
 表示的反应速率
表示的反应速率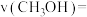
 。
。⑤向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、4 mol
 、2 mol
、2 mol  ,保持温度不变,则化学平衡
,保持温度不变,则化学平衡(3)甲烷、氧气和KOH溶液可组成燃料电池。充入22.4L(折算为标准状况下)甲烷,测得电路中转移5.6mol电子,则甲烷的利用率为
您最近一年使用:0次
2021-11-23更新
|
222次组卷
|
3卷引用:黑龙江省哈尔滨市第一中学校 2021-2022学年高三上学期期末考试理综化学试题
名校
2 . 用 代替
代替 与燃料CO反应,既可以提高燃烧效率,又能得到高纯
与燃料CO反应,既可以提高燃烧效率,又能得到高纯 ,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
①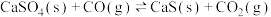
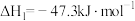
②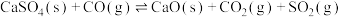
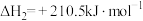
③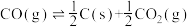
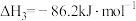
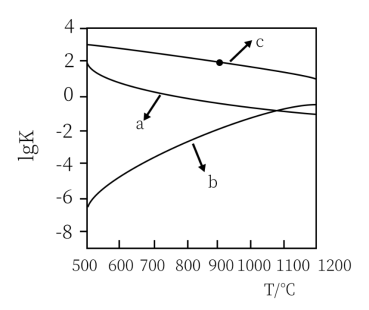
(1)反应①~③的平衡常数的对数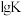 随反应温度T的变化曲线如图中所示,图中曲线b对应反应
随反应温度T的变化曲线如图中所示,图中曲线b对应反应___________ (填①、②或③,判断依据是___________ 。
(2)反应①的
___________ (用表达式表示)。向盛有 的真空恒容容器中充入CO,反应①于900℃达到平衡,平衡时测得
的真空恒容容器中充入CO,反应①于900℃达到平衡,平衡时测得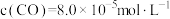 ,结合上图曲线c中相关数据,计算CO的平衡转化率为
,结合上图曲线c中相关数据,计算CO的平衡转化率为___________ (忽略副反应,结果保留2位有效数字)。
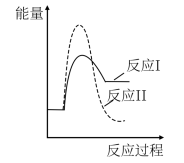
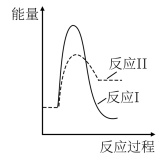
(3)假设某温度下,反应②的速率(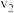 )大于反应①的速率(
)大于反应①的速率(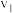 ),则下列反应过程能量变化示意图正确的是
),则下列反应过程能量变化示意图正确的是___________ 。
(4)恒温恒容条件下,假设反应①和②同时发生,且 ,则反应体系中
,则反应体系中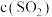 随时间t变化的趋势为
随时间t变化的趋势为___________ 。
 代替
代替 与燃料CO反应,既可以提高燃烧效率,又能得到高纯
与燃料CO反应,既可以提高燃烧效率,又能得到高纯 ,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。①
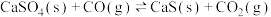
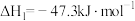
②
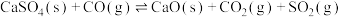
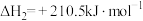
③
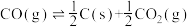
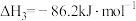
(1)反应①~③的平衡常数的对数
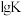 随反应温度T的变化曲线如图中所示,图中曲线b对应反应
随反应温度T的变化曲线如图中所示,图中曲线b对应反应
(2)反应①的

 的真空恒容容器中充入CO,反应①于900℃达到平衡,平衡时测得
的真空恒容容器中充入CO,反应①于900℃达到平衡,平衡时测得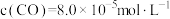 ,结合上图曲线c中相关数据,计算CO的平衡转化率为
,结合上图曲线c中相关数据,计算CO的平衡转化率为(3)假设某温度下,反应②的速率(
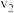 )大于反应①的速率(
)大于反应①的速率(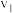 ),则下列反应过程能量变化示意图正确的是
),则下列反应过程能量变化示意图正确的是| A | B | C | D |
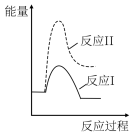 | 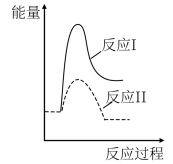 |  |  |
(4)恒温恒容条件下,假设反应①和②同时发生,且
 ,则反应体系中
,则反应体系中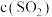 随时间t变化的趋势为
随时间t变化的趋势为
您最近一年使用:0次
名校
3 . 当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。
(1)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热数据如表:
则25℃时 和C(石墨,s)生成
和C(石墨,s)生成 的热化学方程式为
的热化学方程式为___________ 。
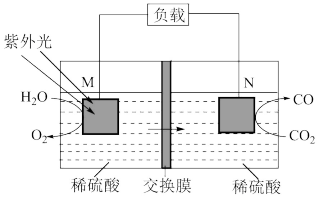
(2)某科研小组用电化学方法将 转化为CO实现再利用,转化的基本原理如图所示。M极的电极反应式
转化为CO实现再利用,转化的基本原理如图所示。M极的电极反应式___________ ,图中箭头所示为___________ 离子(填“ ”或“
”或“ ”)的迁移方向。当转化2mol
”)的迁移方向。当转化2mol 时,外电路转移电子的电量为
时,外电路转移电子的电量为___________ 。(已知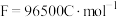 )
)
(3)我国科学家研究 电池,取得了重大科研成果,该电池中,
电池,取得了重大科研成果,该电池中, 为单质锂片,则该电池中的
为单质锂片,则该电池中的 在
在___________ (填“正”或“负”)极发生电化学反应。研究表明,该电池反应产物为碳酸锂和单质碳,且 电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。
电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。
Ⅰ. Ⅱ.
Ⅱ.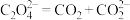
Ⅲ.___________ Ⅳ.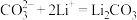
(1)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热数据如表:
| 物质 |  (g) (g) | C(石墨,s) |  |
燃烧热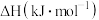 | −285.8 | −393.5 | −3267.5 |
则25℃时
 和C(石墨,s)生成
和C(石墨,s)生成 的热化学方程式为
的热化学方程式为(2)某科研小组用电化学方法将
 转化为CO实现再利用,转化的基本原理如图所示。M极的电极反应式
转化为CO实现再利用,转化的基本原理如图所示。M极的电极反应式 ”或“
”或“ ”)的迁移方向。当转化2mol
”)的迁移方向。当转化2mol 时,外电路转移电子的电量为
时,外电路转移电子的电量为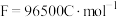 )
)
(3)我国科学家研究
 电池,取得了重大科研成果,该电池中,
电池,取得了重大科研成果,该电池中, 为单质锂片,则该电池中的
为单质锂片,则该电池中的 在
在 电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。
电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。Ⅰ.
 Ⅱ.
Ⅱ.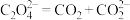
Ⅲ.
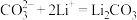
您最近一年使用:0次
名校
4 . 已知热化学方程式: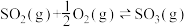
 ,向容器中充入4mol
,向容器中充入4mol 和4mol
和4mol ,当放出157.15kJ热量时,
,当放出157.15kJ热量时, 的转化率最接近于
的转化率最接近于
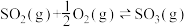
 ,向容器中充入4mol
,向容器中充入4mol 和4mol
和4mol ,当放出157.15kJ热量时,
,当放出157.15kJ热量时, 的转化率最接近于
的转化率最接近于| A.40% | B.50% | C.80% | D.90% |
您最近一年使用:0次
5 . O2对人类有着重要的作用。请回答下列问题:
(1)甲醇是一种绿色可再生能源,已知热化学方程式:
ⅰ. 2CO(g)+O2(g)=2CO2(g) ΔH1=-566.0kJ•mol-1
ⅱ. 2H2(g)+O2(g)=2H2O(g) ΔH2=-483.6kJ•mol-1
ⅲ. CO(g)+2H2(g)=CH3OH(g) ΔH3=-574.4kJ•mol-1
则计算CH3OH(g)+ O2(g)=CO2(g)+2H2O(g)的ΔH=
O2(g)=CO2(g)+2H2O(g)的ΔH=_______ kJ•mol-1。
(2)合成硝酸工艺中涉及到反应:2NO(g)+O2(g)=2NO2(g)、2NO2(g) N2O4(g)。T℃时,在恒容密闭容器中以投料比
N2O4(g)。T℃时,在恒容密闭容器中以投料比 =1:1进行投料,容器内总压强p的变化如下表:
=1:1进行投料,容器内总压强p的变化如下表:
已知:a. 2NO2(g) N2O4(g)可认为迅速达到平衡状态。b.时间t=∞时,NO(g)完全反应。
N2O4(g)可认为迅速达到平衡状态。b.时间t=∞时,NO(g)完全反应。
①已知时间为t1min时,测得容器内O2分压p(O2)=10.6 kPa,则此时NO的分压p(NO)_______ kPa。
②T℃时,可逆反应2NO2(g) N2O4(g)的平衡常数Kp=
N2O4(g)的平衡常数Kp=_______ kPa -1(用平衡分压代替平衡浓度计算,分压=总压×体积分数,写出计算式即可),NO2的平衡转化率为_______ %(保留2位有效数字)。
③若将上述反应容器内温度升高至(T+50)℃,达到平衡时,容器内混合气体的平均相对分子质量减小,则2NO2(g) N2O4(g)ΔH
N2O4(g)ΔH_______ 0(填“>”或“<”)。
(3)人体内化学反应时刻需要O2参与,如广泛存在于肌肉中的肌红蛋白(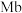 ),具有结合O2的能力,可表示为Mb(aq)+O2(g)
),具有结合O2的能力,可表示为Mb(aq)+O2(g) MbO2(aq)。肌红蛋白的结合度(即转化率α)与平衡时的氧气分压p(O2)密切相关,其变化曲线如图1,37℃时,测得平衡常数K=2(气体和溶液中的溶质分别用分压和物质的量浓度表达)。
MbO2(aq)。肌红蛋白的结合度(即转化率α)与平衡时的氧气分压p(O2)密切相关,其变化曲线如图1,37℃时,测得平衡常数K=2(气体和溶液中的溶质分别用分压和物质的量浓度表达)。
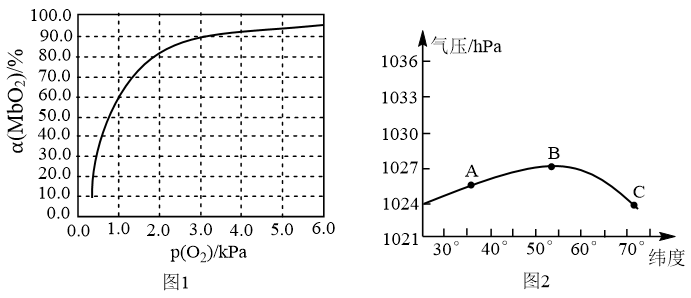
①平衡时,平衡常数表达式K=_______ [用含α和p(O2)的代数式表示];37℃时,测得人正常呼吸时α的最大值为97.7%,则空气中氧气分压p(O2)=_______ kPa(保留3位有效数字)。
②某天不同纬度的大气压变化曲线如图2所示,某运动员处于A、B、C不同位置时,其体内MbO2的浓度最大位置为_______ (填“A”“B”或“C”)。
(1)甲醇是一种绿色可再生能源,已知热化学方程式:
ⅰ. 2CO(g)+O2(g)=2CO2(g) ΔH1=-566.0kJ•mol-1
ⅱ. 2H2(g)+O2(g)=2H2O(g) ΔH2=-483.6kJ•mol-1
ⅲ. CO(g)+2H2(g)=CH3OH(g) ΔH3=-574.4kJ•mol-1
则计算CH3OH(g)+
 O2(g)=CO2(g)+2H2O(g)的ΔH=
O2(g)=CO2(g)+2H2O(g)的ΔH=(2)合成硝酸工艺中涉及到反应:2NO(g)+O2(g)=2NO2(g)、2NO2(g)
 N2O4(g)。T℃时,在恒容密闭容器中以投料比
N2O4(g)。T℃时,在恒容密闭容器中以投料比 =1:1进行投料,容器内总压强p的变化如下表:
=1:1进行投料,容器内总压强p的变化如下表:| t/min | 0 | 40 | 80 | 160 | 260 | 700 |  |
| p/kPa | 33.2 | 28.6 | 27.1 | 26.3 | 25.9 | 25.2 | 22.3 |
已知:a. 2NO2(g)
 N2O4(g)可认为迅速达到平衡状态。b.时间t=∞时,NO(g)完全反应。
N2O4(g)可认为迅速达到平衡状态。b.时间t=∞时,NO(g)完全反应。①已知时间为t1min时,测得容器内O2分压p(O2)=10.6 kPa,则此时NO的分压p(NO)
②T℃时,可逆反应2NO2(g)
 N2O4(g)的平衡常数Kp=
N2O4(g)的平衡常数Kp=③若将上述反应容器内温度升高至(T+50)℃,达到平衡时,容器内混合气体的平均相对分子质量减小,则2NO2(g)
 N2O4(g)ΔH
N2O4(g)ΔH(3)人体内化学反应时刻需要O2参与,如广泛存在于肌肉中的肌红蛋白(
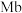 ),具有结合O2的能力,可表示为Mb(aq)+O2(g)
),具有结合O2的能力,可表示为Mb(aq)+O2(g) MbO2(aq)。肌红蛋白的结合度(即转化率α)与平衡时的氧气分压p(O2)密切相关,其变化曲线如图1,37℃时,测得平衡常数K=2(气体和溶液中的溶质分别用分压和物质的量浓度表达)。
MbO2(aq)。肌红蛋白的结合度(即转化率α)与平衡时的氧气分压p(O2)密切相关,其变化曲线如图1,37℃时,测得平衡常数K=2(气体和溶液中的溶质分别用分压和物质的量浓度表达)。
①平衡时,平衡常数表达式K=
②某天不同纬度的大气压变化曲线如图2所示,某运动员处于A、B、C不同位置时,其体内MbO2的浓度最大位置为
您最近一年使用:0次
2021-11-20更新
|
574次组卷
|
2卷引用:黑龙江省大庆铁人中学2021-2022学年高三上学期第二次月考化学试题
6 . SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:
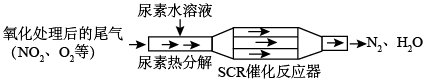
尿素[CO(NH2)2]水溶液热分解为NH3和CO2,请写出CO2的电子式___________ 。
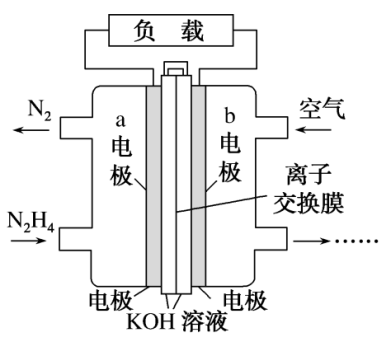
(2)肼(N2H4)可以用作燃料电池的原料。肼的结构式为___________ ;一种以液态肼为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。a电极是电极的___________ 极(填“正”或“负”),a电极的电极反应式为___________ 。
(3)已知:N2(g)+O2(g)=2NO(g)△H1=+180.5kJ·mol-1
C(s)+O2(g)=CO2(g)△H2=-393.5kJ·mol-1
2C(s)+O2(g)=2CO(g)△H3=-221.0kJ·mol-1
若某反应的平衡常数表达式为K=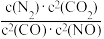 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式___________ 。
(4)已知植物光合作用发生的反应如下:6CO2(g)+6H2O(l)⇌C6H12O6(s)+6O2(g)△H=+669.62kJ/mol,该反应达到化学平衡后,若改变下列条件,CO2转化率增大的是___________ 。
a.增大CO2的浓度b.取走一半C6H12O6c.加入催化剂d.适当升高温度
(5)N2O5的分解反应2N2O5(g)⇌4NO2(g)+O2(g),由实验测得在67℃时N2O5的浓度随时间的变化如下:
计算在0~2min时段,化学反应速率v(NO2)=___________ mol∙L-1∙min-1。
(1)SCR(选择性催化还原)工作原理:

尿素[CO(NH2)2]水溶液热分解为NH3和CO2,请写出CO2的电子式
(2)肼(N2H4)可以用作燃料电池的原料。肼的结构式为

(3)已知:N2(g)+O2(g)=2NO(g)△H1=+180.5kJ·mol-1
C(s)+O2(g)=CO2(g)△H2=-393.5kJ·mol-1
2C(s)+O2(g)=2CO(g)△H3=-221.0kJ·mol-1
若某反应的平衡常数表达式为K=
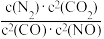 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式(4)已知植物光合作用发生的反应如下:6CO2(g)+6H2O(l)⇌C6H12O6(s)+6O2(g)△H=+669.62kJ/mol,该反应达到化学平衡后,若改变下列条件,CO2转化率增大的是
a.增大CO2的浓度b.取走一半C6H12O6c.加入催化剂d.适当升高温度
(5)N2O5的分解反应2N2O5(g)⇌4NO2(g)+O2(g),由实验测得在67℃时N2O5的浓度随时间的变化如下:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| C(N2O5)/(mol·L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
计算在0~2min时段,化学反应速率v(NO2)=
您最近一年使用:0次
2021-11-19更新
|
103次组卷
|
2卷引用:黑龙江省龙东地区四校2021-2022学年高三上学期第一次联考化学试题
名校
7 . 研究表明I-可以作为水溶液中SO2歧化反应的催化剂:3SO2(g)+2H2O (l)=2H2SO4 (aq)+S(s) ΔH<0;该过程一般通过如下步骤来实现:①SO2(g)+4I-(aq)+4H+(aq)= S(s)+ 2I2(g) + 2H2O(l) ΔH>0;②I2(g)+2H2O(l)+SO2(g)=SO (aq)+4H+(aq)+2I-(aq) ΔH<0;已知反应①为慢反应,示意图中能体现上述反应过程中能量变化的是
(aq)+4H+(aq)+2I-(aq) ΔH<0;已知反应①为慢反应,示意图中能体现上述反应过程中能量变化的是
 (aq)+4H+(aq)+2I-(aq) ΔH<0;已知反应①为慢反应,示意图中能体现上述反应过程中能量变化的是
(aq)+4H+(aq)+2I-(aq) ΔH<0;已知反应①为慢反应,示意图中能体现上述反应过程中能量变化的是A.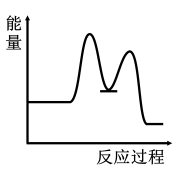 | B.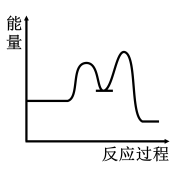 |
C.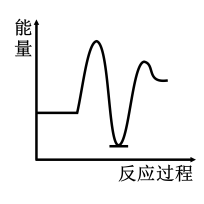 | D.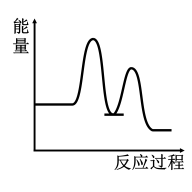 |
您最近一年使用:0次
2021-11-18更新
|
1083次组卷
|
14卷引用:黑龙江省大庆市2022届高三上学期第一次教学质量检测化学试题
黑龙江省大庆市2022届高三上学期第一次教学质量检测化学试题黑龙江省肇东市第四中学2021-2022学年高三12月月考化学试题(已下线)2021年1月浙江高考化学试题变式题21-25黑龙江省哈尔滨市第三十二中学2021-2022学年高三上学期期末考试化学试题黑龙江省大庆市2023-2024学年高三上学期第一次模拟考试化学试题河北省邯郸市第一中学2021-2022学年上学期高三上学期1月调研化学试题广东省珠海市2021-2022学年高二上学期期末考试化学试题广东省三校联考2022-2023学年高二上学期期中考试化学试题湖北省部分省级示范高中(四校联考)2022-2023学年高二上学期期末测试化学试题湖南省宁乡市2022-2023学年高二上学期期末考试化学试题湖北省宜昌市部分省级示范高中校级联合体2022-2023学年高二下学期期中考试化学试题广东省广州市三校2023—2024学年高二上学期期中联考化学考试广东省佛山市顺德区第一中学2023-2024学年高二上学期11月期中考试化学试题广东省广州市为明学校2023-2024学年高二上学期学情调研考化学试题
名校
8 . 工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
(1)已知: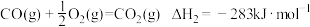

则表示1mol气态甲醇完全燃烧生成 和水蒸气时的热化学方程式为
和水蒸气时的热化学方程式为___________ 。
(2)CO和H2为原料合成甲醇,下列措施中有利于增大该反应的反应速率且利于反应正向进行的是___________(填字母)。
(3) 时,CO和H2为原料合成甲醇,在体积为2L的密闭容器中加入
时,CO和H2为原料合成甲醇,在体积为2L的密闭容器中加入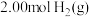 和
和 。CO(g)的物质的量随时间的变化如表:
。CO(g)的物质的量随时间的变化如表:
根据表中数据回答:
①氢气平衡转化率为___________ 。
② 时,该反应的平衡常数为
时,该反应的平衡常数为___________ 。
③保持其它条件不变,向平衡体系中充入1molCO(g)、 、
、 。此时
。此时
___________  (填“>”“<”或“=”)
(填“>”“<”或“=”)
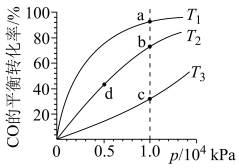
(4)CO和H2为原料合成甲醇,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示,下列说法正确的是___________

(1)已知:
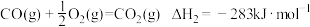

则表示1mol气态甲醇完全燃烧生成
 和水蒸气时的热化学方程式为
和水蒸气时的热化学方程式为(2)CO和H2为原料合成甲醇,下列措施中有利于增大该反应的反应速率且利于反应正向进行的是___________(填字母)。
| A.随时将CH3OH与反应混合物分离 | B.降低反应温度 |
| C.增大体系压强 | D.便用高效催化剂 |
 时,CO和H2为原料合成甲醇,在体积为2L的密闭容器中加入
时,CO和H2为原料合成甲醇,在体积为2L的密闭容器中加入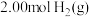 和
和 。CO(g)的物质的量随时间的变化如表:
。CO(g)的物质的量随时间的变化如表:| 时间/s | 0 | 2 | 5 | 10 | 20 | 40 | 80 |
| 物质的量(mol) | 1.00 | 0.50 | 0.375 | 0.25 | 0.20 | 0.20 | 0.20 |
根据表中数据回答:
①氢气平衡转化率为
②
 时,该反应的平衡常数为
时,该反应的平衡常数为③保持其它条件不变,向平衡体系中充入1molCO(g)、
 、
、 。此时
。此时
 (填“>”“<”或“=”)
(填“>”“<”或“=”)(4)CO和H2为原料合成甲醇,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示,下列说法正确的是___________

| A.温度:T1>T2>T3 |
| B.正反应速率:v(a)>v(c)、v(b)>v(d) |
| C.反应速率:v正(d)<v逆(c) |
| D.平均摩尔质量:M(a)>M(c)、M(b)<M(d) |
您最近一年使用:0次
名校
9 . 工业合成三氧化硫的反应为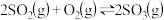

 ,反应过程可用下图模拟(
,反应过程可用下图模拟( 代表氧原子,
代表氧原子, 代表硫原子,
代表硫原子,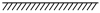 代表催化剂),下列说法正确的是
代表催化剂),下列说法正确的是

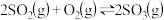

 ,反应过程可用下图模拟(
,反应过程可用下图模拟( 代表氧原子,
代表氧原子, 代表硫原子,
代表硫原子, 代表催化剂),下列说法正确的是
代表催化剂),下列说法正确的是
| A.过程II放热,过程III吸热 |
B.充入2mol 发生上述反应的逆反应,吸收的热量小于198kJ 发生上述反应的逆反应,吸收的热量小于198kJ |
C.催化剂可增大反应的活化分子百分数,使 减小 减小 |
| D.2molSO2和1molO2的总能量小于2molSO3的能量 |
您最近一年使用:0次
2021-11-13更新
|
82次组卷
|
2卷引用:黑龙江省双鸭山市第一中学2021-2022学年高二上学期期中考试化学试题
10 . 氮氧化物(NOx)是一种主要的大气污染物,必须进行处理。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
①ΔH 1___________ 0,ΔH 3___________ 0.(填“>”或“<”)
②N2(g)+O2(g) = 2NO(g) ΔH=___________ kJ·mol-1
(2)利用NH3在一定条件下与NO反应生成无污染的气体。其热化学方程式为:4NH3 (g)+6NO(g) =5N2(g)+6H2O(g) ΔH=-1807.98 kJ·mol-1,下列能表示该反应中能量变化的是___________ (填字母)。
A.
B.
C 。
。
(3)利用甲烷催化还原氮氧化物。已知:
CH4 (g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
H2O(l) = H2O(g) ΔH=+44 kJ·mol-1
则CH4 (g)+2NO2(g)=N2 (g)+CO2(g)+2H2O(g) ΔH=___________ ,1.6 g CH4还原NO2 生成N2和液态水时放出的热量为___________ kJ。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
| 反应 | N2(g)→2N(g) | O2(g)→2O(g) | N(g)+O(g)→NO(g) |
| 反应热 | ΔH 1 | ΔH 2 | ΔH 3 |
| 热量值kJ·mol-1 | 945 | 498 | 630 |
①ΔH 1
②N2(g)+O2(g) = 2NO(g) ΔH=
(2)利用NH3在一定条件下与NO反应生成无污染的气体。其热化学方程式为:4NH3 (g)+6NO(g) =5N2(g)+6H2O(g) ΔH=-1807.98 kJ·mol-1,下列能表示该反应中能量变化的是
A.

B.

C
 。
。(3)利用甲烷催化还原氮氧化物。已知:
CH4 (g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
H2O(l) = H2O(g) ΔH=+44 kJ·mol-1
则CH4 (g)+2NO2(g)=N2 (g)+CO2(g)+2H2O(g) ΔH=
您最近一年使用:0次



