1 . 碳单质及其化合物在生产生活中用途广泛。
I.单质碳经常应用于化学反应中。回答以下问题:
(1)炭黑可以活化氧分子得到活化氧(O*),活化氧可以快速氧化SO2,从而消除雾霾。其活化过程中的能量变化如图所示,则生成活化氧的△H=______ 0(填“>”、“<”或“=”),活化过程中有水时的活化能降低了______ eV。

(2)以焦炭为原料,在高温下与水蒸气反应可制得水煤气,涉及反应如下:
a.C(s)+H2O(g)=CO(g)+H2(g) ΔH1
b.C(s)+2H20(g)=CO2(g)+2H2(g) ΔH2=+90.3kJ·mol-1
c.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.0kJ·mol-1
①ΔH1=______ kJ·mol-1。
②对于反应a,测得在不同温度下H2O(g)的转化率如图所示,图中T1、T2、T3的大小关系为______ 。用物质的平衡分压代替物质的量浓度也可以表示化学反应的平衡常数(Kp),在T1℃、50 MPa时,反应a的平衡常数Kp=______ MPa(已知气体分压=气体总压×各气体的体积分数,结果保留两位小数)。

II.甲醇(CH3OH)是一种重要的化工原料,合成甲醇的主要反应为:CO(g)+2H2(g)=CH3OH(g)。原料气的加工过程中常常混有一定量CO2,为了研究不同温度下CO2对该反应的影响,以CO2、CO和H2的混合气体为原料在一定条件下进行实验,结果表明,原料气各组分含量不同时,反应生成甲醇和副产物甲烷的碳转化率是不相同的。实验数据见下表:
(3)在一定条件下,反应温度越高,碳转化率______ 。
(4)CO2对甲醇合成的影响是______ 。
Ⅲ.甲醇可以制备二甲醚:2CH3OH(g)=CH3OCH3(g)+H2O(g)。经查阅资料:该反应压强平衡常数的计算式为:lnKp=-2.205+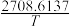 (T为热力学温度:热力学温度=摄氏度+273)。
(T为热力学温度:热力学温度=摄氏度+273)。
(5)在一定温度范围内,随温度升高,甲醇生成二甲醚的倾向______ 。(填“增大”、“减小”或“不变”)。
(6)200℃时,在密闭容器中加入一定量甲醇,反应达到平衡状态时,体系中二甲醚的物质的量分数是______ 。
A.> B.
B.  C.
C.  ~
~ D.
D.  E.<
E.< 
I.单质碳经常应用于化学反应中。回答以下问题:
(1)炭黑可以活化氧分子得到活化氧(O*),活化氧可以快速氧化SO2,从而消除雾霾。其活化过程中的能量变化如图所示,则生成活化氧的△H=

(2)以焦炭为原料,在高温下与水蒸气反应可制得水煤气,涉及反应如下:
a.C(s)+H2O(g)=CO(g)+H2(g) ΔH1
b.C(s)+2H20(g)=CO2(g)+2H2(g) ΔH2=+90.3kJ·mol-1
c.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.0kJ·mol-1
①ΔH1=
②对于反应a,测得在不同温度下H2O(g)的转化率如图所示,图中T1、T2、T3的大小关系为

II.甲醇(CH3OH)是一种重要的化工原料,合成甲醇的主要反应为:CO(g)+2H2(g)=CH3OH(g)。原料气的加工过程中常常混有一定量CO2,为了研究不同温度下CO2对该反应的影响,以CO2、CO和H2的混合气体为原料在一定条件下进行实验,结果表明,原料气各组分含量不同时,反应生成甲醇和副产物甲烷的碳转化率是不相同的。实验数据见下表:
| CO2%-CO%-H2% (体积分数) | 0-30-70 | 4-26-70 | 8-22-70 | 20-10-70 | |||||||||
| 反应温度/℃ | 225 | 235 | 250 | 225 | 235 | 250 | 225 | 235 | 250 | 225 | 235 | 250 | |
| 碳转化率(%) | CH3OH | 4.9 | 8.8 | 11.0 | 19.0 | 33.1 | 56.5 | 17.7 | 33.4 | 54.4 | 8.0 | 12.0 | 22.6 |
| CH4 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 2.8 | 2.8 | 2.8 | |
(3)在一定条件下,反应温度越高,碳转化率
(4)CO2对甲醇合成的影响是
Ⅲ.甲醇可以制备二甲醚:2CH3OH(g)=CH3OCH3(g)+H2O(g)。经查阅资料:该反应压强平衡常数的计算式为:lnKp=-2.205+
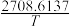 (T为热力学温度:热力学温度=摄氏度+273)。
(T为热力学温度:热力学温度=摄氏度+273)。(5)在一定温度范围内,随温度升高,甲醇生成二甲醚的倾向
(6)200℃时,在密闭容器中加入一定量甲醇,反应达到平衡状态时,体系中二甲醚的物质的量分数是
A.>
 B.
B.  C.
C.  ~
~ D.
D.  E.<
E.< 
您最近一年使用:0次
名校
解题方法
2 . 我国科研人员在银催化简单烷烃的区域选择性方面取得了重要突破,有效克服烷烃 键的惰性并实现其区域选择性活化。一种对烷烃
键的惰性并实现其区域选择性活化。一种对烷烃 键的选择性插入反应进程如图所示。下列说法正确的是
键的选择性插入反应进程如图所示。下列说法正确的是

 键的惰性并实现其区域选择性活化。一种对烷烃
键的惰性并实现其区域选择性活化。一种对烷烃 键的选择性插入反应进程如图所示。下列说法正确的是
键的选择性插入反应进程如图所示。下列说法正确的是
| A.Ⅰ、Ⅱ、Ⅲ三种物质中,最稳定的是Ⅱ |
| B.总反应速率取决于由中间体1生成中间体2的一步 |
| C.升高温度三个反应的速率均加快,有利于提高烷烃的转化率 |
| D.催化剂对化学反应具有选择性,生成不同产物的同时改变了反应的焓变 |
您最近一年使用:0次
2021-01-27更新
|
422次组卷
|
4卷引用:安徽省涡阳县育萃高级中学2020-2021学年高二下学期第一次月考化学试题
3 . 氮氧化物(NO、NO2)、SO2是大气污染物。回答下列问题:
(1)污染物对自然环境造成的污染有____________ (写一种即可)。
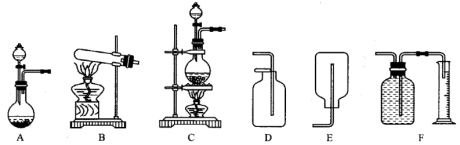
(2)图1包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2应选择的装置是____________ (填字母)。
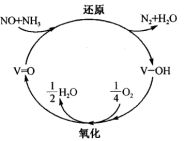
(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。催化反应机理如图2所示,写出该反应发生的化学方程式:____________ 。
(4)目前,NaClO溶液广泛地应用于脱硫脱硝。
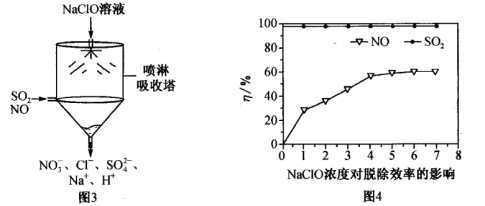
①某课外小组同学设计了如图喷淋吸收塔装置(如图3)。设计该装置的优点是____________ ,脱硝(NO)反应的离子方程式为____________ 。
②如图4为NaClO浓度对脱硫脱硝效率(η/%)的影响。当温度为50℃,溶液的pH=10,c(SO2)=c(NO)=300 mg·m-3,SO2的脱除效率一直维持在98%以上,而NO脱除效率相对较低,其原因是____________ 。
(5)研究表明,ZnO水悬浊液能有效地吸收SO2,然后再经O2催化氧化,可得到硫酸盐。已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-,SO32-的物质的量分数(物质的量分数= )随pH的分布如图5所示。
)随pH的分布如图5所示。
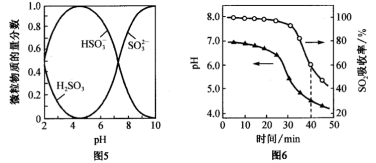
向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40 min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(如图6)。溶液pH几乎不变阶段,主要产物是____________ (填化学式);SO2吸收率迅速降低阶段,主要反应的离子方程式为____________ 。
(1)污染物对自然环境造成的污染有
(2)图1包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2应选择的装置是

(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。催化反应机理如图2所示,写出该反应发生的化学方程式:

(4)目前,NaClO溶液广泛地应用于脱硫脱硝。
①某课外小组同学设计了如图喷淋吸收塔装置(如图3)。设计该装置的优点是
②如图4为NaClO浓度对脱硫脱硝效率(η/%)的影响。当温度为50℃,溶液的pH=10,c(SO2)=c(NO)=300 mg·m-3,SO2的脱除效率一直维持在98%以上,而NO脱除效率相对较低,其原因是

(5)研究表明,ZnO水悬浊液能有效地吸收SO2,然后再经O2催化氧化,可得到硫酸盐。已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-,SO32-的物质的量分数(物质的量分数=
 )随pH的分布如图5所示。
)随pH的分布如图5所示。
向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40 min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(如图6)。溶液pH几乎不变阶段,主要产物是
您最近一年使用:0次
名校
4 . NO是大气中一种重要污染物,可以采用多种方法消除NO的污染。回答下列问题:
(1)CH4还原NO法
已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-116.2 kJ·mol-1;
②N2(g)+O2(g)=2NO(g) △H2=+180 kJ·mol-1;
③CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H3=-863.8 kJ·mol-1。
则CH4与NO反应生成N2、CO2和H2O(g)的热化学方程式为_______ 。
(2)CO还原NO法。CO还原NO的反应为2CO(g)+2NO(g)⇌2CO2(g)+N2(g) △H<0。
①该反应中,既要加快NO的消除速率,又要消除更多的NO,可采取措施有_______ (写出其中一条即可)。
②实验测得:v正=k正·c2(CO)·c2(NO),v逆=k逆·c2(CO2)·c(N2)(k正、k逆为速率常数,只与温度有关)。达到平衡后,只升高温度,k正增大的倍数_______ (填“>”、“<”或“=”) k逆增大的倍数。若在1 L恒容密闭容器中充入1 mol CO和1 mol NO发生上述反应,在一定温度下反应达到平衡时,CO的转化率为40%,则 =
=_______ (计算结果用分数表示)。
(3)NH3还原NO法。NH3还原NO的反应为4NH3(g)+6NO(g)⇌5N2(g)+6H2O(g) △H<0。T℃时,在恒容密闭容器中,测得在不同时间NO和NH3的物质的量如下表:
若反应开始时的压强为P0,则该反应的化学平衡常数Kp=_______ (可用分数表示;用平衡分压代替平衡浓度计算,各气体的分压=气体总压×各气体的物质的量分数)。
(4)SCR脱硝技术的主反应为4NH3(g)+4NO(g)+O2(g)⇌4N2(g)+6H2O(g) △H<0。在密闭容器中起始投入一定量NH3、NO、O2进行反应,测得不同温度下,在相同时间内部分组分的含量如图所示。

①a、b、c三点,主反应速率由大到小的顺序为_______ 。
②解释N2的浓度变化曲线先上升后下降的原因:_______ 。
(1)CH4还原NO法
已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-116.2 kJ·mol-1;
②N2(g)+O2(g)=2NO(g) △H2=+180 kJ·mol-1;
③CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H3=-863.8 kJ·mol-1。
则CH4与NO反应生成N2、CO2和H2O(g)的热化学方程式为
(2)CO还原NO法。CO还原NO的反应为2CO(g)+2NO(g)⇌2CO2(g)+N2(g) △H<0。
①该反应中,既要加快NO的消除速率,又要消除更多的NO,可采取措施有
②实验测得:v正=k正·c2(CO)·c2(NO),v逆=k逆·c2(CO2)·c(N2)(k正、k逆为速率常数,只与温度有关)。达到平衡后,只升高温度,k正增大的倍数
 =
=(3)NH3还原NO法。NH3还原NO的反应为4NH3(g)+6NO(g)⇌5N2(g)+6H2O(g) △H<0。T℃时,在恒容密闭容器中,测得在不同时间NO和NH3的物质的量如下表:
| 时间/min | 0 | 1 | 2 | 3 | 4 |
| n(NO)/mol | 1.2 | 0.90 | 0.72 | 0.60 | 0.60 |
| n(NH3)/mol | 0.90 | 0.70 | 0.58 | 0.50 | 0.50 |
(4)SCR脱硝技术的主反应为4NH3(g)+4NO(g)+O2(g)⇌4N2(g)+6H2O(g) △H<0。在密闭容器中起始投入一定量NH3、NO、O2进行反应,测得不同温度下,在相同时间内部分组分的含量如图所示。

①a、b、c三点,主反应速率由大到小的顺序为
②解释N2的浓度变化曲线先上升后下降的原因:
您最近一年使用:0次
2021-01-06更新
|
225次组卷
|
2卷引用:安徽省池州市东至县2021届高三上学期12月大联考化学试题
5 . 工业上除去电石渣浆 含
含 上清液中的
上清液中的 ,并制取石膏
,并制取石膏 的常用流程如下:
的常用流程如下:

下列说法正确的是
 含
含 上清液中的
上清液中的 ,并制取石膏
,并制取石膏 的常用流程如下:
的常用流程如下:
下列说法正确的是

A. 、 、 在过程Ⅰ、Ⅱ中均起催化剂作用 在过程Ⅰ、Ⅱ中均起催化剂作用 |
B.过程Ⅰ中,反应的离子方程式为 |
C.将10L上清液中的 转化为 转化为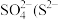 浓度为480 mg·L−1),理论上共需要0.03mol的 浓度为480 mg·L−1),理论上共需要0.03mol的 |
D.常温下,56gCaO溶于水配成1L溶液,溶液中 的数目为 的数目为 个 个 |
您最近一年使用:0次
2021-01-02更新
|
549次组卷
|
5卷引用:安徽省示范高中皖北协作区2020年第22届高三联考理科综合化学
安徽省示范高中皖北协作区2020年第22届高三联考理科综合化学(已下线)小题必刷08 氧化还原反应的规律及应用——2021年高考化学一轮复习小题必刷(通用版)江西省南昌市新建区第二中学2019-2020学年高二下学期期终考试化学试题湖北省龙泉中学、宜昌一中2021届高三下学期2月联合考试化学试题黑龙江省大庆实验中学实验一部2020-2021学年高一下学期开学考试化学试题
解题方法
6 . “丁烯裂解法” 是另一种生产丙烯的方法,但生产过程中伴有生成乙烯的副反应发生,具体反应如下:主反应:3C4H8 4C3H6,副反应:C4H8
4C3H6,副反应:C4H8 2C2H4,下图是平衡时各物质的百分含量随温度或压强的变化趋势:
2C2H4,下图是平衡时各物质的百分含量随温度或压强的变化趋势:
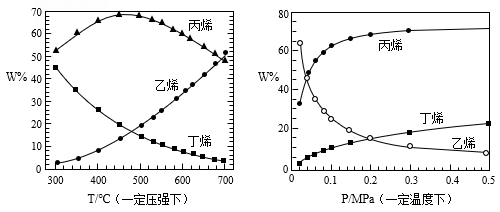
从产物纯度的角度考虑,丙烯和乙烯的质量比越高越好,则下列反应条件最适宜的是
 4C3H6,副反应:C4H8
4C3H6,副反应:C4H8 2C2H4,下图是平衡时各物质的百分含量随温度或压强的变化趋势:
2C2H4,下图是平衡时各物质的百分含量随温度或压强的变化趋势:
从产物纯度的角度考虑,丙烯和乙烯的质量比越高越好,则下列反应条件最适宜的是
| A.300℃ 0.1 MPa | B.700 ℃ 0.1 MPa |
| C.300℃ 0.5 MPa | D.700℃ 0.5 MPa |
您最近一年使用:0次
7 . 已知除去NO的一种反应如下:
主反应:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H
4N2(g)+6H2O(g) △H
副反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)
相同条件下,在甲、乙两种催化剂作用下进行上述反应。下列说法错误的是

主反应:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) △H
4N2(g)+6H2O(g) △H副反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)相同条件下,在甲、乙两种催化剂作用下进行上述反应。下列说法错误的是

| A.△H<0 |
| B.乙催化剂的催化效果要强于甲 |
| C.改变催化剂的选择性,可以减少副反应的发生 |
| D.相同条件下选择高效催化剂,可以提高M点的平衡转化率 |
您最近一年使用:0次
2020-12-14更新
|
348次组卷
|
4卷引用:安徽省淮北市树人高级中学2021-2022学年高二上学期第一次月考化学试题
安徽省淮北市树人高级中学2021-2022学年高二上学期第一次月考化学试题山东省潍坊市2020-2021学年高二上学期期中考试化学试题(已下线)练习5 化学反应的方向与调控-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)山东省泰安第十九中学2021-2022学年高二上学期期中考试化学试题
名校
8 . 下列事实不能用勒夏特列原理解释的是
| A.用排饱和食盐水法收集Cl2 |
| B.温度控制在500℃有利于合成氨反应 |
| C.增大压强有利于氨的合成 |
D.工业制取金属钾Na(l)+KCl(l) NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来 NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来 |
您最近一年使用:0次
2020-11-18更新
|
127次组卷
|
2卷引用:安徽省舒城中学2020-2021学年高二上学期第三次月考化学试题
名校
解题方法
9 . 对于反应2NO(g)+O2(g) 2NO2(g)的反应历程如下:
2NO2(g)的反应历程如下:
第一步:2NO(g)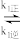 N2O2(g)(快速平衡)
N2O2(g)(快速平衡)
第二步:N2O2(g)+O2(g)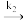 2NO2(g)(慢反应)
2NO2(g)(慢反应)
其中可近似认为第二步反应不影响第一步的平衡,第一步反应中:v正=k1正·c2(NO),v逆=k1逆·c(N2O2),k1正、k1逆为速率常数,仅受温度影响。
下列叙述正确的是( )
 2NO2(g)的反应历程如下:
2NO2(g)的反应历程如下:第一步:2NO(g)
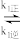 N2O2(g)(快速平衡)
N2O2(g)(快速平衡)第二步:N2O2(g)+O2(g)
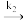 2NO2(g)(慢反应)
2NO2(g)(慢反应)其中可近似认为第二步反应不影响第一步的平衡,第一步反应中:v正=k1正·c2(NO),v逆=k1逆·c(N2O2),k1正、k1逆为速率常数,仅受温度影响。
下列叙述正确的是( )
| A.整个反应的速率由第一步反应速率决定 |
B.同一温度下,平衡时第一步反应的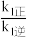 越大,反应正向程度越大 越大,反应正向程度越大 |
| C.第二步反应速率慢,因而平衡转化率也低 |
| D.第一步反应快的原因是第一步反应的活化能比第二步反应的活化能高 |
您最近一年使用:0次
2020-11-17更新
|
331次组卷
|
3卷引用:安徽省皖南名校2020-2021学年高二上学期期中考试化学试题
解题方法
10 . 研究氮及其化合物的性质及转化,对研究自然界中氮的循环有着重大的意义。
(1)科学家研究利用铁触媒合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。

由图可知合成氨反应N2(g)+3H2(g) 2NH3(g)的△H=
2NH3(g)的△H=___ kJ·mol-1。该历程中速率最慢的一步的化学方程式为___ 。
(2)NH3(g)的催化氧化是工业制备硝酸的重要反应。已知氨催化氧化时会发生如下两个竞争反应I、II。
4NH3(g)+5O2(g) 4NO(g)+6H2O(g) I
4NO(g)+6H2O(g) I
4NH3(g)+3O2(g) 2N2(g)+6H2O(g)△H<0 II
2N2(g)+6H2O(g)△H<0 II
为分析某催化剂对该反应的选择性,在1L密闭容器中充入1molNH3和2molO2,测得有关物质的物质的量与温度的关系如图所示。

①该催化剂在低温时选择反应___ (填“I”或“II”)。
②520℃时,4NH3(g)+3O2(g) 2N2(g)+6H2O(g)的平衡常数K=
2N2(g)+6H2O(g)的平衡常数K=___ (不要求得出计算结果,只需列出数字计算式)。
③C点比B点所产生的NO的物质的量少的主要原因是___ 。
(1)科学家研究利用铁触媒合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。

由图可知合成氨反应N2(g)+3H2(g)
 2NH3(g)的△H=
2NH3(g)的△H=(2)NH3(g)的催化氧化是工业制备硝酸的重要反应。已知氨催化氧化时会发生如下两个竞争反应I、II。
4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) I
4NO(g)+6H2O(g) I4NH3(g)+3O2(g)
 2N2(g)+6H2O(g)△H<0 II
2N2(g)+6H2O(g)△H<0 II为分析某催化剂对该反应的选择性,在1L密闭容器中充入1molNH3和2molO2,测得有关物质的物质的量与温度的关系如图所示。

①该催化剂在低温时选择反应
②520℃时,4NH3(g)+3O2(g)
 2N2(g)+6H2O(g)的平衡常数K=
2N2(g)+6H2O(g)的平衡常数K=③C点比B点所产生的NO的物质的量少的主要原因是
您最近一年使用:0次



