1 . 一定温度下,AgCl(s) Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
 Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是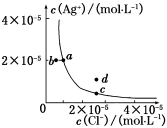
| A.加入AgNO3,可以使溶液由c点变到d点 |
| B.加入少量水,平衡右移,Cl-浓度增大 |
| C.d点没有AgCl沉淀生成 |
| D.c点对应的Ksp等于a点对应的Ksp |
您最近一年使用:0次
2022-12-11更新
|
225次组卷
|
2卷引用:广东顺佛山市顺德区文德学校2021-2022学年高二上学期第二次阶段性测试化学试题
名校
解题方法
2 . 马日夫盐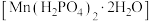 易溶于水,且水溶液呈酸性,主要用作大型机械设备的防锈剂,也用作各种武器等的润滑层和防护层。以软锰矿(主要成分为
易溶于水,且水溶液呈酸性,主要用作大型机械设备的防锈剂,也用作各种武器等的润滑层和防护层。以软锰矿(主要成分为 ,还含少量的FeO、
,还含少量的FeO、 和
和 )为原料制备马日夫盐的一种工艺流程如图所示:
)为原料制备马日夫盐的一种工艺流程如图所示:
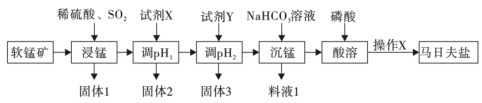
已知常温下,几种离子形成氢氧化物沉淀时,开始沉淀与恰好完全沉淀时的pH如表所示:
回答下列问题:
(1)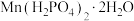 中锰元素的化合价是
中锰元素的化合价是______ 。
(2)浸锰过程中除了 是还原剂外还有一种还原剂,写出该还原剂被氧化的离子方程式
是还原剂外还有一种还原剂,写出该还原剂被氧化的离子方程式____________ 。
(3)固体2的主要成分经处理可得到一种用于生产油漆、涂料的物质,该处理方法是__________ ;调 时,
时, 的范围是
的范围是__________ 。
(4)试剂Y不宜为____________ (填字母)。
A.氨水 B. C.
C.
(5)沉锰过程中有一种无色无味气体生成,写出相应反应的离子方程式____________ 。由表中数据可求出常温下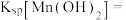
____________ (离子浓度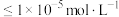 时可认为其沉淀完全)。
时可认为其沉淀完全)。
(6)操作X包括______ 、过滤、洗涤、干燥。马日夫盐可作防锈剂的原因是在防锈处理过程中生成了具有保护作用的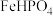 ,处理过程中马日夫盐可转化为
,处理过程中马日夫盐可转化为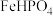 的原理是
的原理是____________ 。
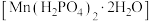 易溶于水,且水溶液呈酸性,主要用作大型机械设备的防锈剂,也用作各种武器等的润滑层和防护层。以软锰矿(主要成分为
易溶于水,且水溶液呈酸性,主要用作大型机械设备的防锈剂,也用作各种武器等的润滑层和防护层。以软锰矿(主要成分为 ,还含少量的FeO、
,还含少量的FeO、 和
和 )为原料制备马日夫盐的一种工艺流程如图所示:
)为原料制备马日夫盐的一种工艺流程如图所示:
已知常温下,几种离子形成氢氧化物沉淀时,开始沉淀与恰好完全沉淀时的pH如表所示:
|
|
|
| |
开始沉淀 | 2.7 | 7.6 | 7.7 | 4.0 |
完全沉淀 | 3.2 | 9.6 | 10.0 | 5.2 |
(1)
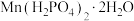 中锰元素的化合价是
中锰元素的化合价是(2)浸锰过程中除了
 是还原剂外还有一种还原剂,写出该还原剂被氧化的离子方程式
是还原剂外还有一种还原剂,写出该还原剂被氧化的离子方程式(3)固体2的主要成分经处理可得到一种用于生产油漆、涂料的物质,该处理方法是
 时,
时, 的范围是
的范围是(4)试剂Y不宜为
A.氨水 B.
 C.
C.
(5)沉锰过程中有一种无色无味气体生成,写出相应反应的离子方程式
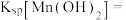
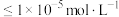 时可认为其沉淀完全)。
时可认为其沉淀完全)。(6)操作X包括
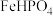 ,处理过程中马日夫盐可转化为
,处理过程中马日夫盐可转化为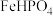 的原理是
的原理是
您最近一年使用:0次
解题方法
3 . 已知25℃时,AgCl的溶度积Ksp=1.8×10-10mol2·L-2,则下列说法正确的是
| A.向饱和AgCl水溶液中加入盐酸,Ksp变大 |
| B.AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-) |
| C.温度一定时,当溶液中c(Ag+)·c(Cl-)=Ksp时,此溶液中必有AgCl沉淀析出 |
| D.在AgCl的悬浊液中加入Na2S溶液,AgCl转化为Ag2S,因为AgCl溶解度大于Ag2S |
您最近一年使用:0次
名校
4 . 在平衡体系Ca(OH)2(s) Ca2+(aq)+2OH-(aq) △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是
Ca2+(aq)+2OH-(aq) △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是
 Ca2+(aq)+2OH-(aq) △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是
Ca2+(aq)+2OH-(aq) △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是| A.加入少量CuCl2固体 | B.加入少量NaCl固体 |
| C.加入少量K2CO3固体 | D.升高体系温度 |
您最近一年使用:0次
2022-12-06更新
|
450次组卷
|
3卷引用:河南省许昌市鄢陵县职业教育中心2021-2022学年高二上学期第一次月考化学试题
5 . 回答下列问题。
(1)某小组同学探究饱和NaClO和 溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和
溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和 溶液,产生大量的白色胶状沉淀。出现上述现象的原因是
溶液,产生大量的白色胶状沉淀。出现上述现象的原因是_________ (请用反应的离子方程式表示)。
(2) 、
、 两种温度下
两种温度下 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
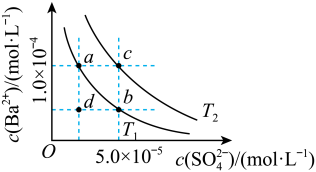
①T1_____ T2(填“<”“>”或“=”), 温度时
温度时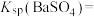
___________ 。
②根据 温度时
温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是______ (填标号)。
A.加入 固体可由a点变为b点
固体可由a点变为b点
B. 温度下,在
温度下,在 曲线上方区域(不含曲线)的任意一点时,均有
曲线上方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成
C.蒸发溶剂可能由d点变为 曲线上a、b之间(不含a、b)的某一点
曲线上a、b之间(不含a、b)的某一点
D.升温可由b点变为d点
③ 温度时,现有0.2mol的
温度时,现有0.2mol的 沉淀,每次用1L饱和
沉淀,每次用1L饱和 溶液(浓度为1.7 mol/L)处理。若使
溶液(浓度为1.7 mol/L)处理。若使 中的
中的 全部转化到溶液中,需要反复处理
全部转化到溶液中,需要反复处理_______ 次。
[提示: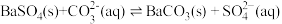 ,
,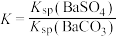 ,
,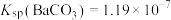 ]
]
(1)某小组同学探究饱和NaClO和
 溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和
溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和 溶液,产生大量的白色胶状沉淀。出现上述现象的原因是
溶液,产生大量的白色胶状沉淀。出现上述现象的原因是(2)
 、
、 两种温度下
两种温度下 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
①T1
 温度时
温度时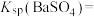
②根据
 温度时
温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是A.加入
 固体可由a点变为b点
固体可由a点变为b点B.
 温度下,在
温度下,在 曲线上方区域(不含曲线)的任意一点时,均有
曲线上方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成C.蒸发溶剂可能由d点变为
 曲线上a、b之间(不含a、b)的某一点
曲线上a、b之间(不含a、b)的某一点D.升温可由b点变为d点
③
 温度时,现有0.2mol的
温度时,现有0.2mol的 沉淀,每次用1L饱和
沉淀,每次用1L饱和 溶液(浓度为1.7 mol/L)处理。若使
溶液(浓度为1.7 mol/L)处理。若使 中的
中的 全部转化到溶液中,需要反复处理
全部转化到溶液中,需要反复处理[提示:
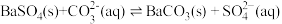 ,
,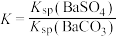 ,
,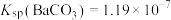 ]
]
您最近一年使用:0次
解题方法
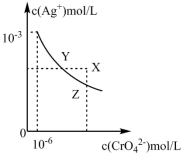
6 . t℃时, 在水中的沉淀溶解平衡曲线如图所示(t℃时
在水中的沉淀溶解平衡曲线如图所示(t℃时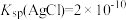 )。下列说法正确的是
)。下列说法正确的是
 在水中的沉淀溶解平衡曲线如图所示(t℃时
在水中的沉淀溶解平衡曲线如图所示(t℃时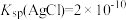 )。下列说法正确的是
)。下列说法正确的是
A.t℃时, 的Ksp数量级是10-9 的Ksp数量级是10-9 |
B.在饱和 溶液中加入 溶液中加入 固体可使溶液由Y点到X点 固体可使溶液由Y点到X点 |
C.t℃时,用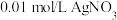 液滴定 液滴定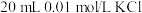 和 和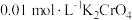 的混合液, 的混合液, 先沉淀 先沉淀 |
D.t℃时: 的平衡常数 的平衡常数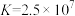 |
您最近一年使用:0次
2022-12-05更新
|
226次组卷
|
2卷引用:辽宁省朝阳市建平县高级中学2021-2022学年高二上学期第二次月考化学试题
解题方法
7 . 已知25℃时Ksp(BaSO4)=1.0×10-10, 在水中的沉淀溶解平衡曲线如图所示,下列叙述
在水中的沉淀溶解平衡曲线如图所示,下列叙述 均指25℃时
均指25℃时 中正确的是
中正确的是
 在水中的沉淀溶解平衡曲线如图所示,下列叙述
在水中的沉淀溶解平衡曲线如图所示,下列叙述 均指25℃时
均指25℃时 中正确的是
中正确的是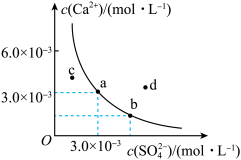
A.升高温度后,a点溶液可以转化为 点溶液 点溶液 |
B.a、 、c、d四点对应的体系中,d点体系最稳定 、c、d四点对应的体系中,d点体系最稳定 |
C.可用饱和 溶液使 溶液使 转化为 转化为 |
D.向a点的溶液中加入等物质的量的 或 或 时析出的沉淀量不同 时析出的沉淀量不同 |
您最近一年使用:0次
名校
8 . 当Mg(OH)2固体在水中溶解达到平衡时:Mg(OH)2 (s)⇌Mg2++2OH- ,为使Mg(OH)2固体的量减少,可加入的物质是
| A.MgSO4 | B.NaOH | C.HCl | D.NaCl |
您最近一年使用:0次
2022-12-04更新
|
646次组卷
|
8卷引用:北京市西城职业学校2021-2021学年高二上学期期中测试化学试题
解题方法
9 . 牙齿表面覆盖的牙釉质是人体中最坚硬的部分,起着保护牙齿的作用,其主要成分为羟基磷酸钙[Ca5(PO4)3OH]。在牙齿表面存在着如下平衡:
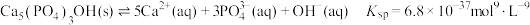
残留在牙齿上的糖发酵会产生H+,这会对牙釉质产生什么影响______ ?应采取哪些措施保护牙齿________ ?
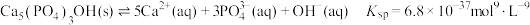
残留在牙齿上的糖发酵会产生H+,这会对牙釉质产生什么影响
您最近一年使用:0次
解题方法
10 . 请运用所学知识判断,向1 mL0.1 mol/LAgNO3溶液中依次滴加1 mL0.1 mol/L的NaCl、NaBr、KI溶液时,会发生什么变化________ 。
您最近一年使用:0次







