解题方法
1 . 下面是两位同学设计的证明碳酸钠样品中含有氯化钠的实验方案。
甲:取样品少许加入试管中,加入适量的蒸馏水使之溶解,配成溶液,然后加入AgNO3溶液,看是否有白色沉淀生成。
乙:取样品少许加入试管中,加入适量的自来水使之溶解,配成溶液,然后滴加稀硝酸酸化的AgNO3溶液,看是否有白色沉淀生成。
(1)两个方案均有不合理之处,请指出:
甲___ 。
乙___ 。
(2)合理的实验方案为___ 。
甲:取样品少许加入试管中,加入适量的蒸馏水使之溶解,配成溶液,然后加入AgNO3溶液,看是否有白色沉淀生成。
乙:取样品少许加入试管中,加入适量的自来水使之溶解,配成溶液,然后滴加稀硝酸酸化的AgNO3溶液,看是否有白色沉淀生成。
(1)两个方案均有不合理之处,请指出:
甲
乙
(2)合理的实验方案为
您最近一年使用:0次
2020-09-07更新
|
254次组卷
|
3卷引用:人教版(2019)高一必修第一册 第二章 第二节课时2 氯气的实验室制法及氯离子的检验
人教版(2019)高一必修第一册 第二章 第二节课时2 氯气的实验室制法及氯离子的检验第3课时 氯气与碱反应及 Cl-的检验(已下线)【精品卷】2.2.3 氯离子的检验课堂例题-人教版2023-2024学年必修第一册
解题方法
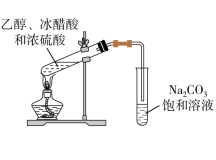
2 . 实验室制备乙酸乙酯的实验装置如图所示,回答下列问题:
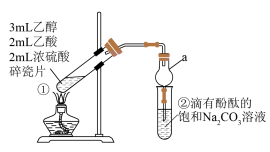
(1)该实验中混合乙醇和浓硫酸的方法是_____ 。
(2)该装置与教材上的相比做了一些改进,其中仪器a的名称_____ ,改进后的装置仍然存在一定的不足,请指出其中的一点_____ 。
(3)试管②中溶液呈红色的原因是_____ 。(用离子方程式表示)。
(4)某实验小组在分离操作中,摇晃了试管②,发现上下两层溶液均变为无色,该小组对褪色原因进行探究。
Ⅰ.经过讨论猜想褪色原因是挥发的乙酸中和碳酸钠。
由实验1、2得出的结论是_____ 。
Ⅱ.查阅资料:酚酞是一种白色晶状粉末,不溶于水,1g酚酞可溶于13mL乙醇或70mL乙醚中。
由实验3、4得出的结论是_____ 。

(1)该实验中混合乙醇和浓硫酸的方法是
(2)该装置与教材上的相比做了一些改进,其中仪器a的名称
(3)试管②中溶液呈红色的原因是
(4)某实验小组在分离操作中,摇晃了试管②,发现上下两层溶液均变为无色,该小组对褪色原因进行探究。
Ⅰ.经过讨论猜想褪色原因是挥发的乙酸中和碳酸钠。
| 编号 | 操作 | 现象 |
| 实验1 | 用pH计测量饱和碳酸钠溶液pH | pH=12.23 |
| 实验2 | 分离出试管②下层液体,用pH计测定pH | pH=12.21 |
Ⅱ.查阅资料:酚酞是一种白色晶状粉末,不溶于水,1g酚酞可溶于13mL乙醇或70mL乙醚中。
| 编号 | 操作 | 现象 |
| 实验3 | 取5mL饱和碳酸钠溶液,滴入几滴酚酞溶液,再加入3mL纯净的乙酸乙酯,振荡 | 碳酸钠溶液先变红,加入乙酸乙酯振荡后褪色 |
| 实验4 | 分离出试管②上层液体,加入饱和碳酸钠溶液,振荡 | 溶液变成浅红色,静置分层后红色消失 |
您最近一年使用:0次
3 . 如图是在实验室进行氨气快速制备与性质实验的组合装置,部分固定装置未画出。

(1)在组装好装置后,若要检验A~E装置的气密性,其操作是首先______ ,然后微热A,观察到E中有气泡冒出,移开酒精灯或松开双手,E中导管中有水柱形成说明装置气密性良好。
(2)装置B中盛放的试剂是________ 。
(3)点燃C处酒精灯,关闭弹簧夹2,打开弹簧夹1,从分液漏斗放出浓氨水至浸没烧瓶中固体后关闭分液漏斗,片刻后,装置C中黑色固体逐渐变红,装置E中溶液里出现大量气泡,同时产生_______ (答现象);从E中逸出液面的气体可以直接排入空气,请写出在C中发生反应的化学方程式:_____ 。
(4)当C中固体全部变红色后,关闭弹簧夹1,慢慢移开酒精灯,待冷却后,称量C中固体质量。若反应前固体质量为16g,反应后固体质量减少2.4g。通过计算确定该固体产物的成分是__________ (用化学式表示)。
(5)在关闭弹簧夹1后,打开弹簧夹2,残余气体进入F中,很快发现装置F中产生白烟,同时发现G中溶液迅速倒吸入F中。写出产生白烟的化学方程式:__________ 。迅速产生倒吸的原因是___________ 。

(1)在组装好装置后,若要检验A~E装置的气密性,其操作是首先
(2)装置B中盛放的试剂是
(3)点燃C处酒精灯,关闭弹簧夹2,打开弹簧夹1,从分液漏斗放出浓氨水至浸没烧瓶中固体后关闭分液漏斗,片刻后,装置C中黑色固体逐渐变红,装置E中溶液里出现大量气泡,同时产生
(4)当C中固体全部变红色后,关闭弹簧夹1,慢慢移开酒精灯,待冷却后,称量C中固体质量。若反应前固体质量为16g,反应后固体质量减少2.4g。通过计算确定该固体产物的成分是
(5)在关闭弹簧夹1后,打开弹簧夹2,残余气体进入F中,很快发现装置F中产生白烟,同时发现G中溶液迅速倒吸入F中。写出产生白烟的化学方程式:
您最近一年使用:0次
名校
解题方法
4 . 利用图示装置组合,能达到实验室制取气体目的的是( )
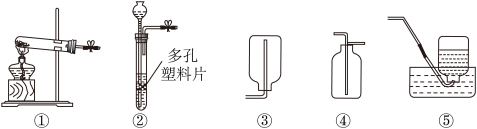

| A.大理石和稀硫酸反应,用②④制取二氧化碳,随时控制反应的发生与停止 |
| B.氯酸钾和二氧化锰混合,用①③制取氧气,不能随时控制反应的发生与停止 |
| C.双氧水和二氧化锰粉末,用②⑤制取氧气,随时控制反应的发生与停止 |
| D.锌粒和稀硫酸反应,用②③制取氢气,随时控制反应的发生与停止 |
您最近一年使用:0次
解题方法
5 . 某化学小组在学习元素周期律后,对教材中Fe2+氧化为Fe3+的实验进一步思考,并提出问题:Cl2能将Fe2+氧化为Fe3+,那么Br2和I2能否将Fe2+氧化为Fe3+?
(一)理论推测
部分同学认为Br2和I2都可能将Fe2+氧化为Fe3+,他们思考的依据是___ 。
部分同学认为Br2和I2都不能将Fe2+氧化为Fe3+,还有同学认为Br2能将Fe2+氧化为Fe3+而I2不能。他们思考的依据是从上到下卤素单质氧化性减弱。
(二)设计实验进行验证
在大试管中加适量铁粉,加入10mL稀盐酸,振荡试管,充分反应后,铁粉有剩余,取上层清液进行下列实验。
(三)实验现象的分析与解释
(I)同学甲认为①中现象说明溴水能将Fe2+氧化,离子方程式为___ 。
同学乙认为应该补充实验,才能得出同学甲的结论。请你帮助同学乙完成实验:
实验2:
(II)该小组同学对②中溶液呈黄色的原因展开了讨论:
可能1:碘水与FeCl2溶液不反应,黄色是碘水稀释后的颜色。
可能2:___ 。
实验3:进行实验以确定可能的原因。
同学丙认为该实验现象可以说明是“可能2”成立,同学丁认为不严谨,理由是___ 。
于是,同学丁重新设计实验得出结论:在本次实验条件下,碘水与FeCl2溶液反应的程度很小。
(III)Cl2、Br2、I2氧化Fe2+的能力逐渐减弱,用原子结构解释原因:___ 。
(一)理论推测
部分同学认为Br2和I2都可能将Fe2+氧化为Fe3+,他们思考的依据是
部分同学认为Br2和I2都不能将Fe2+氧化为Fe3+,还有同学认为Br2能将Fe2+氧化为Fe3+而I2不能。他们思考的依据是从上到下卤素单质氧化性减弱。
(二)设计实验进行验证
在大试管中加适量铁粉,加入10mL稀盐酸,振荡试管,充分反应后,铁粉有剩余,取上层清液进行下列实验。
| 试管 | 操作 | 现象 |
| ① | 先向试管中加入2mLFeCl2溶液,再滴加少量红棕色的溴水,振荡试管 | 溶液为黄色 |
| ② | 先向试管中加入2mLFeCl2溶液,再滴加少量棕黄色的碘水,振荡试管 | 溶液为黄色 |
(三)实验现象的分析与解释
(I)同学甲认为①中现象说明溴水能将Fe2+氧化,离子方程式为
同学乙认为应该补充实验,才能得出同学甲的结论。请你帮助同学乙完成实验:
实验2:
| 操作 | 应该观察到的现象 |
| (3) | (4) |
(II)该小组同学对②中溶液呈黄色的原因展开了讨论:
可能1:碘水与FeCl2溶液不反应,黄色是碘水稀释后的颜色。
可能2:
实验3:进行实验以确定可能的原因。
| 操作 | 现象 |
| 向试管②所得溶液中继续加入0.5mLCCl4,充分振荡,静置一段时间后。取出上层溶液,滴加KSCN溶液 | 静置后,上层溶液几乎无色,下层溶液为紫色;上层溶液滴加KSCN溶液后,出现浅红色 |
同学丙认为该实验现象可以说明是“可能2”成立,同学丁认为不严谨,理由是
于是,同学丁重新设计实验得出结论:在本次实验条件下,碘水与FeCl2溶液反应的程度很小。
(III)Cl2、Br2、I2氧化Fe2+的能力逐渐减弱,用原子结构解释原因:
您最近一年使用:0次
6 . 实验是化学研究的基础。 下列对实验现象的描述错误的是
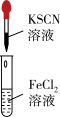 | 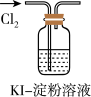 | 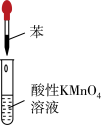 |  |
| ① | ② | ③ | ④ |
| A.实验①中溶液无明显现象 |
| B.实验②中溶液变为蓝色 |
| C.实验③中酸性高锰酸钾溶液紫色褪去 |
| D.实验④ 右侧试管中溶液分层, 上层为无色透明油状液体 |
您最近一年使用:0次
7 . 实验是化学学习的重要手段。下列有关实验设计或实验现象描述中,正确的是( ).
| A.可用酚酞溶液一次性鉴别稀盐酸、石灰水和食盐水三种无色溶液 |
| B.可用Fe粉除去FeSO4溶液中含有的少量H2SO4 |
| C.常温下能导电的固体物质一定是金属单质 |
| D.能使燃着的木条熄灭的气体一定是CO2 |
您最近一年使用:0次
名校
解题方法
8 . 下列实验操作正确的是
| A.制备乙酸乙酯时,将乙醇和乙酸依次加入到浓硫酸中 |
| B.蒸馏实验完毕后,应该先停止加热,过一会儿再停止向冷凝管中通冷凝水 |
| C.为测定新制氯水的 pH,用玻璃棒蘸取液体滴在 pH 试纸上,与标准比色卡对照即可 |
D.在未知溶液中滴加 BaCl2 溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存 在 或 或 |
您最近一年使用:0次
名校
9 . 下图为制取无水氯化铁粉末的装置,已知无水氯化铁粉末很容易吸水生成结晶水合物FeCl3+6H2O=FeCl3·6H2O。

(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):①接____ ,___ 接___ ;___ 接___ 。
(2)装置A烧瓶中发生的反应,氧化剂是____ (填物质名称),装置B中反应的化学方程式是_____ 。
(3)装置E的作用是_____ 。
(4)装置A、B中的酒精灯应先点燃_____ 处(填“A”或“B")的酒精灯。
(5)这套实验装置是否完整?____ (填“是”或“否”),若不完整,还须补充_____ 装置(若第一问填“ 是”,则此问不需要作答)。

(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):①接
(2)装置A烧瓶中发生的反应,氧化剂是
(3)装置E的作用是
(4)装置A、B中的酒精灯应先点燃
(5)这套实验装置是否完整?
您最近一年使用:0次
2020-07-30更新
|
245次组卷
|
2卷引用:辽宁省大连市2019-2020学年高一上学期期末考试化学试题
解题方法
10 . 某兴趣小组同学进行乙醛的银镜反应,实验操作步骤如下:
A.在试管里先注入少量NaOH溶液,振荡,然后加热煮沸。把NaOH溶液倒去后,再用蒸馏水洗净试管备用。
B.在洗净的试管里配制银氨溶液。
C.沿试管壁加入乙醛稀溶液。
D.加热。请回答下列问题:
(1)步骤A中加NaOH溶液振荡,加热煮沸的目的是:________________________ 。
(2)步骤D应选择的加热方法是_________ (填下列装置编号)

(3)乙醛发生银镜反应的化学方程式为:_______________________________ 。
(4)该兴趣小组的同学还对乙醛进行银镜反应的最佳实验条件进行了探究(部分实验数据如下表):
①实验1和实验2,探究的是_________________________________ 。
②当银氨溶液的量为1 mL,乙醛的量为3滴,温度为55℃,反应混合液pH为11时,出现银镜的时间为_________________________ min。(填范围)
③你认为探究乙醛进行银镜反应的最佳条件,除了测定银镜出现的时间外,还需要比较不同条件下形成的银镜的____________________ 。
A.在试管里先注入少量NaOH溶液,振荡,然后加热煮沸。把NaOH溶液倒去后,再用蒸馏水洗净试管备用。
B.在洗净的试管里配制银氨溶液。
C.沿试管壁加入乙醛稀溶液。
D.加热。请回答下列问题:
(1)步骤A中加NaOH溶液振荡,加热煮沸的目的是:
(2)步骤D应选择的加热方法是

(3)乙醛发生银镜反应的化学方程式为:
(4)该兴趣小组的同学还对乙醛进行银镜反应的最佳实验条件进行了探究(部分实验数据如下表):
实验变量 实验序号 | 银氨溶液 | 乙醛的 量/滴 |  | 反应混合液 | 出现银镜的 |
1 | 1 | 3 | 65 | 11 | 5 |
2 | 1 | 3 | 45 | 11 | 6.5 |
3 | 1 | 5 | 65 | 11 | 4 |
②当银氨溶液的量为1 mL,乙醛的量为3滴,温度为55℃,反应混合液pH为11时,出现银镜的时间为
③你认为探究乙醛进行银镜反应的最佳条件,除了测定银镜出现的时间外,还需要比较不同条件下形成的银镜的
您最近一年使用:0次



