名校
1 . Ⅰ.回答下列问题:
(1)用硫酸滴定氨水,应选用_______ 做指示剂,滴定终点颜色变化为_______ ,并保持半分钟不变。(NH4)2SO4溶液显酸性的原因:_______ (用离子方程式说明)。
(2)部分弱酸的电离平衡常数如表:
室温下四种溶液:①0.1mol/LHCOONa, ②0.1mol/LNaClO,③0.1mol/LNa2CO3,④0.1mol/LNaHSO3,四种溶液的pH由大到小的关系为_______ (填序号)。
(3)写出把足量CO2通入NaClO溶液中的离子方程式_______ 。
Ⅱ.活动小组同学采用如下装置制备NaNO2(装置可重复使用,部分夹持仪器已省略)。
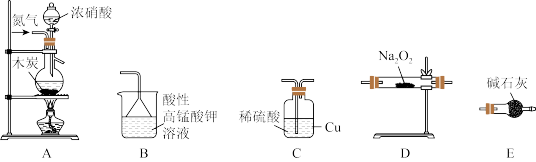
已知:①2NO+Na2O2=2NaNO2
②酸性条件下,NO、NO2都能与 反应生成
反应生成 和Mn2+
和Mn2+
③NaNO2能使酸性高锰酸钾溶液褪色。
(4)实验装置的连接顺序A→_______ 。
(5)C瓶内发生反应的离子方程式为_______ 。
(6)为了测定亚硝酸钠的含量,称取4.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol/L的酸性KMnO4溶液进行滴定,实验所得数据如下表:
①第一组实验数据出现较明显异常,造成异常的原因可能是_______ (填字母序号)。
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.滴定前滴定管尖嘴中有气泡,滴定后滴定管尖嘴无气泡
c.滴入最后一滴KMnO4溶液,溶液呈浅红色,立即停止滴定
d.观察滴定终点时俯视读数
②根据表中数据进行计算,所制得的固体中亚硝酸钠的质量分数为_______ 。
(1)用硫酸滴定氨水,应选用
(2)部分弱酸的电离平衡常数如表:
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25°C) | Ka=1.77×10-4 | Ka=4.0×10-8 | Ka1=4.3×10-7,Ka2=4.7×10-11 | Ka1=1.54×10-2,Ka2=1.02×10-7 |
(3)写出把足量CO2通入NaClO溶液中的离子方程式
Ⅱ.活动小组同学采用如下装置制备NaNO2(装置可重复使用,部分夹持仪器已省略)。

已知:①2NO+Na2O2=2NaNO2
②酸性条件下,NO、NO2都能与
 反应生成
反应生成 和Mn2+
和Mn2+③NaNO2能使酸性高锰酸钾溶液褪色。
(4)实验装置的连接顺序A→
(5)C瓶内发生反应的离子方程式为
(6)为了测定亚硝酸钠的含量,称取4.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol/L的酸性KMnO4溶液进行滴定,实验所得数据如下表:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.滴定前滴定管尖嘴中有气泡,滴定后滴定管尖嘴无气泡
c.滴入最后一滴KMnO4溶液,溶液呈浅红色,立即停止滴定
d.观察滴定终点时俯视读数
②根据表中数据进行计算,所制得的固体中亚硝酸钠的质量分数为
您最近一年使用:0次
名校
2 . MnSO4•H2O是一种浅粉色晶体,易溶于水。是饲料中常用的添加剂,也是电解锰及其他锰盐的原料,工业用途广泛。某同学设计下列实验装置制备硫酸锰:

回答下列问题:
(1)装置I盛放的固体药品是_____ (填化学式)。
(2)装置II中反应的容器名称是_____ ,化学方程式为_____ 。该实验中提高反应速率的措施有_____ ;反应后从溶液得到MnSO4•H2O的操作为_____ 。
(3)兴趣小组同学拟继续研究硫酸锰晶体高温分解的固体产物,经查资料可知:硫酸锰晶体高温下的分解产物为Mn3O4、SO2、SO3及水蒸气。将101.4gMnSO4•H2O充分加热反应后,生成SO2的物质的量为_____ mol。
(4)测定饲料中硫酸锰含量常将饲料溶于水,以磷酸作络合剂,用硝酸铵作氧化剂,将试样中的二价锰定量氧化成三价锰,过量的硝酸铵立即与产生的亚硝酸盐反应生成N2而消除其影响。然后加入指示剂,用硫酸亚铁铵[Fe(NH4)2(SO4)2•6H2O]标准溶液滴定生成的三价锰,溶液由红色变为亮黄色为滴定终点。有关离子反应方程式为:
2Mn2++ +4
+4 +2H+=2[Mn(PO4)2]3-+
+2H+=2[Mn(PO4)2]3-+  +H2O
+H2O
 +
+ =N2↑+2H2O
=N2↑+2H2O
[Mn(PO4)2]3-+Fe2+=Mn2++[Fe2(PO4)2]3-
取ag饲料,消耗浓度为cmol·L-1的硫酸亚铁铵标准溶液VmL,则饲料中MnSO4•H2O的质量分数为_____ (用含a、c、V的表达式表示),若滴定前平视读数,滴后俯视,则会导致测定结果_____ (填“偏大”、“偏小”或“无影响”)。

回答下列问题:
(1)装置I盛放的固体药品是
(2)装置II中反应的容器名称是
(3)兴趣小组同学拟继续研究硫酸锰晶体高温分解的固体产物,经查资料可知:硫酸锰晶体高温下的分解产物为Mn3O4、SO2、SO3及水蒸气。将101.4gMnSO4•H2O充分加热反应后,生成SO2的物质的量为
(4)测定饲料中硫酸锰含量常将饲料溶于水,以磷酸作络合剂,用硝酸铵作氧化剂,将试样中的二价锰定量氧化成三价锰,过量的硝酸铵立即与产生的亚硝酸盐反应生成N2而消除其影响。然后加入指示剂,用硫酸亚铁铵[Fe(NH4)2(SO4)2•6H2O]标准溶液滴定生成的三价锰,溶液由红色变为亮黄色为滴定终点。有关离子反应方程式为:
2Mn2++
 +4
+4 +2H+=2[Mn(PO4)2]3-+
+2H+=2[Mn(PO4)2]3-+  +H2O
+H2O +
+ =N2↑+2H2O
=N2↑+2H2O[Mn(PO4)2]3-+Fe2+=Mn2++[Fe2(PO4)2]3-
取ag饲料,消耗浓度为cmol·L-1的硫酸亚铁铵标准溶液VmL,则饲料中MnSO4•H2O的质量分数为
您最近一年使用:0次
解题方法
3 . 山梨酸钾是一种低毒、安全、高效的食品防腐剂,具有非常强的抑制霉菌与腐败菌的作用。一种制备方法如下:

I.制备山梨酸钾:
步骤1:在如图所示的反应装置中,加入5 g巴豆醛、10 g丙二酸和1 g吡啶,室温搅拌20分钟。
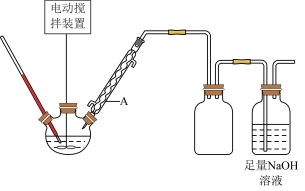
步骤2:缓慢升温至95 °C,保温95~100 °C反应3~4小时,待CO2放出后,用冰水浴降温至10°C以下,缓慢加入10%的稀硫酸,控制滴加速度使温度低于20°C,至pH约为4~5为止。
步骤3:冷冻过夜,抽滤,结晶用冰水洗涤,得山梨酸粗品。在95~100 °C水浴中,用60%乙醇溶解,抽滤,母液在-10~5°C下结晶,得山梨酸纯品。
步骤4:将山梨酸纯品、KOH、乙醇按2:1:8.6(质量比)倒入烧瓶中,并加入少量水,在60~70 °C水浴中搅拌,回流至反应液透明,迅速在冰水浴中冷却,所得晶体抽滤并烘干,即可得白色山梨酸钾晶体。
(1)仪器A的名称是_______ ;从平衡移动的角度解释“步骤1”中加入吡啶的作用_______ 。
(2)“步骤2”中的加热方式采用油浴,不采用水浴,原因是_______ ;加入稀硫酸将pH调至4~5的目的是_______ 。
(3)由山梨酸粗品制得纯品的提纯方法是_______ 。
(4)若最终制得3.0 g山梨酸钾晶体,则产率为_______ %。
II.测定食品中山梨酸钾含量(杂质不参与反应):
取待测食品m g,将其中的山梨酸钾浓缩、提取后,用盐酸酸化得白色晶体。将白色晶体用试剂X溶解后,配成250mL溶液。取25mL配好的溶液,以酚酞为指示剂,用cmol·L-1的标准NaOH溶液滴定,三次平行实验测得消耗标准液的平均体积为V mL。
(5)①溶解白色晶体的试剂X可选用_______ ;(填选项序号)
A.蒸馏水 B.乙醇 C.稀盐酸
②待测食品中山梨酸钾的质量分数为_______ %。(用含字母的代数式表示)

| 名称 | 分子式 | 分子量 | 熔点(°C) | 沸点(°C) | 性质 |
| 山梨酸钾 | C6H7O2 K | 150 | 270(分解) | — | 易溶于水和乙醇 |
| 山梨酸 | C6H8O2 | 112 | 132 | 228 | 微溶于水,易溶于有机溶剂 |
| 巴豆醛 | C4 H6O | 70 | -76.5 | 104 | 微溶于水,可溶于有机溶剂 |
| 丙二酸 | C3H4O4 | 104 | 135 | 140(分解) | 易溶于水,与有机物可混溶 |
| 吡啶 | C5H5N | 79 | -41.6 | 115.3 | 显碱性,可与山梨酸反应 |
步骤1:在如图所示的反应装置中,加入5 g巴豆醛、10 g丙二酸和1 g吡啶,室温搅拌20分钟。

步骤2:缓慢升温至95 °C,保温95~100 °C反应3~4小时,待CO2放出后,用冰水浴降温至10°C以下,缓慢加入10%的稀硫酸,控制滴加速度使温度低于20°C,至pH约为4~5为止。
步骤3:冷冻过夜,抽滤,结晶用冰水洗涤,得山梨酸粗品。在95~100 °C水浴中,用60%乙醇溶解,抽滤,母液在-10~5°C下结晶,得山梨酸纯品。
步骤4:将山梨酸纯品、KOH、乙醇按2:1:8.6(质量比)倒入烧瓶中,并加入少量水,在60~70 °C水浴中搅拌,回流至反应液透明,迅速在冰水浴中冷却,所得晶体抽滤并烘干,即可得白色山梨酸钾晶体。
(1)仪器A的名称是
(2)“步骤2”中的加热方式采用油浴,不采用水浴,原因是
(3)由山梨酸粗品制得纯品的提纯方法是
(4)若最终制得3.0 g山梨酸钾晶体,则产率为
II.测定食品中山梨酸钾含量(杂质不参与反应):
取待测食品m g,将其中的山梨酸钾浓缩、提取后,用盐酸酸化得白色晶体。将白色晶体用试剂X溶解后,配成250mL溶液。取25mL配好的溶液,以酚酞为指示剂,用cmol·L-1的标准NaOH溶液滴定,三次平行实验测得消耗标准液的平均体积为V mL。
(5)①溶解白色晶体的试剂X可选用
A.蒸馏水 B.乙醇 C.稀盐酸
②待测食品中山梨酸钾的质量分数为
您最近一年使用:0次
4 . 亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。某化学兴趣小组设计实验制备NaNO2并探究其性质。
查阅资料信息:①2NO+Na2O2 =2NaNO2;2NO2 +Na2O2=2NaNO3.
②酸性KMnO4溶液可将低价氮的氧化物或酸根离子氧化为 。
。
(1)NaNO2的制备(夹持装置和加热装置均已略,已检查装置气密性)。
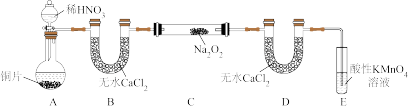
①若没有装置B,则装置C中Na2O2与水发生反应:_______ (填化学方程式)。
②制得的NaNO2固体中混有的杂质主要为NaNO3,改进措施是在装置A、B间添加_______ ,提高NaNO2的纯度。
③装置E中发生的主要反应的离子方程式为_______ 。
(2)验证亚硝酸钠与70%硫酸反应的气体产物为NO和NO2的混合气体。
已知:FeSO4溶液可吸收NO;NO2的沸点为21° C ,熔点为-11° C 。
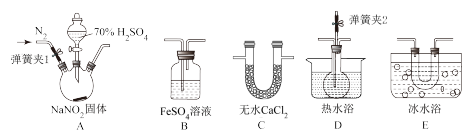
①为了检验装置A中生成的气体产物,装置的连接顺序是A→_______ 。(按气流方向从左到右)
②反应前应打开弹簧夹1, 先通入一段时间氮气,目的是_______ 。
③再关闭弹簧夹1,打开分液漏斗活塞,滴入70%硫酸后,装置A中产生红棕色气体。
设计实验检验装置A中产生的气体含有NO的操作及现象:_______ 。
(3)查阅资料知:酸性条件下NaNO2具有氧化性。利用所供试剂,设计实验方案验证此信息:_______ (供选用的试剂有NaNO2溶液、FeSO4溶液、稀硫酸、KSCN溶液)
(4)测定某亚硝酸钠样品的纯度。
设该样品的杂质均不与酸性KMnO4溶液反应,可用酸性KMnO4溶液测定NaNO2的含量。称取2.0 g亚硝酸钠样品溶于水配成250 mL溶液,取出25. 00 mL溶液于锥形瓶中,再用0. 1000 mol· L-1的酸性KMnO4标准溶液进行滴定,消耗酸性KMnO4标准溶液的体积如表:
该亚硝酸钠样品中NaNO2的质量分数为_______ 。
查阅资料信息:①2NO+Na2O2 =2NaNO2;2NO2 +Na2O2=2NaNO3.
②酸性KMnO4溶液可将低价氮的氧化物或酸根离子氧化为
 。
。(1)NaNO2的制备(夹持装置和加热装置均已略,已检查装置气密性)。

①若没有装置B,则装置C中Na2O2与水发生反应:
②制得的NaNO2固体中混有的杂质主要为NaNO3,改进措施是在装置A、B间添加
③装置E中发生的主要反应的离子方程式为
(2)验证亚硝酸钠与70%硫酸反应的气体产物为NO和NO2的混合气体。
已知:FeSO4溶液可吸收NO;NO2的沸点为21° C ,熔点为-11° C 。

①为了检验装置A中生成的气体产物,装置的连接顺序是A→
②反应前应打开弹簧夹1, 先通入一段时间氮气,目的是
③再关闭弹簧夹1,打开分液漏斗活塞,滴入70%硫酸后,装置A中产生红棕色气体。
设计实验检验装置A中产生的气体含有NO的操作及现象:
(3)查阅资料知:酸性条件下NaNO2具有氧化性。利用所供试剂,设计实验方案验证此信息:
(4)测定某亚硝酸钠样品的纯度。
设该样品的杂质均不与酸性KMnO4溶液反应,可用酸性KMnO4溶液测定NaNO2的含量。称取2.0 g亚硝酸钠样品溶于水配成250 mL溶液,取出25. 00 mL溶液于锥形瓶中,再用0. 1000 mol· L-1的酸性KMnO4标准溶液进行滴定,消耗酸性KMnO4标准溶液的体积如表:
| 实验组 | 第一组 | 第二组 | 第三组 | 第四组 |
| 消耗酸性KMnO4标准溶液的体积/mL | 9.97 | 10.02 | 12. 01 | 10. 01 |
您最近一年使用:0次
2022-05-27更新
|
396次组卷
|
5卷引用:河北省秦皇岛市2022届高三三模化学试题
河北省秦皇岛市2022届高三三模化学试题(已下线)专题16 化学实验综合题-2022年高考真题模拟题分项汇编河南省2022届高三下学期仿真模拟大联考理科综合化学试题(已下线)新疆博乐高级中学2022届高三第一次诊断性测试理科综合化学试卷广东省部分学校2022届高三下学期高考冲刺化学试题
2022·江苏·模拟预测
解题方法
5 . 铁矿石中含铁量的测定是铁元素提炼的基础和前提,目前主要采用重铬酸钾法测定铁矿石中的铁含量,其流程如图所示:
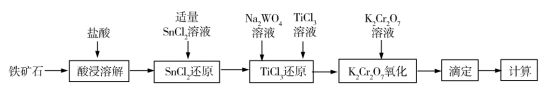
已知:①氧化性顺序: >Fe3+>WO
>Fe3+>WO ;
;
②Sn在溶液中的主要存在形式为Sn2+和SnCl ;
;
③二苯胺磺酸钠可作氧化还原指示剂,氧化型为紫红色,还原型为无色。
回答下列问题:
(1)提高“酸浸溶解”速率可采取的措施有_______ (任写两条)。
(2)“SnCl2还原”过程的离子反应方程式为_______ 。
(3)“SnCl2还原”后溶液仍呈浅黄色,而“TiCl3还原”后溶液呈现蓝色溶液(五价钨溶液为蓝色),则蓝色溶液中铁元素的主要存在形式为_______ ,Na2WO4的作用为_______ 。
(4)滴定前先进行“K2Cr2O7氧化”,即滴加K2Cr2O7溶液至溶液蓝色褪去,请分析该过程的目的是_______ 。
(5)“滴定”过程以二苯胺磺酸钠为指示剂,用酸性K2Cr2O7标准溶液滴定,滴定的反应离子方程式为_______ ;平行滴定5次,其中一组数据异常,所测c(Fe3+)偏大,原因可能是_______ (填标号)。
A.滴定终点读数时仰视滴定管刻度线
B.摇动锥形瓶时有液体溅出
C.未进行“K2Cr2O7氧化”过程就开始滴定
D.加入二苯胺磺酸钠指示剂的量过多
(6)现称取mg铁矿石进行测定,“滴定”时共消耗VmLcmol·L−1K2Cr2O7,则该铁矿石中铁的质量分数为_______ (用含m、c、V的代数式表示)。

已知:①氧化性顺序:
 >Fe3+>WO
>Fe3+>WO ;
;②Sn在溶液中的主要存在形式为Sn2+和SnCl
 ;
;③二苯胺磺酸钠可作氧化还原指示剂,氧化型为紫红色,还原型为无色。
回答下列问题:
(1)提高“酸浸溶解”速率可采取的措施有
(2)“SnCl2还原”过程的离子反应方程式为
(3)“SnCl2还原”后溶液仍呈浅黄色,而“TiCl3还原”后溶液呈现蓝色溶液(五价钨溶液为蓝色),则蓝色溶液中铁元素的主要存在形式为
(4)滴定前先进行“K2Cr2O7氧化”,即滴加K2Cr2O7溶液至溶液蓝色褪去,请分析该过程的目的是
(5)“滴定”过程以二苯胺磺酸钠为指示剂,用酸性K2Cr2O7标准溶液滴定,滴定的反应离子方程式为
A.滴定终点读数时仰视滴定管刻度线
B.摇动锥形瓶时有液体溅出
C.未进行“K2Cr2O7氧化”过程就开始滴定
D.加入二苯胺磺酸钠指示剂的量过多
(6)现称取mg铁矿石进行测定,“滴定”时共消耗VmLcmol·L−1K2Cr2O7,则该铁矿石中铁的质量分数为
您最近一年使用:0次
6 . 硫脲 是一种白色、有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
是一种白色、有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
(1)①硫脲中硫的化合价为___________ ;与硫脲互为同分异构体且能与 溶液发生显色反应的化合物的化学式为
溶液发生显色反应的化合物的化学式为___________ 。
②可用酸性 溶液滴定硫脲,已知
溶液滴定硫脲,已知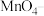 被还原为
被还原为 ,
, 被氧化为
被氧化为 、
、 及
及 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(2)某化学实验小组同学用 与
与 (石灰氮)合成硫脲并测定硫脲含量。
(石灰氮)合成硫脲并测定硫脲含量。
①制备 溶液,所用装置如图(已知酸性:
溶液,所用装置如图(已知酸性: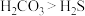 ):
):
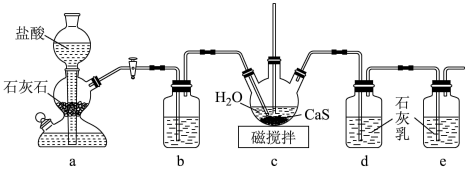
装置b中盛放的试剂是___________ ,装置c中的长直导管的作用是___________ 。
②制备硫脲:将 与
与 溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱。合适的加热方式是
溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱。合适的加热方式是___________ ;该反应的化学方程式为___________ 。
③测定硫脲含量的方法如下:
步骤1:准确称取a g产品,经溶解等步骤最后在500 mL容量瓶中定容。
步骤2:准确量取20.00mL配制好的溶液注入碘量瓶中,加入
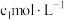
 的标准溶液及适量的NaOH溶液,于暗处放置10 min。[相关反应:
的标准溶液及适量的NaOH溶液,于暗处放置10 min。[相关反应: ,
,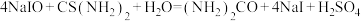 ]
]
步骤3:加水及适量的盐酸,摇匀。
步骤4:用 标准
标准 溶液滴定剩余的
溶液滴定剩余的 (相关反应:
(相关反应: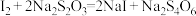 ),加入淀粉溶液,滴定至终点时消耗
),加入淀粉溶液,滴定至终点时消耗 溶液
溶液 。
。
“步骤4”滴定至终点时的颜色变化是___________ ,产品中 的质量分数为
的质量分数为___________ (列出计算式)。
 是一种白色、有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
是一种白色、有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:(1)①硫脲中硫的化合价为
 溶液发生显色反应的化合物的化学式为
溶液发生显色反应的化合物的化学式为②可用酸性
 溶液滴定硫脲,已知
溶液滴定硫脲,已知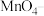 被还原为
被还原为 ,
, 被氧化为
被氧化为 、
、 及
及 ,该反应的离子方程式为
,该反应的离子方程式为(2)某化学实验小组同学用
 与
与 (石灰氮)合成硫脲并测定硫脲含量。
(石灰氮)合成硫脲并测定硫脲含量。①制备
 溶液,所用装置如图(已知酸性:
溶液,所用装置如图(已知酸性: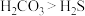 ):
):
装置b中盛放的试剂是
②制备硫脲:将
 与
与 溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱。合适的加热方式是
溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱。合适的加热方式是③测定硫脲含量的方法如下:
步骤1:准确称取a g产品,经溶解等步骤最后在500 mL容量瓶中定容。
步骤2:准确量取20.00mL配制好的溶液注入碘量瓶中,加入

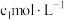
 的标准溶液及适量的NaOH溶液,于暗处放置10 min。[相关反应:
的标准溶液及适量的NaOH溶液,于暗处放置10 min。[相关反应: ,
,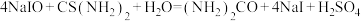 ]
]步骤3:加水及适量的盐酸,摇匀。
步骤4:用
 标准
标准 溶液滴定剩余的
溶液滴定剩余的 (相关反应:
(相关反应: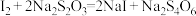 ),加入淀粉溶液,滴定至终点时消耗
),加入淀粉溶液,滴定至终点时消耗 溶液
溶液 。
。“步骤4”滴定至终点时的颜色变化是
 的质量分数为
的质量分数为
您最近一年使用:0次
名校
7 . 二氧化钒(VO2)是一种新型热敏材料。实验室以V2O5为原料合成用于制备VO2的氧钒(IV)碱式碳酸铵晶体,过程如下:
V2O5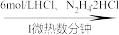 VOCl2溶液
VOCl2溶液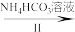 (NH4)5[(VO)6(CO3)4(OH)9]·10H2O
(NH4)5[(VO)6(CO3)4(OH)9]·10H2O
回答下列问题:
(1)步骤I中生成VOCl2的同时生成一种无色无污染的气体,该反应的化学方程式为_______ 。已知:氧化性:V2O5>Cl2,则加入N2H4·2HCl的作用是_______ 。
(2)步骤II可在如图装置(气密性良好)中进行。已知:VO2+能被O2氧化。
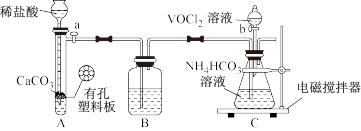
装置B中盛装的试剂是_______ ;向C中通入是CO2的作用是_______ 。
(3)加完VOCl2溶液后继续搅拌数分钟,使反应完全,小心取下分液漏斗,停止通气,立即塞上橡胶塞,将锥形瓶置于CO2保护下的干燥器中,静置过夜,得到紫色晶体,过滤。此时紫色晶体上残留的杂质离子主要为_______ ,接下来的简要操作是_______ ,最后用乙醚洗涤2-3次,干燥后称重。(所用药品为:饱和NH4HCO3溶液,无水乙醇)。
(4)测定氧钒(IV)碱式碳酸铵晶体粗产品中钒的含量。称量5.1000g样品于锥形瓶中,用硫酸溶液溶解后得到含VO2+的溶液,加稍过量的0.0200 mol/L的KMnO4溶液将VO2+氧化为VO ,充分反应后加入特定的还原剂X除去过量的KMnO4,最后用0.0800 mol/L的(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗体积为30.00mL。(滴定反应:
,充分反应后加入特定的还原剂X除去过量的KMnO4,最后用0.0800 mol/L的(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗体积为30.00mL。(滴定反应: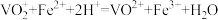 )
)
①在该实验条件下,还原剂X与Mn2+、VO2+的还原性由大到小为_______ 。
②粗产品中钒元素的质量分数为_______ 。(保留四位有效数字)
V2O5
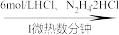 VOCl2溶液
VOCl2溶液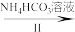 (NH4)5[(VO)6(CO3)4(OH)9]·10H2O
(NH4)5[(VO)6(CO3)4(OH)9]·10H2O回答下列问题:
(1)步骤I中生成VOCl2的同时生成一种无色无污染的气体,该反应的化学方程式为
(2)步骤II可在如图装置(气密性良好)中进行。已知:VO2+能被O2氧化。

装置B中盛装的试剂是
(3)加完VOCl2溶液后继续搅拌数分钟,使反应完全,小心取下分液漏斗,停止通气,立即塞上橡胶塞,将锥形瓶置于CO2保护下的干燥器中,静置过夜,得到紫色晶体,过滤。此时紫色晶体上残留的杂质离子主要为
(4)测定氧钒(IV)碱式碳酸铵晶体粗产品中钒的含量。称量5.1000g样品于锥形瓶中,用硫酸溶液溶解后得到含VO2+的溶液,加稍过量的0.0200 mol/L的KMnO4溶液将VO2+氧化为VO
 ,充分反应后加入特定的还原剂X除去过量的KMnO4,最后用0.0800 mol/L的(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗体积为30.00mL。(滴定反应:
,充分反应后加入特定的还原剂X除去过量的KMnO4,最后用0.0800 mol/L的(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗体积为30.00mL。(滴定反应: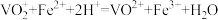 )
)①在该实验条件下,还原剂X与Mn2+、VO2+的还原性由大到小为
②粗产品中钒元素的质量分数为
您最近一年使用:0次
2022-03-22更新
|
1079次组卷
|
5卷引用:河北省衡水中学2022届高三第一次模拟考试化学试题
名校
8 . 2020年初,突如其来的新型冠状肺炎在全世界肆虐,依据研究,含氯消毒剂可以有效消灭新冠病毒,为阻断疫情做出了巨大贡献。二氧化氯(ClO2)就是其中一种高效消毒灭菌剂,但其稳定性较差,可转化为NaClO2保存。分别利用吸收法和电解法两种方法得到较稳定的NaClO2。其工艺流程示意图如图所示:

已知:(Ⅰ)纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
(Ⅱ)饱和NaClO2溶液在温度低于38 ℃时析出的晶体是NaClO2·3H2O,高于38 ℃时析出的晶体是NaClO2,高于60 ℃时NaClO2分解成NaClO3和NaCl。
(1)步骤1中,生成C1O2的离子方程式是_______ ,通入空气的作用是_________ 。
(2)方法1中,反应的离子方程式是_________________ ,利用方法1制NaClO2时,温度不能超过20 ℃,可能的原因是______ 。
(3)方法2中,将ClO2通入电解槽的阴极室,饱和NaCl溶液加入电解槽的阳极室,电解一段时间后,可得到产品,写出电解时阴极的电极反应式________________ 。
(4)步骤3中从NaClO2溶液中获得NaClO2晶体的操作步骤为:①减压,55 ℃蒸发结晶;②趁热过滤;③__________________ ;④低于60 ℃干燥,得到成品。
(5)为测定制得的晶体中NaClO2的含量,做如下操作:
①称取a g样品于烧杯中,加入适量蒸馏水溶解后加过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应。将所得混合液配成100 mL待测溶液。
②移取25.00 mL待测溶液于锥形瓶中,用b mol·L−1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得消耗标准溶液的体积的平均值为c mL(已知:I2+2 =2I−+
=2I−+ )。样品中NaClO2的质量分数为
)。样品中NaClO2的质量分数为_____ 。(用含a、b、c的代数式表示)。在滴定操作正确无误的情况下,测得结果偏高,可能的原因是_______________ (用离子方程式和文字表示)。

已知:(Ⅰ)纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
(Ⅱ)饱和NaClO2溶液在温度低于38 ℃时析出的晶体是NaClO2·3H2O,高于38 ℃时析出的晶体是NaClO2,高于60 ℃时NaClO2分解成NaClO3和NaCl。
(1)步骤1中,生成C1O2的离子方程式是
(2)方法1中,反应的离子方程式是
(3)方法2中,将ClO2通入电解槽的阴极室,饱和NaCl溶液加入电解槽的阳极室,电解一段时间后,可得到产品,写出电解时阴极的电极反应式
(4)步骤3中从NaClO2溶液中获得NaClO2晶体的操作步骤为:①减压,55 ℃蒸发结晶;②趁热过滤;③
(5)为测定制得的晶体中NaClO2的含量,做如下操作:
①称取a g样品于烧杯中,加入适量蒸馏水溶解后加过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应。将所得混合液配成100 mL待测溶液。
②移取25.00 mL待测溶液于锥形瓶中,用b mol·L−1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得消耗标准溶液的体积的平均值为c mL(已知:I2+2
 =2I−+
=2I−+ )。样品中NaClO2的质量分数为
)。样品中NaClO2的质量分数为
您最近一年使用:0次
2021-11-12更新
|
429次组卷
|
3卷引用:河北省唐山市第一中学2021-2022学年高三上学期期中考试化学试题
2022·河北·模拟预测
解题方法
9 . MnSO4是一种重要的化工产品。以菱锰矿(主要成分为MnCO3,还含有Fe3O4、FeO、CoO等)为原料制备MnSO4晶体的工艺流程如图。

回答下列问题:
(1)为提高酸浸率,可采用的方法是____ (填一种即可)。
(2)沉淀池Ⅰ中,加入MnO2的作用是___ 。
已知酸浸后c(Mn2+)=0.4mol·L-1,Ksp[Fe(OH)3]=4×10-38,Ksp[Fe(OH)2]=8×10-16,Ksp[Mn(OH)2]=4×10-14,则加入氨水调节溶液pH的范围是______ (已知离子浓度≤10-5mol·L-1时沉淀完全;lg2=0.3)。
(3)沉淀2的主要成分是___ 。
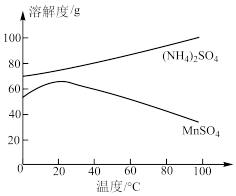
(4)如图为MnSO4和(NH4)2SO4的溶解度曲线。从含MnSO4的溶液[含杂质(NH4)2SO4]中提取MnSO4晶体的操作为___ 、洗涤、干燥。
(5)受实际条件限制,酸浸池所得的废渣中还含有锰元素,其含量测定方法如下。
ⅰ.称取6.4g废渣,加酸将锰元素全部溶出成Mn2+,过滤,将滤液定容于250mL容量瓶中;
ⅱ.取25.00mL溶液于锥形瓶中,加入少量催化剂和过量(NH4)2S2O8溶液,加热、充分反应后,煮沸溶液[已知(NH4)2S2O8具有氧化性,受热易分解];
ⅲ.用0.1000mol·L-1(NH4)2Fe(SO4)2溶液滴定。
ⅳ.进行三次平行实验,滴定至终点时消耗(NH4)2Fe(SO4)2溶液的平均体积为24.00mL,MnO 重新变成Mn2+。
重新变成Mn2+。
①ⅱ中煮沸溶液的目的是____ 。
②废渣中锰元素的质量分数为___ 。(保留两位有效数字)

回答下列问题:
(1)为提高酸浸率,可采用的方法是
(2)沉淀池Ⅰ中,加入MnO2的作用是
已知酸浸后c(Mn2+)=0.4mol·L-1,Ksp[Fe(OH)3]=4×10-38,Ksp[Fe(OH)2]=8×10-16,Ksp[Mn(OH)2]=4×10-14,则加入氨水调节溶液pH的范围是
(3)沉淀2的主要成分是
(4)如图为MnSO4和(NH4)2SO4的溶解度曲线。从含MnSO4的溶液[含杂质(NH4)2SO4]中提取MnSO4晶体的操作为

(5)受实际条件限制,酸浸池所得的废渣中还含有锰元素,其含量测定方法如下。
ⅰ.称取6.4g废渣,加酸将锰元素全部溶出成Mn2+,过滤,将滤液定容于250mL容量瓶中;
ⅱ.取25.00mL溶液于锥形瓶中,加入少量催化剂和过量(NH4)2S2O8溶液,加热、充分反应后,煮沸溶液[已知(NH4)2S2O8具有氧化性,受热易分解];
ⅲ.用0.1000mol·L-1(NH4)2Fe(SO4)2溶液滴定。
ⅳ.进行三次平行实验,滴定至终点时消耗(NH4)2Fe(SO4)2溶液的平均体积为24.00mL,MnO
 重新变成Mn2+。
重新变成Mn2+。①ⅱ中煮沸溶液的目的是
②废渣中锰元素的质量分数为
您最近一年使用:0次
解题方法
10 . 无水四氯化锡( )可用于制作导电玻璃,导电玻璃广泛用于液晶显示屏、薄膜太阳能电池基底等。可用如图装置制备四氯化锡(部分夹持装置已略去):
)可用于制作导电玻璃,导电玻璃广泛用于液晶显示屏、薄膜太阳能电池基底等。可用如图装置制备四氯化锡(部分夹持装置已略去):

有关信息如下表:
回答下列问题:
(1)仪器A的名称为_______ ,仪器A中发生反应的离子方程式为_______ 。
(2)将装置如图连接好之后,首先应进行的操作为_______ ,而后慢慢滴入浓盐酸,待观察到丁装置中充满黄绿色气体后,开始加热丁装置,锡熔化后适当增大氯气流量并继续加热丁装置。
(3)戊装置中球形冷凝管的冷水进口为_______ (填“a”或“b”)。
(4)己装置中碱石灰的作用是_______ 。
(5) 和
和 的反应产物可能会有
的反应产物可能会有 和
和 ,为防止产品中带入
,为防止产品中带入 ,除了通入过量氯气外,应控制温度在
,除了通入过量氯气外,应控制温度在_______ ~_______  范围内。
范围内。
(6)为了确认丁装置中有 生成,可选用以下_______(填标号)检验。
生成,可选用以下_______(填标号)检验。
(7)碘氧化法滴定分析产品中 (Ⅱ)的含量。准确称取
(Ⅱ)的含量。准确称取 产品于锥形瓶中,用适量浓盐酸溶解,淀粉溶液作指示剂,用
产品于锥形瓶中,用适量浓盐酸溶解,淀粉溶液作指示剂,用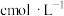 碘标准溶液滴定。实验中达到滴定终点的颜色变化为
碘标准溶液滴定。实验中达到滴定终点的颜色变化为_______ ,若此时消耗碘标准溶液 ,则产品中
,则产品中 (Ⅱ)的质量分数为
(Ⅱ)的质量分数为_______ (用字母表示)。
 )可用于制作导电玻璃,导电玻璃广泛用于液晶显示屏、薄膜太阳能电池基底等。可用如图装置制备四氯化锡(部分夹持装置已略去):
)可用于制作导电玻璃,导电玻璃广泛用于液晶显示屏、薄膜太阳能电池基底等。可用如图装置制备四氯化锡(部分夹持装置已略去):
有关信息如下表:
| 化学式 |  |  |  |
熔点 | 232 | 246 |  |
沸点 | 2260 | 652 | 114 |
| 其他性质 | 银白色固体金属 | 无色晶体, (Ⅱ)易被 (Ⅱ)易被 、 、 等氧化成 等氧化成 (Ⅳ) (Ⅳ) | 无色液体,易水解 |
(1)仪器A的名称为
(2)将装置如图连接好之后,首先应进行的操作为
(3)戊装置中球形冷凝管的冷水进口为
(4)己装置中碱石灰的作用是
(5)
 和
和 的反应产物可能会有
的反应产物可能会有 和
和 ,为防止产品中带入
,为防止产品中带入 ,除了通入过量氯气外,应控制温度在
,除了通入过量氯气外,应控制温度在 范围内。
范围内。(6)为了确认丁装置中有
 生成,可选用以下_______(填标号)检验。
生成,可选用以下_______(填标号)检验。| A.稀盐酸 | B.酸性高锰酸钾溶液 |
C.加入少量含有 的 的 溶液 溶液 | D. 稀溶液 稀溶液 |
 (Ⅱ)的含量。准确称取
(Ⅱ)的含量。准确称取 产品于锥形瓶中,用适量浓盐酸溶解,淀粉溶液作指示剂,用
产品于锥形瓶中,用适量浓盐酸溶解,淀粉溶液作指示剂,用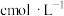 碘标准溶液滴定。实验中达到滴定终点的颜色变化为
碘标准溶液滴定。实验中达到滴定终点的颜色变化为 ,则产品中
,则产品中 (Ⅱ)的质量分数为
(Ⅱ)的质量分数为
您最近一年使用:0次
2021-11-05更新
|
199次组卷
|
3卷引用:河北省邢台市“五岳联盟”部分重点学校2021-2022学年高三上学期期中考试化学试题



