名校
1 . 下列实验现象及结论均正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 氯化亚铁溶液中滴加酸性KMnO4溶液 | KMnO4溶液褪色 | 亚铁离子具有还原性 |
| B | 向溴化钾溶液中加入过量的新制氯水,再加入碘化钾淀粉溶液 | 溶液变成蓝色 | 氧化性:Cl2>Br2>I2 |
| C | 向某待测液中加入氢氧化钠溶液 | 产生白色沉淀 | 溶液中含有Fe2+ |
| D | 向某溶液中加入盐酸,无现象,再加入BaCl2溶液 | 产生白色沉淀 | 该溶液中含SO42- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 如图为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素原子的核电荷数为X元素的2倍。下列说法正确的是
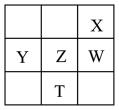

| A.简单离子半径:Z<W |
| B.Y、Z、W元素的最高价氧化物对应的水化物的酸性依次减弱 |
| C.根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性 |
| D.X、W、Z元素的原子半径及它们的简单气态氢化物的热稳定性均依次增大 |
您最近一年使用:0次
名校
解题方法
3 . 氯气和漂白粉是现代工业和生活中常用的杀菌消毒剂,某兴趣小组利用所给仪器制备纯净干燥的氯气,并模拟工业制漂白粉,请回答下列问题:
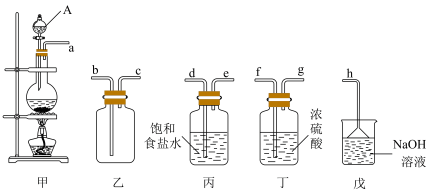
Ⅰ.氯气的制备
(1)A仪器的名称是___________ 。
(2)制取纯净氯气(必须防止尾气污染)对应装置接口的连接顺序为:a___________ 。
(3)写出实验室用浓盐酸和二氧化锰制氯气的离子方程式___________ ;浓盐酸在反应中体现了___________ (填字母序号)。
A.酸性 B.氧化性 C.还原性 D.不稳定性
Ⅱ.漂白粉的制备
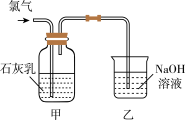
(4)①写出制漂白粉的化学方程式___________ 。
②装置乙的作用是___________ ,写出所发生反应的离子方程式:___________ 。

Ⅰ.氯气的制备
(1)A仪器的名称是
(2)制取纯净氯气(必须防止尾气污染)对应装置接口的连接顺序为:a
(3)写出实验室用浓盐酸和二氧化锰制氯气的离子方程式
A.酸性 B.氧化性 C.还原性 D.不稳定性
Ⅱ.漂白粉的制备

(4)①写出制漂白粉的化学方程式
②装置乙的作用是
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题
(1)实验室常用二氧化锰和浓盐酸制备氯气,其反应为: HCl(浓)+
HCl(浓)+ MnO2
MnO2
 Cl2↑+
Cl2↑+ MnCl2+
MnCl2+ H2O,请完成该化学方程式的配平
H2O,请完成该化学方程式的配平______ 。
(2)已知高锰酸钾和浓盐酸也可用于制备氯气,其反应为:2KMnO4+16HCl(浓)=2KCl+2MnCl2↑+5Cl2↑+8H2O。
①浓盐酸在反应中显示出来的性质是___________ (填序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②该反应中,___________ 是氧化剂(填写化学式,下同),___________ 是氧化产物,___________ 元素被氧化。产生1分子Cl2,转移的电子为___________ 个。
③用单线桥法表示电子得失的方向和数目:___________ 。
(1)实验室常用二氧化锰和浓盐酸制备氯气,其反应为:
 HCl(浓)+
HCl(浓)+ MnO2
MnO2
 Cl2↑+
Cl2↑+ MnCl2+
MnCl2+ H2O,请完成该化学方程式的配平
H2O,请完成该化学方程式的配平(2)已知高锰酸钾和浓盐酸也可用于制备氯气,其反应为:2KMnO4+16HCl(浓)=2KCl+2MnCl2↑+5Cl2↑+8H2O。
①浓盐酸在反应中显示出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②该反应中,
③用单线桥法表示电子得失的方向和数目:
您最近一年使用:0次
名校
5 . 根据所学知识,回答下列问题:
(1)下表是对一些物质进行分类
其中 Na2O2中O____ 价,它____ 碱性氧化物(填“是”或“不是”)
(2)过氧化钠水溶液中加入几滴紫色石蕊试液,现象:___________ ,写出过氧化钠与水反应的离子方程式:___________ 。
(3)实验室氯气不能排放在空气中,可用氢氧化钠溶液处理,其原因是:__________ 。氯气通入到⑥的溶液中的离子方程式:___________ 。
(4)如何要检验某溶液中是否含有钾元素,可以用操作方法:___________ 。
(5)实验室通过反应KMnO4+HCl(浓)—MnCl2+KCl+Cl2↑+H2O(未配平)制备氯气,反应中氯化氢表现出的性质是_____ 。(填写字母)
a.还原性 b.酸性 c.氧化性
请配平该反应,并用双线桥标电子转移的方向和数目:___________ 。
(1)下表是对一些物质进行分类
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 单质 |
| 化学式 | ①H2SO4 ②HCl | ③NaOH ④Ba(OH)2 | ⑤NaHCO3 ⑥NaI | ⑦CO2 ⑧Na2O2 | ⑨O2 ⑩Cl2 |
(2)过氧化钠水溶液中加入几滴紫色石蕊试液,现象:
(3)实验室氯气不能排放在空气中,可用氢氧化钠溶液处理,其原因是:
(4)如何要检验某溶液中是否含有钾元素,可以用操作方法:
(5)实验室通过反应KMnO4+HCl(浓)—MnCl2+KCl+Cl2↑+H2O(未配平)制备氯气,反应中氯化氢表现出的性质是
a.还原性 b.酸性 c.氧化性
请配平该反应,并用双线桥标电子转移的方向和数目:
您最近一年使用:0次
12-13高一下·黑龙江鹤岗·期中
名校
解题方法
6 . 以下关于锂、钠、钾、铷、铯的叙述不正确的是( )
①氢氧化物中碱性最强的是CsOH
②单质熔点最高的是铯
③与O2反应均可得到多种氧化物
④它们的密度依次增大,要保存在煤油中
⑤其单质的还原性依次增强
⑥它们对应离子的氧化性依次增强
①氢氧化物中碱性最强的是CsOH
②单质熔点最高的是铯
③与O2反应均可得到多种氧化物
④它们的密度依次增大,要保存在煤油中
⑤其单质的还原性依次增强
⑥它们对应离子的氧化性依次增强
| A.①③⑤ | B.②④⑥ | C.②③④⑥ | D.①⑤ |
您最近一年使用:0次
2020-03-27更新
|
302次组卷
|
11卷引用:2015-2016学年四川省成都七中高一下第一次阶段测化学卷
2015-2016学年四川省成都七中高一下第一次阶段测化学卷2015-2016学年四川省成都市七中高一下学期期中化学试卷四川省遂宁市射洪县射洪中学校2019-2020学年高一下学期第一次学月考试化学试题四川省达州市第一中学校2021-2022学年高一下学期第一次月考化学试题(已下线)2012-2013学年黑龙江省鹤岗一中高一下学期期中考试化学试卷2015-2016学年湖南省长郡中学高一下期中化学试卷云南省富宁县三中2019-2020学年高一上学期期末考试化学试题天津市第九十五中学2019-2020学年高一下学期3月检测考试化学试题甘肃省天水市秦安县第一中学2019-2020学年高一上学期期末考试化学试题广西南宁市沛鸿高中2020-2021学年高一3月月考化学试题内蒙古赤峰市元宝山区第一中学2021-2022学年高一下学期4月月考化学试题
7 . 下列实验操作、实验现象以及所得出的结论均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向蓝色石蕊试纸上滴加氯水 | 试纸由蓝变红,后颜色褪去 | 氯气具有强氧化性和漂白性 |
| B | 将草酸溶液逐滴滴入酸性高锰酸钾溶液中至过量 | 溶液紫红色逐渐褪色 | 草酸溶液具有还原性 |
| C | 用玻璃棒蘸取溶液在酒精灯火焰上灼烧 | 火焰呈黄色 | 溶液中含Na+ |
| D | 向某溶液中加入盐酸酸化的BaCl2溶液 | 有白色沉淀产生 | 该溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 重铬酸铵[(NH4)2Cr2O7](M=252 g·mol-1)常用作分析试剂、催化剂及媒染剂等。某化学兴趣小组对重铬酸铵的一些性质及组成进行探究。已知: + H2O
+ H2O 2
2 +2H+。回答下列问题:
+2H+。回答下列问题:
(1)在试管中加入少量重铬酸铵样品,滴加足量6 mol·L-1 NaOH溶液,振荡、微热。产生的现象是______________________ 。
(2)为探究重铬酸铵的分解产物,按下图连接好装置,在A中加入2.52 g重铬酸铵样品进行实验。

①实验过程中通入N2的主要目的是___________ 。
②实验过程中,若发现加热温度不够,如何改进?___________ 。
③C装置的作用是___________ 。加热A至恒重,观察到B中固体由白变蓝,D中酚酞溶液不变色,同时测得A中剩余固体1.52 g、B增重0.72 g,另外分解产物中还含有N2,则重铬酸铵受热分解的化学方程式为___________ 。
(3)为探究溶液酸性增强对铬(VI)盐溶液氧化性或Na2SO3溶液还原性的影响,该小组利用下图装置继续实验(已知物质氧化性与还原性强弱差异越大,电压越大)。

a.K闭合时,记录电压。
b.向U型管左侧溶液中滴加硫酸至pH=2后,电压增大了y。
c.继续向U型管右侧溶液中滴加硫酸后,无气体逸出,电压几乎不变。
①上述实验得出结论:___________ ;酸性增强,对Na2SO3溶液还原性几乎无影响。
②有同学认为:随着溶液酸性的增强,溶液中O2的氧化性增强也会使电压增大。补做实验:U型管左管中改为盛放___________ 溶液;然后向左管中滴加硫酸至pH=2后,测得电压增大了z,若z_____ y(填“>”、“<”或“=”),则证明实验结论不受影响。
 + H2O
+ H2O 2
2 +2H+。回答下列问题:
+2H+。回答下列问题:(1)在试管中加入少量重铬酸铵样品,滴加足量6 mol·L-1 NaOH溶液,振荡、微热。产生的现象是
(2)为探究重铬酸铵的分解产物,按下图连接好装置,在A中加入2.52 g重铬酸铵样品进行实验。

①实验过程中通入N2的主要目的是
②实验过程中,若发现加热温度不够,如何改进?
③C装置的作用是
(3)为探究溶液酸性增强对铬(VI)盐溶液氧化性或Na2SO3溶液还原性的影响,该小组利用下图装置继续实验(已知物质氧化性与还原性强弱差异越大,电压越大)。

a.K闭合时,记录电压。
b.向U型管左侧溶液中滴加硫酸至pH=2后,电压增大了y。
c.继续向U型管右侧溶液中滴加硫酸后,无气体逸出,电压几乎不变。
①上述实验得出结论:
②有同学认为:随着溶液酸性的增强,溶液中O2的氧化性增强也会使电压增大。补做实验:U型管左管中改为盛放
您最近一年使用:0次
9 . 储氢碳纳米管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的碳纳米颗粒杂质,这种碳纳米颗粒可用氧化气化法提纯,反应的化学方程式为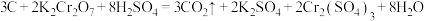 。
。
回答下列问题:
(1)该反应中,还原剂是___________ (填元素式),被还原的元素是___________ (填化学符号)。
(2)该反应中, 表现出
表现出___________ (填“氧化性”或“还原性”), 发生了
发生了___________ (填“氧化反应”或“还原反应”)。
(3) 在该反应中表现出___________(填字母)。
在该反应中表现出___________(填字母)。
(4)该反应中,还原产物是___________ (填化学式)。
(5)每生成2个 分子,转移
分子,转移___________ 个电子。
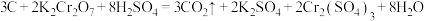 。
。回答下列问题:
(1)该反应中,还原剂是
(2)该反应中,
 表现出
表现出 发生了
发生了(3)
 在该反应中表现出___________(填字母)。
在该反应中表现出___________(填字母)。| A.只有酸性 | B.只有氧化性 | C.酸性和氧化性 | D.酸性和还原性 |
(5)每生成2个
 分子,转移
分子,转移
您最近一年使用:0次
名校
10 . 硫代硫酸钠晶体(Na2S2O3∙5H2O,M=248g∙mol−1)可用作定影剂、还原剂。回答下列问题:
(1)已知:Na2S2O3为易溶于水的固体,往Na2S2O3溶液中加入稀盐酸会发生歧化反应 +2H+=S↓+SO2↑+2H2O。BaS2O3为难溶于水的固体。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
+2H+=S↓+SO2↑+2H2O。BaS2O3为难溶于水的固体。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
试剂:稀盐酸、稀H2SO4、BaCl2溶液、Na2CO3溶液、H2O2溶液
(2)利用K2Cr2O7标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制:称取1.2000g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在______ 中溶解,完全溶解后,全部转移至100mL_______ 中,加蒸馏水至______ 。
②滴定:取0.00950mol∙L−1的K2Cr2O7(强氧化性物质,其还原产物为Cr3+)标准溶液20.00mL,硫酸酸化后加入过量KI(强还原性物质),发生反应的离子方程式为_____ 然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应I2+2 =
=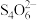 +2I-加入淀粉溶液作为指示剂,继续滴定,当溶液由蓝色变为无色且2半分钟不复原,即为终点。平行滴定3次,样品溶液的平均用量为24.80mL,则样品纯度为
+2I-加入淀粉溶液作为指示剂,继续滴定,当溶液由蓝色变为无色且2半分钟不复原,即为终点。平行滴定3次,样品溶液的平均用量为24.80mL,则样品纯度为_____ %(保留1位小数)。
(1)已知:Na2S2O3为易溶于水的固体,往Na2S2O3溶液中加入稀盐酸会发生歧化反应
 +2H+=S↓+SO2↑+2H2O。BaS2O3为难溶于水的固体。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
+2H+=S↓+SO2↑+2H2O。BaS2O3为难溶于水的固体。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:试剂:稀盐酸、稀H2SO4、BaCl2溶液、Na2CO3溶液、H2O2溶液
实验步骤 | 现象 |
①取少量样品,加入除氧蒸馏水 | ②固体完全溶解得无色澄清溶液 |
③ | ④有淡黄色沉淀和刺激性气体产生 |
⑤静置, | ⑥ |
①溶液配制:称取1.2000g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在
②滴定:取0.00950mol∙L−1的K2Cr2O7(强氧化性物质,其还原产物为Cr3+)标准溶液20.00mL,硫酸酸化后加入过量KI(强还原性物质),发生反应的离子方程式为
 =
=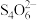 +2I-加入淀粉溶液作为指示剂,继续滴定,当溶液由蓝色变为无色且2半分钟不复原,即为终点。平行滴定3次,样品溶液的平均用量为24.80mL,则样品纯度为
+2I-加入淀粉溶液作为指示剂,继续滴定,当溶液由蓝色变为无色且2半分钟不复原,即为终点。平行滴定3次,样品溶液的平均用量为24.80mL,则样品纯度为
您最近一年使用:0次
2020-12-28更新
|
99次组卷
|
2卷引用:四川省雅安中学2020-2021学年高一12月月考化学试题



