名校
解题方法
1 . 三氯化钌( )是重要的化工原料,广泛应用于催化、电镀、电解阳极、电子工业等。从
)是重要的化工原料,广泛应用于催化、电镀、电解阳极、电子工业等。从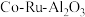 催化剂废料中分离制各
催化剂废料中分离制各 和
和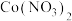 的一种工艺流程如图所示。
的一种工艺流程如图所示。
(1)基态 原子的价电子排布式为
原子的价电子排布式为___________ 。
(2)“焙烧”后所得固体主要成分为 、
、 、
、 和
和___________ 。
(3)“还原”过程会产生 和
和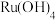 沉淀,该反应的化学方程式为
沉淀,该反应的化学方程式为______________________ 。
(4)“酸溶”过程中,先加入盐酸溶解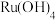 ,然后加入盐酸羟胺(
,然后加入盐酸羟胺( )得到
)得到 和
和 。则该两种产物的物质的量之比为
。则该两种产物的物质的量之比为___________ 。
(5)“蒸发结晶”在真空度为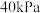 时进行(此时水的沸点是
时进行(此时水的沸点是 ),其目的是
),其目的是___________ 。
(6)若维持 不变,让
不变,让 沉淀完全(
沉淀完全( 浓度不高于
浓度不高于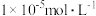 ),则混合体系中
),则混合体系中 的浓度不低于
的浓度不低于___________ 。[已知: ,
,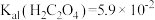 ,
, 结果保留三位小数]
结果保留三位小数]
(7)“沉钴”时,若得到的是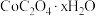 晶体,该反应的离子方程式为
晶体,该反应的离子方程式为______________________ 。
(8)该流程中,还有一种重要成分 未提取,你认为在哪一步骤后进行最合适:
未提取,你认为在哪一步骤后进行最合适:___________ 。
 )是重要的化工原料,广泛应用于催化、电镀、电解阳极、电子工业等。从
)是重要的化工原料,广泛应用于催化、电镀、电解阳极、电子工业等。从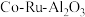 催化剂废料中分离制各
催化剂废料中分离制各 和
和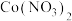 的一种工艺流程如图所示。
的一种工艺流程如图所示。
(1)基态
 原子的价电子排布式为
原子的价电子排布式为(2)“焙烧”后所得固体主要成分为
 、
、 、
、 和
和(3)“还原”过程会产生
 和
和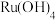 沉淀,该反应的化学方程式为
沉淀,该反应的化学方程式为(4)“酸溶”过程中,先加入盐酸溶解
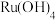 ,然后加入盐酸羟胺(
,然后加入盐酸羟胺( )得到
)得到 和
和 。则该两种产物的物质的量之比为
。则该两种产物的物质的量之比为(5)“蒸发结晶”在真空度为
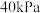 时进行(此时水的沸点是
时进行(此时水的沸点是 ),其目的是
),其目的是(6)若维持
 不变,让
不变,让 沉淀完全(
沉淀完全( 浓度不高于
浓度不高于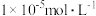 ),则混合体系中
),则混合体系中 的浓度不低于
的浓度不低于 ,
,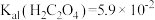 ,
, 结果保留三位小数]
结果保留三位小数](7)“沉钴”时,若得到的是
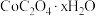 晶体,该反应的离子方程式为
晶体,该反应的离子方程式为(8)该流程中,还有一种重要成分
 未提取,你认为在哪一步骤后进行最合适:
未提取,你认为在哪一步骤后进行最合适:
您最近一年使用:0次
2024-01-09更新
|
1292次组卷
|
6卷引用:湖南省株洲市2024届高三上学期教学质量统一检测化学试题
湖南省株洲市2024届高三上学期教学质量统一检测化学试题湖南省株洲市2023-2024学年高三上学期教学质量统一检测化学试卷2024届湖南省长沙市雅礼中学高三下学期3月综合测试(一)化学试题(已下线)专题08 工艺流程综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)大题01 化工流程综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)2024届江西省贵溪市实验中学高三下学期5月模拟考试压轴(三)化学试卷
名校
2 . 稀土是一种重要的战略资源,我国是稀土储量最大的国家。铈( )是一种典型的稀土元素,其在自然界中主要以氟碳铈矿(主要成分为
)是一种典型的稀土元素,其在自然界中主要以氟碳铈矿(主要成分为 )形式存在。工业上利用氟碳铈矿制取
)形式存在。工业上利用氟碳铈矿制取 的一种工艺流程如图:
的一种工艺流程如图:

下列说法错误的是
 )是一种典型的稀土元素,其在自然界中主要以氟碳铈矿(主要成分为
)是一种典型的稀土元素,其在自然界中主要以氟碳铈矿(主要成分为 )形式存在。工业上利用氟碳铈矿制取
)形式存在。工业上利用氟碳铈矿制取 的一种工艺流程如图:
的一种工艺流程如图:
下列说法错误的是
A.倍烧过程中氧化剂与还原剂的物质的量之比为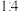 |
B.通过操作Ⅱ(包含酸溶、蒸发结晶)即可得到纯净的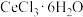 |
| C.酸浸过程中用稀硫酸和双氧水替代盐酸可体现环境友好 |
D. 中阴离子的空间构型为正四面体 中阴离子的空间构型为正四面体 |
您最近一年使用:0次
2024-01-09更新
|
409次组卷
|
4卷引用:湖南省株洲市2024届高三上学期教学质量统一检测化学试题
3 . 氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(1)过氧化钠可用作潜水艇和消防员呼吸面具中的供氧剂,其主要原理为: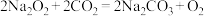 。其中Na2O2的阴、阳离子个数比为
。其中Na2O2的阴、阳离子个数比为________ 。每消耗2个CO2分子,转移电子的数目为________ 个。在下列选项中选择,上述反应中Na2O2是________ (填字母,下同),O2是________ .
A.氧化剂 B.还原剂 C.氧化产物 D.还原产物
若要反应产生64.0gO2,同时消耗Na2O2的质量约为________ g。
(2)汽车尾气系统中均安装了催化转化器。汽车尾气中有毒的CO和NO在催化剂高温条件下发生反应,生成两种无毒气体。上述反应的化学方程式为: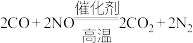 用单线桥标出反应中电子转移的方向和数目
用单线桥标出反应中电子转移的方向和数目________ 。
该反应中,氧化产物与还原产物的分子数之比为________ 。
(3)亚硝酸钠NaNO2像食盐一样有咸味,毒性很强,误食会导致血红蛋白中的Fe2+转化为Fe3+,可服用维生素C解毒。关于该过程的叙述,不正确的是________(填字母)。
(1)过氧化钠可用作潜水艇和消防员呼吸面具中的供氧剂,其主要原理为:
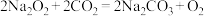 。其中Na2O2的阴、阳离子个数比为
。其中Na2O2的阴、阳离子个数比为A.氧化剂 B.还原剂 C.氧化产物 D.还原产物
若要反应产生64.0gO2,同时消耗Na2O2的质量约为
(2)汽车尾气系统中均安装了催化转化器。汽车尾气中有毒的CO和NO在催化剂高温条件下发生反应,生成两种无毒气体。上述反应的化学方程式为:
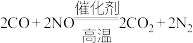 用单线桥标出反应中电子转移的方向和数目
用单线桥标出反应中电子转移的方向和数目该反应中,氧化产物与还原产物的分子数之比为
(3)亚硝酸钠NaNO2像食盐一样有咸味,毒性很强,误食会导致血红蛋白中的Fe2+转化为Fe3+,可服用维生素C解毒。关于该过程的叙述,不正确的是________(填字母)。
| A.亚硝酸钠的氧化性强于Fe3+ | B.维生素C是还原剂 |
| C.维生素C的还原性强于Fe2+ | D.亚硝酸钠是还原剂 |
您最近一年使用:0次
解题方法
4 . 二氧化氯 具有强氧化性,常用于饮用水的消毒,是国际上公认的绿色消毒剂,在水处理时自身被还原为
具有强氧化性,常用于饮用水的消毒,是国际上公认的绿色消毒剂,在水处理时自身被还原为 。某实验小组利用如下装置制备、收集
。某实验小组利用如下装置制备、收集 并验证其化学性质,化学方程式为
并验证其化学性质,化学方程式为 。请回答下列问题:
。请回答下列问题:
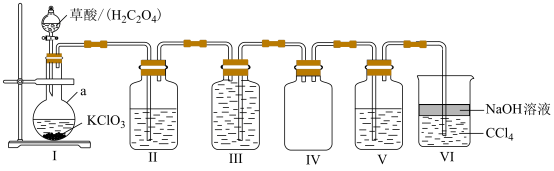
(1)装置I中仪器a的名称为___________ 。
(2)同学们查找数据发现:
① 在
在 溶液中的溶解度较小;
溶液中的溶解度较小;
② 与
与 溶液发生反应:____
溶液发生反应:____ ____
____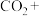 ____
____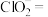 ____
____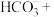 ____
____ ____
____ 。
。
请配平该离子方程式___________ 。
(3)装置II和III中均盛有饱和 溶液,请指出它们的作用。
溶液,请指出它们的作用。
装置II:___________ ,装置III:___________ 。
(4)装置V中盛有淀粉碘化钾溶液,实验时观察到的现象为___________ ;装置VI中 的作用是
的作用是___________ 。
(5)消毒效率一般以单位质量氧化剂所得的电子数表示,则 和
和 消毒效率更高的是
消毒效率更高的是___________ 。
 具有强氧化性,常用于饮用水的消毒,是国际上公认的绿色消毒剂,在水处理时自身被还原为
具有强氧化性,常用于饮用水的消毒,是国际上公认的绿色消毒剂,在水处理时自身被还原为 。某实验小组利用如下装置制备、收集
。某实验小组利用如下装置制备、收集 并验证其化学性质,化学方程式为
并验证其化学性质,化学方程式为 。请回答下列问题:
。请回答下列问题:
(1)装置I中仪器a的名称为
(2)同学们查找数据发现:
①
 在
在 溶液中的溶解度较小;
溶液中的溶解度较小;②
 与
与 溶液发生反应:____
溶液发生反应:____ ____
____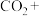 ____
____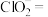 ____
____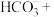 ____
____ ____
____ 。
。请配平该离子方程式
(3)装置II和III中均盛有饱和
 溶液,请指出它们的作用。
溶液,请指出它们的作用。装置II:
(4)装置V中盛有淀粉碘化钾溶液,实验时观察到的现象为
 的作用是
的作用是(5)消毒效率一般以单位质量氧化剂所得的电子数表示,则
 和
和 消毒效率更高的是
消毒效率更高的是
您最近一年使用:0次
5 . 硫酸亚铁铵晶体 俗称莫尔盐,是分析化学中的重要试剂,其化学性质与
俗称莫尔盐,是分析化学中的重要试剂,其化学性质与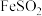 相近,但在空气中比一般的亚铁盐稳定。某同学在实验室中以铁粉与硫酸铵为原料按如下流程制备莫尔盐并测其产率(产率=
相近,但在空气中比一般的亚铁盐稳定。某同学在实验室中以铁粉与硫酸铵为原料按如下流程制备莫尔盐并测其产率(产率= )。
)。
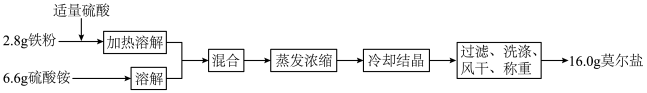
请回答下列问题:
(1)向莫尔盐溶液中加入氨水,久置后产生红褐色沉淀,该红褐色沉淀为___________ (填化学式)。莫尔盐溶液也能使酸性 溶液褪色,反应的离子方程式为
溶液褪色,反应的离子方程式为___________ 。
(2)用适量硫酸溶解铁粉时,还原产物是___________ (填化学式)。
(3)蒸发浓缩时,溶液应装在___________ 中(填仪器名称)。蒸发时不能蒸干溶液,而要在有晶体析出时立刻停止加热,原因是___________
(4)某同学通过上述流程制得莫尔盐16.0g,则实验产率为___________ (保留1位小数)。
 俗称莫尔盐,是分析化学中的重要试剂,其化学性质与
俗称莫尔盐,是分析化学中的重要试剂,其化学性质与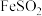 相近,但在空气中比一般的亚铁盐稳定。某同学在实验室中以铁粉与硫酸铵为原料按如下流程制备莫尔盐并测其产率(产率=
相近,但在空气中比一般的亚铁盐稳定。某同学在实验室中以铁粉与硫酸铵为原料按如下流程制备莫尔盐并测其产率(产率= )。
)。
请回答下列问题:
(1)向莫尔盐溶液中加入氨水,久置后产生红褐色沉淀,该红褐色沉淀为
 溶液褪色,反应的离子方程式为
溶液褪色,反应的离子方程式为(2)用适量硫酸溶解铁粉时,还原产物是
(3)蒸发浓缩时,溶液应装在
(4)某同学通过上述流程制得莫尔盐16.0g,则实验产率为
您最近一年使用:0次
名校
6 . 中华文化,博大精深,其中蕴含着许多化学知识。下列古诗词中对应的化学知识错误的是
| A.“铸铁作锄犁,春耕待秋熟”体现了金属的延展性 |
| B.“何意百炼刚,化为绕指柔”中,经“百炼”的钢硬度比纯铁的硬度小 |
| C.“西真人醉忆仙家,飞佩丹霞羽化”中所呈现的丹霞地貌是由于岩层中含有Fe2O3 |
| D.《秋浦歌》所描绘的“炉火照天地,红星乱紫烟”的冶炼过程中涉及到了氧化还原反应 |
您最近一年使用:0次
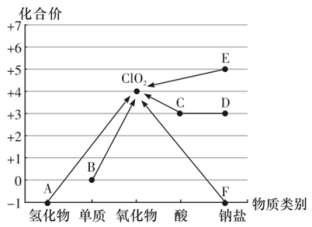
7 . 已知 气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒,以含氯物质为原料,利用“价―类”关系可设计以下
气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒,以含氯物质为原料,利用“价―类”关系可设计以下 制备方案,有关下列物质说法正确的是
制备方案,有关下列物质说法正确的是
 气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒,以含氯物质为原料,利用“价―类”关系可设计以下
气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒,以含氯物质为原料,利用“价―类”关系可设计以下 制备方案,有关下列物质说法正确的是
制备方案,有关下列物质说法正确的是
| A.物质E、F所含化学键的类型完全相同 |
| B.物质D与E中阴离子中心原子杂化类型完全相同 |
C.若由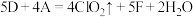 制得1mol 制得1mol ,则过程中转移电子数为 ,则过程中转移电子数为 |
D.已知常温下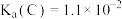 ,则C与强碱反应生成D与水在常温下的平衡常数 ,则C与强碱反应生成D与水在常温下的平衡常数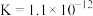 |
您最近一年使用:0次
8 . 为增强铝合金的耐磨性与耐腐蚀性,常采用铬酸氧化法钝化铝合金表面。铬酸洗液(主要成分为重铬酸H2Cr2O7)与铝合金接触后发生如下反应 (反应未配平)。下列关于此反应的叙述不正确的是
(反应未配平)。下列关于此反应的叙述不正确的是
 (反应未配平)。下列关于此反应的叙述不正确的是
(反应未配平)。下列关于此反应的叙述不正确的是| A.钝化膜中的铬以+6价形式存在 | B.反应物中的铬元素只有 被还原 被还原 |
C.每消耗 转移6 mol电子 转移6 mol电子 | D.反应发生后铬酸洗液酸性减弱 |
您最近一年使用:0次
2023-12-23更新
|
70次组卷
|
2卷引用:湖南省长沙市名校联合体2023-2024学年高一上学期第二次联考化学试题
9 . 某化学兴趣小组在研究“铁及其化合物性质”时,发现向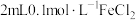 溶液中滴加2滴
溶液中滴加2滴 溶液,无明显现象,再滴加
溶液,无明显现象,再滴加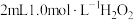 溶液(pH约为5),溶液先变红,后褪色,并有气泡产生。为了弄清楚产生这种异常现象的原因,他们进行了如下探究:
溶液(pH约为5),溶液先变红,后褪色,并有气泡产生。为了弄清楚产生这种异常现象的原因,他们进行了如下探究:
(1)溶液先变红的原因是___________ (用两个离子方程式表示)。
(2)同学们对溶液褪色的原因提出了不同的看法并进行实验:
I.甲同学认为是 被
被 还原。
还原。
取褪色后溶液,滴加___________ ,无明显现象,证明甲同学观点不正确。
II.乙同学认为是 被氧化。
被氧化。
取褪色后溶液,滴加KSCN溶液,出现红色。
根据上述实验现象,同学们认为溶液褪色的原因可能有两种:
乙同学认为 被
被 氧化。
氧化。
丙同学认为___________ 。
为了探究溶液褪色的原因究竟是上述的哪一种,该兴趣小组进行了如下实验。
向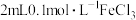 溶液中滴加2滴
溶液中滴加2滴 溶液,后通入
溶液,后通入 。发现溶液
。发现溶液___________ ,证明溶液褪色的原因不是乙同学认为的原因,而是丙同学认为的原因。
(3)该兴趣小组通过查阅资料,发现 可以被氧化成
可以被氧化成 和两种可直接排放到空气中的气体。设计实验方案验证褪色后的溶液中存在
和两种可直接排放到空气中的气体。设计实验方案验证褪色后的溶液中存在 :
:___________ 。
(4)写出上述实验中 被氧化的离子方程式:
被氧化的离子方程式:___________ 。
(5)根据题目所给信息及实验现象推断物质还原性强弱:
___________  (填“>”或“<”),理由:
(填“>”或“<”),理由:___________ 。
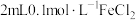 溶液中滴加2滴
溶液中滴加2滴 溶液,无明显现象,再滴加
溶液,无明显现象,再滴加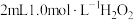 溶液(pH约为5),溶液先变红,后褪色,并有气泡产生。为了弄清楚产生这种异常现象的原因,他们进行了如下探究:
溶液(pH约为5),溶液先变红,后褪色,并有气泡产生。为了弄清楚产生这种异常现象的原因,他们进行了如下探究:(1)溶液先变红的原因是
(2)同学们对溶液褪色的原因提出了不同的看法并进行实验:
I.甲同学认为是
 被
被 还原。
还原。取褪色后溶液,滴加
II.乙同学认为是
 被氧化。
被氧化。取褪色后溶液,滴加KSCN溶液,出现红色。
根据上述实验现象,同学们认为溶液褪色的原因可能有两种:
乙同学认为
 被
被 氧化。
氧化。丙同学认为
为了探究溶液褪色的原因究竟是上述的哪一种,该兴趣小组进行了如下实验。
向
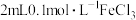 溶液中滴加2滴
溶液中滴加2滴 溶液,后通入
溶液,后通入 。发现溶液
。发现溶液(3)该兴趣小组通过查阅资料,发现
 可以被氧化成
可以被氧化成 和两种可直接排放到空气中的气体。设计实验方案验证褪色后的溶液中存在
和两种可直接排放到空气中的气体。设计实验方案验证褪色后的溶液中存在 :
:(4)写出上述实验中
 被氧化的离子方程式:
被氧化的离子方程式:(5)根据题目所给信息及实验现象推断物质还原性强弱:

 (填“>”或“<”),理由:
(填“>”或“<”),理由:
您最近一年使用:0次
2023-12-23更新
|
155次组卷
|
2卷引用:湖南省长沙市南雅中学2023-2024学年高一上学期第三次12月月考化学试卷
名校
10 . 某小组为了探究影响 溶液与
溶液与 溶液在酸性[所用试剂浓度:
溶液在酸性[所用试剂浓度:
 ]条件下反应速率的因素,设计的实验方案如表所示。混合溶液的体积变化忽略不计,下列说法错误的是
]条件下反应速率的因素,设计的实验方案如表所示。混合溶液的体积变化忽略不计,下列说法错误的是
 溶液与
溶液与 溶液在酸性[所用试剂浓度:
溶液在酸性[所用试剂浓度:
 ]条件下反应速率的因素,设计的实验方案如表所示。混合溶液的体积变化忽略不计,下列说法错误的是
]条件下反应速率的因素,设计的实验方案如表所示。混合溶液的体积变化忽略不计,下列说法错误的是| 实验 编号 | 实验 温度/K | 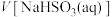 |  | 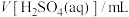 | 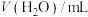 | 褪色时间 /min |
| 1 | 298 | 4.0 | 2 | 2 |  | 8 |
| 2 | 298 | 5.0 | 2 | 2 | 1 | 6 |
| 3 | 303 | 5.0 |  | 2 | 1 | 2 |
A. |
B.该反应的离子方程式为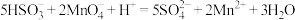 |
C.实验1中 的反应速率为 的反应速率为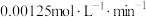 |
| D.实验2和3探究的是温度对反应速率的影响 |
您最近一年使用:0次
2023-12-21更新
|
405次组卷
|
4卷引用:湖南省常德市安乡县第一中学2023-2024学年高三上学期12月月考化学试题



