解题方法
1 .  及其水合物在建筑、工业农业、医药中有着广泛应用。一种以铁菱镁矿(主要成分是
及其水合物在建筑、工业农业、医药中有着广泛应用。一种以铁菱镁矿(主要成分是 ,还含有
,还含有 、
、 及少量
及少量 )为原料制备
)为原料制备 的工艺流程如图所示:
的工艺流程如图所示:

回答下列问题:
(1)“焙烧”时通常要将矿石粉碎,目的是___________ 。写出该过程中发生氧化还原反应的化学方程式___________ 。
(2)“滤渣1”的主要成分是___________ 。
(3)从物质分离提纯的角度考虑,“沉铁”时“X”应选用下列物质中的___________(填字母)。
(4)25℃时,为保证“沉铁”充分,至少要将溶液的pH调节到___________ (已知:①25℃, ,
, ;②一般认为,离子浓度小于
;②一般认为,离子浓度小于 时该离子即沉降完全)。检验“沉铁”充分的实验方法是
时该离子即沉降完全)。检验“沉铁”充分的实验方法是___________ 。
(5)根据 的溶解度随温度变化的情况(如图所示),由“滤液”获得
的溶解度随温度变化的情况(如图所示),由“滤液”获得 的“一系列操作”是将温度控制在67.5℃以上,蒸发结晶、
的“一系列操作”是将温度控制在67.5℃以上,蒸发结晶、___________ 、___________ 、干燥。

(6)除 外,人们发现
外,人们发现 也有着广泛应用。
也有着广泛应用。
① 可看作是
可看作是 中的一个O原子被S原子取代的产物,
中的一个O原子被S原子取代的产物, 的空间结构是
的空间结构是___________ 。
② 的晶胞是
的晶胞是 与
与 构成的长方体,
构成的长方体, 在晶胞中的位置如图所示。已知晶胞的体积为V
在晶胞中的位置如图所示。已知晶胞的体积为V ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,
, 晶体的摩尔体积
晶体的摩尔体积
___________  (列出计算式)。
(列出计算式)。

 及其水合物在建筑、工业农业、医药中有着广泛应用。一种以铁菱镁矿(主要成分是
及其水合物在建筑、工业农业、医药中有着广泛应用。一种以铁菱镁矿(主要成分是 ,还含有
,还含有 、
、 及少量
及少量 )为原料制备
)为原料制备 的工艺流程如图所示:
的工艺流程如图所示:
回答下列问题:
(1)“焙烧”时通常要将矿石粉碎,目的是
(2)“滤渣1”的主要成分是
(3)从物质分离提纯的角度考虑,“沉铁”时“X”应选用下列物质中的___________(填字母)。
| A.氨水 | B.NaOH溶液 | C.MgO | D. |
(4)25℃时,为保证“沉铁”充分,至少要将溶液的pH调节到
 ,
, ;②一般认为,离子浓度小于
;②一般认为,离子浓度小于 时该离子即沉降完全)。检验“沉铁”充分的实验方法是
时该离子即沉降完全)。检验“沉铁”充分的实验方法是(5)根据
 的溶解度随温度变化的情况(如图所示),由“滤液”获得
的溶解度随温度变化的情况(如图所示),由“滤液”获得 的“一系列操作”是将温度控制在67.5℃以上,蒸发结晶、
的“一系列操作”是将温度控制在67.5℃以上,蒸发结晶、
(6)除
 外,人们发现
外,人们发现 也有着广泛应用。
也有着广泛应用。①
 可看作是
可看作是 中的一个O原子被S原子取代的产物,
中的一个O原子被S原子取代的产物, 的空间结构是
的空间结构是②
 的晶胞是
的晶胞是 与
与 构成的长方体,
构成的长方体, 在晶胞中的位置如图所示。已知晶胞的体积为V
在晶胞中的位置如图所示。已知晶胞的体积为V ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,
, 晶体的摩尔体积
晶体的摩尔体积
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2024-03-17更新
|
428次组卷
|
2卷引用:广西壮族自治区河池市2024届高三高考联合模拟考试(3月)化学试题
名校
解题方法
2 .  是高效安全灭菌消毒剂,部分性质如下:
是高效安全灭菌消毒剂,部分性质如下:
实验室可利用反应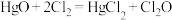 制取
制取 ,装置如图所示:
,装置如图所示:_______ 。
(2)装置①中制取氯气时需要 盐酸,若加入盐酸的体积是
盐酸,若加入盐酸的体积是 ,制取氯气的物质的量小于
,制取氯气的物质的量小于 ,除了考虑盐酸的挥发和生成水的因素外,最主要的原因是
,除了考虑盐酸的挥发和生成水的因素外,最主要的原因是_______ 。
(3)③中试剂的名称是_______ 。
(4)④中反应氧化剂和还原剂物质的量比值是_______ 。
(5)⑥中 与水反应制取
与水反应制取 ,反应的化学方程式是
,反应的化学方程式是_______ ; 中混有盐酸,原因是
中混有盐酸,原因是_______ (用化学方程式表示)。
(6)⑦中 溶液能吸收多余的氯气,防止污染空气,发生反应的离子方程式是
溶液能吸收多余的氯气,防止污染空气,发生反应的离子方程式是_______ 。
 是高效安全灭菌消毒剂,部分性质如下:
是高效安全灭菌消毒剂,部分性质如下:| 物理性质 | 化学性质 |
| 常温下,具有强烈刺激性气味的黄棕色气体 熔点:  ℃;沸点:3.8℃;42℃以上分解为 ℃;沸点:3.8℃;42℃以上分解为 和 和 。 。 | 强氧化性;与有机物、还原剂接触或浓度过高时会发生爆炸;易溶于水且会与水反应生成次氯酸 |
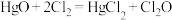 制取
制取 ,装置如图所示:
,装置如图所示: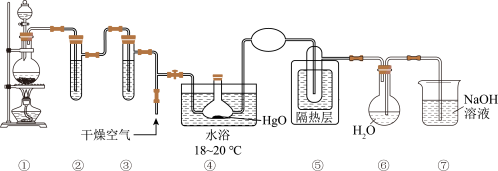
(2)装置①中制取氯气时需要
 盐酸,若加入盐酸的体积是
盐酸,若加入盐酸的体积是 ,制取氯气的物质的量小于
,制取氯气的物质的量小于 ,除了考虑盐酸的挥发和生成水的因素外,最主要的原因是
,除了考虑盐酸的挥发和生成水的因素外,最主要的原因是(3)③中试剂的名称是
(4)④中反应氧化剂和还原剂物质的量比值是
(5)⑥中
 与水反应制取
与水反应制取 ,反应的化学方程式是
,反应的化学方程式是 中混有盐酸,原因是
中混有盐酸,原因是(6)⑦中
 溶液能吸收多余的氯气,防止污染空气,发生反应的离子方程式是
溶液能吸收多余的氯气,防止污染空气,发生反应的离子方程式是
您最近一年使用:0次
2024-03-11更新
|
39次组卷
|
2卷引用:广西河池市八校联考2023-2024学年高一上学期12月月考化学试题
名校
解题方法
3 . 化学与生产、生活密切相关。下列对应关系错误的是
| A.湿手不可以直接接触电源——电解质溶液能够导电 |
| B.食物腐败——涉及氧化还原反应 |
C.漂白液可作消毒剂——漂白液的有效成分是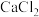 |
| D.下水井盖由生铁铸造——生铁硬度高于纯铁 |
您最近一年使用:0次
名校
解题方法
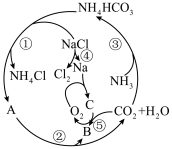
4 . 某些化合物具有如图所示的转化关系,其中A、B、C均为含有钠元素的化合物,部分转化的条件省略。 极易溶于水。
极易溶于水。
回答下列问题:
(1)A为___________ (填化学式,下同),B为___________ ,C为___________
(2) 的摩尔质量为
的摩尔质量为___________ ;要获得高浓度的 溶液,需向水中先通入
溶液,需向水中先通入___________ (填“ ”或“
”或“ ”)。
”)。
(3)反应④中氧化产物和还原产物的质量之比为___________ (填最简整数比);反应⑤中转移 电子时,生成
电子时,生成___________  (换算成标准状况下)
(换算成标准状况下) 。
。
(4)现有 由A、B形成的混合物,加入
由A、B形成的混合物,加入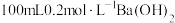 溶液(过量),充分反应后,过滤、洗涤、干燥,称量所得固体质量为
溶液(过量),充分反应后,过滤、洗涤、干燥,称量所得固体质量为 。
。
①配制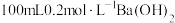 溶液需要的玻璃仪器有烧杯、量筒、玻璃棒、
溶液需要的玻璃仪器有烧杯、量筒、玻璃棒、___________ ;配制过程中,下列情况会导致配制结果偏低的是___________ 。(填标号)。
a.称量的 中含有少量
中含有少量
b.定容时未冷却至室温
c.定容时溶液超过刻度线,迅速用胶头滴管吸出多余液体
d.将配制好的溶液倒入试剂瓶中时有少量液体溅到试剂瓶外
② 原混合物中,A与B的物质的量之比
原混合物中,A与B的物质的量之比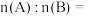
___________ (填最简整数比)。
 极易溶于水。
极易溶于水。回答下列问题:
(1)A为
(2)
 的摩尔质量为
的摩尔质量为 溶液,需向水中先通入
溶液,需向水中先通入 ”或“
”或“ ”)。
”)。(3)反应④中氧化产物和还原产物的质量之比为
 电子时,生成
电子时,生成 (换算成标准状况下)
(换算成标准状况下) 。
。(4)现有
 由A、B形成的混合物,加入
由A、B形成的混合物,加入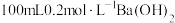 溶液(过量),充分反应后,过滤、洗涤、干燥,称量所得固体质量为
溶液(过量),充分反应后,过滤、洗涤、干燥,称量所得固体质量为 。
。①配制
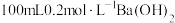 溶液需要的玻璃仪器有烧杯、量筒、玻璃棒、
溶液需要的玻璃仪器有烧杯、量筒、玻璃棒、a.称量的
 中含有少量
中含有少量
b.定容时未冷却至室温
c.定容时溶液超过刻度线,迅速用胶头滴管吸出多余液体
d.将配制好的溶液倒入试剂瓶中时有少量液体溅到试剂瓶外
②
 原混合物中,A与B的物质的量之比
原混合物中,A与B的物质的量之比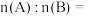
您最近一年使用:0次
2024-02-28更新
|
44次组卷
|
2卷引用:广西桂林市恭城瑶族自治县民族高级中学2023-2024学年高一下学期开学考试化学试题
5 . 锅炉水中溶解的氧气易对锅炉造成腐蚀,为了保证锅炉安全正常使用,常使用联氨( )处理锅炉水中溶解的氧,部分转化关系如图所示。下列说法错误的是
)处理锅炉水中溶解的氧,部分转化关系如图所示。下列说法错误的是
 )处理锅炉水中溶解的氧,部分转化关系如图所示。下列说法错误的是
)处理锅炉水中溶解的氧,部分转化关系如图所示。下列说法错误的是
A.液态 不能导电 不能导电 |
| B.反应①②③④均属于氧化还原反应 |
C.反应②中,每生成 ,同时生成 ,同时生成 |
D.反应①的电子转移可表示为 |
您最近一年使用:0次
2024-02-28更新
|
67次组卷
|
2卷引用:广西桂林市恭城瑶族自治县民族高级中学2023-2024学年高一下学期开学考试化学试题
名校
6 . 回答下列问题。
I.写出下列化学方程式:
(1)向Na2O2中通入CO2:___________ ;
(2)制Fe(OH)2时,白色沉淀迅速变灰绿色,最终变红褐色的反应原理:___________ ;
(3)制漂白粉原理:___________ ;
(4)高温下Fe与水蒸气反应:___________ 。
Ⅱ.写出下列离子方程式:
(5)SO2通入碘水中:___________ ;
(6)Al粉与NaOH溶液反应:___________ ;
(7)酸性条件下,向含铬废水中加FeSO4,将 还原为Cr3+:
还原为Cr3+:___________ ;
(8)制Fe(OH)3胶体:___________ 。
I.写出下列化学方程式:
(1)向Na2O2中通入CO2:
(2)制Fe(OH)2时,白色沉淀迅速变灰绿色,最终变红褐色的反应原理:
(3)制漂白粉原理:
(4)高温下Fe与水蒸气反应:
Ⅱ.写出下列离子方程式:
(5)SO2通入碘水中:
(6)Al粉与NaOH溶液反应:
(7)酸性条件下,向含铬废水中加FeSO4,将
 还原为Cr3+:
还原为Cr3+:(8)制Fe(OH)3胶体:
您最近一年使用:0次
名校
解题方法
7 . 氯是一种典型的非金属元素,具有多种化合价,可以形成食盐、漂白粉等多种含氯化合物。从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。以下是氯元素的“价类二维图”的部分信息。
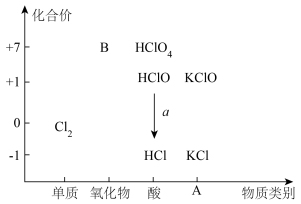
请回答下列问题:
(1)缺失的类别A为___________ ,物质B为___________ (填化学式),能够实现图中a转化的反应方程式为___________ (写一个即可)
(2)已知: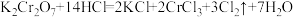 ,按要求完成下列问题。
,按要求完成下列问题。
①用双线桥标明电子转移方向和数目:___________ 。
②该反应中,氧化剂是___________ ,还原剂是___________ ,还原性
___________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
③ 完全反应,产生的
完全反应,产生的 在标准状况下的体积为
在标准状况下的体积为___________ L,
(3)写出 在强碱性介质中与
在强碱性介质中与 反应生成
反应生成 的离子方程式为
的离子方程式为___________ 。

请回答下列问题:
(1)缺失的类别A为
(2)已知:
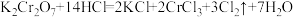 ,按要求完成下列问题。
,按要求完成下列问题。①用双线桥标明电子转移方向和数目:
②该反应中,氧化剂是

 (填“大于”或“小于”)。
(填“大于”或“小于”)。③
 完全反应,产生的
完全反应,产生的 在标准状况下的体积为
在标准状况下的体积为(3)写出
 在强碱性介质中与
在强碱性介质中与 反应生成
反应生成 的离子方程式为
的离子方程式为
您最近一年使用:0次
8 . 铝和铁是地壳中含量较多的金属元素,其单质和化合物广泛应用于日常生活中。回答下列问题:
(1)工业制印刷电路板的原理为用 做腐蚀液,将覆铜板上不需要的铜腐蚀。写出相关反应的离子方程式:
做腐蚀液,将覆铜板上不需要的铜腐蚀。写出相关反应的离子方程式:_______ 。
(2)向 溶液中加入
溶液中加入 溶液时,生成的
溶液时,生成的_______ 色絮状沉淀最终变为_______ 色的_______ (填化学式)。
(3)甲、乙两烧杯中分别盛有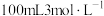 盐酸和
盐酸和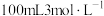 氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为1:2(同温同压下),则加入铝粉的质量为
氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为1:2(同温同压下),则加入铝粉的质量为_______ g。
(4)如图是从铝土矿(主要成分为 ,还含有少量
,还含有少量 等杂质)中提取
等杂质)中提取 并生产
并生产 的工艺流程:
的工艺流程:
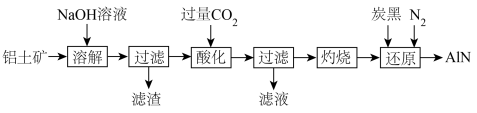
①“滤渣”的主要成分为_______ (填化学式,下同),滤液中溶液的主要成分为_______ 。
②向“滤渣”中加入稀硫酸后,检验反应后溶液中存在 的试剂为
的试剂为_______ (填字母)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液
③过滤操作中需要用到的玻璃仪器有_______ 。
④“还原”时,炭黑在高温下被氧化为 ,该还原过程中发生的化学反应方程式为
,该还原过程中发生的化学反应方程式为_______ 。
(1)工业制印刷电路板的原理为用
 做腐蚀液,将覆铜板上不需要的铜腐蚀。写出相关反应的离子方程式:
做腐蚀液,将覆铜板上不需要的铜腐蚀。写出相关反应的离子方程式:(2)向
 溶液中加入
溶液中加入 溶液时,生成的
溶液时,生成的(3)甲、乙两烧杯中分别盛有
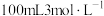 盐酸和
盐酸和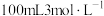 氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为1:2(同温同压下),则加入铝粉的质量为
氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为1:2(同温同压下),则加入铝粉的质量为(4)如图是从铝土矿(主要成分为
 ,还含有少量
,还含有少量 等杂质)中提取
等杂质)中提取 并生产
并生产 的工艺流程:
的工艺流程:
①“滤渣”的主要成分为
②向“滤渣”中加入稀硫酸后,检验反应后溶液中存在
 的试剂为
的试剂为A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液③过滤操作中需要用到的玻璃仪器有
④“还原”时,炭黑在高温下被氧化为
 ,该还原过程中发生的化学反应方程式为
,该还原过程中发生的化学反应方程式为
您最近一年使用:0次
名校
9 . “价一类”二维图可以从物质类别、化合价角度认识物质的性质及其转化关系。以下是氯的“价一类”二维图部分信息如图所示,请回答下列问题:

(1)乙的颜色是_______ ;丙可以代替乙成为新时代自来水消毒剂,则丙的化学式_______ 。
(2)戊转化为乙需要加入_______ (填“还原剂”或“氧化剂”)。
(3)往石蕊试液通入乙,溶液先变红后褪色,其中起作用的是图中的_______ (填序号)
A.甲 B.乙 C.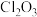 D.丙 E.戊 F.
D.丙 E.戊 F. G.
G.
(4) 是酸性氧化物,其与
是酸性氧化物,其与 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
(5)一定温度下,乙与 溶液反应生成
溶液反应生成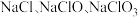 的混合物,若
的混合物,若 与
与 的物质的量之比为
的物质的量之比为 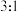 ,则氧化剂与还原剂的物质的量之比为
,则氧化剂与还原剂的物质的量之比为_______ 。

(1)乙的颜色是
(2)戊转化为乙需要加入
(3)往石蕊试液通入乙,溶液先变红后褪色,其中起作用的是图中的
A.甲 B.乙 C.
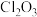 D.丙 E.戊 F.
D.丙 E.戊 F. G.
G.
(4)
 是酸性氧化物,其与
是酸性氧化物,其与 溶液反应的离子方程式为
溶液反应的离子方程式为(5)一定温度下,乙与
 溶液反应生成
溶液反应生成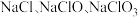 的混合物,若
的混合物,若 与
与 的物质的量之比为
的物质的量之比为 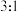 ,则氧化剂与还原剂的物质的量之比为
,则氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
名校
10 . 下列3个反应可发生:
①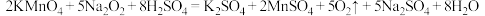
②把 通入
通入 溶液中:
溶液中: (碱式硫酸铁)
(碱式硫酸铁)
③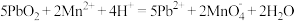
下列有关说法正确的是
①
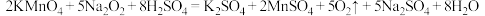
②把
 通入
通入 溶液中:
溶液中: (碱式硫酸铁)
(碱式硫酸铁)③
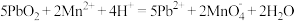
下列有关说法正确的是
A.反应①中, 既作氧化剂也作还原剂 既作氧化剂也作还原剂 |
B.反应①和②中,若 的物质的量相同,则转移电子数也相同 的物质的量相同,则转移电子数也相同 |
| C.反应②既属于四种基本反应类型之一,也属于氧化还原反应,还属于离子反应 |
D.上述3个反应中作氧化剂的物质中氧化性最强的是 |
您最近一年使用:0次



