名校
1 . 作为食品添加剂时,亚硝酸钠 可以增加肉类的鲜度,抑制微生物,保持肉制品的结构和营养价值;但是过量振入会导致中毒。某实验小组设计实验制备亚硝酸钠并进行含量测定。
可以增加肉类的鲜度,抑制微生物,保持肉制品的结构和营养价值;但是过量振入会导致中毒。某实验小组设计实验制备亚硝酸钠并进行含量测定。
Ⅰ 制备
制备
实验室以木炭、浓硝酸、 为主要原料按照如图所示装置制备亚硝酸钠
为主要原料按照如图所示装置制备亚硝酸钠 加热装置及部分夹持装置已略去
加热装置及部分夹持装置已略去 ,反应原理为:
,反应原理为:
回答下列问题:
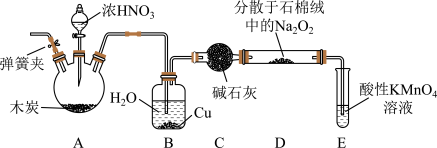
(1)连接好装置之后,下一步实验操作是______ 。
(2) 装置中铜的作用是
装置中铜的作用是______ 。
(3) 装置用于尾气处理,E中反应的离子方程式为
装置用于尾气处理,E中反应的离子方程式为______ 。
(4)实验结束阶段,熄灭酒精灯之后继续通入 直至装置冷却。此时通入
直至装置冷却。此时通入 的目的是
的目的是______ 。
Ⅱ 含量的测定
含量的测定
查阅资料可知:酸性 溶液可将
溶液可将 氧化为
氧化为 ,
, 还原成
还原成 。
。
(5)溶液配制:称取装置D中反应后的固体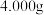 ,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至250mL的
,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至250mL的______ 中,加蒸馏水至______ 。
滴定:取 溶液于锥形瓶中,用
溶液于锥形瓶中,用 酸性
酸性 溶液进行滴定,实验数据如下表所示:
溶液进行滴定,实验数据如下表所示:
(6)第4组实验数据出现异常,造成这种异常的原因可能是______  双项选择
双项选择 。
。
A.锥形瓶洗净后未干燥 滴定终了仰视读数
滴定终了仰视读数
C.滴定终了俯视读数 酸式滴定管用蒸馏水洗净后未用标准液润洗
酸式滴定管用蒸馏水洗净后未用标准液润洗
(7)根据表中数据,计算所得固体中亚硝酸钠的质量分数______ 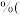 保留2位小数
保留2位小数 。
。
 可以增加肉类的鲜度,抑制微生物,保持肉制品的结构和营养价值;但是过量振入会导致中毒。某实验小组设计实验制备亚硝酸钠并进行含量测定。
可以增加肉类的鲜度,抑制微生物,保持肉制品的结构和营养价值;但是过量振入会导致中毒。某实验小组设计实验制备亚硝酸钠并进行含量测定。Ⅰ
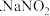 制备
制备实验室以木炭、浓硝酸、
 为主要原料按照如图所示装置制备亚硝酸钠
为主要原料按照如图所示装置制备亚硝酸钠 加热装置及部分夹持装置已略去
加热装置及部分夹持装置已略去 ,反应原理为:
,反应原理为:
回答下列问题:

(1)连接好装置之后,下一步实验操作是
(2)
 装置中铜的作用是
装置中铜的作用是(3)
 装置用于尾气处理,E中反应的离子方程式为
装置用于尾气处理,E中反应的离子方程式为(4)实验结束阶段,熄灭酒精灯之后继续通入
 直至装置冷却。此时通入
直至装置冷却。此时通入 的目的是
的目的是Ⅱ
 含量的测定
含量的测定查阅资料可知:酸性
 溶液可将
溶液可将 氧化为
氧化为 ,
, 还原成
还原成 。
。(5)溶液配制:称取装置D中反应后的固体
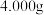 ,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至250mL的
,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至250mL的滴定:取
 溶液于锥形瓶中,用
溶液于锥形瓶中,用 酸性
酸性 溶液进行滴定,实验数据如下表所示:
溶液进行滴定,实验数据如下表所示:| 滴定次数 | 1 | 2 | 3 | 4 |
 溶液体积 溶液体积 | 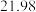 | 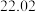 |  | 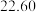 |
 双项选择
双项选择 。
。A.锥形瓶洗净后未干燥
 滴定终了仰视读数
滴定终了仰视读数C.滴定终了俯视读数
 酸式滴定管用蒸馏水洗净后未用标准液润洗
酸式滴定管用蒸馏水洗净后未用标准液润洗(7)根据表中数据,计算所得固体中亚硝酸钠的质量分数
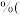 保留2位小数
保留2位小数 。
。
您最近一年使用:0次
2020-11-14更新
|
144次组卷
|
2卷引用:宁夏石嘴山市平罗中学2021-2022学年高三上学期期中考试化学试题
名校
解题方法
2 . 已知某一反应体系反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2,则关于该反应体系说法错误的是
| A.该反应的化学方程式为2H2CrO4+3H2O2═2Cr(OH)3↓+3O2↑+2H2O |
| B.该反应中的氧化剂是H2O2,还原产物是O2 |
| C.氧化性:H2CrO4 > O2 |
| D.如反应转移了0.3mol电子,则产生的气体在标准状况下体积为3.36L |
您最近一年使用:0次
2020-11-07更新
|
192次组卷
|
9卷引用:2017届宁夏银川一中高三上学期第一次月考理综化学试卷
3 . 如下图在衬白纸的玻璃片中央放置适量的KMnO4颗粒,在周围分别滴加一滴含有酚酞的澄清石灰水、FeCl2溶液,然后在KMnO4晶体上滴加适量的浓盐酸,迅速盖好表面皿。提示:实验室中所用的少量氯气可以用下述原理制取:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,此反应在常温下即能进行。
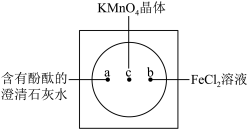
(1)氧化剂与还原剂物质的量之比为____________ ,氧化产物为_______ 。
(2)产生0.1molCl2,则转移电子的物质的量为______ mol。
(3)b处离子方程式是___________ 。
(4)高锰酸钾标准溶液经常用来滴定测量物质的含量。配平并完成下列高锰酸钾滴定草酸反应的离子方程式:_____  +
+______ H2C2O4+______  =
=____  +
+_____ CO2↑+___________

(1)氧化剂与还原剂物质的量之比为
(2)产生0.1molCl2,则转移电子的物质的量为
(3)b处离子方程式是
(4)高锰酸钾标准溶液经常用来滴定测量物质的含量。配平并完成下列高锰酸钾滴定草酸反应的离子方程式:
 +
+ =
= +
+
您最近一年使用:0次
2011·云南昆明·一模
名校
4 . 把图b的碎纸片补充到图a中,可得到一个完整的离子方程式。下列有关该离子方程式的说法正确的是( )


| A.配平后的化学计量数依次为3、1、2、6、3 |
| B.若有1 mol S被氧化,则生成2 mol S2- |
| C.氧化剂与还原剂的物质的量之比为1∶2 |
| D.2 mol S参加反应有3 mol电子发生转移 |
您最近一年使用:0次
2020-10-10更新
|
158次组卷
|
18卷引用:宁夏银川市唐徕中学2023-2024学年高三上学期期中考试化学试题
宁夏银川市唐徕中学2023-2024学年高三上学期期中考试化学试题(已下线)2011届云南省昆明市高三复习5月适应性检测(理综)化学部分(已下线)2011届江西省临川二中高三下学期第一次模拟考试(理综)化学部分(已下线)2012届四川省成都外国语学校高三第二次月考理科综合化学试卷(已下线)2012届浙江省重点中学协作体高三3月调研理综部分(已下线)2013学年湖北省广水市育才高中高三第一次月考化学试卷黑龙江省伊春市第二中学2017-2018学年高二下学期期末考试化学试题山东省枣庄市第二中学2020届高三上学期第一次阶段性检测化学试题(已下线)考点03 氧化还原反应——《备战2020年高考精选考点专项突破题集》夯基提能2020届高三化学选择题对题专练——氧化还原反应的实际应用(提升练)2020届高三化学化学二轮复习——高考常考题:情境下氧化还原反应方程式书写【精编选择26题】(已下线)专题四 氧化还原反应(提分特训)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训云南文山州马关县第一中学2019-2020学年高一上学期期末考试化学试题福建省安溪一中、养正中学、惠安一中、泉州实验中学2019-2020学年高二下学期期末联考化学试题山东省德州市齐河县实验中学2021届高三第一次月考化学试题甘肃省张掖市第二中学2021届高三上学期9月月考化学试题(已下线)押新高考卷10题 氧化还原反应-备战2022年高考化学临考题号押题(新高考通版)(已下线)第14讲 硫、二氧化硫【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)
名校
解题方法
5 . 下列解释有关实验现象的离子方程式错误的是
| 选项 | 实验操作 | 实验现象 | 离子方程式 |
| A | 大理石中加入足量醋酸溶液 | 大理石逐渐溶解 | CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
| B | 新制氯水中加过量氢氧化钠溶液 | 溶液由黄绿色变无色 | Cl2+2OH-=Cl-+ClO-+H2O |
| C | 酸性KMnO4溶液中加H2O2溶液 | 溶液紫色褪去,有气泡产生 | 2MnO +3H2O2+10H+=2Mn2++3O2↑+8H2O +3H2O2+10H+=2Mn2++3O2↑+8H2O |
| D | 将稀硫酸滴入淀粉-KI溶液中 | 在空气中放置一段时间后,溶液呈蓝色 | 4H++4I-+O2=2I2+2H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-10-10更新
|
537次组卷
|
8卷引用:宁夏回族自治区固原市第一中学2021届高三上学期第四次月考理综化学试题
名校
解题方法
6 . 金属及其化合物在生产中用途广泛。从含铜丰富的自然资源黄铜矿(CuFeS2)中冶炼铜的工艺流程如图:
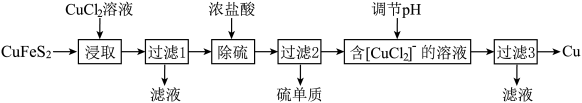
已知:CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为___ 。
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为___ 。
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是___ 。(填离子符号)
(4)过滤3所得滤液中可以循环使用的物质有___ 和___ 。为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为___ 。
(5)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,发生的反应为6CuFeS2+13O2 3Cu2S+2Fe3O4+9O2,Cu2S+O2
3Cu2S+2Fe3O4+9O2,Cu2S+O2 2Cu+SO2。此工艺与前一工艺相比主要缺点有
2Cu+SO2。此工艺与前一工艺相比主要缺点有____ (任答一点)。

已知:CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是
(4)过滤3所得滤液中可以循环使用的物质有
(5)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,发生的反应为6CuFeS2+13O2
 3Cu2S+2Fe3O4+9O2,Cu2S+O2
3Cu2S+2Fe3O4+9O2,Cu2S+O2 2Cu+SO2。此工艺与前一工艺相比主要缺点有
2Cu+SO2。此工艺与前一工艺相比主要缺点有
您最近一年使用:0次
7 . 用CuS、Cu2S处理酸性废水中的Cr2O ,发生反应如下:
,发生反应如下:
反应Ⅰ:CuS+Cr2O +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)
反应Ⅱ:Cu2S+Cr2O +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)
下列有关说法正确的是( )
 ,发生反应如下:
,发生反应如下:反应Ⅰ:CuS+Cr2O
 +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)反应Ⅱ:Cu2S+Cr2O
 +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)下列有关说法正确的是( )
A.反应Ⅰ和Ⅱ中Cu2+、SO 都是氧化产物 都是氧化产物 |
| B.反应Ⅱ中还原剂、氧化剂的物质的量之比为2∶5 |
C.处理1molCr2O 时反应Ⅰ、Ⅱ中消耗H+的物质的量相等 时反应Ⅰ、Ⅱ中消耗H+的物质的量相等 |
D.反应Ⅰ、Ⅱ中每处理1molCr2O ,转移电子的数目相等 ,转移电子的数目相等 |
您最近一年使用:0次
2020-10-03更新
|
153次组卷
|
2卷引用:宁夏银川一中2021届高三上学期第二次月考理综化学试题
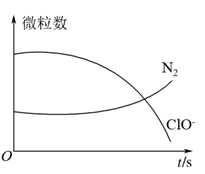
8 . 某离子反应涉及H2O、ClO-、 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
| A.该反应中Cl-为氧化产物 |
| B.消耗1个还原剂微粒,转移6e- |
C. 被ClO-氧化成N2 被ClO-氧化成N2 |
| D.反应后溶液的酸性减弱 |
您最近一年使用:0次
2020-10-02更新
|
1134次组卷
|
8卷引用:宁夏回族自治区石嘴山市平罗中学2020届高三上学期期中考试化学试题
9 . 过氧化氢H2O2(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是______ (填字母)。
(2)H2O2既体现氧化性又体现还原性的反应是_______ (填字母)。
(3)在稀硫酸中,KMnO4和H2O2能构成原电池。其中负极反应为:H2O2-2e-=2H++O2↑,正极反应: +5e-+8H+=Mn2++4H2O,写出该氧化还原反应的离子方程式:
+5e-+8H+=Mn2++4H2O,写出该氧化还原反应的离子方程式:___________ 。
(4)在K2Cr2O7+14HCl=2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3mol电子转移时生成Cl2的体积为______ (标准状况),被氧化的HCl的物质的量为___________ 。
(5)除去镁粉中混入的铝粉杂质用____ 溶解、___ 方法分离,化学反应方程式为___ 。
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是
(2)H2O2既体现氧化性又体现还原性的反应是
(3)在稀硫酸中,KMnO4和H2O2能构成原电池。其中负极反应为:H2O2-2e-=2H++O2↑,正极反应:
 +5e-+8H+=Mn2++4H2O,写出该氧化还原反应的离子方程式:
+5e-+8H+=Mn2++4H2O,写出该氧化还原反应的离子方程式:(4)在K2Cr2O7+14HCl=2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3mol电子转移时生成Cl2的体积为
(5)除去镁粉中混入的铝粉杂质用
您最近一年使用:0次
14-15高一上·浙江宁波·期中
名校
解题方法
10 . 羟胺( )是一种还原剂,能将某些氧化剂还原。现用25.00mL
)是一种还原剂,能将某些氧化剂还原。现用25.00mL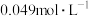 羟胺溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的
羟胺溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的 恰好与24.50mL
恰好与24.50mL '酸性
'酸性 溶液完全反应。已知:
溶液完全反应。已知: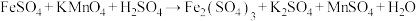 (未配平),则羟胺的氧化产物是
(未配平),则羟胺的氧化产物是
 )是一种还原剂,能将某些氧化剂还原。现用25.00mL
)是一种还原剂,能将某些氧化剂还原。现用25.00mL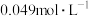 羟胺溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的
羟胺溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的 恰好与24.50mL
恰好与24.50mL '酸性
'酸性 溶液完全反应。已知:
溶液完全反应。已知: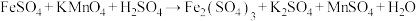 (未配平),则羟胺的氧化产物是
(未配平),则羟胺的氧化产物是A. | B. | C.NO | D. |
您最近一年使用:0次
2020-09-23更新
|
394次组卷
|
15卷引用:宁夏固原市第一中学2023届高三上学期第一次月考化学试题
宁夏固原市第一中学2023届高三上学期第一次月考化学试题(已下线)2014-2015浙江省宁波市效实中学高一上学期期中化学试卷2014-2015浙江省杭州市西湖中学高一12月月考化学试卷2018-2019学年人教版高中化学必修一模块综合测评题(A)2018-2019学年苏教版高中化学必修一 模块综合测评(A)【全国百强校】吉林省实验中学2019届高三上学期期中考试化学试题江西省上饶中学2019届高三上学期期中考试化学试题2020届高三化学二轮复习 氧化还原反应过关检测(强化训练)(已下线)【南昌新东方】莲塘一中化学高一10月份高一必修第一册(鲁科2019)考试帮 模块综合测评B卷福建师范大学第二附属中学2020届高三上学期期中考试化学试题(已下线)【苏州新东方】 江苏省吴江中学2021-2022学年高二上学期开学检测化学试卷辽宁省沈阳市第一二〇中学2021-2022学年高一上学期期中考试化学试题(已下线)第一章 化学物质及其变化 第5练 氧化还原反应的计算与方程式的配平(已下线)第5讲 氧化还原反应方程式的配平与计算



