名校
1 . 实验室用50mL浓盐酸跟足量的氯酸钾固体共热制取氯气,反应的化学方程式为(未配平)KClO3+HCl—KCl+Cl2↑+H2O。
(1)配平上述反应化学方程式:______ 。
(2)若产生0.1molCl2,则转移电子的物质的量为_______ mol。
(3)在该反应中,如有6molCl2生成,被氧化的HCl的物质的量是_____ mol,转移电子是______ mol。
(4)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与 物质的量之比为1∶1的混合液,反应的化学方程式是
物质的量之比为1∶1的混合液,反应的化学方程式是_____ 。
(5)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)_____ 。
(1)配平上述反应化学方程式:
(2)若产生0.1molCl2,则转移电子的物质的量为
(3)在该反应中,如有6molCl2生成,被氧化的HCl的物质的量是
(4)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与
 物质的量之比为1∶1的混合液,反应的化学方程式是
物质的量之比为1∶1的混合液,反应的化学方程式是(5)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题:
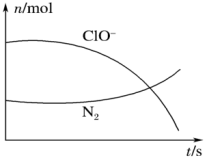
(1)某反应体系中有H2O、ClO-、NH 、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式_______ ,消耗1 mol还原剂,转移电子数为_______ 。
(2)Fe2+的还原性较强,实验室的氯化亚铁溶液常因氧化而变质,除去杂质的方法是_______ ,相关反应的离子方程式是_______ 。
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,当有68 g NH3参加反应时,被氧化的物质为_______ ,生成的还原产物的质量为_______ g。
(4)K2FeO4(铁元素为+6价)可用作水处理剂,它可由以下反应制得,请配平下列离子方程式_____ 。
_______Cl2 + _______ Fe(OH)3+_______ OH- = _______ FeO + _______ Cl- +_______ H2O
+ _______ Cl- +_______ H2O
(1)某反应体系中有H2O、ClO-、NH
 、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
(2)Fe2+的还原性较强,实验室的氯化亚铁溶液常因氧化而变质,除去杂质的方法是
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,当有68 g NH3参加反应时,被氧化的物质为
(4)K2FeO4(铁元素为+6价)可用作水处理剂,它可由以下反应制得,请配平下列离子方程式
_______Cl2 + _______ Fe(OH)3+_______ OH- = _______ FeO
 + _______ Cl- +_______ H2O
+ _______ Cl- +_______ H2O
您最近一年使用:0次
名校
解题方法
3 . 已知Mn2O 与S2-在酸性溶液中能发生反应: Mn2O
与S2-在酸性溶液中能发生反应: Mn2O +3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O
+3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O 中锰元素的化合价是
中锰元素的化合价是
 与S2-在酸性溶液中能发生反应: Mn2O
与S2-在酸性溶液中能发生反应: Mn2O +3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O
+3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O 中锰元素的化合价是
中锰元素的化合价是| A.+2 | B.+4 | C.+3 | D.+6 |
您最近一年使用:0次
2022-02-28更新
|
848次组卷
|
36卷引用:宁夏青铜峡市高级中学2020-2021学年高一12月月考化学试题
宁夏青铜峡市高级中学2020-2021学年高一12月月考化学试题河南省安阳市第三十六中学2017-2018学年高一上学期期中考试化学试题安徽省阜阳市第三中学2018-2019学年高一下学期开学考试化学试题夯基提能2020届高三化学选择题对题专练——氧化还原反应的实际应用广东省2020年普通高中学业水平考试化学合格性考试模拟试题(七)陕西省汉中市龙岗学校2019-2020学年高一上学期期末考试化学试题(已下线)【南昌新东方】江西省九江一中2013-2014学年高一上学期期中考试化学试题广东省珠海市第二中学2019-2020学年高一上学期期中考试化学试题广东省中山纪念中学2019-2020学年高一上学期第二次段考化学试题山东省济宁市邹城兖矿一中2020-2021学年度高一9月月考化学试题吉林公主岭范家屯一中2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】30湖南省岳阳市楚雄中学2020-2021学年高一上学期期中考试化学试题广东省湛江市第四中学2020-2021学年高一上学期期中考试化学试题北京市铁路第二中学2020-2021学年高一上学期期中考试化学试题(已下线)【南昌新东方】9. 2020 高一上 铁路一中 刘惠文 钟欣(已下线)【浙江新东方】双师 (55)河北衡水市第十四中学2020-2021学年高一上学期三调考试化学试题天津市滨海新区2020-2021学年高一上学期期末考试化学试题河北省衡水市武邑武罗学校2020-2021学年高一上学期期中考试化学试题新疆巴音郭楞蒙古自治州第二中学2021届高三上学期第一次摸底考试化学试题河北省衡水市武强中学2020-2021学年高一上学期第一次月考化学试题云南省玉溪市江川区第二中学2020-2021学年高一下学期竞赛化学试题黑龙江省鸡西市第一中学2020-2021学年高一上学期第一次月考化学试题四川省成都市第七中学2021-2022学年高一上学期期中考试化学试题四川省攀枝花市第十五中学校2021-2022学年高一上学期期中考试化学试题安徽省安庆市第十中学2021-2022学年高一上学期10月月考化学试题江苏省宿迁市泗阳县实验高级中学2021-2022学年高一上学期第二次调研测试化学试题广东省梅州市兴宁市叶塘中学2021-2022学年高一上学期摸底考试化学试题浙江省绿谷联盟2022-2023学年高一上学期10月份考试化学试题 黑龙江省鹤岗市第一中学2022-2023学年高一上学期10月月考化学试题山西省晋城市第一中学校2022-2023学年高一上学期第二次调研考试化学试题四川省仁寿县铧强中学2021-2022学年高一上学期半期考试化学试题云南省昆明市第八中学2020-2021学年高一上学期期中考试化学试题(已下线)专题七 氧化还原反应天津市宁河区2023-2024学年高一上学期期末考试化学试题
名校
4 . 空气吹出法是工业规模海水提溴的常用方法,流程如下:

下列说法不正确的是

下列说法不正确的是
A.获得工业 的方法是过滤 的方法是过滤 |
| B.步骤②③的目的是富集溴元素 |
C.步骤①发生的主要反应为: |
D.步骤②发生的主要反应为: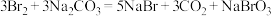 |
您最近一年使用:0次
2022-02-21更新
|
293次组卷
|
6卷引用:宁夏石嘴山市平罗中学2021-2022学年高一下学期第一次月考化学试题
宁夏石嘴山市平罗中学2021-2022学年高一下学期第一次月考化学试题陕西省渭南市临渭区2021-2022学年高一上学期期末教学质量检测化学试题(已下线)第八章 化学与可持续发展(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)吉林省吉林市第一中学2022-2023学年高一6月月考(线上)化学试题黑龙江省大庆市大庆中学2022-2023学年高一下学期7月期末考试化学试题(已下线)第八章 化学与可持续发展【单元测试B卷】
名校
解题方法
5 . 铁有许多重要的化合物,除中学化学常见的三种氧化物和两种氢氧化物外,还有许多盐。 是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。现用绿矾对某工厂废水(含有强氧化性离子
是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。现用绿矾对某工厂废水(含有强氧化性离子 )进行处理。
)进行处理。
(1)绿矾除用铁粉与硫酸反应生成外,工业上还可用空气、水、黄铁矿(主要成分为 )来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:
)来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:___________ 。
(2)试配平:___________
___________Fe2++___________ +___________=___________Fe3++___________Cr3++___________H2O
+___________=___________Fe3++___________Cr3++___________H2O
 是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。现用绿矾对某工厂废水(含有强氧化性离子
是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。现用绿矾对某工厂废水(含有强氧化性离子 )进行处理。
)进行处理。(1)绿矾除用铁粉与硫酸反应生成外,工业上还可用空气、水、黄铁矿(主要成分为
 )来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:
)来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:(2)试配平:
___________Fe2++___________
 +___________=___________Fe3++___________Cr3++___________H2O
+___________=___________Fe3++___________Cr3++___________H2O
您最近一年使用:0次
名校
6 . 某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2;已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是___________ 。
(2)该反应中,发生还原反应的过程是___________ →___________ 。
(3)写出该反应的化学方程式,并标出电子转移的方向和数目___________
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为___________ 。
(5)完成并配平化学方程式:Na2Sx+NaClO+NaOH=Na2SO4+NaCl+H2O,___________ 。
(6)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂与氧化剂物质的量之比为___________ 。
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式,并标出电子转移的方向和数目
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
(5)完成并配平化学方程式:Na2Sx+NaClO+NaOH=Na2SO4+NaCl+H2O,
(6)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂与氧化剂物质的量之比为
您最近一年使用:0次
名校
解题方法
7 . 下列离子方程式书写正确的是
A.向明矾溶液中滴加氢氧化钡至溶液呈中性:3Ba2++6OH-+2Al3++3SO =2Al(OH)3↓+3BaSO4↓ =2Al(OH)3↓+3BaSO4↓ |
| B.向Ca(ClO)2溶液通入过量的CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO |
| C.FeSO4酸性溶液暴露在空气中:4Fe2++O2+2H2O=4Fe3++4OH- |
D.CuSO4溶液与少量的Ba(OH)2溶液:Ba2++ =BaSO4↓ =BaSO4↓ |
您最近一年使用:0次
名校
解题方法
8 . 无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业上可由铝土矿(主要成分是Al2O3和Fe2O3)和焦炭制备,流程如图:
已知:AlCl3、FeCl3分别在183℃、315℃时升华

回答下列问题:
(1)请写出焙烧炉中发生反应的化学方程式:_____________________________________ 。
(2)请写出氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式:__________________________________ 。
(3)700℃时,升华器中物质经充分反应后需降温实现FeCl3和AlCl3的分离。控制合适的温度范围是__________ 。
(4)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。
mg样品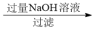 NaAlO2溶液
NaAlO2溶液 Al(OH)3
Al(OH)3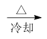 ngAl2O3
ngAl2O3
步骤中通CO2至过量的原因是:_______________________________ ,反应的离子方程式为:________________________ 计算该样品中AlCl3的质量分数为________ (结果用m、n表示,不必化简)。
已知:AlCl3、FeCl3分别在183℃、315℃时升华

回答下列问题:
(1)请写出焙烧炉中发生反应的化学方程式:
(2)请写出氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式:
(3)700℃时,升华器中物质经充分反应后需降温实现FeCl3和AlCl3的分离。控制合适的温度范围是
(4)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。
mg样品
 NaAlO2溶液
NaAlO2溶液 Al(OH)3
Al(OH)3 ngAl2O3
ngAl2O3步骤中通CO2至过量的原因是:
您最近一年使用:0次
名校
解题方法
9 . Ⅰ.明胶是水溶性蛋白质混合物,溶于水形成胶体。工业明胶含有重金属 ,对人体有害。
,对人体有害。
(1)已知 中
中 是一种酸根离子,则
是一种酸根离子,则 属于
属于___________ (填“酸”“碱”“盐”或“氧化物”), 中铁元素的化合价为
中铁元素的化合价为___________ 价。
(2)明胶的水溶液和 溶液共同具有的性质是
溶液共同具有的性质是___________ (填字母)。
A.都不稳定,密封放置会产生沉淀 B.两者均有丁达尔效应 C.分散质粒子都可通过滤纸
Ⅱ. 是银白色金属,化学性质稳定,
是银白色金属,化学性质稳定, 价和
价和 价为常见价态。工业上以铬铁矿(主要成分为
价为常见价态。工业上以铬铁矿(主要成分为 ,含
,含
 等杂质)为主要原料生产金属铬和强氧化剂重铬酸钠
等杂质)为主要原料生产金属铬和强氧化剂重铬酸钠 ,其主要工艺流程如下。
,其主要工艺流程如下。

查阅资料:常温下, 不溶于水,有强氧化性,在碱性条件下,能将
不溶于水,有强氧化性,在碱性条件下,能将 转化为
转化为 。
。
(3)工业上常采用热还原法制备金属铬,写出以 为原料,利用铝热反应制取金属铬的化学方程式:
为原料,利用铝热反应制取金属铬的化学方程式:___________ 。
(4)酸化滤液D时,用硫酸而不用盐酸,可能的原因是___________ 。
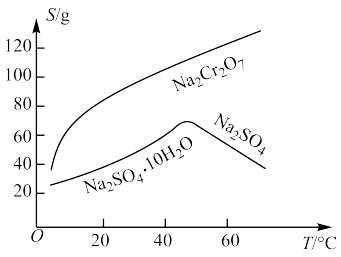
(5)固体E的主要成分是 ,根据下图分析操作a为
,根据下图分析操作a为___________ 、___________ 。
(6)电镀厂产生的镀铜废水中往往含有一定量的 ,处理该废水常用还原沉淀法,具体流程如下:
,处理该废水常用还原沉淀法,具体流程如下:

① 的化学性质与
的化学性质与 相似。在上述生产过程中加入
相似。在上述生产过程中加入 溶液时要控制溶液的
溶液时要控制溶液的 不能过高,是因为
不能过高,是因为___________ (用离子方程式表示)。
②下列溶液中可以代替上述流程中 溶液的是
溶液的是___________ (填字母)。
A.浓硫酸 B.酸性 溶液 C.
溶液 C. 溶液
溶液
③上述流程中,每消耗0.1mol 转移0.8mole-,则加入
转移0.8mole-,则加入 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为___________ 。
 ,对人体有害。
,对人体有害。(1)已知
 中
中 是一种酸根离子,则
是一种酸根离子,则 属于
属于 中铁元素的化合价为
中铁元素的化合价为(2)明胶的水溶液和
 溶液共同具有的性质是
溶液共同具有的性质是A.都不稳定,密封放置会产生沉淀 B.两者均有丁达尔效应 C.分散质粒子都可通过滤纸
Ⅱ.
 是银白色金属,化学性质稳定,
是银白色金属,化学性质稳定, 价和
价和 价为常见价态。工业上以铬铁矿(主要成分为
价为常见价态。工业上以铬铁矿(主要成分为 ,含
,含
 等杂质)为主要原料生产金属铬和强氧化剂重铬酸钠
等杂质)为主要原料生产金属铬和强氧化剂重铬酸钠 ,其主要工艺流程如下。
,其主要工艺流程如下。
查阅资料:常温下,
 不溶于水,有强氧化性,在碱性条件下,能将
不溶于水,有强氧化性,在碱性条件下,能将 转化为
转化为 。
。(3)工业上常采用热还原法制备金属铬,写出以
 为原料,利用铝热反应制取金属铬的化学方程式:
为原料,利用铝热反应制取金属铬的化学方程式:(4)酸化滤液D时,用硫酸而不用盐酸,可能的原因是
(5)固体E的主要成分是
 ,根据下图分析操作a为
,根据下图分析操作a为
(6)电镀厂产生的镀铜废水中往往含有一定量的
 ,处理该废水常用还原沉淀法,具体流程如下:
,处理该废水常用还原沉淀法,具体流程如下:
①
 的化学性质与
的化学性质与 相似。在上述生产过程中加入
相似。在上述生产过程中加入 溶液时要控制溶液的
溶液时要控制溶液的 不能过高,是因为
不能过高,是因为②下列溶液中可以代替上述流程中
 溶液的是
溶液的是A.浓硫酸 B.酸性
 溶液 C.
溶液 C. 溶液
溶液③上述流程中,每消耗0.1mol
 转移0.8mole-,则加入
转移0.8mole-,则加入 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为
您最近一年使用:0次
2021-12-04更新
|
86次组卷
|
2卷引用:宁夏石嘴山市平罗中学2021-2022学年高三上学期期中考试化学试题
名校
10 . 下列离子方程式正确的是
A. 溶液与盐酸反应: 溶液与盐酸反应: |
B.足量酸性 溶液与双氧水反应: 溶液与双氧水反应: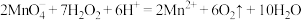 |
C. 的 的 溶液和 溶液和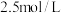 的 的 溶液等体积混合: 溶液等体积混合: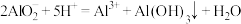 |
D.向 溶液中滴加少量氯水,反应的离子方程式为:2Br-+Cl2=Br2+2Cl- 溶液中滴加少量氯水,反应的离子方程式为:2Br-+Cl2=Br2+2Cl- |
您最近一年使用:0次



