名校
1 . 磷酸亚铁锂(LiFePO4)电池工作电压适中、放电功率高、在高温和高热环境下的稳定性高,是新能源汽车的动力电池之一、一种利用硫酸法生产钛白粉过程的副产物硫酸亚铁(含钛、铜、锰、铅、锌、钙、镁等杂质离子)制备磷酸亚铁锂的生产流程如图:
已知:FePO4可溶于pH小于2的酸性溶液。
回答下列问题:
(1)铁在元素周期中的位置是___________ ,FePO4·2H2O中Fe元素的化合价是___________ 。
(2)操作2的名称是___________ 。
(3)TiO2是一种白色颜料,用TiCl4制备TiO2·xH2O的化学方程式是___________ 。
(4)滤液2与磷酸、双氧水生成FePO4·2H2O的离子方程式为___________ ,向滤液2中加入NaOH溶液调节溶液的pH,将溶液的pH控制在2.0的原因是___________ 。
(5)聚丙烯的作用是___________ 。
(6)LiFePO4的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成4个正八面体和4个正四面体,电池充电时,LiFePO4作极___________ (“阴”或“阳”),脱出部分Li+,进而转化为Li1-xFePO4,Li1-xFePO4结构示意图如(b)所示,则其中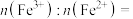
___________ 。

| 物质 | FeS | Mns | CuS | PbS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 1.6×10-24 |
回答下列问题:
(1)铁在元素周期中的位置是
(2)操作2的名称是
(3)TiO2是一种白色颜料,用TiCl4制备TiO2·xH2O的化学方程式是
(4)滤液2与磷酸、双氧水生成FePO4·2H2O的离子方程式为
(5)聚丙烯的作用是
(6)LiFePO4的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成4个正八面体和4个正四面体,电池充电时,LiFePO4作极
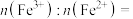

您最近一年使用:0次
名校
解题方法
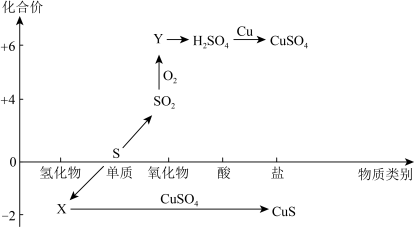
2 . 硫及其化合物的“价-类”二维图如下图所示,回答下列问题:___________ ,Y的化学式是___________ 。
(2)检验 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入___________ ,无明显现象,再加入___________ 溶液,若产生白色沉淀,则溶液中含有 。
。
(3)CuS与足量浓硫酸反应也可制得SO2,该反应的化学方程式为:CuS+4H2SO4(浓) CuSO4+4SO2↑+4H2O。
CuSO4+4SO2↑+4H2O。
①请用“双线桥”法标明该反应电子转移的方向和数目___________ 。
②当有1.5NA电子发生转移时,理论上生成SO2的体积(标准状况)为___________ L。
(2)检验
 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入 。
。(3)CuS与足量浓硫酸反应也可制得SO2,该反应的化学方程式为:CuS+4H2SO4(浓)
 CuSO4+4SO2↑+4H2O。
CuSO4+4SO2↑+4H2O。①请用“双线桥”法标明该反应电子转移的方向和数目
②当有1.5NA电子发生转移时,理论上生成SO2的体积(标准状况)为
您最近一年使用:0次
解题方法
3 . Ⅰ、化学实验中,通常需要使用到硫酸
(1)向Na2S2O3溶液滴加稀硫酸,产生淡黄色沉淀,写出反应的离子方程式___________ 。
(2)向硫酸酸化的KMnO4溶液中滴加草酸溶液,紫红色褪去。写出反应的离子方程式___________ 。
Ⅱ、氢气作为一种清洁能源,一直是能源研究的热点,工业上制取氢气有多种方法:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=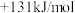
②CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=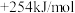
③CH4(g)+H2O(g)=CO(g)+3H2(g) △H3=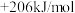
④CH3OH(1)=CO(g)+2H2(g) △H4=
(3)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式___________ 。反应②需要在___________ (高温、低温)下才能自发进行
(4)几种化学键的键能如下表所示:
根据以上有关反应的△H,计算x=___________ 。
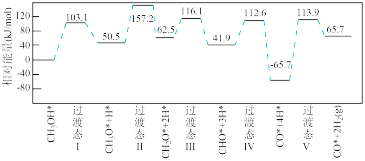
(5)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ: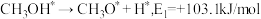
方式Ⅱ:
活化能E值推测,甲醇脱氢过程中主要历程的方式为___________ (填"Ⅰ"或"Ⅱ")。计算机模拟的各步反应的能量变化示意图如下。___________ 。
(1)向Na2S2O3溶液滴加稀硫酸,产生淡黄色沉淀,写出反应的离子方程式
(2)向硫酸酸化的KMnO4溶液中滴加草酸溶液,紫红色褪去。写出反应的离子方程式
Ⅱ、氢气作为一种清洁能源,一直是能源研究的热点,工业上制取氢气有多种方法:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=
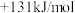
②CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=
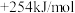
③CH4(g)+H2O(g)=CO(g)+3H2(g) △H3=
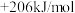
④CH3OH(1)=CO(g)+2H2(g) △H4=

(3)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式
(4)几种化学键的键能如下表所示:
| 化学键 | C=O | H—H | 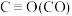 | C—H | O—H |
| 键能/kJ·mol-1 | 803 | 436 | x | 414 | 463 |
(5)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ:
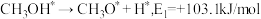
方式Ⅱ:

活化能E值推测,甲醇脱氢过程中主要历程的方式为
您最近一年使用:0次
解题方法
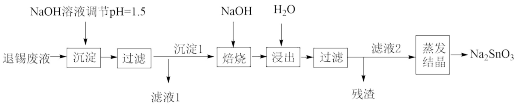
4 . 电子印制工业产生的某退锡废液含硝酸、锡化合物及少量Fe3+和Cu2+等,对其处理的流程如图。
(1)Na2SnO3的回收
①产品Na2SnO3中Sn的化合价是___________ 。
②退锡工艺是利用稀HNO3与Sn反应生成Sn2+,且无气体生成,则生成的硝酸盐是___________ ,废液中的Sn2+易转化成SnO2·xH2O。
③沉淀1的主要成分是SnO2,焙烧时,与NaOH反应的化学方程式为___________ 。
(2)滤液1的处理
①滤液1中Fe3+和Cu2+的浓度相近,加入NaOH溶液,先得到的沉淀是___________ 。
②25℃时,为了使Cu2+沉淀完全,需调节溶液H+浓度不大于___________ mol•L-1.
(3)产品中锡含量的测定
称取产品1.500g,用大量盐酸溶解,在CO2保护下,先用Al片将Sn4+还原为Sn2+,再用0.1000mol•L-1KIO3标准溶液滴定,以淀粉作指示剂滴定过程中IO 被还原为I—,终点时消耗KIO3溶液20.00mL。
被还原为I—,终点时消耗KIO3溶液20.00mL。
终点时的现象为___________ ,产生I2的离子反应方程式为___________ 。
| 化学式 | Sn(OH)4(或SnO2·2H2O) | Fe(OH)3 | Cu(OH)2 |
| 溶度积 | 1.0×10-56 | 4×10-38 | 2.5×10-20 |
①产品Na2SnO3中Sn的化合价是
②退锡工艺是利用稀HNO3与Sn反应生成Sn2+,且无气体生成,则生成的硝酸盐是
③沉淀1的主要成分是SnO2,焙烧时,与NaOH反应的化学方程式为
(2)滤液1的处理
①滤液1中Fe3+和Cu2+的浓度相近,加入NaOH溶液,先得到的沉淀是
②25℃时,为了使Cu2+沉淀完全,需调节溶液H+浓度不大于
(3)产品中锡含量的测定
称取产品1.500g,用大量盐酸溶解,在CO2保护下,先用Al片将Sn4+还原为Sn2+,再用0.1000mol•L-1KIO3标准溶液滴定,以淀粉作指示剂滴定过程中IO
 被还原为I—,终点时消耗KIO3溶液20.00mL。
被还原为I—,终点时消耗KIO3溶液20.00mL。终点时的现象为
您最近一年使用:0次
名校
5 .  是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下: 是粉红色固体,难溶于水。
是粉红色固体,难溶于水。
(1)Si在元素周期表的位置是___________ 。 的电子式为
的电子式为___________ 。
(2)烧渣是LiCl、 和
和 的混合物,“500℃焙烧”的化学方程式为
的混合物,“500℃焙烧”的化学方程式为___________ 。
(3)鉴别洗净的“滤饼3”和 中阳离子的常用方法是
中阳离子的常用方法是___________ 。
(4)实验室过滤操作时使用的玻璃仪器除玻璃棒还有___________ 。
(5)实验室检验 是否沉淀完全的操作是
是否沉淀完全的操作是___________ 。
(6)“850℃煅烧”时的化学方程式为___________ 。
 是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下: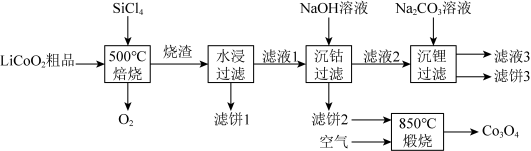
 是粉红色固体,难溶于水。
是粉红色固体,难溶于水。(1)Si在元素周期表的位置是
 的电子式为
的电子式为(2)烧渣是LiCl、
 和
和 的混合物,“500℃焙烧”的化学方程式为
的混合物,“500℃焙烧”的化学方程式为(3)鉴别洗净的“滤饼3”和
 中阳离子的常用方法是
中阳离子的常用方法是(4)实验室过滤操作时使用的玻璃仪器除玻璃棒还有
(5)实验室检验
 是否沉淀完全的操作是
是否沉淀完全的操作是(6)“850℃煅烧”时的化学方程式为
您最近一年使用:0次
名校
解题方法
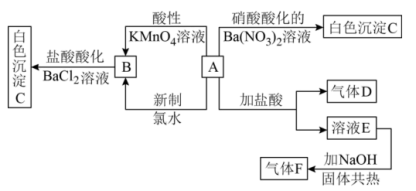
6 . 一种白色晶体A极易溶于水,将A配成溶液进行如下框图所示的实验,实验现象及转化关系如下列框图所示。其中A为正盐,气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝。
(1)写出下列物质化学式:A___________ ;C___________ ;
(2)写出F的电子式:___________ ;
(3)写出溶液E与 共热反应的离子方程式:
共热反应的离子方程式:___________ ;
(4)写出A和新制氯水反应的离子方程式:___________ 。
(1)写出下列物质化学式:A
(2)写出F的电子式:
(3)写出溶液E与
 共热反应的离子方程式:
共热反应的离子方程式:(4)写出A和新制氯水反应的离子方程式:
您最近一年使用:0次
7 . 高锰酸钾生产过程中产生的废锰渣(主要成分为MnO2、KOH、MgO和Fe2O3)可用于制备MnSO4晶体,工艺流程如下:
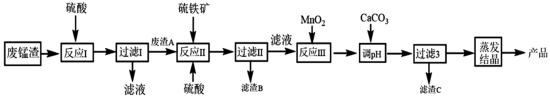
该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:
回答以下问题:
(1)MnSO4中阴离子的空间构型为___________ 、阳离子的价电子排布式为___________ 。
(2)提高“反应I”速率可采取的措施是___________ (除“加热”外,任写一种),滤渣A的主要成分为___________ (填化学式)。
(3)“反应II”中硫铁矿(FeS2)的作用为___________ 。
(4)“反应III”的离子方程式为___________ 。
(5)“调pH”步骤中,应调节pH不低于___________ 。

该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀pH | 2.10 | 7.45 | 9 27 27 | 9.60 |
| 完全沉淀pH | 3.20 | 8.95 | 10.87 | 11.13 |
(1)MnSO4中阴离子的空间构型为
(2)提高“反应I”速率可采取的措施是
(3)“反应II”中硫铁矿(FeS2)的作用为
(4)“反应III”的离子方程式为
(5)“调pH”步骤中,应调节pH不低于
您最近一年使用:0次
名校
解题方法
8 . 以Al2O3为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废Pd-Al2O3催化剂(主要含有Pd、Al2O3,还有少量PdO、SiO2、C)为原料制备氯化钯的流程如下:
(1)“焙烧”能有效清除废催化剂表面的积碳,打开Al2O3载体对钯的包裹,提高“氯化浸出”率。依据下图可判断“焙烧”的温度和时间应控制在___________ ,若焙烧时间过长,导致“氯化浸出”率下降可能的原因是___________ 。___________ ,通过该工序可将Pd转化为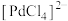 ,
,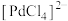 呈平面四边形,则
呈平面四边形,则 的杂化轨道类型为
的杂化轨道类型为___________ (填字母)。
A.sp2杂化 B.sp3杂化 C.dsp2杂化 D.dsp3杂化
(3)滤渣1为___________ ,滤渣2为___________ 。
(4)就“沉钯”中获得的 进行“热分解”,生成的气体可返回
进行“热分解”,生成的气体可返回___________ 工序继续使用。
(5)工业上也可用 还原
还原 制取海绵Pd,且对环境友好,该反应的化学方程式为
制取海绵Pd,且对环境友好,该反应的化学方程式为___________ 。
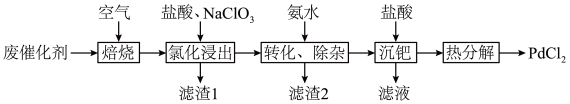
(1)“焙烧”能有效清除废催化剂表面的积碳,打开Al2O3载体对钯的包裹,提高“氯化浸出”率。依据下图可判断“焙烧”的温度和时间应控制在

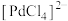 ,
,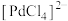 呈平面四边形,则
呈平面四边形,则 的杂化轨道类型为
的杂化轨道类型为A.sp2杂化 B.sp3杂化 C.dsp2杂化 D.dsp3杂化
(3)滤渣1为
(4)就“沉钯”中获得的
 进行“热分解”,生成的气体可返回
进行“热分解”,生成的气体可返回(5)工业上也可用
 还原
还原 制取海绵Pd,且对环境友好,该反应的化学方程式为
制取海绵Pd,且对环境友好,该反应的化学方程式为
您最近一年使用:0次
2024-04-02更新
|
520次组卷
|
4卷引用:东北三省2024届高三下学期三校二模联考化学试题
名校
9 . Li2CO3是制备锂离子电极材料LiFePO4的重要原料。以盐湖卤水(主要含有NaCl、MgCl2、LiCl和Na2B4O7等)为原料提取Li2CO3并制备LiFePO4的工艺流程如图所示:

已知:“日晒蒸发喷雾干燥”后固体含NaCl、LiCl、MgCl2•6H2O等。
(1)硼酸在水中的溶解度随温度的变化关系如图所示:
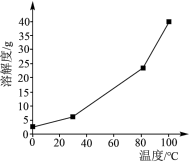
已知:H3BO3+H2O⇌[B(OH)4]-+H+。6.2gH3BO3最多与______ mL2.5mol/LNaOH溶液完全反应。“酸化脱硼”中采用______ (填“加热”或“冷却”),其目的是______ 。
(2)“水浸”后的溶液中溶质的主要成分是______ 。
(3)“蒸发分解”生成Li2CO3的化学方程式为______ 。
(4)已知不同温度下蒸发分解得到Li2CO3的产率及其溶解度随温度的变化关系如图所示。则“蒸发分解”的最佳温度是______ ,制得的Li2CO3沉淀需要进行洗涤,具体操作为______ 。
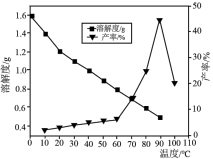
(5)制备LiFePO4时同时生成CO2,其中FePO4与C6H12O6物质的量之比为24:1,该化学反应方程式为______ 。

已知:“日晒蒸发喷雾干燥”后固体含NaCl、LiCl、MgCl2•6H2O等。
(1)硼酸在水中的溶解度随温度的变化关系如图所示:

已知:H3BO3+H2O⇌[B(OH)4]-+H+。6.2gH3BO3最多与
(2)“水浸”后的溶液中溶质的主要成分是
(3)“蒸发分解”生成Li2CO3的化学方程式为
(4)已知不同温度下蒸发分解得到Li2CO3的产率及其溶解度随温度的变化关系如图所示。则“蒸发分解”的最佳温度是

(5)制备LiFePO4时同时生成CO2,其中FePO4与C6H12O6物质的量之比为24:1,该化学反应方程式为
您最近一年使用:0次
名校
解题方法
10 . 绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分,某化学兴趣小组利用工厂的废铁屑(主要成分为Fe,此外还含有少量Cu、Al,Al2O3和Fe2O3)制备磁性Fe3O4胶体粒子、绿矾和净水剂Na2FeO4的实验流程如图:
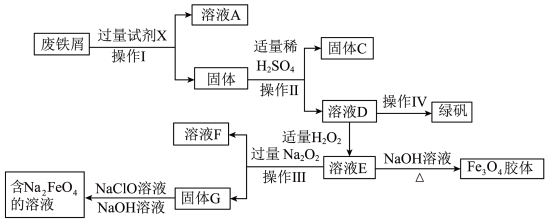
请回答下列问题:
(1)试剂X化学式为______ 。
(2)铁元素在元素周期表的位置为______ 。
(3)固体C化学名称为______ 。溶液D中加入 溶液,无红色产生,原因是
溶液,无红色产生,原因是______ (用离子方程式表示)。
(4)为得到绿矾晶体需要将溶液D倒入______ (填仪器名称)中进行浓缩,结晶。
(5)D中加入适量H2O2生成E的离子方程式______ 。若D中含3amolFe2+,则理论上加入______  H2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。
H2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。
(6)由固体G生成Na2FeO4的离子方程式为______ 。

请回答下列问题:
(1)试剂X化学式为
(2)铁元素在元素周期表的位置为
(3)固体C化学名称为
 溶液,无红色产生,原因是
溶液,无红色产生,原因是(4)为得到绿矾晶体需要将溶液D倒入
(5)D中加入适量H2O2生成E的离子方程式
 H2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。
H2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。(6)由固体G生成Na2FeO4的离子方程式为
您最近一年使用:0次



