1 . 健康人体内含铁元素大约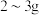 ,人体内铁元素以亚铁离子和三价铁离子的形式存在,
,人体内铁元素以亚铁离子和三价铁离子的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充含
易被吸收,所以给贫血者补充铁元素时,应补充含 的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如图实验:
的存在,设计并进行了如图实验:_____ ;试剂2的化学式为_____ 。
(2)加入新制氯水,溶液中发生反应的离子方程式是_____ 。
(3)加入试剂2时溶液为淡红色说明“速力非”中的 已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有_____ 性。
(4)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:______ 。
(5) 溶液存放时应在试剂瓶中加入
溶液存放时应在试剂瓶中加入______ ,防止 被氧化。
被氧化。
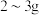 ,人体内铁元素以亚铁离子和三价铁离子的形式存在,
,人体内铁元素以亚铁离子和三价铁离子的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充含
易被吸收,所以给贫血者补充铁元素时,应补充含 的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如图实验:
的存在,设计并进行了如图实验:
(2)加入新制氯水,溶液中发生反应的离子方程式是
(3)加入试剂2时溶液为淡红色说明“速力非”中的
 已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有(4)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:(5)
 溶液存放时应在试剂瓶中加入
溶液存放时应在试剂瓶中加入 被氧化。
被氧化。
您最近半年使用:0次
2 . 除去下列物质中所含的少量杂质(括号内为杂质),所选除杂试剂正确的是
A. :饱和碳酸氢钠溶液洗气 :饱和碳酸氢钠溶液洗气 | B. 溶液( 溶液( ):加入过量盐酸 ):加入过量盐酸 |
C.CO2(HCl): 溶液 溶液 | D. 溶液( 溶液( ):加入足量铁粉,过滤 ):加入足量铁粉,过滤 |
您最近半年使用:0次
解题方法
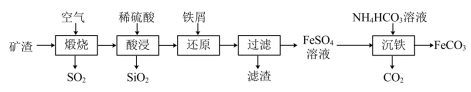
3 . 利用金属矿渣(含有FeS2、SiO2及Cu2O)制备FeCO3的实验流程如下。已知煅烧过程中FeS2和Cu2O转化为Fe2O3和CuO。 的反应外,还发生反应的
的反应外,还发生反应的离子方程式 有___________ 、___________ 。
(2)检验Fe3+是否完全被还原的实验操作是___________ 。
(3)FeSO4溶液浓度的测定。取制得的FeSO4溶液25.00mL,置于锥形瓶中,加入一定量的酸溶液,用0.1000mol/L的KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液19.50mL。计算FeSO4溶液的物质的是浓度___________ 。(写出计算过程)
(4)制备 FeCO3.写出“沉铁”步骤发生反应的离子方程式 :___________ 。
 的反应外,还发生反应的
的反应外,还发生反应的(2)检验Fe3+是否完全被还原的实验操作是
(3)FeSO4溶液浓度的测定。取制得的FeSO4溶液25.00mL,置于锥形瓶中,加入一定量的酸溶液,用0.1000mol/L的KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液19.50mL。计算FeSO4溶液的物质的是浓度
(4)制备 FeCO3.写出“沉铁”步骤发生反应的
您最近半年使用:0次
解题方法
4 . 价类二维图是学习元素及其化合物知识的重要模型。铁元素的价类二维图如图,下列有关说法不正确的是
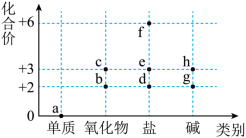
| A.a能导电,能被磁体吸引 | B.铁的氧化物只有b、c |
| C.e转化为f需加入氧化剂 | D.物质g在空气中不能长时间稳定存在 |
您最近半年使用:0次
5 . 某研究小组为了探究铁质材料(碳素钢) 和浓硫酸反应的产物,利用下列装置进行了实验探究活动。______ ;请写出碳参与反应的化学方程式______ 。
(2)实验开始后,观察到装置B和装置C中溶液均褪色。B中溶液褪色体现了 的
的______ 性,C中溶液褪色体现了 的
的______ 性。
(3)实验过程中观察到______ 现象时,说明有 气体生成。实验过程中观察到
气体生成。实验过程中观察到______ 现象时,说明反应产物中还有 生成。
生成。
(4)装置I中碱石灰的作用______ 。
(5)请设计实验方案,检验碳素钢和浓硫酸反应所得溶液中铁元素的化合价______ 。

(2)实验开始后,观察到装置B和装置C中溶液均褪色。B中溶液褪色体现了
 的
的 的
的(3)实验过程中观察到
 气体生成。实验过程中观察到
气体生成。实验过程中观察到 生成。
生成。(4)装置I中碱石灰的作用
(5)请设计实验方案,检验碳素钢和浓硫酸反应所得溶液中铁元素的化合价
您最近半年使用:0次
6 . 下列离子方程式正确的是
A.向 溶液中加入过量氮水: 溶液中加入过量氮水: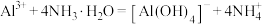 |
B.向 溶液中加入氯化铁溶液: 溶液中加入氯化铁溶液: |
C.将过量 通入“84”消毒液中: 通入“84”消毒液中: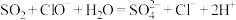 |
D.向碳酸氢铵溶液中加入少量氢氧化钠溶液: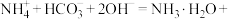  |
您最近半年使用:0次
名校
7 . 某化学兴趣小组研究浓硝酸与KSCN溶液的反应。
资料:Ⅰ.SCN‒中S、C、N元素的化合价依次为:-2价、+4价、-3价。
Ⅱ.SCN‒的性质类似卤素离子,能被氧化为(SCN)2,(SCN)2可聚合为红色的(SCN)x。
Ⅲ.NO2可溶于浓硝酸。
(1)实验一:___________ (填化学式)。
(2)实验二:研究SCN‒的转化产物。
a.将实验一ⅲ中的气体通入Ba(OH)2和NaOH的混合溶液中,有白色沉淀生成。
b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量KMnO4溶液,不褪色。
c.另取少量实验一ⅲ中试管内的溶液加入BaCl2溶液,产生大量白色沉淀。
①甲同学根据实验一iii的现象推断SCN‒的氧化产物中一定有NO2,乙同学认为证据不足,理由是___________ 。
②通过b证实了红棕色气体中不含SO2,证据是___________ 。
③由上述实验现象可知:SCN‒转化的最终产物中一定有___________ 。
(3)实验三:研究实验一ⅲ中“静置一段时间后,突然剧烈反应,红色迅速褪去”的原因。丙同学设计了实验三,与实验一进行对比,证实了一定浓度的NO2能加快浓硝酸氧化(SCN)x的化学反应速率。
实验三:___________ 。
②操作2是___________ 。
资料:Ⅰ.SCN‒中S、C、N元素的化合价依次为:-2价、+4价、-3价。
Ⅱ.SCN‒的性质类似卤素离子,能被氧化为(SCN)2,(SCN)2可聚合为红色的(SCN)x。
Ⅲ.NO2可溶于浓硝酸。
(1)实验一:
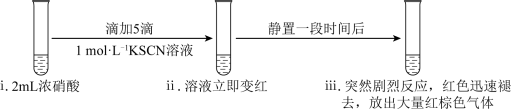
(2)实验二:研究SCN‒的转化产物。
a.将实验一ⅲ中的气体通入Ba(OH)2和NaOH的混合溶液中,有白色沉淀生成。
b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量KMnO4溶液,不褪色。
c.另取少量实验一ⅲ中试管内的溶液加入BaCl2溶液,产生大量白色沉淀。
①甲同学根据实验一iii的现象推断SCN‒的氧化产物中一定有NO2,乙同学认为证据不足,理由是
②通过b证实了红棕色气体中不含SO2,证据是
③由上述实验现象可知:SCN‒转化的最终产物中一定有
(3)实验三:研究实验一ⅲ中“静置一段时间后,突然剧烈反应,红色迅速褪去”的原因。丙同学设计了实验三,与实验一进行对比,证实了一定浓度的NO2能加快浓硝酸氧化(SCN)x的化学反应速率。
实验三:
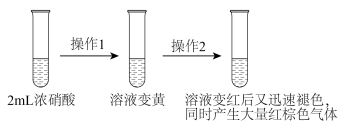
②操作2是
您最近半年使用:0次
名校
解题方法
8 . 某化学实验小组同学利用如图所示装置制备氨气,并探究氨气的性质(部分仪器已略去)。___________ 。
(2)干燥氨气可选用的试剂是___________ (填序号)。
①浓H2SO4 ②碱石灰 ③P2O5
(3)收集氨气时,氨气的进气口为___________ (填“a”或“b”)。
(4)证明烧瓶中氨气集满的方法是___________ 。
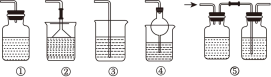
(5)为防止环境污染,下列装置中(盛放的液体均为水)可用于吸收多余氨气的是___________ (填序号)。___________ (填选项代号)。
a.装置Ⅰ中红色Fe2O3粉末变为黑色粉末,经检验是一种铁的氧化物
b.装置Ⅱ中无水CuSO4粉末变为蓝色
c.装置Ⅲ无水CaCl2的质量增加
d.生成一种无色无味气体,该气体无污染
(7)小组同学继续对(6)装置I反应后黑色粉末的组成进行探究。
(8)结合(6)(7)实验,写出(6)中NH3还原Fe2O3的化学方程式___________ 。
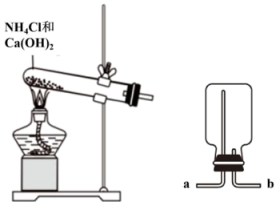
(2)干燥氨气可选用的试剂是
①浓H2SO4 ②碱石灰 ③P2O5
(3)收集氨气时,氨气的进气口为
(4)证明烧瓶中氨气集满的方法是
(5)为防止环境污染,下列装置中(盛放的液体均为水)可用于吸收多余氨气的是
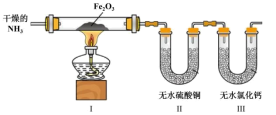
a.装置Ⅰ中红色Fe2O3粉末变为黑色粉末,经检验是一种铁的氧化物
b.装置Ⅱ中无水CuSO4粉末变为蓝色
c.装置Ⅲ无水CaCl2的质量增加
d.生成一种无色无味气体,该气体无污染
(7)小组同学继续对(6)装置I反应后黑色粉末的组成进行探究。
| 操作 | 现象 | 结论或离子方程式 |
| 步骤1:取少量黑色粉末于小烧杯中,加入过量盐酸 | 黑色粉末全部溶解,无气泡产生,溶液呈浅绿色 | 溶液中可能含有Fe2+ |
| 步骤2:取步骤1少量溶液于试管中,滴入2-3滴KSCN溶液,振荡 | 溶液颜色 | 溶液中不含有Fe3+ |
| 步骤3:向步骤2试管中滴入少量氯水 | 溶液变红色 | 涉及离子方程式有 Fe(SCN)3 Fe(SCN)3 |
您最近半年使用:0次
名校
9 . 氰化氢(HCN,一元弱酸,易挥发)主要应用于电镀、采矿、药物合成等工业生产。HCN,CN-能抑制人体组织细胞内酶的活性,不能直接排放到环境中。
(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是 将CN-转化为SCN-和
将CN-转化为SCN-和 。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,___________ 。
(2)Cu2+可催化过氧化氢氧化废水中的CN-。
①反应不能在酸性条件下进行,原因是___________ 。
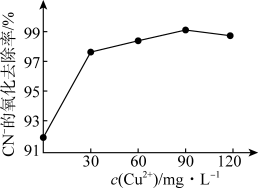
②在含氰废水总景、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过90mg·L-1时,CN-的氧化去除率有所下降,原因是___________ 。 ,其反应的离子方程式为
,其反应的离子方程式为___________ 。
(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应:HCN(g)+H2O(g) NH3(g)+CO(g) △H>0
NH3(g)+CO(g) △H>0
除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是___________ 。
(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是
 将CN-转化为SCN-和
将CN-转化为SCN-和 。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,(2)Cu2+可催化过氧化氢氧化废水中的CN-。
①反应不能在酸性条件下进行,原因是
②在含氰废水总景、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过90mg·L-1时,CN-的氧化去除率有所下降,原因是
 ,其反应的离子方程式为
,其反应的离子方程式为(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应:HCN(g)+H2O(g)
 NH3(g)+CO(g) △H>0
NH3(g)+CO(g) △H>0除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是

您最近半年使用:0次
10 . 室温下,下列实验方案能得出相应结论的是
| 选项 | 方案 | 结论 |
| A | 将灼热的木炭加入浓硝酸中,有红棕色气体产生 | 木炭在加热条件下能与浓硝酸反应 |
| B | CO还原Fe2O3实验中,Fe2O3是否全部被还原 | 向CO还原Fe2O3所得到的产物中加入稀盐酸,再滴加KSCN溶液,观察颜色变化 |
| C | 向Fe(NO3)2和KSCN的混合溶液中滴入酸化的AgNO3溶液振荡,溶液颜色变红 | 氧化性:Ag+>Fe3+ |
| D | 把熔嵌在玻璃棒上的铂丝放在酒精灯外焰上灼烧至与原来的火焰颜色相同时为止。用铂丝蘸取待测液,在外焰上灼烧,观察到火焰呈黄色 | 待测液中含有Na元素 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



