名校
解题方法
1 . 中国科学家首次用 改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸二甲酯加氢的主要反应有:
改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸二甲酯加氢的主要反应有:
①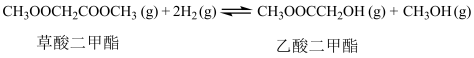
②
③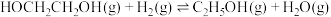
其他条件相同时,相同时间内温度对产物选择性的影响结果如图。

已知:i.
ii.450~500K,反应③的平衡常数远大于反应①和反应②的平衡常数
下列说法不正确 的是
 改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸二甲酯加氢的主要反应有:
改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸二甲酯加氢的主要反应有:①
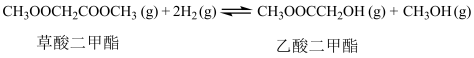
②

③
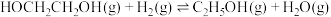
其他条件相同时,相同时间内温度对产物选择性的影响结果如图。

已知:i.

ii.450~500K,反应③的平衡常数远大于反应①和反应②的平衡常数
下列说法
| A.制乙二醇适宜的温度范围是470~480K |
| B.实验条件下反应③的活化的最高,升温更有利于反应③ |
| C.减压可提高乙二醇的平衡产率 |
D.铜基催化剂用 改性后反应速率增大,可以降低反应所需的压强 改性后反应速率增大,可以降低反应所需的压强 |
您最近半年使用:0次
2023-05-11更新
|
739次组卷
|
3卷引用:北京市西城区2023届高三二模化学试题
2 . 近年观测数据表明,京津冀地区硝酸盐区域性污染逐年减轻。氮氧化物是硝酸盐的前体物,科学家致力于氮氧化物的深度减排。回答下列问题:
(1)NO在空气中存在如下反应:
 ,该反应共有两步,第一步反应为
,该反应共有两步,第一步反应为
 ;请写出第二步反应的热化学方程式(
;请写出第二步反应的热化学方程式( 用含
用含 、
、 的式子来表示):
的式子来表示):___________ 。
(2)温度为T1,在两个容积均为1L的恒容密闭容器中仅发生反应: 。
。
容器I中5min达到平衡。相关数据如表所示:
①容器II在反应的起始阶段向___________ (“正反应”、“逆反应”、“达平衡”)方向进行。
②达到平衡时,容器I与容器II中的总压强之比为___________ 。
A.>1 B.=1 C.<1
(3)可用 去除NO,其反应原理
去除NO,其反应原理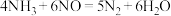 。不同温度条件下
。不同温度条件下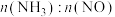 的物质的量之比分别为4∶1,3∶1、1∶3时,得到NO脱除率曲线如下图所示:
的物质的量之比分别为4∶1,3∶1、1∶3时,得到NO脱除率曲线如下图所示:
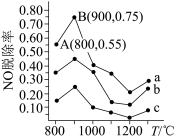
①曲线a中,NO的起始浓度为 ,从A点到B点经过0.8s,该时间段内NO的脱除速率为
,从A点到B点经过0.8s,该时间段内NO的脱除速率为___________  。
。
②曲线b对应 与NO的物质的量之比是
与NO的物质的量之比是___________ 。
(4)还可用间接电解法除NO。其原理如图所示:
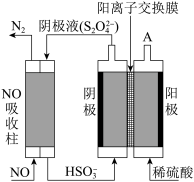
①写出电解池阴极的电极反应式___________ 。
②从A口中出来的气体的是___________ 。
③用离子方程式表示吸收柱中除去NO的原理___________ 。
(1)NO在空气中存在如下反应:

 ,该反应共有两步,第一步反应为
,该反应共有两步,第一步反应为
 ;请写出第二步反应的热化学方程式(
;请写出第二步反应的热化学方程式( 用含
用含 、
、 的式子来表示):
的式子来表示):(2)温度为T1,在两个容积均为1L的恒容密闭容器中仅发生反应:
 。
。容器I中5min达到平衡。相关数据如表所示:
| 容器编号 | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | ||
 |  |  |  | |
| I | 0.6 | 0 | 0 | 0.2 |
| II | 0.3 | 0.5 | 0.2 | |
②达到平衡时,容器I与容器II中的总压强之比为
A.>1 B.=1 C.<1
(3)可用
 去除NO,其反应原理
去除NO,其反应原理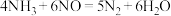 。不同温度条件下
。不同温度条件下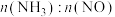 的物质的量之比分别为4∶1,3∶1、1∶3时,得到NO脱除率曲线如下图所示:
的物质的量之比分别为4∶1,3∶1、1∶3时,得到NO脱除率曲线如下图所示:
①曲线a中,NO的起始浓度为
 ,从A点到B点经过0.8s,该时间段内NO的脱除速率为
,从A点到B点经过0.8s,该时间段内NO的脱除速率为 。
。②曲线b对应
 与NO的物质的量之比是
与NO的物质的量之比是(4)还可用间接电解法除NO。其原理如图所示:

①写出电解池阴极的电极反应式
②从A口中出来的气体的是
③用离子方程式表示吸收柱中除去NO的原理
您最近半年使用:0次
名校
解题方法
3 . 一定温度下,在恒容的密闭容器内,将2molSO2和1molO2混合发生反应:2SO2(g)+O2(g) 2SO3(g) △H<0。回答下列问题:
2SO3(g) △H<0。回答下列问题:
(1)升高温度,混合气体的密度______ (填“变大”“变小”或“不变”)。
(2)若反应达到平衡后,再充入O2,平衡将______ (填“正向”“向”或“不”)移动,SO2的转化率______ (填“增大”“减小”或“不变”)。
(3)若反应达到平衡后,将c(SO2)、c(O2)、c(SO3)同时增大1倍,平衡将______ 移动。
(4)如图表示合成SO3反应在某段时间t0→t6中反应速率与时间的曲线图,t1、t3、t4时刻分别改变某一外界条件,它们依次为______ 、______ 、______ ;SO3的体积分数最小的平衡时间段是______ (填序号)。

 2SO3(g) △H<0。回答下列问题:
2SO3(g) △H<0。回答下列问题:(1)升高温度,混合气体的密度
(2)若反应达到平衡后,再充入O2,平衡将
(3)若反应达到平衡后,将c(SO2)、c(O2)、c(SO3)同时增大1倍,平衡将
(4)如图表示合成SO3反应在某段时间t0→t6中反应速率与时间的曲线图,t1、t3、t4时刻分别改变某一外界条件,它们依次为

您最近半年使用:0次
4 . 已知 催化加氢合成乙醇的反应原理为
催化加氢合成乙醇的反应原理为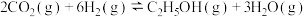 。设
。设 为起始时的投料比,即
为起始时的投料比,即 。
。 的平衡转化率与压强、温度和投料比的关系如图所示,下列有关说法错误的是
的平衡转化率与压强、温度和投料比的关系如图所示,下列有关说法错误的是

 催化加氢合成乙醇的反应原理为
催化加氢合成乙醇的反应原理为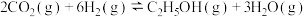 。设
。设 为起始时的投料比,即
为起始时的投料比,即 。
。 的平衡转化率与压强、温度和投料比的关系如图所示,下列有关说法错误的是
的平衡转化率与压强、温度和投料比的关系如图所示,下列有关说法错误的是
A.图1中投料比相同,温度从高到低的顺序为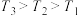 |
B.图2中投料比由大到小的顺序为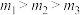 |
C.若图1中投料比 ,a点时乙醇的分压为 ,a点时乙醇的分压为 |
D.若图2中投料比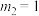 ,随着温度的升高,该平衡体系中 ,随着温度的升高,该平衡体系中 的百分含量逐渐减小 的百分含量逐渐减小 |
您最近半年使用:0次
名校
5 . 高纯度的氢氟酸是制造芯片的重要原料之一。
(1)氟原子激发态的电子排布式有_____ (选填编号,下同),其中能量较高的是_____ 。
A.1s22s22p43s1 B.1s22s22p43d2 C.1s22s12p5 D.1s22s22p33p2
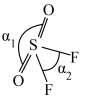
SO2F2的分子结构如图所示,键角α1>α2的主要原因是______ 。
(2)HF无论是气态还是在水溶液中均可二聚形成(HF)2。HF能二聚的原因是_____ ,写出(HF)2发生第二步电离的电离方程式:_____ 。
(3)已知:HF(aq) H+(aq)+F-(aq) △H=-10.4kJ•mol-1
H+(aq)+F-(aq) △H=-10.4kJ•mol-1
H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ•mol-1
则HF(aq)+NaOH(aq)=NaF(aq)+H2O(l)的△H=______ kJ•mol-1。
如图为恒温、带有可自由移动隔板的刚性容器。当两边分别充入4g氦气和20g单分子态的HF气体时,隔板位于“5”处,隔板两边容器内的压强均为100kPa。

若固定隔板位于“5”处,当右侧容器内反应2HF(g) (HF)2(g)达到平衡状态时,右侧容器内压强为p1;松开隔板,隔板移至“6”处并达到新的平衡,此时右侧容器压强为p2。
(HF)2(g)达到平衡状态时,右侧容器内压强为p1;松开隔板,隔板移至“6”处并达到新的平衡,此时右侧容器压强为p2。
(4)p1_____ p2(选填“A:>”“B:<”或“C:=”)。该温度下,2HF(g) (HF)2(g)反应的平衡常数Kp=
(HF)2(g)反应的平衡常数Kp=_____ kPa-1。
(5)若将上述容器改为绝热容器,固定隔板在“5”处,下列不能说明右侧容器内反应已达平衡状态的是____ (选填编号)。
A.容器右侧气体的密度不再改变
B.容器右侧的温度不再改变
C.容器右侧气体的压强不再改变
D.容器右侧气体的平均相对分子质量不再改变
E.2v(HF)正=v[(HF)2]逆
某温度下,将分析浓度(总浓度)相同的HCl、HF和CH3COOH三种溶液,分别加水稀释时,溶液pH变化如图所示。图中,氢氟酸溶液在稀释初期的pH上升较快。

(6)据此判断,(HF)2与HF的酸性相比,较强的是_____ [选填“A:(HF)2”或“B:HF”]。
(7)NaF和HF的混合液具有一定的缓冲能力,即加入少量的酸或碱时,溶液的pH基本保持不变。用电离平衡理论解释NaF和HF混合液具有一定缓冲能力的原因______ 。
(1)氟原子激发态的电子排布式有
A.1s22s22p43s1 B.1s22s22p43d2 C.1s22s12p5 D.1s22s22p33p2
SO2F2的分子结构如图所示,键角α1>α2的主要原因是

(2)HF无论是气态还是在水溶液中均可二聚形成(HF)2。HF能二聚的原因是
(3)已知:HF(aq)
 H+(aq)+F-(aq) △H=-10.4kJ•mol-1
H+(aq)+F-(aq) △H=-10.4kJ•mol-1H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ•mol-1
则HF(aq)+NaOH(aq)=NaF(aq)+H2O(l)的△H=
如图为恒温、带有可自由移动隔板的刚性容器。当两边分别充入4g氦气和20g单分子态的HF气体时,隔板位于“5”处,隔板两边容器内的压强均为100kPa。

若固定隔板位于“5”处,当右侧容器内反应2HF(g)
 (HF)2(g)达到平衡状态时,右侧容器内压强为p1;松开隔板,隔板移至“6”处并达到新的平衡,此时右侧容器压强为p2。
(HF)2(g)达到平衡状态时,右侧容器内压强为p1;松开隔板,隔板移至“6”处并达到新的平衡,此时右侧容器压强为p2。(4)p1
 (HF)2(g)反应的平衡常数Kp=
(HF)2(g)反应的平衡常数Kp=(5)若将上述容器改为绝热容器,固定隔板在“5”处,下列不能说明右侧容器内反应已达平衡状态的是
A.容器右侧气体的密度不再改变
B.容器右侧的温度不再改变
C.容器右侧气体的压强不再改变
D.容器右侧气体的平均相对分子质量不再改变
E.2v(HF)正=v[(HF)2]逆
某温度下,将分析浓度(总浓度)相同的HCl、HF和CH3COOH三种溶液,分别加水稀释时,溶液pH变化如图所示。图中,氢氟酸溶液在稀释初期的pH上升较快。

(6)据此判断,(HF)2与HF的酸性相比,较强的是
(7)NaF和HF的混合液具有一定的缓冲能力,即加入少量的酸或碱时,溶液的pH基本保持不变。用电离平衡理论解释NaF和HF混合液具有一定缓冲能力的原因
您最近半年使用:0次
名校
解题方法
6 . 可逆反应aA(g)+bB(s) cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是

 cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
| A.使用催化剂C的物质的量分数增加 |
| B.已知T2>T1,升高温度能提高A的转化率 |
| C.已知p2>p1,则化学计量数:a<c+d |
| D.若该反应在恒容中进行,通入氦气(不参与反应),使压强增大,将加快该反应的速率 |
您最近半年使用:0次
解题方法
7 . “节能减排”和“低碳经济”的一项重要课题就是如何将 转化为可利用的资源。
转化为可利用的资源。
Ⅰ.目前工业上有一种方法是用 来生产燃料甲醇。
来生产燃料甲醇。
已知: 的燃烧热
的燃烧热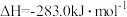
反应①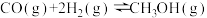
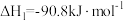
反应②
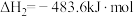
反应③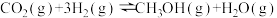

(1)
___________ ,反应③的
___________ (填“>”或“<”)0,反应③在___________ (填“高温”、“低温”或“任何温度”)下能自发进行。
(2)恒温条件下,在某恒容密闭容器中,按照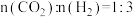 投料仅发生反应③,起始气体总压强为
投料仅发生反应③,起始气体总压强为 ,测得
,测得 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
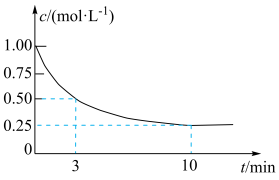
①从反应开始到3min, 的平均反应速率
的平均反应速率
___________  ;试在图中绘制出
;试在图中绘制出 的浓度随时间变化的图像
的浓度随时间变化的图像___________ 。
②该反应的平衡常数
___________ (填含 的表达式)。
的表达式)。
(3)恒温条件下,在某恒压密闭容器中仅发生反应①,当反应达到平衡后,向平衡体系中通入惰性气体,平衡___________ (填“向正反应方向移动”、“向逆反应方向移动”或“不移动”)。
 转化为可利用的资源。
转化为可利用的资源。Ⅰ.目前工业上有一种方法是用
 来生产燃料甲醇。
来生产燃料甲醇。已知:
 的燃烧热
的燃烧热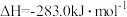
反应①
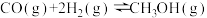
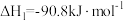
反应②

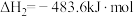
反应③
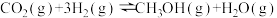

(1)


(2)恒温条件下,在某恒容密闭容器中,按照
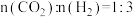 投料仅发生反应③,起始气体总压强为
投料仅发生反应③,起始气体总压强为 ,测得
,测得 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
①从反应开始到3min,
 的平均反应速率
的平均反应速率
 ;试在图中绘制出
;试在图中绘制出 的浓度随时间变化的图像
的浓度随时间变化的图像②该反应的平衡常数

 的表达式)。
的表达式)。(3)恒温条件下,在某恒压密闭容器中仅发生反应①,当反应达到平衡后,向平衡体系中通入惰性气体,平衡
您最近半年使用:0次
名校
8 . 在特定条件下, 和
和 发生反应:
发生反应: ,
, ,且测得合成
,且测得合成 反应的速率与参与反应的物质的浓度的关系为:
反应的速率与参与反应的物质的浓度的关系为: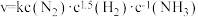 。下列有关叙述错误的是
。下列有关叙述错误的是
 和
和 发生反应:
发生反应: ,
, ,且测得合成
,且测得合成 反应的速率与参与反应的物质的浓度的关系为:
反应的速率与参与反应的物质的浓度的关系为: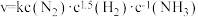 。下列有关叙述错误的是
。下列有关叙述错误的是A.当 的百分含量不再变化时,反应达到化学平衡 的百分含量不再变化时,反应达到化学平衡 |
B.加压, 增加的倍数大于 增加的倍数大于 增加的倍数 增加的倍数 |
C.升高温度, 的平衡转化率降低 的平衡转化率降低 |
D.该条件下,分离出 可提高 可提高 转化率,但反应速率将降低 转化率,但反应速率将降低 |
您最近半年使用:0次
2023-05-07更新
|
286次组卷
|
3卷引用:湖南省常德市第一中学2022~2023学年高二上学期期中考试化学试题
湖南省常德市第一中学2022~2023学年高二上学期期中考试化学试题新疆生产建设兵团第二师八一中学2022-2023学年高二下学期期末考试化学试题(已下线)专题05 化学反应的方向 化学反应的调控 -【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
解题方法
9 . 含碳化合物的合成与转化具有重要的研究价值和现实意义。由合成气(主要成分为 ,
, 和
和 )制甲醇,涉及的原理为:
)制甲醇,涉及的原理为:
①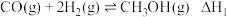
②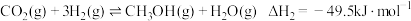
③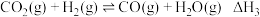
(1)反应①的
___________  ,该反应自发进行的条件为
,该反应自发进行的条件为___________ 。(填“高温”或“低温”)
(2)在 的恒压反应器中,按照
的恒压反应器中,按照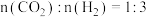 投料,测得体系中平衡时
投料,测得体系中平衡时 和
和 的选择性[
的选择性[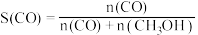 ,
, ]及
]及 的平衡转化率随温度的变化如图a所示。
的平衡转化率随温度的变化如图a所示。
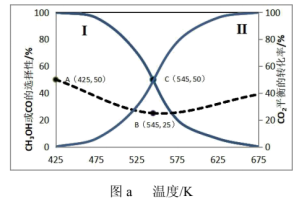
①曲线Ⅰ代表___________ 的选择性随温度变化曲线。
②反应③在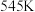 时的平衡常数
时的平衡常数
___________ 。(用分数表示)
(3)不同压强下,按照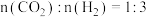 投料,实验测得
投料,实验测得 的平衡转化率和
的平衡转化率和 的平衡产率随温度变化如图所示:
的平衡产率随温度变化如图所示:

已知: 的平衡产率
的平衡产率
①其中纵坐标表示 的平衡产率的是图
的平衡产率的是图___________ (填“b”或“c”),该图中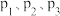 由大到小的顺序是
由大到小的顺序是___________ 。
②图c中, 温度时,三条曲线几乎交于一点的原因是
温度时,三条曲线几乎交于一点的原因是___________ 。
 ,
, 和
和 )制甲醇,涉及的原理为:
)制甲醇,涉及的原理为:①
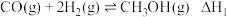
②
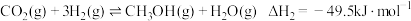
③
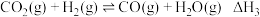
| 化学键 |  |  |  |  |  |
 | 436 | 343 | 1076 | 465 | 413 |

 ,该反应自发进行的条件为
,该反应自发进行的条件为(2)在
 的恒压反应器中,按照
的恒压反应器中,按照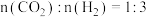 投料,测得体系中平衡时
投料,测得体系中平衡时 和
和 的选择性[
的选择性[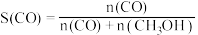 ,
, ]及
]及 的平衡转化率随温度的变化如图a所示。
的平衡转化率随温度的变化如图a所示。
①曲线Ⅰ代表
②反应③在
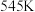 时的平衡常数
时的平衡常数
(3)不同压强下,按照
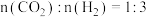 投料,实验测得
投料,实验测得 的平衡转化率和
的平衡转化率和 的平衡产率随温度变化如图所示:
的平衡产率随温度变化如图所示:
已知:
 的平衡产率
的平衡产率
①其中纵坐标表示
 的平衡产率的是图
的平衡产率的是图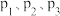 由大到小的顺序是
由大到小的顺序是②图c中,
 温度时,三条曲线几乎交于一点的原因是
温度时,三条曲线几乎交于一点的原因是
您最近半年使用:0次
10 . 工业上 傕化氧化可制得
傕化氧化可制得 ,主要反应如下:
,主要反应如下:
反应I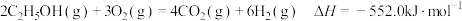
反应II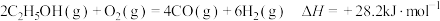
还可能发生下列副反应:
反应III
反应IV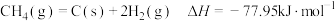
反应V
研究发现,在实验条件下,乙醇的转化率都接近 .
. 下,氧醇比为0.6时,部分气体产物(
下,氧醇比为0.6时,部分气体产物( 、
、 、
、 和
和 )的平衡分压
)的平衡分压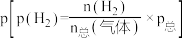 随温度的变化如图所示。已知:用气体物质的分压替换浓度计算得到的平衡常数称为分压平衡常数
随温度的变化如图所示。已知:用气体物质的分压替换浓度计算得到的平衡常数称为分压平衡常数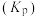 。下列说法正确的是
。下列说法正确的是

 傕化氧化可制得
傕化氧化可制得 ,主要反应如下:
,主要反应如下:反应I
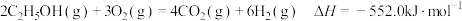
反应II
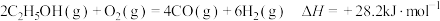
还可能发生下列副反应:
反应III

反应IV
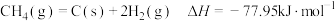
反应V

研究发现,在实验条件下,乙醇的转化率都接近
 .
. 下,氧醇比为0.6时,部分气体产物(
下,氧醇比为0.6时,部分气体产物( 、
、 、
、 和
和 )的平衡分压
)的平衡分压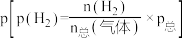 随温度的变化如图所示。已知:用气体物质的分压替换浓度计算得到的平衡常数称为分压平衡常数
随温度的变化如图所示。已知:用气体物质的分压替换浓度计算得到的平衡常数称为分压平衡常数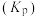 。下列说法正确的是
。下列说法正确的是
| A.500K时,反应体系中一定有积碳产生 |
B.曲线①表示 的平衡分压随温度的变化 的平衡分压随温度的变化 |
C.720K时,反应IV的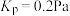 |
| D.其他条件一定,增加体系压强,产物中氢气的量增多 |
您最近半年使用:0次



