名校
1 . 回答下列问题:
(1)某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知A、B、C均为气体)。
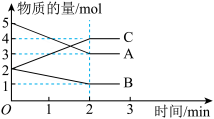
①该反应的化学方程式为_______ 。
②反应开始至2min时,B的平均反应速率为_______ 。
(2)为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积气体所需的时间。
①请完成此实验设计:其中
_______ ,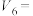
_______ 。
②该同学最后得出的结论为当加入少量 溶液时,生成氢气的速率会大大提高,但当加入的
溶液时,生成氢气的速率会大大提高,但当加入的 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:_______ 。
(3)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO: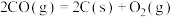 。已知该反应的
。已知该反应的 ,该设想能否实现?
,该设想能否实现?_______ (填“能”或“否”),依据是:_______ 。
(1)某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知A、B、C均为气体)。

①该反应的化学方程式为
②反应开始至2min时,B的平均反应速率为
(2)为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积气体所需的时间。
实验 混合溶液 | A | B | C | D | E | F |
4 mol·L  溶液/mL 溶液/mL | 30 |  |  |  |  | 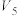 |
饱和 溶液/mL 溶液/mL | 0 | 0.5 | 2.5 | 5 |  | 20 |
 /mL /mL | 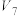 | 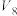 |  | 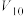 | 10 | 0 |

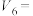
②该同学最后得出的结论为当加入少量
 溶液时,生成氢气的速率会大大提高,但当加入的
溶液时,生成氢气的速率会大大提高,但当加入的 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:(3)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:
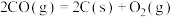 。已知该反应的
。已知该反应的 ,该设想能否实现?
,该设想能否实现?
您最近一年使用:0次
2 . 基元反应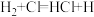 的能量变化如图所示。下列说法不正确的是
的能量变化如图所示。下列说法不正确的是

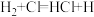 的能量变化如图所示。下列说法不正确的是
的能量变化如图所示。下列说法不正确的是
A.该基元反应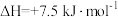 | B.过渡态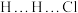 能量高,不稳定 能量高,不稳定 |
C.加入催化剂,则 小于 小于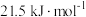 | D.若 ,则该反应在任何温度下都能自发进行 ,则该反应在任何温度下都能自发进行 |
您最近一年使用:0次
名校
3 . 下列叙述正确的是
A. , , 的反应一定能自发进行 的反应一定能自发进行 |
| B.升高温度增加了反应物中活化分子百分数 |
| C.化学反应必须发生有效碰撞,但有效碰撞不一定发生化学反应 |
D.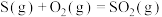  , ,  ;则: ;则: |
您最近一年使用:0次
4 . 2022年6月5日,我国长征二号运载火箭搭载神舟十四号载人飞船顺利升空,其动力燃料是偏二甲肼,火箭发射时只要将其和四氧化二氮在发动机燃烧室混合即可,核心反应为: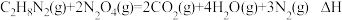 。对于该反应下列说法不正确的是
。对于该反应下列说法不正确的是
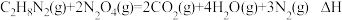 。对于该反应下列说法不正确的是
。对于该反应下列说法不正确的是A.用 表示键能之和,该反应 表示键能之和,该反应 (反应物) (反应物) (生成物) (生成物) |
B.由该热化学反应方程式可知,偏二甲肼的燃烧热为 |
| C.该反应物的总能量大于生成物总能量 |
D.该反应的 , , ,反应在任意条件下均能自发进行 ,反应在任意条件下均能自发进行 |
您最近一年使用:0次
名校
5 . 以 为原料合成
为原料合成 涉及的反应如下:
涉及的反应如下:
I.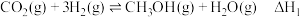
Ⅱ.
Ⅲ.
回答下列问题:
(1)计算反应I的
___________  ,该反应在
,该反应在___________ (填“高温”、“低温”或“任意温度”)下能自发。
(2)在 下,按照
下,按照 投料,假设只发生反应I和Ⅱ,平衡时,
投料,假设只发生反应I和Ⅱ,平衡时, 和
和 在含碳产物物质的量分数及
在含碳产物物质的量分数及 的转化率随温度的变化如图:
的转化率随温度的变化如图:
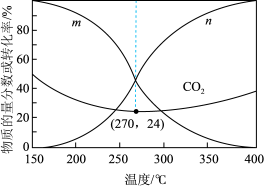
①图中代表 的曲线为
的曲线为___________ (填“m”或“n”)。
②解释 范围内
范围内 转化率随温度升高而降低的原因
转化率随温度升高而降低的原因___________ 。
③下列说法正确的是___________ (填字母)。
A.温度越高,越有利于工业生产
B.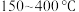 范围内,温度升高,
范围内,温度升高, 的平衡产量先减小后增大
的平衡产量先减小后增大
C.随着温度逐渐升高,混合气体的平均相对分子质量几乎又变回起始的状态
④已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ;则
;则 时
时 的分压为
的分压为___________  (用最简分数),反应II的平衡常数
(用最简分数),反应II的平衡常数 为
为___________ (列出算式即可)。
 为原料合成
为原料合成 涉及的反应如下:
涉及的反应如下:I.
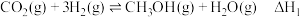
Ⅱ.

Ⅲ.

回答下列问题:
(1)计算反应I的

 ,该反应在
,该反应在(2)在
 下,按照
下,按照 投料,假设只发生反应I和Ⅱ,平衡时,
投料,假设只发生反应I和Ⅱ,平衡时, 和
和 在含碳产物物质的量分数及
在含碳产物物质的量分数及 的转化率随温度的变化如图:
的转化率随温度的变化如图:
①图中代表
 的曲线为
的曲线为②解释
 范围内
范围内 转化率随温度升高而降低的原因
转化率随温度升高而降低的原因③下列说法正确的是
A.温度越高,越有利于工业生产

B.
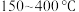 范围内,温度升高,
范围内,温度升高, 的平衡产量先减小后增大
的平衡产量先减小后增大C.随着温度逐渐升高,混合气体的平均相对分子质量几乎又变回起始的状态
④已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
 ;则
;则 时
时 的分压为
的分压为 (用最简分数),反应II的平衡常数
(用最简分数),反应II的平衡常数 为
为
您最近一年使用:0次
2024-03-02更新
|
126次组卷
|
2卷引用:安徽省六安第一中学2023-2024学年高二上学期期末考试化学试题
名校
6 . 下列说法正确的是
| A.增大压强,活化分子百分数增多,化学反应速率增大 |
B.C(石墨,s)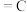 (金刚石,s) (金刚石,s) 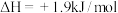 ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
C.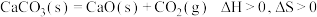 ,不论在何种条件下都不可能自发进行 ,不论在何种条件下都不可能自发进行 |
D.在恒温恒容下,发生反应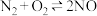 ,若在容器中充入 ,若在容器中充入 ,正、逆反应的速率均不变 ,正、逆反应的速率均不变 |
您最近一年使用:0次
名校
7 . 恒容密闭容器中发生反应
 。下列说法正确的是
。下列说法正确的是

 。下列说法正确的是
。下列说法正确的是A.室温下能自发进行,表明该反应的 |
| B.保持温度一定,充入氩气使反应速率加快 |
| C.加入合适的催化剂,既能改变反应历程又能降低活化能 |
D.其他条件一定,再通入适量 , , 和 和 的转化率都将增大 的转化率都将增大 |
您最近一年使用:0次
2024-02-29更新
|
85次组卷
|
2卷引用:四川省德阳市高中2023-2024学年学年高二上学期期末教学质量检测考试化学试题
名校
解题方法
8 . 下列化学理论、化工生产或实验事实引出的结论不正确的是
| 选项 | 事实 | 结论 |
| A | 化学反应的历程一般为:普通反应物分子 活化分子 活化分子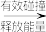 产物分子 产物分子 | 普通分子吸收能量转化为活化分子,活化分子间有适当的取向时,才能发生有效碰撞,生成产物分子 |
| B | 把Ba(OH)2•8H2O晶体与氯化铵晶体放入烧杯,用玻璃棒快速搅拌,烧杯变凉 | 反应物的总能量低于生成物的总能量 |
| C | 2NO(g)+2CO(g)=N2(g)+2CO2(g)反应△S<0,但是此反应可以自发进行 | 要判断反应自发进行的方向,必须综合考虑反应体系的焓变和熵变 |
| D | 在2L的密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g),把密闭容器的容积改为1L,重新发生该反应 2NH3(g),把密闭容器的容积改为1L,重新发生该反应 | 化学反应速率减慢 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-29更新
|
64次组卷
|
2卷引用:湖北省武汉市新洲区第一中学2024届高二上学期期末联考化学试题
名校
解题方法
9 . 下列说法正确的是
| A.凡是放热反应都是自发的,因为吸热反应都是非自发的 |
| B.自发反应的熵一定增大,非自发反应的熵一定减小 |
C.反应 能自发进行,则该反应的 能自发进行,则该反应的 |
D.常温下,反应 不能自发进行,则该反应的 不能自发进行,则该反应的 |
您最近一年使用:0次
名校
解题方法
10 . 某MOFs多孔材料孔径大小和形状恰好将N2O4固定,能高选择性吸附NO2。废气中NO2被吸附后,经处理能全部转化为HNO3。原理示意图如下。
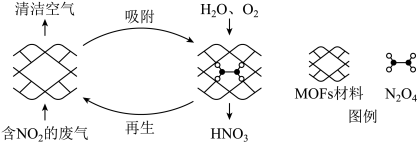
下列说法正确的是

下列说法正确的是
| A.每获得0.4molHNO3时,消耗的NO2的体积为8.96L |
| B.催化剂能加快反应速率,且能提高NO2的平衡转化率 |
| C.由NO2转化为N2O4的反应是一个熵增的反应 |
D.若反应 能自发,则说明该反应为放热反应 能自发,则说明该反应为放热反应 |
您最近一年使用:0次



