解题方法
1 . 高砷烟尘(主要成分有 、PbO、
、PbO、 、ZnO、
、ZnO、 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 和金属铟的工业流程如下:
和金属铟的工业流程如下: 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;
② 在90℃~95℃易分解为
在90℃~95℃易分解为 ,
, 难溶于水;
难溶于水;
③ 。
。
回答下列问题:
(1)“高压酸浸”时,As的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过 时,As的浸出率随硫酸浓度增大而略微减小的原因可能为
时,As的浸出率随硫酸浓度增大而略微减小的原因可能为________ ,滤渣的主要成分为________ (填化学式)。 ,发生反应的离子方程式为
,发生反应的离子方程式为________ 。已知 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为
 ,
, 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
________ 。
(3)“还原”后溶液酸性增强,主要原因是________ (用离子方程式表示)。
(4)“结晶”操作为________ 、过滤、洗涤、干燥。
(5)“萃余液”中含有的金属阳离子为________ (填离子符号),将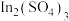 溶液电解得到金属钢,阴极的电极反应式为
溶液电解得到金属钢,阴极的电极反应式为________ 。
 、PbO、
、PbO、 、ZnO、
、ZnO、 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 和金属铟的工业流程如下:
和金属铟的工业流程如下:
 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;②
 在90℃~95℃易分解为
在90℃~95℃易分解为 ,
, 难溶于水;
难溶于水;③
 。
。回答下列问题:
(1)“高压酸浸”时,As的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过
 时,As的浸出率随硫酸浓度增大而略微减小的原因可能为
时,As的浸出率随硫酸浓度增大而略微减小的原因可能为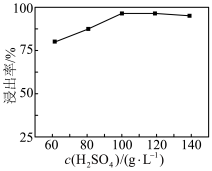
 ,发生反应的离子方程式为
,发生反应的离子方程式为 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为
 ,
, 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
(3)“还原”后溶液酸性增强,主要原因是
(4)“结晶”操作为
(5)“萃余液”中含有的金属阳离子为
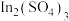 溶液电解得到金属钢,阴极的电极反应式为
溶液电解得到金属钢,阴极的电极反应式为
您最近一年使用:0次
2024-06-01更新
|
85次组卷
|
2卷引用:2024届陕西省安康市安康市高新中学,安康中学高新分校高三下学期模拟预测理综试题-高中化学
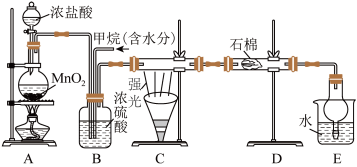
2 . 美国宇航局科学家确认火星大气中存在甲烷气体,可能来自火星火山活动或者生命活动,这一发现将为寻找火星生命带来希望。某课外活动小组利用如图所示装置探究烃类物质的性质,根据题意,回答下列问题:
Ⅰ.烷烃可以发生取代反应。向下图的A制取氯气,并向B中通入一定量的甲烷气体,于C处用强光照射硬质玻璃管。______ 。
(2)B有三种功能:①控制气流速度;②混匀混合气体;③______ 。
(3)写出装置C中 与
与 反应生成氯仿的化学方程式
反应生成氯仿的化学方程式____________ 。
(4)装置D的石棉浸有足量 溶液,装置E中盛有
溶液,装置E中盛有 溶液,均用于除去尾气中的
溶液,均用于除去尾气中的 、
、 等,其中E中倒置球形干燥管的作用是
等,其中E中倒置球形干燥管的作用是______ 。
(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为______(选填编号)。
(6)有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法______ (填“正确”或“不正确”),理由是______ 。
(7)实验中生成的油状液滴中的氯仿可作局部麻醉剂,常因保存不慎而被空气氧化,产生剧毒气体——光气,反应的化学方程式为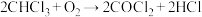 。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是
。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是______ 。
A.氢氧化钠溶液 B.硝酸银溶液 C.稀盐酸 D.水
E.湿润的蓝色石蕊试纸 F.湿润的无色酚酞试纸
Ⅱ.丙烯是三大合成材料的基本原料之一,其用量最大的是生产聚丙烯。
(8)丙烯能够使溴的四氯化碳溶液褪色,该反应的化学方程式为____________ 。
(9)聚丙烯(PP)可制成薄膜、包装材料等,丙烯在催化剂条件下合成聚丙烯的化学方程式是____________ 。
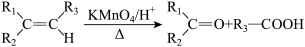
(10)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系:______ 。
Ⅰ.烷烃可以发生取代反应。向下图的A制取氯气,并向B中通入一定量的甲烷气体,于C处用强光照射硬质玻璃管。
(2)B有三种功能:①控制气流速度;②混匀混合气体;③
(3)写出装置C中
 与
与 反应生成氯仿的化学方程式
反应生成氯仿的化学方程式(4)装置D的石棉浸有足量
 溶液,装置E中盛有
溶液,装置E中盛有 溶液,均用于除去尾气中的
溶液,均用于除去尾气中的 、
、 等,其中E中倒置球形干燥管的作用是
等,其中E中倒置球形干燥管的作用是(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为______(选填编号)。
| A.结晶法 | B.蒸馏法 | C.萃取分液法 | D.水洗分液法 |
(6)有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法
(7)实验中生成的油状液滴中的氯仿可作局部麻醉剂,常因保存不慎而被空气氧化,产生剧毒气体——光气,反应的化学方程式为
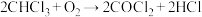 。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是
。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是A.氢氧化钠溶液 B.硝酸银溶液 C.稀盐酸 D.水
E.湿润的蓝色石蕊试纸 F.湿润的无色酚酞试纸
Ⅱ.丙烯是三大合成材料的基本原料之一,其用量最大的是生产聚丙烯。
(8)丙烯能够使溴的四氯化碳溶液褪色,该反应的化学方程式为
(9)聚丙烯(PP)可制成薄膜、包装材料等,丙烯在催化剂条件下合成聚丙烯的化学方程式是
(10)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系:
您最近一年使用:0次
解题方法
3 . 羰基钻催化剂可在温和条件下催化氢甲酰化反应,其结构为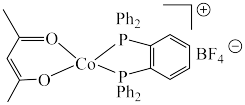 (Ph代表苯基)。回答下列问题:
(Ph代表苯基)。回答下列问题:
(2)羰基钴催化剂中位于第二周期的元素中,电负性由小到大的顺序为
 的晶体类型相同,
的晶体类型相同, 的熔点高于羰基钴催化剂的原因是
的熔点高于羰基钴催化剂的原因是(3)羰基钴催化剂阳离子中Co处于平面四边形中心,羰基钴催化剂中采取
 杂化的元素种数为
杂化的元素种数为 形成羰基钴催化剂过程中,
形成羰基钴催化剂过程中,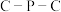 键角
键角(4)一种掺Co催化剂的晶胞结构及晶胞沿面对角线投影如下图所示。晶胞中与Co最近的氧原子所构成的几何形状为
 ,晶体的密度为
,晶体的密度为 ,则距离最近的两个氧原子间的距离为
,则距离最近的两个氧原子间的距离为 、
、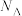 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-06-01更新
|
81次组卷
|
2卷引用:2024届陕西省安康市安康市高新中学,安康中学高新分校高三下学期模拟预测理综试题-高中化学
名校
解题方法
4 . 亚硝酸钙 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。 溶液能将NO氧化为
溶液能将NO氧化为 。
。
回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通 ,其目的是
,其目的是________ 。通 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是________ 。
(2)仪器a的名称为________ ,装置D中盛装的试剂是________ (填名称),装置E的作用是________ 。
(3)制备的产品 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为________ ,样品中 的纯度为
的纯度为________ (用含m、V的式子表示)。
 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。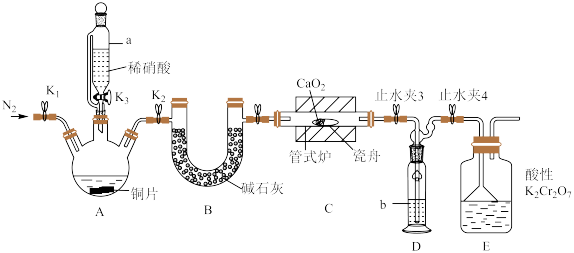
 溶液能将NO氧化为
溶液能将NO氧化为 。
。回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通
 ,其目的是
,其目的是 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是(2)仪器a的名称为
(3)制备的产品
 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: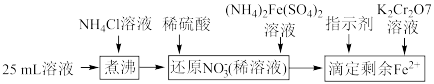
 ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为 的纯度为
的纯度为
您最近一年使用:0次
2024-06-01更新
|
297次组卷
|
7卷引用:2024届陕西省安康市安康市高新中学,安康中学高新分校高三下学期模拟预测理综试题-高中化学
解题方法
5 . 下列仪器在相应实验中选用合理的是

| A.蒸馏海水:①②③⑤ |
| B.实验室分离碘单质和氯化钠的混合物:③⑦ |
C.用碳酸钠和稀硫酸制备 :⑥ :⑥ |
D.用酸性高锰酸钾标准溶液测定溶液中 含量:④⑤ 含量:④⑤ |
您最近一年使用:0次
2024-06-01更新
|
36次组卷
|
2卷引用:2024届陕西省安康市安康市高新中学,安康中学高新分校高三下学期模拟预测理综试题-高中化学
6 . 科教兴国,我国科技发展在多个领域获得突破。下列说法错误的是
| A.新能源甲醇燃料电池汽车在行驶时其能量的转化形式:电能→化学能 |
| B.新一代航空发动机陶瓷基复合材料:具有耐高温、耐腐蚀特性 |
| C.利用高纯硅可以制成通信设备的芯片:高纯硅是广泛的半导体材料 |
| D.火焰喷雾技术制备纳米材料:在高温火焰喷雾中形成的胶体属于气溶胶 |
您最近一年使用:0次
2024-06-01更新
|
179次组卷
|
2卷引用:2024届陕西省安康市安康市高新中学,安康中学高新分校高三下学期模拟预测理综试题-高中化学
名校
7 . 一种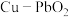 双极膜电池可长时间工作,其工作原理如图所示。已知双极膜中间层中的
双极膜电池可长时间工作,其工作原理如图所示。已知双极膜中间层中的 解离为
解离为 和
和 。下列说法错误的是
。下列说法错误的是
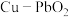 双极膜电池可长时间工作,其工作原理如图所示。已知双极膜中间层中的
双极膜电池可长时间工作,其工作原理如图所示。已知双极膜中间层中的 解离为
解离为 和
和 。下列说法错误的是
。下列说法错误的是
A.电极电势: 电极 电极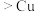 电极 电极 |
B.双极膜中 解离出的 解离出的 透过膜q向Cu电极移动 透过膜q向Cu电极移动 |
C.Cu电极的电极反应式为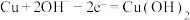 |
| D.双极膜中质量每减少18g,左侧溶液中硫酸质量减少98g |
您最近一年使用:0次
2024-06-01更新
|
204次组卷
|
7卷引用:2024届陕西省安康市安康市高新中学,安康中学高新分校高三下学期模拟预测理综试题-高中化学
解题方法
8 .  -呋喃丙烯酸是一种重要的有机酸,其实验室制备原理如下:
-呋喃丙烯酸是一种重要的有机酸,其实验室制备原理如下: -呋喃丙烯酸的步骤如下:向三颈烧瓶中依次加入丙二酸、糠醛和吡啶,在95℃下回流2小时,停止反应;将混合物倒入装有100mL蒸馏水的烧杯中,加入固体碳酸钠中和至弱碱性,加入活性炭后煮沸5~10min脱色,趁热过滤;滤液在冰水浴中边搅拌边滴加浓盐酸至不再有沉淀生成,抽滤,用冷水洗涤2~3次,得到粗产品。实验装置如图所示。
-呋喃丙烯酸的步骤如下:向三颈烧瓶中依次加入丙二酸、糠醛和吡啶,在95℃下回流2小时,停止反应;将混合物倒入装有100mL蒸馏水的烧杯中,加入固体碳酸钠中和至弱碱性,加入活性炭后煮沸5~10min脱色,趁热过滤;滤液在冰水浴中边搅拌边滴加浓盐酸至不再有沉淀生成,抽滤,用冷水洗涤2~3次,得到粗产品。实验装置如图所示。___________ 。
(2)与酒精灯加热相比,使用油浴加热的优点是___________ 。
(3)三颈烧瓶中反应已完成的标志是___________ 。
(4)分离出晶体时需减压抽滤,装置如图所示,抽滤的优点是___________ 。
称取mg -呋喃丙烯酸样品,加入1∶1的乙醇水溶液中,滴入2~3滴酚酞作指示剂,用浓度为
-呋喃丙烯酸样品,加入1∶1的乙醇水溶液中,滴入2~3滴酚酞作指示剂,用浓度为 的氢氧化钠标准溶液滴定至终点,做3组平行实验,所消耗NaOH溶液的平均体积为VmL。
的氢氧化钠标准溶液滴定至终点,做3组平行实验,所消耗NaOH溶液的平均体积为VmL。
①滴定管需要用标准溶液润洗,润洗滴定管的具体操作为___________ 。
②产品的纯度是___________ (以质量分数表示)。
③下列操作会使测定结果偏大的是___________ (填标号)。
A.称量样品时,将样品放在托盘天平的右盘
B.加热回流阶段,油浴时没有搅拌,出现焦化现象
C.滴定过程中,读数时,滴定前仰视,滴定后俯视
D.滴定前,尖嘴管有气泡,滴定后无气泡
 -呋喃丙烯酸是一种重要的有机酸,其实验室制备原理如下:
-呋喃丙烯酸是一种重要的有机酸,其实验室制备原理如下: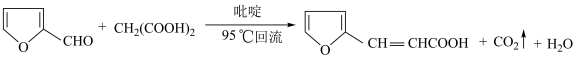
 -呋喃丙烯酸的步骤如下:向三颈烧瓶中依次加入丙二酸、糠醛和吡啶,在95℃下回流2小时,停止反应;将混合物倒入装有100mL蒸馏水的烧杯中,加入固体碳酸钠中和至弱碱性,加入活性炭后煮沸5~10min脱色,趁热过滤;滤液在冰水浴中边搅拌边滴加浓盐酸至不再有沉淀生成,抽滤,用冷水洗涤2~3次,得到粗产品。实验装置如图所示。
-呋喃丙烯酸的步骤如下:向三颈烧瓶中依次加入丙二酸、糠醛和吡啶,在95℃下回流2小时,停止反应;将混合物倒入装有100mL蒸馏水的烧杯中,加入固体碳酸钠中和至弱碱性,加入活性炭后煮沸5~10min脱色,趁热过滤;滤液在冰水浴中边搅拌边滴加浓盐酸至不再有沉淀生成,抽滤,用冷水洗涤2~3次,得到粗产品。实验装置如图所示。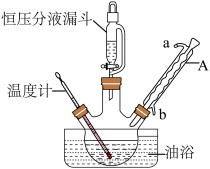
(2)与酒精灯加热相比,使用油浴加热的优点是
(3)三颈烧瓶中反应已完成的标志是
(4)分离出晶体时需减压抽滤,装置如图所示,抽滤的优点是
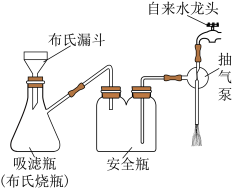
称取mg
 -呋喃丙烯酸样品,加入1∶1的乙醇水溶液中,滴入2~3滴酚酞作指示剂,用浓度为
-呋喃丙烯酸样品,加入1∶1的乙醇水溶液中,滴入2~3滴酚酞作指示剂,用浓度为 的氢氧化钠标准溶液滴定至终点,做3组平行实验,所消耗NaOH溶液的平均体积为VmL。
的氢氧化钠标准溶液滴定至终点,做3组平行实验,所消耗NaOH溶液的平均体积为VmL。①滴定管需要用标准溶液润洗,润洗滴定管的具体操作为
②产品的纯度是
③下列操作会使测定结果偏大的是
A.称量样品时,将样品放在托盘天平的右盘
B.加热回流阶段,油浴时没有搅拌,出现焦化现象
C.滴定过程中,读数时,滴定前仰视,滴定后俯视
D.滴定前,尖嘴管有气泡,滴定后无气泡
您最近一年使用:0次
2024-06-01更新
|
148次组卷
|
3卷引用:2024届陕西省商洛市高三下学期第五次模拟检测理综试题-高中化学
名校
解题方法
9 . CuCl为白色固体,难溶于水和乙醇,潮湿时易被氧化,常用作催化剂、杀菌剂、媒染剂、脱色剂。以废弃铁铜合金为原料制备CuCl的流程如图所示: ;②常温下,
;②常温下, 。
。
请回答下列问题:
(1)用再生液“浸取”铁铜合金不需要额外加热的原因可能为________ ;该阶段被氧化的铜元素与被还原的铜元素的质量之比为________ 。
(2)“氧化”阶段中最适宜的投料比为________ (填字母)。
a. b.
b. c.
c. d.
d.
(3)“中和”阶段的离子方程式为________ 。
(4)为了防止CuCl被氧化,上述流程中采取的两个措施是________ 。
(5)“中和”阶段会有部分铜元素被氧化。为了综合利用滤渣Fe和滤液,以提高CuCl的产率,试简述其方案:________ 。
(6)常温下, 在配体L的水溶液中形成
在配体L的水溶液中形成 ,其反应的平衡常数为K,
,其反应的平衡常数为K, 的平衡常数为
的平衡常数为________ (用含K的代数式表示)。
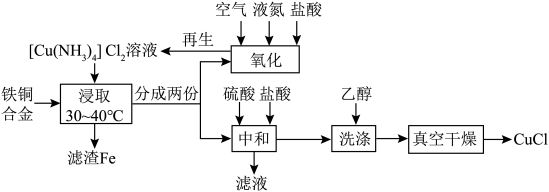
 ;②常温下,
;②常温下, 。
。请回答下列问题:
(1)用再生液“浸取”铁铜合金不需要额外加热的原因可能为
(2)“氧化”阶段中最适宜的投料比为
a.
 b.
b. c.
c. d.
d.
(3)“中和”阶段的离子方程式为
(4)为了防止CuCl被氧化,上述流程中采取的两个措施是
(5)“中和”阶段会有部分铜元素被氧化。为了综合利用滤渣Fe和滤液,以提高CuCl的产率,试简述其方案:
(6)常温下,
 在配体L的水溶液中形成
在配体L的水溶液中形成 ,其反应的平衡常数为K,
,其反应的平衡常数为K, 的平衡常数为
的平衡常数为
您最近一年使用:0次
2024-06-01更新
|
101次组卷
|
2卷引用:陕西省西安市第一中学2023-2024学年高三下学期4月二模考试化学试题
解题方法
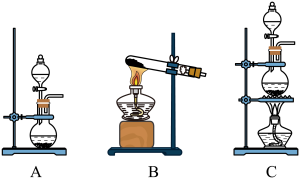
10 . 探究是创新的源泉,某化学兴趣小组进行了制备氯气并探究卤素性质的实验。
(1)用二氧化锰与浓盐酸制备氯气,应选择的发生装置是_______ (填字母代号),该反应体现了浓盐酸的酸性和_______ (填“氧化性”或“还原性”)。
①甲中反应的离子方程式为_______ ,向反应后的橙黄色溶液中滴加 KI-淀粉溶液,溶液变为蓝色,通过上述实验_______ (填“能”或“不能”)得出氧化性:Cl2>Br2>I2。
②乙装置中 NaOH 溶液的作用为_______ ,其主要反应的化学方程式为_______ 。
(1)用二氧化锰与浓盐酸制备氯气,应选择的发生装置是
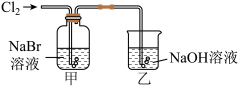
①甲中反应的离子方程式为
②乙装置中 NaOH 溶液的作用为
您最近一年使用:0次



