1 . 硅单质及其化合物应用广泛。请回答下列问题:
(1)硅元素在元素周期表的位置是_______ 。
(2)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:_______ 。
该生产过程中可以循环使用的物质是_______ 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式_______ 。
(3)新型陶瓷材料氮化硅(Si3N4)可应用于原子反应堆,一种制备氮化硅的反应如下:
3SiO2+6C+2N2 Si3N4+6CO。若消耗24g C时,反应过程中转移的电子为
Si3N4+6CO。若消耗24g C时,反应过程中转移的电子为_______ mol。
(4)实验室装氢氧化钠溶液的玻璃试剂瓶,不选择玻璃塞,请用化学方程式表明原因:_______ 。
(1)硅元素在元素周期表的位置是
(2)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:
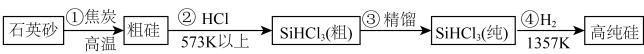
该生产过程中可以循环使用的物质是
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式
(3)新型陶瓷材料氮化硅(Si3N4)可应用于原子反应堆,一种制备氮化硅的反应如下:
3SiO2+6C+2N2
 Si3N4+6CO。若消耗24g C时,反应过程中转移的电子为
Si3N4+6CO。若消耗24g C时,反应过程中转移的电子为(4)实验室装氢氧化钠溶液的玻璃试剂瓶,不选择玻璃塞,请用化学方程式表明原因:
您最近一年使用:0次
2 . I.完成下列问题。
(1)烃A的结构简式为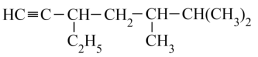 ,用系统命名法命名烃A:
,用系统命名法命名烃A:___________ 。
(2) 中含有的官能团的名称为
中含有的官能团的名称为___________ 。
II. 2014年中国十大科技成果之一是:我国科学家成功实现甲烷在催化剂及无氧条件下,一步高效生产乙烯、芳烃和氢气等化学品,为天然气化工开发了一条革命性技术。以甲烷为原料合成部分化工产品流程如图(部分反应条件已略去):___________ ;
(4)反应⑦的化学反应类型为___________ ;
(5)写出下列反应的化学方程式(注明反应条件):
反应⑥为___________ 。
反应⑨为___________ ;
(6) 有多种同分异构体,其中一种同分异构体中不同化学环境的氢原子数目比3:1:1,写出该同分异构体的结构简式:
有多种同分异构体,其中一种同分异构体中不同化学环境的氢原子数目比3:1:1,写出该同分异构体的结构简式:___________ ;
(1)烃A的结构简式为
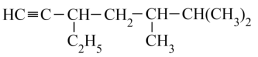 ,用系统命名法命名烃A:
,用系统命名法命名烃A:(2)
 中含有的官能团的名称为
中含有的官能团的名称为II. 2014年中国十大科技成果之一是:我国科学家成功实现甲烷在催化剂及无氧条件下,一步高效生产乙烯、芳烃和氢气等化学品,为天然气化工开发了一条革命性技术。以甲烷为原料合成部分化工产品流程如图(部分反应条件已略去):

(4)反应⑦的化学反应类型为
(5)写出下列反应的化学方程式(注明反应条件):
反应⑥为
反应⑨为
(6)
 有多种同分异构体,其中一种同分异构体中不同化学环境的氢原子数目比3:1:1,写出该同分异构体的结构简式:
有多种同分异构体,其中一种同分异构体中不同化学环境的氢原子数目比3:1:1,写出该同分异构体的结构简式:
您最近一年使用:0次
名校
解题方法
3 . 回答下列问题:
I.下表中的数据是破坏1 物质中的化学键所消耗的能量,回答下列问题
物质中的化学键所消耗的能量,回答下列问题
(1)下列氢化物中最稳定的是___________ (填标号)。
A.HCl B.HBr C.HI
(2)按照反应I2+H2=2HI,生成2 mol HI___________ (填“吸收”或“放出”)的热量为___________ kJ。
(3)某化学反应过程能量变化如图所示,该化学反应可能是___________(填标号)
II.某温度时,在一个2 L的密闭容器中, A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据回答下列问题:___________ ;
(5)从开始至2min末,A的平均反应速率为___________ ;
(6)2min时反应达到平衡,容器内混合气体的平均相对分子质量比起始时___________ (填“大”,“小”或“相等”,下同),混合气体密度比起始时___________ 。
(7)在某一时刻采取下列措施能使该反应速率减小的是___________(填标号)。
I.下表中的数据是破坏1
 物质中的化学键所消耗的能量,回答下列问题
物质中的化学键所消耗的能量,回答下列问题| 物质 |  |  |  |  |  |  |  |
| 键能/kJ | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
(1)下列氢化物中最稳定的是
A.HCl B.HBr C.HI
(2)按照反应I2+H2=2HI,生成2 mol HI
(3)某化学反应过程能量变化如图所示,该化学反应可能是___________(填标号)

| A.NaOH+HCl=NaCl+H2O |
| B.Fe+H2SO4=FeSO4+H2↑ |
| C.2Na2O2+2H2O=4NaOH+O2↑ |
| D.Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O |
II.某温度时,在一个2 L的密闭容器中, A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据回答下列问题:
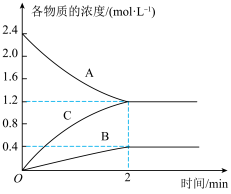
(5)从开始至2min末,A的平均反应速率为
(6)2min时反应达到平衡,容器内混合气体的平均相对分子质量比起始时
(7)在某一时刻采取下列措施能使该反应速率减小的是___________(填标号)。
| A.加催化剂 | B.降低温度 |
| C.容积不变,充入A | D.容积不变,从容器中分离出A |
您最近一年使用:0次
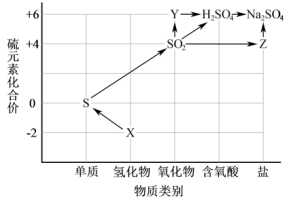
4 . 不同价态含硫物质间的转化是自然界硫循环的物质基础。下图是硫及其部分化合物的“价类二维图”及相互转化关系。
1.斜方硫和单斜硫是两种不同的硫单质,它们的关系是_____。
2.写出上图中物质的化学式:X_____ ;Y_____ 。
3.写出 转化为Y的化学方程式
转化为Y的化学方程式_____ 。
4.已知Z为正盐,根据图中转化关系可知Z的化学式为_____ ;检验Z是否变质的方法是_____ 。
1.斜方硫和单斜硫是两种不同的硫单质,它们的关系是_____。
| A.同位素 | B.同素异形体 | C.同分异构体 | D.同系物 |
3.写出
 转化为Y的化学方程式
转化为Y的化学方程式4.已知Z为正盐,根据图中转化关系可知Z的化学式为
您最近一年使用:0次
名校
5 . 回答下列问题。
Ⅰ:为有效降低含氮化物的排放量,又能充分利用化学能,合作小组利用反应 设计如图所示电池(离子交换膜对溶液里的离子具有选择透过能力)。
设计如图所示电池(离子交换膜对溶液里的离子具有选择透过能力)。_______ (填正极或负极),电子的移动方向:_______ 经负载至_______ (填电极A或电极B)
(2)负极的电极反应为:_______ 。
(3)同温同压时,左右两侧电极室中产生的气体体积比为_______ 。
Ⅱ:原电池装置如图所示,回答下列问题。_______ 。
(5)浸有饱和KCl溶液的滤纸条的作用是什么:_______ 。
(6)滤纸条中K+移向_______ ,Cl-移向_______ (填甲池或者乙池)。
Ⅰ:为有效降低含氮化物的排放量,又能充分利用化学能,合作小组利用反应
 设计如图所示电池(离子交换膜对溶液里的离子具有选择透过能力)。
设计如图所示电池(离子交换膜对溶液里的离子具有选择透过能力)。
(2)负极的电极反应为:
(3)同温同压时,左右两侧电极室中产生的气体体积比为
Ⅱ:原电池装置如图所示,回答下列问题。
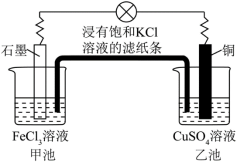
(5)浸有饱和KCl溶液的滤纸条的作用是什么:
(6)滤纸条中K+移向
您最近一年使用:0次
名校
6 . 化学电池的发明,是贮能和供能技术的巨大进步。
(1)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是___________ (填字母)。
A.锌锰电池工作一段时间后碳棒会变细
B.氢氧燃料电池可将化学能直接转变为电能
C.铅蓄电池负极是PbO2,正极是Pb
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。___________ (填“A”或“B”)电极入口通甲烷,其电极反应式为___________ 。工作一段时间后,电解质溶液的pH将___________ (填“变大”、“变小”或“不变”)。
(3)有人设想利用电化学原理除去SO2,并将化学能转化为电能。装置图如下。___________ 。(填“a”或“b”)
②写出a电极的电极反应___________ 。
(4)某同学欲把反应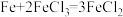 设计成原电池,请画出简易的原电池装置图
设计成原电池,请画出简易的原电池装置图________ 。
(1)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是
A.锌锰电池工作一段时间后碳棒会变细
B.氢氧燃料电池可将化学能直接转变为电能
C.铅蓄电池负极是PbO2,正极是Pb
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
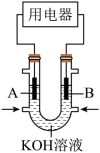
(3)有人设想利用电化学原理除去SO2,并将化学能转化为电能。装置图如下。

②写出a电极的电极反应
(4)某同学欲把反应
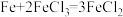 设计成原电池,请画出简易的原电池装置图
设计成原电池,请画出简易的原电池装置图
您最近一年使用:0次
名校
解题方法
7 . 处理工业废气中的氮氧化物NOx对于环境保护具有重要的意义。
(1)催化还原法。NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:_______ 。
②用Fe做催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图2所示,脱氮效果最佳的c(NO2)/c(NO)=______ 。按最佳脱氮率,每生成2molN2,转移电子数目为_______ 。
(2)可用NaClO2将氮氧化物转化成NO ,碱性条件下NaClO2去除NO反应的离子方程式为
,碱性条件下NaClO2去除NO反应的离子方程式为_______ 。
(3)对NO和NO2脱除后产生的含NO 溶液可用如图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为
溶液可用如图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为_______ 。
(1)催化还原法。NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:

②用Fe做催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图2所示,脱氮效果最佳的c(NO2)/c(NO)=
(2)可用NaClO2将氮氧化物转化成NO
 ,碱性条件下NaClO2去除NO反应的离子方程式为
,碱性条件下NaClO2去除NO反应的离子方程式为(3)对NO和NO2脱除后产生的含NO
 溶液可用如图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为
溶液可用如图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为
您最近一年使用:0次
解题方法
8 . 氯碱工业的生产原理是_____ (写化学方程式)。检验阳极产物的方法是_____ 。
您最近一年使用:0次
名校
解题方法
9 . 请用所学知识填空。
(1)相对分子质量为128的烷烃习惯性命名为:_______ 。
(2)硝酸是重要的化工原料,下图为合成氨以及氨氧化制硝酸的流程图,请结合你所学的知识回答以下问题:_______ (填序号)。
b.②反应的化学方程式为_______ 。
(3)①若A、B电极材料分别为铜和锌,溶液C为稀硫酸溶液,电流表指针发生偏转,则B电极上发生的电极反应为_______ 。
②若A、B电极材料分别为铜和银,溶液C为氯化铁溶液,则B电极上发生的电极反应为_______ ;若有0.2mol电子通过导线,则负极减轻_______ g。
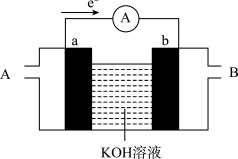
(4)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。_______ (填“A”或“B”)口通入。假设使用的“燃料”是H2,a极的电极反应式为_______ 。
(1)相对分子质量为128的烷烃习惯性命名为:
(2)硝酸是重要的化工原料,下图为合成氨以及氨氧化制硝酸的流程图,请结合你所学的知识回答以下问题:
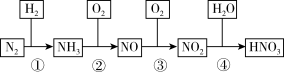
b.②反应的化学方程式为
(3)①若A、B电极材料分别为铜和锌,溶液C为稀硫酸溶液,电流表指针发生偏转,则B电极上发生的电极反应为
②若A、B电极材料分别为铜和银,溶液C为氯化铁溶液,则B电极上发生的电极反应为
(4)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.300℃时,向2L的恒容密闭容器中,充入等物质的量的 和
和 使之发生反应
使之发生反应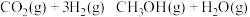 ,测得各物质的量浓度变化如图所示:
,测得各物质的量浓度变化如图所示: 的浓度随时间的变化为曲线
的浓度随时间的变化为曲线_____ (填“a”“b”或“c”);2min内的平均反应速率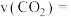
_____ 。
(2)已知:反应至2min时,改变了某一反应条件。2min时改变的条件可能为:_____。
(3)能说明上述反应达到平衡状态的是_____ (填字母)。
a.
b.混合气体的密度不随时间的变化而变化
c.
d.混合气体的平均摩尔质量不随时间的变化而变化
(4)5min时,容器内气体总压强与反应前容器内气体总压强之比为_____ 。
Ⅱ.向两个容积固定为2L的密闭容器中分别充入比例相同,但总量不同的 和
和 气体,
气体, 的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如图所示。
的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如图所示。_____ (选填“吸热”或“放热”)反应,
(6)判断图中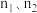 相对大小:
相对大小: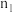 *
*_____ * 。(选填“<”或“>”)
。(选填“<”或“>”)
 和
和 使之发生反应
使之发生反应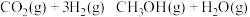 ,测得各物质的量浓度变化如图所示:
,测得各物质的量浓度变化如图所示:
 的浓度随时间的变化为曲线
的浓度随时间的变化为曲线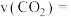
(2)已知:反应至2min时,改变了某一反应条件。2min时改变的条件可能为:_____。
| A.升高温度 | B.加催化剂 |
| C.减小容器体积,增大压强 | D.增大反应物浓度 |
(3)能说明上述反应达到平衡状态的是
a.

b.混合气体的密度不随时间的变化而变化
c.

d.混合气体的平均摩尔质量不随时间的变化而变化
(4)5min时,容器内气体总压强与反应前容器内气体总压强之比为
Ⅱ.向两个容积固定为2L的密闭容器中分别充入比例相同,但总量不同的
 和
和 气体,
气体, 的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如图所示。
的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如图所示。
(6)判断图中
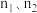 相对大小:
相对大小: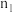 *
* 。(选填“<”或“>”)
。(选填“<”或“>”)
您最近一年使用:0次



