1 . 镍及其化合物在工业上有广泛的应用。工业上用镍矿渣(主要含 、NiS,还含FeO、
、NiS,还含FeO、 、MgO、CaO和
、MgO、CaO和 )制备
)制备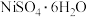 的过程如图所示(已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表)。
的过程如图所示(已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表)。

(1) 的价电子排布式为
的价电子排布式为_______ ;电离一个电子需要吸收的能量
_______________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
(2)“酸溶”过程中,NiS发生反应的离子方程式为_________________________ ;如何判断 已足量:
已足量:______________________ (写出具体操作过程)。
(3)滤渣1的成分有_______________ 。
(4)滤渣3的成分为 和
和 。若滤液1中
。若滤液1中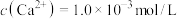 ,当滤液2中
,当滤液2中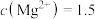
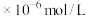 时,除钙率为
时,除钙率为_______________ (忽略沉淀前后溶液体积变化)。(已知: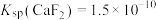 、
、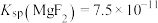 )
)
(5)“滤液2”加入碳酸钠溶液后所得沉淀可表示为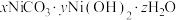 。进行下列实验:称取干燥沉淀样品3.41g,隔绝空气加热,剩余固体质量随温度变化的曲线如图所示(500℃~750℃条件下加热,收集到的气体产物只有一种,750℃以上残留固体为NiO),则该样品的化学式为
。进行下列实验:称取干燥沉淀样品3.41g,隔绝空气加热,剩余固体质量随温度变化的曲线如图所示(500℃~750℃条件下加热,收集到的气体产物只有一种,750℃以上残留固体为NiO),则该样品的化学式为_________________ 。

(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。由 溶液获得稳定的
溶液获得稳定的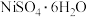 晶体的操作M依次是蒸发浓缩、
晶体的操作M依次是蒸发浓缩、_______________ 、过滤、洗涤、干燥。
 、NiS,还含FeO、
、NiS,还含FeO、 、MgO、CaO和
、MgO、CaO和 )制备
)制备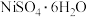 的过程如图所示(已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表)。
的过程如图所示(已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表)。
金属离子 |
|
|
|
|
开始沉淀时的pH | 6.8 | 2.2 | 7.5 | 9.4 |
沉淀完全时的pH | 9.2 | 3.2 | 9.0 | 12.4 |
 的价电子排布式为
的价电子排布式为
 (填“大于”或“小于”)。
(填“大于”或“小于”)。(2)“酸溶”过程中,NiS发生反应的离子方程式为
 已足量:
已足量:(3)滤渣1的成分有
(4)滤渣3的成分为
 和
和 。若滤液1中
。若滤液1中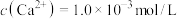 ,当滤液2中
,当滤液2中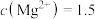
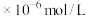 时,除钙率为
时,除钙率为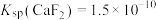 、
、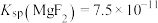 )
)(5)“滤液2”加入碳酸钠溶液后所得沉淀可表示为
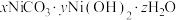 。进行下列实验:称取干燥沉淀样品3.41g,隔绝空气加热,剩余固体质量随温度变化的曲线如图所示(500℃~750℃条件下加热,收集到的气体产物只有一种,750℃以上残留固体为NiO),则该样品的化学式为
。进行下列实验:称取干燥沉淀样品3.41g,隔绝空气加热,剩余固体质量随温度变化的曲线如图所示(500℃~750℃条件下加热,收集到的气体产物只有一种,750℃以上残留固体为NiO),则该样品的化学式为
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。由
 溶液获得稳定的
溶液获得稳定的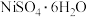 晶体的操作M依次是蒸发浓缩、
晶体的操作M依次是蒸发浓缩、温度 | 低于30.8℃ | 30.8℃~53.8℃ | 53.8℃~280℃ | 280℃ |
晶体形态 |
|
| 多种结晶水合物 |
|
您最近一年使用:0次
名校
解题方法
2 . 已知硫酸亚铁铵[ ](俗称莫尔盐)可溶于水,在
](俗称莫尔盐)可溶于水,在 时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
Ⅰ. 探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验。装置C中可观察到的现象是_______ ,由此可知分解产物中有_______ (填化学式)。
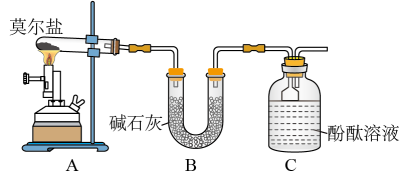
(2)乙同学认为莫尔盐晶体分解的产物中还可能含有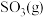 、
、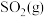 及
及 。为验证产物的存在,用下列装置进行实验。
。为验证产物的存在,用下列装置进行实验。
①乙同学的实验中,装置依次连按的合理顺序为:A→H→→→→G。_______
②证明含有 的实验现象是
的实验现象是_______ 。
Ⅱ. 为测定硫酸亚铁铵纯度,称取mg莫尔盐样品,配成 溶液。甲、乙两位同学设计了如下两个实验方案。
溶液。甲、乙两位同学设计了如下两个实验方案。
甲方案:取 样品溶液用
样品溶液用 的酸性
的酸性 溶液分三次进行测定。
溶液分三次进行测定。
乙方案(通过 测定):实验设计装置如图所示。取
测定):实验设计装置如图所示。取 样品溶液进行该实验。
样品溶液进行该实验。
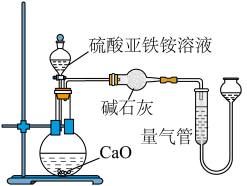
请回答:
(3)乙方案中量气管中最佳试剂是_______ 。
a. 水 b. 饱和 溶液 c.
溶液 c.  d. 饱和
d. 饱和 溶液
溶液
(4)乙方案中收集完气体并恢复至室温,为了减小实验误差,读数前应进行的操作是_______ 。
(5)若测得 为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
为VL(已折算为标准状况下),则硫酸亚铁铵纯度为_______ (列出计算式)。
 ](俗称莫尔盐)可溶于水,在
](俗称莫尔盐)可溶于水,在 时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
时分解,其探究其化学性质,甲、乙两同学设计了如下实验。Ⅰ. 探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验。装置C中可观察到的现象是

(2)乙同学认为莫尔盐晶体分解的产物中还可能含有
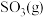 、
、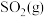 及
及 。为验证产物的存在,用下列装置进行实验。
。为验证产物的存在,用下列装置进行实验。 | 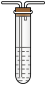 |  | 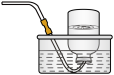 |  |
| D. 品红溶液 | E.  溶液 溶液 | F.  溶液和足量盐酸 溶液和足量盐酸 | G. 排水集气法 | H.安全瓶 |
②证明含有
 的实验现象是
的实验现象是Ⅱ. 为测定硫酸亚铁铵纯度,称取mg莫尔盐样品,配成
 溶液。甲、乙两位同学设计了如下两个实验方案。
溶液。甲、乙两位同学设计了如下两个实验方案。甲方案:取
 样品溶液用
样品溶液用 的酸性
的酸性 溶液分三次进行测定。
溶液分三次进行测定。乙方案(通过
 测定):实验设计装置如图所示。取
测定):实验设计装置如图所示。取 样品溶液进行该实验。
样品溶液进行该实验。
请回答:
(3)乙方案中量气管中最佳试剂是
a. 水 b. 饱和
 溶液 c.
溶液 c.  d. 饱和
d. 饱和 溶液
溶液(4)乙方案中收集完气体并恢复至室温,为了减小实验误差,读数前应进行的操作是
(5)若测得
 为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
您最近一年使用:0次
2023-01-21更新
|
769次组卷
|
3卷引用:山东省青岛第五十八中学2022-2023学年高一上学期期末考试化学试题
解题方法
3 . 草酸(H2C2O4)及其盐类化合物在化学工业中有重要作用。请回答下列问题:
(1)实验室中可以在 用浓硝酸在硝酸汞催化下氧化乙炔(C2H2)气体来制备草酸。其主要装置如图所示。
用浓硝酸在硝酸汞催化下氧化乙炔(C2H2)气体来制备草酸。其主要装置如图所示。
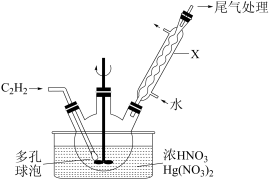
 的电子式为
的电子式为_______ ;仪器X的名称为_______ ;装置中浓硝酸的还原产物为 ,生成草酸的化学方程式为
,生成草酸的化学方程式为_______ ,若反应温度高于 ,生成草酸的速率会减慢,主要原因是
,生成草酸的速率会减慢,主要原因是_______ 。
(2)三草酸合铁酸钾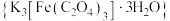 为绿色晶体,溶于水,难溶于乙醇,可作有机反应的催化剂。某实验小组用
为绿色晶体,溶于水,难溶于乙醇,可作有机反应的催化剂。某实验小组用 为原料制备三草酸合铁酸钾的步骤如下:
为原料制备三草酸合铁酸钾的步骤如下:
①称取 晶体,溶解,加硫酸酸化,边搅拌边加入
晶体,溶解,加硫酸酸化,边搅拌边加入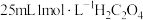 溶液,静置,析出黄色的
溶液,静置,析出黄色的 沉淀,过滤并洗涤沉淀
沉淀,过滤并洗涤沉淀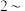 3次。
3次。
②将上述 沉淀溶解在
沉淀溶解在 饱和草酸钾溶液中,再加入
饱和草酸钾溶液中,再加入 饱和
饱和 溶液,保持溶液温度为
溶液,保持溶液温度为 ,缓慢滴加
,缓慢滴加 溶液,不断搅拌,沉淀慢慢变为深棕色;加热至沸腾
溶液,不断搅拌,沉淀慢慢变为深棕色;加热至沸腾 ,再加入
,再加入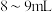 草酸溶液,控制
草酸溶液,控制 为
为 ,变为绿色透明的三草酸合铁酸钾溶液。
,变为绿色透明的三草酸合铁酸钾溶液。
③加热浓缩,缓慢加入95%的乙醇,冷却结晶、过滤,洗涤晶体 次,干燥、称量。
次,干燥、称量。
其中生成 的化学方程式为
的化学方程式为_______ ;保持溶液温度为 所采用的加热方式是
所采用的加热方式是_______ ,加热至沸腾 的目的是
的目的是_______ ;洗涤晶体所用试剂为_______ 。
(3)制得的三草酸合铁酸钾晶体中往往会混有少量草酸。为测定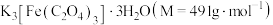 的纯度,进行如下实验:
的纯度,进行如下实验:
称取样品 ,加稀硫酸溶解后配成
,加稀硫酸溶解后配成 溶液。取
溶液。取 配制的溶液,用浓度为
配制的溶液,用浓度为 的
的 溶液滴定至终点时消耗
溶液滴定至终点时消耗 溶液
溶液 ,已知:
,已知: ,样品中
,样品中 的质量分数为
的质量分数为_______ (结果保留三位有效数字)。
(1)实验室中可以在
 用浓硝酸在硝酸汞催化下氧化乙炔(C2H2)气体来制备草酸。其主要装置如图所示。
用浓硝酸在硝酸汞催化下氧化乙炔(C2H2)气体来制备草酸。其主要装置如图所示。
 的电子式为
的电子式为 ,生成草酸的化学方程式为
,生成草酸的化学方程式为 ,生成草酸的速率会减慢,主要原因是
,生成草酸的速率会减慢,主要原因是(2)三草酸合铁酸钾
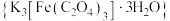 为绿色晶体,溶于水,难溶于乙醇,可作有机反应的催化剂。某实验小组用
为绿色晶体,溶于水,难溶于乙醇,可作有机反应的催化剂。某实验小组用 为原料制备三草酸合铁酸钾的步骤如下:
为原料制备三草酸合铁酸钾的步骤如下:①称取
 晶体,溶解,加硫酸酸化,边搅拌边加入
晶体,溶解,加硫酸酸化,边搅拌边加入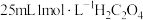 溶液,静置,析出黄色的
溶液,静置,析出黄色的 沉淀,过滤并洗涤沉淀
沉淀,过滤并洗涤沉淀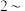 3次。
3次。②将上述
 沉淀溶解在
沉淀溶解在 饱和草酸钾溶液中,再加入
饱和草酸钾溶液中,再加入 饱和
饱和 溶液,保持溶液温度为
溶液,保持溶液温度为 ,缓慢滴加
,缓慢滴加 溶液,不断搅拌,沉淀慢慢变为深棕色;加热至沸腾
溶液,不断搅拌,沉淀慢慢变为深棕色;加热至沸腾 ,再加入
,再加入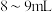 草酸溶液,控制
草酸溶液,控制 为
为 ,变为绿色透明的三草酸合铁酸钾溶液。
,变为绿色透明的三草酸合铁酸钾溶液。③加热浓缩,缓慢加入95%的乙醇,冷却结晶、过滤,洗涤晶体
 次,干燥、称量。
次,干燥、称量。其中生成
 的化学方程式为
的化学方程式为 所采用的加热方式是
所采用的加热方式是 的目的是
的目的是(3)制得的三草酸合铁酸钾晶体中往往会混有少量草酸。为测定
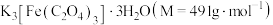 的纯度,进行如下实验:
的纯度,进行如下实验:称取样品
 ,加稀硫酸溶解后配成
,加稀硫酸溶解后配成 溶液。取
溶液。取 配制的溶液,用浓度为
配制的溶液,用浓度为 的
的 溶液滴定至终点时消耗
溶液滴定至终点时消耗 溶液
溶液 ,已知:
,已知: ,样品中
,样品中 的质量分数为
的质量分数为
您最近一年使用:0次
2023-01-20更新
|
446次组卷
|
4卷引用:超重点8 碳酸盐、草酸盐的创新考查
4 . 煤化学链技术具有成本低、能耗低的 捕集特性。以铁矿石(主要含铁物质为
捕集特性。以铁矿石(主要含铁物质为 )为载氧体的煤化学链制氢⼯艺如下图。测定反应前后不同价态铁的含量,对工艺优化和运行监测具有重要意义。
)为载氧体的煤化学链制氢⼯艺如下图。测定反应前后不同价态铁的含量,对工艺优化和运行监测具有重要意义。

(1)进入燃烧反应器前,铁矿石需要粉碎,煤需要烘干研磨,其目的是___________ 。
(2)分离燃烧反应器中产生的 (g)和
(g)和 ,可进行
,可进行 高纯捕集和封存,其分离方法是
高纯捕集和封存,其分离方法是___________ 。
(3)测定铁矿石中全部铁元素含量。
i.配制铁矿石待测液:铁矿石加酸溶解,向其中滴加氯化亚锡( )溶液。
)溶液。
ii.用重铬酸钾( )标准液滴定可测定样品中全部铁元素含量。配制铁矿石待测液时
)标准液滴定可测定样品中全部铁元素含量。配制铁矿石待测液时 溶液过量会对测定结果产生影响,分析影响结果及其原因
溶液过量会对测定结果产生影响,分析影响结果及其原因___________ 。
(4)测定燃烧反应后产物中单质铁含量:取a g样品,用 溶液充分浸取(FeO不溶于该溶液),向分离出的浸取液中滴加b
溶液充分浸取(FeO不溶于该溶液),向分离出的浸取液中滴加b
 溶标准液,消耗
溶标准液,消耗 标准液V mL。已知
标准液V mL。已知 被还原为
被还原为 ,样品中单质铁的质量分数为
,样品中单质铁的质量分数为___________ 。
(5)⼯艺中不同价态铁元素含量测定结果如下。
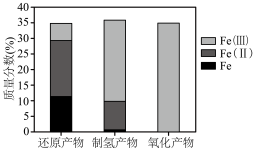
①制氢产物主要为 ,写出蒸汽反应器中发生反应的化学方程式
,写出蒸汽反应器中发生反应的化学方程式___________ 。
②⼯艺中可循环使用的物质是___________ (填化学式)。
 捕集特性。以铁矿石(主要含铁物质为
捕集特性。以铁矿石(主要含铁物质为 )为载氧体的煤化学链制氢⼯艺如下图。测定反应前后不同价态铁的含量,对工艺优化和运行监测具有重要意义。
)为载氧体的煤化学链制氢⼯艺如下图。测定反应前后不同价态铁的含量,对工艺优化和运行监测具有重要意义。
(1)进入燃烧反应器前,铁矿石需要粉碎,煤需要烘干研磨,其目的是
(2)分离燃烧反应器中产生的
 (g)和
(g)和 ,可进行
,可进行 高纯捕集和封存,其分离方法是
高纯捕集和封存,其分离方法是(3)测定铁矿石中全部铁元素含量。
i.配制铁矿石待测液:铁矿石加酸溶解,向其中滴加氯化亚锡(
 )溶液。
)溶液。ii.用重铬酸钾(
 )标准液滴定可测定样品中全部铁元素含量。配制铁矿石待测液时
)标准液滴定可测定样品中全部铁元素含量。配制铁矿石待测液时 溶液过量会对测定结果产生影响,分析影响结果及其原因
溶液过量会对测定结果产生影响,分析影响结果及其原因(4)测定燃烧反应后产物中单质铁含量:取a g样品,用
 溶液充分浸取(FeO不溶于该溶液),向分离出的浸取液中滴加b
溶液充分浸取(FeO不溶于该溶液),向分离出的浸取液中滴加b
 溶标准液,消耗
溶标准液,消耗 标准液V mL。已知
标准液V mL。已知 被还原为
被还原为 ,样品中单质铁的质量分数为
,样品中单质铁的质量分数为(5)⼯艺中不同价态铁元素含量测定结果如下。

①制氢产物主要为
 ,写出蒸汽反应器中发生反应的化学方程式
,写出蒸汽反应器中发生反应的化学方程式②⼯艺中可循环使用的物质是
您最近一年使用:0次
5 . KI可用作利尿剂、治疗慢性支气管炎,实验室中制备一定量KI的过程及实验装置(加热及夹持装置已省略)如右:

回答下列问题:
(1)仪器a的名称是___________ ,“碱溶”时,用水浴加热的优点是 ___________ 。
(2)“碱溶”时,碘发生歧化反应,氧化产物可用于加碘盐的生产中,则“碱溶”时氧化产物与还原产物的物质的量之比为___________ ,若“碱溶”时,KOH过量,通硫化氢时,写出“还原”时发生反应的离子方程式___________ 。
(3)烧杯中X不可以选用的试剂___________ 。(填标号)
a.NaOH b.CuSO4 c.KMnO4 d.硝酸
(4)为测定KI的纯度,称取0.5g 样品溶于水,然后用0. 0500mol·L-1的酸性KMnO4标准溶液滴定(10I- +2 +16H+ = 5I2+2Mn2+ +8H2O),判断滴定终点的现象是
+16H+ = 5I2+2Mn2+ +8H2O),判断滴定终点的现象是___________ , 若滴定终点时平均消耗11. 80mL标准溶液,则样品的纯度为___________ (保留两位有效数字),若滴定终点读数时仰视刻度线,则测定KI纯度的结果___________ (填 “偏大”或“偏小”)。
(5)某温度时,H2S溶液中H2S、HS-、S2-在含硫粒子总浓度中所占分数δ随溶液pH的变化关系如图,若FeS恰好溶解,溶液中的c(Fe2+)=0.1mol·L-1,c(H2S)=6.0×10-9mol·L-1,应控制溶液pH等于___________ (已知该温度时,FeS的Ksp为6.0×10-18)。


回答下列问题:
(1)仪器a的名称是
(2)“碱溶”时,碘发生歧化反应,氧化产物可用于加碘盐的生产中,则“碱溶”时氧化产物与还原产物的物质的量之比为
(3)烧杯中X不可以选用的试剂
a.NaOH b.CuSO4 c.KMnO4 d.硝酸
(4)为测定KI的纯度,称取0.5g 样品溶于水,然后用0. 0500mol·L-1的酸性KMnO4标准溶液滴定(10I- +2
 +16H+ = 5I2+2Mn2+ +8H2O),判断滴定终点的现象是
+16H+ = 5I2+2Mn2+ +8H2O),判断滴定终点的现象是(5)某温度时,H2S溶液中H2S、HS-、S2-在含硫粒子总浓度中所占分数δ随溶液pH的变化关系如图,若FeS恰好溶解,溶液中的c(Fe2+)=0.1mol·L-1,c(H2S)=6.0×10-9mol·L-1,应控制溶液pH等于

您最近一年使用:0次
名校
6 . 铁有两种氯化物,都是重要的化工试剂。查阅有关资料如下:
【氯化铁】熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
【氯化亚铁】熔点为670℃,易升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用下图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。
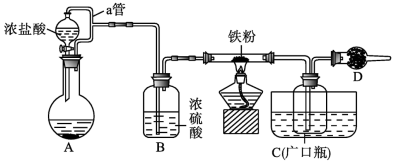
请回答下列问题。
(1)在装置A中,a管的作用是___________ ,用 与浓盐酸反应制取氯气的化学方程式为
与浓盐酸反应制取氯气的化学方程式为____________ 。
(2)仪器D的名称是___________ ,D中装的药品是碱石灰,其作用是___________ 。
(3)定量分析。取装置C中的产物,按以下步骤进行测定:①称取4.60 g产品溶于过量的稀盐酸中;②加入足量的氯水;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40 g。
则该样品中铁元素的质量分数为___________ %(保留一位小数)。
(4)用题中所给的装置制得的产品中会含有氯化亚铁杂质,从而导致铁元素含量___________ (填“相等”“偏高”或“偏低”)。为避免产生氯化亚铁杂质,对题中所给的装置提出一种合理的改进方法:_______________________________ 。
【氯化铁】熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
【氯化亚铁】熔点为670℃,易升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用下图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。

请回答下列问题。
(1)在装置A中,a管的作用是
 与浓盐酸反应制取氯气的化学方程式为
与浓盐酸反应制取氯气的化学方程式为(2)仪器D的名称是
(3)定量分析。取装置C中的产物,按以下步骤进行测定:①称取4.60 g产品溶于过量的稀盐酸中;②加入足量的氯水;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40 g。
则该样品中铁元素的质量分数为
(4)用题中所给的装置制得的产品中会含有氯化亚铁杂质,从而导致铁元素含量
您最近一年使用:0次
2023-01-15更新
|
118次组卷
|
2卷引用:河北省邢台市第一中学2022-2023学年高一上学期期末考试化学试题
解题方法
7 . 某煤化工厂废水含有大量有机物、氨氮、氰化物、悬浮颗粒等有害物质。处理流程如图所示。
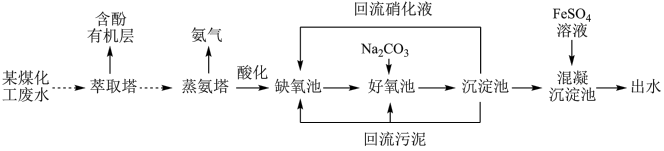
(1)萃取塔中经过_______ (填写操作名称)可将含酚有机层分离出来。
(2)蒸氨塔中需要连续加入碱液并保持较高温度。请从化学平衡角度解释回答下列问题。
①写出蒸氨塔中主要的化学平衡的离子方程式:_______ 。
②加入碱液以及保持较高温度的原因:_______ 。
(3)缺氧池中含有 及CN-,其中CN-(C为+2价)可被回流硝化液中的
及CN-,其中CN-(C为+2价)可被回流硝化液中的 氧化为无毒气体。请预测CN-反应后的产物为
氧化为无毒气体。请预测CN-反应后的产物为_______ 和_______ 。请分析由蒸氨塔到缺氧池工序酸化的目的:_______ 。
(4)好氧池中富含O2与 反应后的产物为
反应后的产物为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:_______ 。
(5)下列关于混凝沉淀池中的说法合理的是_______ (填写序号)。
a.混凝沉淀池溶液的pH控制在8.3左右
b.FeSO4水解产生Fe(OH)2胶体,吸附水中的悬浮颗粒
c.相同条件下,使用Fe2(SO4)3可获得相同的混凝效果
(6)出水检测
甲醛法可以测定水样中 的含量,其反应原理为
的含量,其反应原理为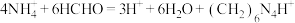 ,然后用NaOH标准溶液滴定反应生成的酸[滴定时,
,然后用NaOH标准溶液滴定反应生成的酸[滴定时,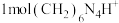 与1molH+相当]。
与1molH+相当]。
实验步骤:
i.移取VmL出水样品,以酚酞为指示剂,用cmol/LNaOH标准液滴定至终点,中和样品中的酸。消耗NaOH溶液的体积为V1mL;
ii.另取同样体积的样品,加入足量的中性甲醛溶液,摇匀,静置5min后,加入1~2滴酚酞溶液,用NaOH标准溶液滴定至终点,消耗NaOH溶液的体积为V2mL。
①步骤ii中滴定至终点的现象为_______ 。
②该水样中残留 浓度为
浓度为_______ mol/L。

| 离子 | 开始沉淀pH | 完全沉淀pH |
| Fe2+ | 6.3 | 8.3 |
| Fe3+ | 2.7 | 3.7 |
(2)蒸氨塔中需要连续加入碱液并保持较高温度。请从化学平衡角度解释回答下列问题。
①写出蒸氨塔中主要的化学平衡的离子方程式:
②加入碱液以及保持较高温度的原因:
(3)缺氧池中含有
 及CN-,其中CN-(C为+2价)可被回流硝化液中的
及CN-,其中CN-(C为+2价)可被回流硝化液中的 氧化为无毒气体。请预测CN-反应后的产物为
氧化为无毒气体。请预测CN-反应后的产物为(4)好氧池中富含O2与
 反应后的产物为
反应后的产物为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(5)下列关于混凝沉淀池中的说法合理的是
a.混凝沉淀池溶液的pH控制在8.3左右
b.FeSO4水解产生Fe(OH)2胶体,吸附水中的悬浮颗粒
c.相同条件下,使用Fe2(SO4)3可获得相同的混凝效果
(6)出水检测
甲醛法可以测定水样中
 的含量,其反应原理为
的含量,其反应原理为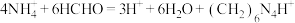 ,然后用NaOH标准溶液滴定反应生成的酸[滴定时,
,然后用NaOH标准溶液滴定反应生成的酸[滴定时,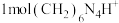 与1molH+相当]。
与1molH+相当]。实验步骤:
i.移取VmL出水样品,以酚酞为指示剂,用cmol/LNaOH标准液滴定至终点,中和样品中的酸。消耗NaOH溶液的体积为V1mL;
ii.另取同样体积的样品,加入足量的中性甲醛溶液,摇匀,静置5min后,加入1~2滴酚酞溶液,用NaOH标准溶液滴定至终点,消耗NaOH溶液的体积为V2mL。
①步骤ii中滴定至终点的现象为
②该水样中残留
 浓度为
浓度为
您最近一年使用:0次
8 . 铜是人类最早冶炼的金属之一、在地壳中,铜主要以硫化物、氧化物或碳酸盐形式存在,其主要矿石为黄铜矿( )、辉铜矿(
)、辉铜矿( )、铜矿(
)、铜矿( )和孔雀石(
)和孔雀石( )。尽管地壳中铁的丰度高于铜,但人类发展炼铁技术的时间较晚。有关铜及其化合物转化的部分工业流程(或转化关系)如下:
)。尽管地壳中铁的丰度高于铜,但人类发展炼铁技术的时间较晚。有关铜及其化合物转化的部分工业流程(或转化关系)如下: (黑色)、
(黑色)、 (红棕色)、碱式硫酸铜(蓝绿色,如
(红棕色)、碱式硫酸铜(蓝绿色,如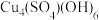 、
、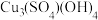 )等。生锈使青铜器的表面呈现出最显著的特征。这一层通常不会改变青铜器的形状,而且铜绿的性质相对稳定,因此通常不会损坏青铜器。然而,如果青铜与含氯物质接触,则可能会形成
)等。生锈使青铜器的表面呈现出最显著的特征。这一层通常不会改变青铜器的形状,而且铜绿的性质相对稳定,因此通常不会损坏青铜器。然而,如果青铜与含氯物质接触,则可能会形成 和
和 ,这被称为“粉末锈病”,这种铜锈会通过以下反应引起“青铜病”:
,这被称为“粉末锈病”,这种铜锈会通过以下反应引起“青铜病”: 与
与 和
和 反应,产生
反应,产生 和
和 (反应3)。形成的
(反应3)。形成的 不是致密相,进而
不是致密相,进而 穿透松散相,与
穿透松散相,与 结合并侵蚀
结合并侵蚀 ,从而形成
,从而形成 和
和 (反应2)。这些反应反复发生,直到器皿完全损坏。
(反应2)。这些反应反复发生,直到器皿完全损坏。
可以从废青铜(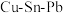 合金)中制备胆矾(
合金)中制备胆矾(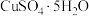 )。称取一定量的青铜废料,放入烧杯中,在通风橱中小心地向烧杯中加入浓硝酸。在反应过程中,释放出红棕色气体(B),形成蓝绿色溶液(C)与白色沉淀(D)的混合物。过滤后,向滤液中添加
)。称取一定量的青铜废料,放入烧杯中,在通风橱中小心地向烧杯中加入浓硝酸。在反应过程中,释放出红棕色气体(B),形成蓝绿色溶液(C)与白色沉淀(D)的混合物。过滤后,向滤液中添加 水溶液,然后形成蓝色溶液E和白色沉淀F。浓缩溶液E和蓝色微晶(晶粒),冷却溶液可获得粗产物(G)。
水溶液,然后形成蓝色溶液E和白色沉淀F。浓缩溶液E和蓝色微晶(晶粒),冷却溶液可获得粗产物(G)。
回答下面问题:
(1)写出反应2~3的化学方程式__________ 。
(2)已知在反应1过程中 所有元素化合价都发生了改变,写出固体A的化学式
所有元素化合价都发生了改变,写出固体A的化学式__________ 。
(3)写出B、D、F和G的化学式__________ 。
(4)分别写出溶液C和E中的主要阴离子和阳离子__________ 。
(5)为了测试产品纯度,称量0.2765g样品至250mL碘量瓶中,并用缓冲溶液溶解。向烧瓶中添加1g ,摇晃10秒后,将混合物在黑暗中保持10分钟。加水稀释后,用0.05036mol·L-1
,摇晃10秒后,将混合物在黑暗中保持10分钟。加水稀释后,用0.05036mol·L-1 标准溶液滴定,滴定终点时消耗20.80mL标准溶液,求出产物的纯度(质量分数)
标准溶液滴定,滴定终点时消耗20.80mL标准溶液,求出产物的纯度(质量分数) __________ 。
(6)对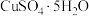 进行了热重分析,其重量随温度的变化如下图所示,求出过程中先后得到的三种固体的化学式
进行了热重分析,其重量随温度的变化如下图所示,求出过程中先后得到的三种固体的化学式__________ 。
 )、辉铜矿(
)、辉铜矿( )、铜矿(
)、铜矿( )和孔雀石(
)和孔雀石( )。尽管地壳中铁的丰度高于铜,但人类发展炼铁技术的时间较晚。有关铜及其化合物转化的部分工业流程(或转化关系)如下:
)。尽管地壳中铁的丰度高于铜,但人类发展炼铁技术的时间较晚。有关铜及其化合物转化的部分工业流程(或转化关系)如下: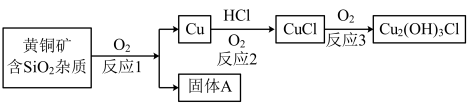
 (黑色)、
(黑色)、 (红棕色)、碱式硫酸铜(蓝绿色,如
(红棕色)、碱式硫酸铜(蓝绿色,如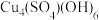 、
、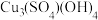 )等。生锈使青铜器的表面呈现出最显著的特征。这一层通常不会改变青铜器的形状,而且铜绿的性质相对稳定,因此通常不会损坏青铜器。然而,如果青铜与含氯物质接触,则可能会形成
)等。生锈使青铜器的表面呈现出最显著的特征。这一层通常不会改变青铜器的形状,而且铜绿的性质相对稳定,因此通常不会损坏青铜器。然而,如果青铜与含氯物质接触,则可能会形成 和
和 ,这被称为“粉末锈病”,这种铜锈会通过以下反应引起“青铜病”:
,这被称为“粉末锈病”,这种铜锈会通过以下反应引起“青铜病”: 与
与 和
和 反应,产生
反应,产生 和
和 (反应3)。形成的
(反应3)。形成的 不是致密相,进而
不是致密相,进而 穿透松散相,与
穿透松散相,与 结合并侵蚀
结合并侵蚀 ,从而形成
,从而形成 和
和 (反应2)。这些反应反复发生,直到器皿完全损坏。
(反应2)。这些反应反复发生,直到器皿完全损坏。可以从废青铜(
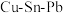 合金)中制备胆矾(
合金)中制备胆矾(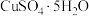 )。称取一定量的青铜废料,放入烧杯中,在通风橱中小心地向烧杯中加入浓硝酸。在反应过程中,释放出红棕色气体(B),形成蓝绿色溶液(C)与白色沉淀(D)的混合物。过滤后,向滤液中添加
)。称取一定量的青铜废料,放入烧杯中,在通风橱中小心地向烧杯中加入浓硝酸。在反应过程中,释放出红棕色气体(B),形成蓝绿色溶液(C)与白色沉淀(D)的混合物。过滤后,向滤液中添加 水溶液,然后形成蓝色溶液E和白色沉淀F。浓缩溶液E和蓝色微晶(晶粒),冷却溶液可获得粗产物(G)。
水溶液,然后形成蓝色溶液E和白色沉淀F。浓缩溶液E和蓝色微晶(晶粒),冷却溶液可获得粗产物(G)。回答下面问题:
(1)写出反应2~3的化学方程式
(2)已知在反应1过程中
 所有元素化合价都发生了改变,写出固体A的化学式
所有元素化合价都发生了改变,写出固体A的化学式(3)写出B、D、F和G的化学式
(4)分别写出溶液C和E中的主要阴离子和阳离子
(5)为了测试产品纯度,称量0.2765g样品至250mL碘量瓶中,并用缓冲溶液溶解。向烧瓶中添加1g
 ,摇晃10秒后,将混合物在黑暗中保持10分钟。加水稀释后,用0.05036mol·L-1
,摇晃10秒后,将混合物在黑暗中保持10分钟。加水稀释后,用0.05036mol·L-1 标准溶液滴定,滴定终点时消耗20.80mL标准溶液,求出产物的纯度(质量分数)
标准溶液滴定,滴定终点时消耗20.80mL标准溶液,求出产物的纯度(质量分数) (6)对
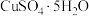 进行了热重分析,其重量随温度的变化如下图所示,求出过程中先后得到的三种固体的化学式
进行了热重分析,其重量随温度的变化如下图所示,求出过程中先后得到的三种固体的化学式
您最近一年使用:0次
9 . 叠氮化钠( )常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如下:
)常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如下:
①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入 。
。
④冷却,向产物中加入乙醇(降低 的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。

已知:Ⅰ. 是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
Ⅱ.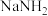 熔点210℃,沸点400℃,在水溶液中易水解。
熔点210℃,沸点400℃,在水溶液中易水解。
请回答下列问题:
(1)实验室若采用固体加热方式制取氨气的化学方程式为_______ 。
(2)步骤①中先加热通氨气的目的是_______ ;步骤②氨气与熔化的钠反应生成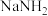 的化学方程式为
的化学方程式为_______ ;步骤③中最适宜的加热方式为_______ (填“水浴加热”,“油浴加热”)
(3)图中仪器a用的材料是铁质而不用玻璃,其主要原因是_______ 。
(4)汽车经撞击后30毫秒内,会引发叠氮化钠迅速分解为两种单质,其中氧化产物和还原产物的质量之比为_______ 。
(5)步骤④中用乙醚洗涤的主要原因除因其易挥发,有利于产品快速干燥外,还因为_______ 。
(6)实验室用滴定法测定叠氮化钠样品中 的质量分数:
的质量分数:
①将2.500g试样配成500.00mL溶液。
②取50.00mL溶液置于锥形瓶中,加入50.00mL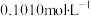
 溶液。
溶液。
③充分反应后,将溶液稍稀释,向溶液中加入8mL浓硫酸,滴入3滴邻菲啰啉指示液,用 标准溶液滴定过量的
标准溶液滴定过量的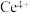 ,消耗溶液体29.00mL。测定过程的反应方程式为:
,消耗溶液体29.00mL。测定过程的反应方程式为: ;
; ;
;
试样中 的质量分数为
的质量分数为_______ (保留小数点后一位)。
 )常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如下:
)常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如下:①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入
 。
。④冷却,向产物中加入乙醇(降低
 的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
已知:Ⅰ.
 是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;Ⅱ.
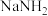 熔点210℃,沸点400℃,在水溶液中易水解。
熔点210℃,沸点400℃,在水溶液中易水解。请回答下列问题:
(1)实验室若采用固体加热方式制取氨气的化学方程式为
(2)步骤①中先加热通氨气的目的是
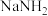 的化学方程式为
的化学方程式为(3)图中仪器a用的材料是铁质而不用玻璃,其主要原因是
(4)汽车经撞击后30毫秒内,会引发叠氮化钠迅速分解为两种单质,其中氧化产物和还原产物的质量之比为
(5)步骤④中用乙醚洗涤的主要原因除因其易挥发,有利于产品快速干燥外,还因为
(6)实验室用滴定法测定叠氮化钠样品中
 的质量分数:
的质量分数:①将2.500g试样配成500.00mL溶液。
②取50.00mL溶液置于锥形瓶中,加入50.00mL
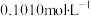
 溶液。
溶液。③充分反应后,将溶液稍稀释,向溶液中加入8mL浓硫酸,滴入3滴邻菲啰啉指示液,用
 标准溶液滴定过量的
标准溶液滴定过量的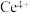 ,消耗溶液体29.00mL。测定过程的反应方程式为:
,消耗溶液体29.00mL。测定过程的反应方程式为: ;
; ;
;试样中
 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
10 .  是灭杀新冠病毒的消毒剂之一,是一种无色易挥发,易溶于水的液体,受热易分解。有强烈刺激性气味,有腐蚀性,对人的眼睛、皮肤、黏膜、上呼吸道等有强烈刺激作用。
是灭杀新冠病毒的消毒剂之一,是一种无色易挥发,易溶于水的液体,受热易分解。有强烈刺激性气味,有腐蚀性,对人的眼睛、皮肤、黏膜、上呼吸道等有强烈刺激作用。
(1) 为过氧乙酸,推测过氧乙酸可能具有的化学性质:
为过氧乙酸,推测过氧乙酸可能具有的化学性质:___________ 。
(2)简述 易溶于水的原因:
易溶于水的原因:___________ 。
(3)某实验小组,利用高浓度的双氧水和乙酸在固体酸作催化剂和加热的条件下合成少量 ,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水。已知乙酸丁酯的密度为
,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水。已知乙酸丁酯的密度为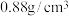 ,难溶于水。部分实验装置如图所示。
,难溶于水。部分实验装置如图所示。

①写出制备 的化学方程式:
的化学方程式:___________ 。
②B的名称:___________ 。
③反应体系分离出水时采用减压的目的:___________ 。
(4) (含有少量
(含有少量 杂质)的含量测定流程如图。(已知过氧乙酸不与高锰酸钾反应)
杂质)的含量测定流程如图。(已知过氧乙酸不与高锰酸钾反应)

① 被
被 还原,产物之一为
还原,产物之一为 ,其离子方程式为
,其离子方程式为___________ 。
②若样品体积为 ,加入
,加入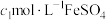 溶液
溶液 ,消耗
,消耗 溶液
溶液 ,则
,则 含量为
含量为___________  。
。
③若用 溶液除
溶液除 时,不慎滴加
时,不慎滴加 过量,则导致最终测定
过量,则导致最终测定 的含量
的含量___________ (填“偏高”“偏低”或“不变”)。
 是灭杀新冠病毒的消毒剂之一,是一种无色易挥发,易溶于水的液体,受热易分解。有强烈刺激性气味,有腐蚀性,对人的眼睛、皮肤、黏膜、上呼吸道等有强烈刺激作用。
是灭杀新冠病毒的消毒剂之一,是一种无色易挥发,易溶于水的液体,受热易分解。有强烈刺激性气味,有腐蚀性,对人的眼睛、皮肤、黏膜、上呼吸道等有强烈刺激作用。(1)
 为过氧乙酸,推测过氧乙酸可能具有的化学性质:
为过氧乙酸,推测过氧乙酸可能具有的化学性质:(2)简述
 易溶于水的原因:
易溶于水的原因:(3)某实验小组,利用高浓度的双氧水和乙酸在固体酸作催化剂和加热的条件下合成少量
 ,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水。已知乙酸丁酯的密度为
,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水。已知乙酸丁酯的密度为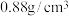 ,难溶于水。部分实验装置如图所示。
,难溶于水。部分实验装置如图所示。
①写出制备
 的化学方程式:
的化学方程式:②B的名称:
③反应体系分离出水时采用减压的目的:
(4)
 (含有少量
(含有少量 杂质)的含量测定流程如图。(已知过氧乙酸不与高锰酸钾反应)
杂质)的含量测定流程如图。(已知过氧乙酸不与高锰酸钾反应)
①
 被
被 还原,产物之一为
还原,产物之一为 ,其离子方程式为
,其离子方程式为②若样品体积为
 ,加入
,加入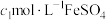 溶液
溶液 ,消耗
,消耗 溶液
溶液 ,则
,则 含量为
含量为 。
。③若用
 溶液除
溶液除 时,不慎滴加
时,不慎滴加 过量,则导致最终测定
过量,则导致最终测定 的含量
的含量
您最近一年使用:0次






